Химические свойства самого распространенного металла
Алюминий — активный металл. Он устойчив на воздухе, при нормальной температуре быстро окисляется, покрываясь плотной пленкой оксида, которая защищает металл от дальнейшего разрушения.
- Взаимодействие алюминия с другими веществами
- Взаимодействие с неметаллами
- Взаимодействие алюминия с водородом
- Алюминий и его водородная пористость
- Гидрид алюминия
- Содержание
- Молекулярная структура
- Физические свойства
- Химические свойства
- Получение
- Применение
- Алюминий. Химия алюминия и его соединений
- Алюминий
- Положение в периодической системе химических элементов
- Электронное строение алюминия и свойства
- Физические свойства
- Нахождение в природе
- Способы получения
- Качественные реакции
- Химические свойства
Взаимодействие алюминия с другими веществами
При обычных условиях не взаимодействует с водой даже в состоянии кипения. При удалении защитной оксидной пленки алюминий вступает в энергичное взаимодействие с водяным паром воздуха, превращаясь в рыхлую массу гидроксида алюминия с выделением водорода и тепла. Уравнение реакции:
2Al + 6H₂O = 2Al(OH)₃ + 3H₂
Если снять защитную оксидную пленку с алюминия, то металл вступает в активное взаимодействие с кислородом. При этом порошок алюминия сгорает, образуя оксид. Уравнение реакции:
Этот металл также активно взаимодействует со многими кислотами. При реакции с соляной кислотой наблюдается выделение водорода:
2Al + 6HCl = 2AlCl₃ + 3H₂
При обычных условиях концентрированная азотная кислота не взаимодействует с алюминием, так как будучи сильным окислителем, она делает оксидную пленку еще крепче. По этой причине азотная кислота хранится и перевозится в алюминиевой посуде.
Алюминий при обычной температуре пассивируется разбавленной азотной и концентрированной серной кислотами. В горячей серной кислоте металл растворяется:
2Al + 4H₂SO4 = Al₂(SO4)₃ + S + 4H₂O
Взаимодействие с неметаллами
Алюминий реагирует с галогенами, серой, азотом, углеродом и всеми неметаллами. Для протекания реакции необходимо нагревание, после чего взаимодействие происходит с выделением большого количества тепла.
Взаимодействие алюминия с водородом
Алюминий непосредственно с водородом не реагирует, хотя известно твердое полимерное соединение алан, в котором существуют так называемые трехцентровые связи. При температуре выше 100 градусов Цельсия алан необратимо разлагается на простые вещества. Гидрид алюминия бурно реагирует с водой.
Алюминий напрямую не реагирует с водородом: металл образует соединения путем потери электронов, которые принимаются другими элементами. Атомы водорода не принимают электроны, которые отдают металлы для образования соединений. «Принуждать» атомы водорода принять электроны с образованием твердых ионных соединений (гидридов) могут только очень реактивные металлы (калий, натрий, магний, кальций). Для прямого синтеза гидрида алюминия из водорода и алюминия требуется огромное давление (около 2 миллиардов атмосфер) и температура выше 800 К. Здесь вы сможете узнать о химических свойствах других металлов.
Следует отметить, что водород — это единственный газ, заметно растворяющийся в алюминии и его сплавах. Растворимость водорода изменяется пропорционально температуре и квадратному корню из давления. Растворимость водорода в жидком алюминии значительно выше, чем в твердом. Это свойство незначительно изменяется в зависимости от химического состава сплавов.
Алюминий и его водородная пористость
Образование в алюминии пузырей водорода непосредственно зависит от скорости охлаждения и затвердевания, а также от наличия центров зарождения для выделения водорода — захваченных внутрь расплава оксидов. Для образования пористости алюминия необходимо значительное превышение содержания растворенного водорода по сравнению с растворимостью водорода в твердом алюминии. При отсутствии центров зарождения для выделения водорода требуется относительно высокая концентрация вещества.
Расположение водорода в затвердевшем алюминии зависит от уровня его содержания в жидком алюминии и условий, при которых происходило затвердевание. Так как водородная пористость — это результат механизмов зарождения и роста, контролируемых диффузией, то такие процессы, как снижение концентрации водорода и увеличение скорости затвердевания, подавляют зарождение и рост пор. Из-за этого выполненные методом литья в разъемный кокиль отливки металла более подвержены дефектам, связанным с водородом, чем отливки, изготовленные методом литья под давлением.
Есть разные источники попадания водорода в алюминий.
Шихтовые материалы (лом, слитки, литейный возврат, оксиды, песок и смазки, применяющиеся при механической обработке). Эти загрязнители — потенциальные источники водорода, образовавшегося при химическом разложении паров воды или восстановлении органических веществ.
Плавильные инструменты. Скребки, пики, лопаты являются источником водорода. Оксиды и остатки флюсов на инструментах впитывают влагу из окружающего воздуха. Печные огнеупоры, распределительные каналы, ковши для отбора проб, известковые желоба и цементные растворы — потенциальные источники водорода.
Атмосфера печи. Если плавильная печь работает на мазуте или на природном газе, возможно неполное сгорание топлива с образованием свободного водорода.
Флюсы (гигроскопичные соли, готовые мгновенно впитывать воду). По этой причине влажный флюс неизбежно вносит в расплав водород, образовавшийся при химическом разложении воды.
Литейные формы. В процессе заполнения литейной формы жидкий алюминий течет турбулентно и захватывает воздух во внутренний объем. Если воздух не успеет выйти из формы до начала затвердевания алюминия, то водовод проникнет в металл.
Гидрид алюминия
| Гидрид алюминия | |
|---|---|
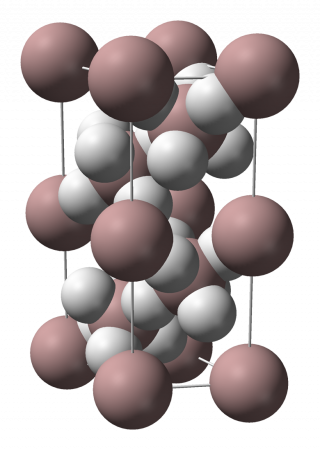 | |
| Систематическое наименование | Гидрид алюминия |
| Традиционные названия | Гидрид алюминия, гидрид алюминия III, алан |
| Хим. формула | (AlH3)n |
| Рац. формула | AlH3 |
| Состояние | твёрдое |
| Молярная масса | 30,005 г/моль |
| Плотность | 1,45 |
| Температура | |
| • разложения | 105 |
| Энтальпия | |
| • образования | − 12 кДж/моль |
| Рег. номер CAS | 7784-21-6 |
| PubChem | 14488 |
| Рег. номер EINECS | 232-053-2 |
| SMILES | |
| ChEBI | 30136 |
| ChemSpider | 13833 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Гидрид алюминия — AlH3, неорганическое бинарное соединение алюминия с водородом. В нормальных условиях — бесцветное или белое твёрдое вещество, имеющее полимерную структуру: (AlH3)n.
Впервые был получен в 1942 году действием тлеющего электрического разряда на смесь триметилалюминия и водорода.
Используется как компонент ракетного топлива, мощный восстановитель в органическом синтезе и в качестве катализатора для реакций полимеризации.
Содержание
- 1 Молекулярная структура
- 2 Физические свойства
- 3 Химические свойства
- 4 Получение
- 5 Применение
Молекулярная структура
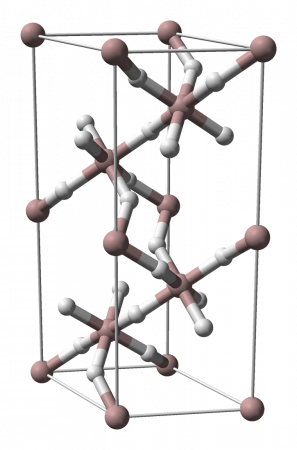
В обычных условиях гидрид алюминия имеет полимерную молекулярную структуру (AlH3)n, при этом его кристаллическая форма существует в семи полиморфных модификациях: α-(AlH3)n, α 1 -(AlH3)n, β-(AlH3)n, δ-(AlH3)n, ε-(AlH3)n, γ-(AlH3)n, ζ-(AlH3)n.
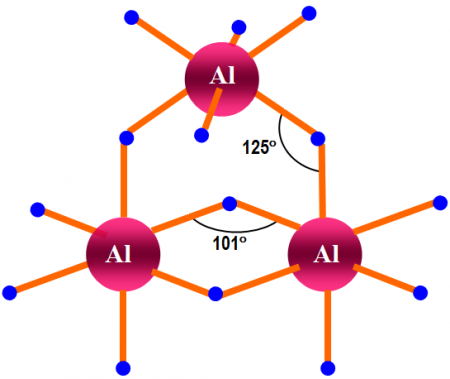
Самой устойчивой является модификация α-(AlH3)n, имеющая гексагональную сингонию (пространственная группа R3c, а = 4,449 Å, b = 4,449 Å, c = 11,804 Å). Длина связи Al—H составляет 1,72 Å, длина связи Al—Al: 3,24 Å. Структура α-(AlH3)n представляет собой совокупность октаэдров АlН6, объединенных шестью трехцентровыми двухэлектронными связями Аl—Н—Аl в кристаллический каркас.
Модификация γ-(AlH3)n существует в ромбической сингонии, пространственная группа Pnnm (а = 5,3806 Å, b = 7,3555 Å, c = 5,77509 Å). Ячейка кристаллической решётки гидрида состоит из двух октаэдров AlH6, длина связи Al—Al составляет 2,606 Å. Особенностью структуры является наличие разветвлённой двойной мостиковой связи Al—2H—Al (длина связи Al—H: 1,68—1,70 Å) в дополнение к обычной связи Al—H—Al (длина связи Al—H: 1,77—1,78 Å). Из-за наличия больших полостей в кристаллической структуре γ-(AlH3)n, данная модификация имеет плотность примерно на 11 % меньше, чем α-(AlH3)n.
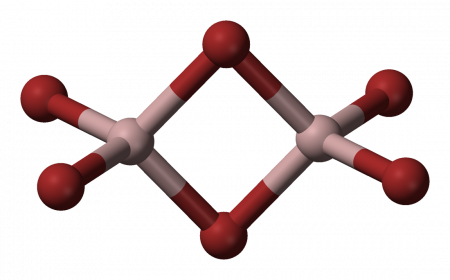
При взаимодействии распылённых лазером атомов алюминия с водородом при сверхнизких температурах (3,5 K) с последующим ультрафиолетовым излучением и нормализацией при 6,5 K, в продуктах фотолиза можно обнаружить структуры димера Al2H6, аналогичные структуре диборана B2H6. Димер (см. структуру на рисунке) очень неустойчив в конденсированном состоянии, поэтому его существование обнаружилось лишь спустя примерно пятьдесят лет после открытия гидрида алюминия.
В 2007 году группа учёных из США воздействовала на алюминий плазменным потоком атомов водорода и обнаружила, что в результате образуются различные анионные полиядерные гидриды алюминия, среди которых особый интерес вызвал анион Al4H6 − , чей нейтральный гибрид Al4H6 по расчётам должен отличаться заметной стабильностью. Структурно соединение должно представлять искажённый тетраэдр с вершинами — атомами алюминия, в котором атомы водорода образуют четыре терминальные связи Al–H и две мостиковые связи Al–H–Al. Большой энергетический порог между высшими занятыми и низшими свободными молекулярными орбиталями в сочетании с исключительно высоким значением теплоты сгорания позволяют предположить, что этот гидрид алюминия может представлять собой перспективный материал для ракетного топлива.
Физические свойства
Гидрид алюминия представляет собой твёрдое белое или бесцветное вещество. Плотность 1,45 (по другим данным 1,47) г/см³. Растворим в тетрагидрофуране (5 г в 100 г растворителя при 19,5 °C).
- стандартная энтальпия образования, ΔH o 298: −12 кДж/моль (по другим данным: −11,43±0,84 кДж/моль);
- стандартная энтропия, S o 298: 30 Дж/(моль·K) (по другим данным: 30,06±0,42 Дж/(моль·K));
- стандартная энергия Гиббса, ΔG o 298: 46 кДж/моль (по другим данным: 46,52±0,96 кДж/моль).
Большое содержание водорода в гидриде алюминия обуславливает ряд его свойств, связанных с проблемой высокотемпературной сверхпроводимости: в области давлений
60 ГПа и температуре
1000 K он обладает полупроводниковым механизмом проводимости, а в области высоких давлений и температур (до 90 ГПа и 2000 K) его проводимость сопоставима с металлической электропроводностью водорода.
Химические свойства
- Соединение нестабильно: при нагревании выше 100 °C разлагается:
2 AlH3 → to 2 Al + 3 H2
- Бурно взаимодействует с водой:
AlH3 + 3 H2O → Al(OH)3 + 3 H2 ↑
- С диэтиловым эфиром образует высокореакционный, но относительно стабильный комплекс переменного состава, который часто используется для синтетических целей:
AlH3 + n(C2H5)2O → AlH3 ⋅ n(C2H5)2O Аналогичный комплекс образуется с другими низшими алифатическими эфирами, а также с триметиламином: AlH3 • N(CH3)3. Последний взаимодействует с водой со взрывом. Для стабилизации гидрида алюминия также можно использовать комплексы с другими аминами, например с N-метилпирролидином (NMP): AlH3 • NMP и AlH3 • (NMP)2.
- Гидрид алюминия — очень сильный восстановитель. Он способен восстановить углекислый газ до метана:
4 AlH3 + 3 CO2 → to 3 CH4 + 2 Al2O3 Известны многочисленные реакции восстановления органических соединений с использованием гидрида алюминия.
- Взаимодействует с гидридом лития, образуя алюмогидрид:
AlH3 + LiH → (C2H5)2O LiAlH4 Медленно вступает в реакцию с дибораном, образуя борогидрид алюминия (точнее тетрагидридоборат алюминия): 2 AlH3 + B2H6 → 2 Al(BH4)3
Получение
Используемый сегодня принципиальный метод получения чистого гидрида алюминия из гидрида лития в среде диэтилового эфира был предложен ещё в 1947 году:
Хлорид лития выпадает в осадок до момента полимеризации AlH3 и отделяется от эфирного раствора, из которого путём дальнейшей отгонки эфира получают комплекс гидрида алюминия с диэтиловым эфиром.
Также гидрид алюминия по аналогии можно получить реакцией алюмогидрида лития с серной кислотой, хлоридом бериллия, хлоридом цинка, хлороводородом и алкилгалогенидами:
2 LiAlH4 + H2SO4 → 2 AlH3 + Li2SO4 + 2 H2 LiAlH4 + HCl → AlH3 + LiCl + H2 2 LiAlH4 + BeCl2 → 2 AlH3 + 2 LiCl + BeH2 2 LiAlH4 + ZnCl2 → 2 AlH3 + 2 LiCl + ZnH2 LiAlH4 + R−CH2−Cl → AlH3 + LiCl + R−CH3
Вместо алюмогидрида лития можно использовать алюмогидрид натрия:
Для получения чистого гидрида (без примесей растворителя) эфирный комплекс подвергают нагреванию в вакууме с добавлением бензола или в присутствии небольших количеств LiAlH4 или смеси LiAlH4+LiBH4. При этом сперва получаются β-AlH3 и γ-AlH3 модификации, которые затем переходят в более стабильный α-AlH3.
Другим способом получения несольватированного эфиром гидрида алюминия, является электролиз алюмогидрида натрия в среде тетрагидрофурана.
Среди прочих методов отметим синтез с использованием гидрида магния:
Долгое время считалось, что гидрид алюминия невозможно получить прямым взаимодействием элементов, поэтому для его синтеза использовали приведённые выше косвенные методы. Однако, в 1992 году группа российских учёных осуществила прямой синтез гидрида из водорода и алюминия, используя высокое давление (выше 2 ГПа) и температуру (более 800 K). Вследствие очень жёстких условий протекания реакции, в настоящий момент метод имеет лишь теоретическое значение.
Применение
Гидрид алюминия находит широкое применение в органическом синтезе в качестве сильнейшего восстанавливающего агента.
В связи с тем, что гидрид алюминия представляет собой соединение с высоким содержанием водорода (10,1 %), он используется в производстве ракетных топлив и некоторых взрывчатых веществ, а также для систем хранения и генерации в автономных энергетических водородных установках.
Алюминий. Химия алюминия и его соединений
Бинарные соединения алюминия
Алюминий
Положение в периодической системе химических элементов
Алюминий расположен в главной подгруппе III группы (или в 13 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение алюминия и свойства
Электронная конфигурация алюминия в основном состоянии :
+13Al 1s 2 2s 2 2p 6 3s 2 3p 1 1s 



Электронная конфигурация алюминия в возбужденном состоянии :
+13Al * 1s 2 2s 2 2p 6 3s 1 3p 2 1s 



Алюминий проявляет парамагнитные свойства. Алюминий на воздухе быстро образует прочные оксидные плёнки, защищающие поверхность от дальнейшего взаимодействия, поэтому устойчив к коррозии.
Физические свойства
Алюминий – лёгкий металл серебристо-белого цвета, легко поддающийся формовке, литью, механической обработке. Обладает высокой тепло- и электропроводностью.
Температура плавления 660 о С, температура кипения 1450 о С, плотность алюминия 2,7 г/см 3 .
Алюминий — один из наиболее ценных цветных металлов для вторичной переработки. На протяжении последних лет, цена на лом алюминия в пунктах приема непреклонно растет. По ссылке можно узнать о том, как сдать лом алюминия.
Нахождение в природе
Алюминий — самый распространенный металл в природе, и 3-й по распространенности среди всех элементов (после кислорода и кремния). Содержание в земной коре — около 8%.
В природе алюминий встречается в виде соединений:
Корунд Al2O3. Красный корунд называют рубином, синий корунд называют сапфиром.
Способы получения
Алюминий образует прочную химическую связь с кислородом. Поэтому традиционные способы получения алюминия восстановлением из оксида протекают требуют больших затрат энергии. Для промышленного получения алюминия используют процесс Холла-Эру. Для понижения температуры плавления оксид алюминия растворяют в расплавленном криолите (при температуре 960-970 о С) Na3AlF6, а затем подвергают электролизу с углеродными электродами. При растворении в расплаве криолита оксид алюминия распадается на ионы:
На катоде происходит восстановление ионов алюминия:
Катод: Al 3+ +3e → Al 0
На аноде происходит окисление алюминат-ионов:
Суммарное уравнение электролиза расплава оксида алюминия:
Лабораторный способ получения алюминия заключается в восстановлении алюминия из безводного хлорида алюминия металлическим калием:
AlCl3 + 3K → Al + 3KCl
Качественные реакции
Качественная реакция на ионы алюминия — взаимодействие избытка солей алюминия с щелочами . При этом образуется белый аморфный осадок гидроксида алюминия.
Например , хлорид алюминия взаимодействует с гидроксидом натрия:
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
При дальнейшем добавлении щелочи амфотерный гидроксид алюминия растворяется с образованием тетрагидроксоалюмината:
Обратите внимание , если мы поместим соль алюминия в избыток раствора щелочи, то белый осадок гидроксида алюминия не образуется, т.к. в избытке щелочи соединения алюминия сразу переходят в комплекс:
AlCl3 + 4NaOH = Na[Al(OH)4] + 3NaCl
Соли алюминия можно обнаружить с помощью водного раствора аммиака. При взаимодействии растворимых солей алюминия с водным раствором аммиака также в ыпадает полупрозрачный студенистый осадок гидроксида алюминия.
AlCl3 + 3NH3·H2O = Al(OH)3 ↓ + 3NH4Cl
Al 3+ + 3NH3·H2O = Al(OH)3 ↓ + 3NH4 +
Видеоопыт взаимодействия раствора хлорида алюминия с раствором аммиака можно посмотреть здесь.
Химические свойства
1. Алюминий – сильный восстановитель . Поэтому он реагирует со многими неметаллами .
1.1. Алюминий реагируют с галогенами с образованием галогенидов:
1.2. Алюминий реагирует с серой с образованием сульфидов:
1.3. Алюминий реагируют с фосфором . При этом образуются бинарные соединения — фосфиды:
Al + P → AlP
1.4. С азотом алюминий реагирует при нагревании до 1000 о С с образованием нитрида:
2Al + N2 → 2AlN
1.5. Алюминий реагирует с углеродом с образованием карбида алюминия:
1.6. Алюминий взаимодействует с кислородом с образованием оксида:
Видеоопыт взаимодействия алюминия с кислородом воздуха (горение алюминия на воздухе) можно посмотреть здесь.
2. Алюминий взаимодействует со сложными веществами:
2.1. Реагирует ли алюминий с водой? Ответ на этот вопрос вы без труда найдете, если покопаетесь немного в своей памяти. Наверняка хотя бы раз в жизни вы встречались с алюминиевыми кастрюлями или алюминиевыми столовыми приборами. Такой вопрос я любил задавать студентам на экзаменах. Что самое удивительное, ответы я получал разные — у кого-то алюминий таки реагировал с водой. И очень, очень многие сдавались после вопроса: «Может быть, алюминий реагирует с водой при нагревании?» При нагревании алюминий реагировал с водой уже у половины респондентов))
Тем не менее, несложно понять, что алюминий все-таки с водой в обычных условиях (да и при нагревании) не взаимодействует. И мы уже упоминали, почему: из-за образования оксидной пленки . А вот если алюминий очистить от оксидной пленки (например, амальгамировать), то он будет взаимодействовать с водой очень активно с образованием гидроксида алюминия и водорода:
2Al 0 + 6 H2 + O → 2 Al +3 ( OH)3 + 3 H2 0
Амальгаму алюминия можно получить, выдержав кусочки алюминия в растворе хлорида ртути ( II ):
3HgCl2 + 2Al → 2AlCl3 + 3Hg
Видеоопыт взаимодействия амальгамы алюминия с водой можно посмотреть здесь.
2.2. Алюминий взаимодействуют с минеральными кислотами (с соляной, фосфорной и разбавленной серной кислотой). При этом образуются соль и водород.
Например , алюминий бурно реагирует с соляной кислотой :
2Al + 6HCl = 2AlCl3 + 3H2↑
2.3. При обычных условиях алюминий не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат алюминия и вода:
2.4. Алюминий не реагирует с концентрированной азотной кислотой также из-за пассивации.
С разбавленной азотной кислотой алюминий реагирует с образованием молекулярного азота:
При взаимодействии алюминия в виде порошка с очень разбавленной азотной кислотой может образоваться нитрат аммония:
2.5. Алюминий – амфотерный металл, поэтому он взаимодействует с щелочами . При взаимодействии алюминия с раствором щелочи образуется тетрагидроксоалюминат и водород:
2Al + 2NaOH + 6H2O → 2Na[Al(OH)4] + 3H2 ↑
Видеоопыт взаимодействия алюминия со щелочью и водой можно посмотреть здесь.
Алюминий реагирует с расплавом щелочи с образованием алюмината и водорода:
2Al + 6NaOH → 2Na3AlO3 + 3H2 ↑
Эту же реакцию можно записать в другом виде (в ЕГЭ рекомендую записывать реакцию именно в таком виде):
2Al + 6NaOH → 2NaAlO2 + 3H2↑ + 2Na2O
2.6. Алюминий восстанавливает менее активные металлы из оксидов . Процесс восстановления металлов из оксидов называется алюмотермия .
Например , алюминий вытесняет медь из оксида меди (II). Реакция очень экзотермическая:
2Al + 3CuO → 3Cu + Al2O3
Еще пример : алюминий восстанавливает железо из железной окалины, оксида железа (II, III):
Восстановительные свойства алюминия также проявляются при взаимодействии его с сильными окислителями: пероксидом натрия, нитратами и нитритами в щелочной среде, перманганатами, соединениями хрома (VI):