электролиз воды это разложение воды на ее элементарные составляющие под действием электрического тока. При этом водород и молекулярный кислород образуются на двух инертных поверхностях, H2 и O2. Эти две поверхности более известны под названием электродов.
Теоретически, объем Н2 образуется должен быть в два раза больше объема O2. Почему? Поскольку молекула воды имеет отношение H / O, равное 2, то есть два H для каждого кислорода. Это соотношение проверяется непосредственно с помощью его химической формулы H2О. Однако многие экспериментальные факторы влияют на полученные объемы.
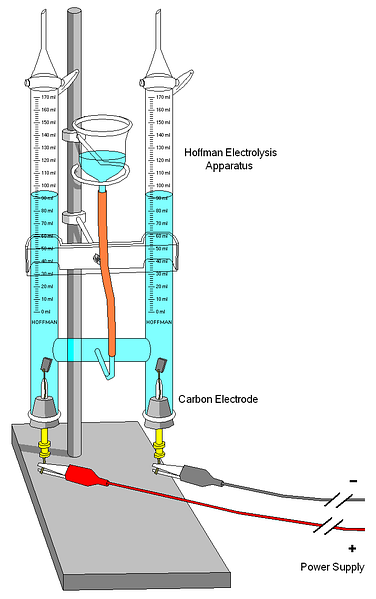
Если электролиз проводят внутри труб, погруженных в воду (верхнее изображение), столб воды меньшей высоты соответствует водороду, поскольку на поверхности жидкости присутствует большее количество газа, оказывающего давление. Пузырьки окружают электроды и в конечном итоге поднимаются после истечения давления пара воды.
Обратите внимание, что трубки отделены друг от друга таким образом, что существует низкая миграция газов от одного электрода к другому. В низких масштабах это не представляет неизбежного риска; но в промышленных масштабах газовая смесь Н2 и O2 Это очень опасно и взрывоопасно.
По этой причине электрохимические ячейки, в которых проводится электролиз воды, очень дороги; им нужны конструкция и элементы, которые гарантируют, что газы никогда не смешиваются, выгодная подача тока, высокая концентрация электролитов, специальные электроды (электрокатализаторы) и механизмы для хранения H.2 произведенный.
Электрокатализаторы представляют собой трение и в то же время крылья для прибыльности электролиза воды. Некоторые состоят из оксидов благородных металлов, таких как платина и иридий, цены на которые очень высоки. Именно в этот момент исследователи объединяют усилия для разработки эффективных, стабильных и дешевых электродов..
Причиной этих усилий является ускорение образования О2, который дается на более низких скоростях по сравнению с H2. Это замедляется электродом, где образуется О2 как общее следствие, применение потенциала намного больше, чем необходимо (перенапряжение); что то же самое, чтобы снизить производительность и более высокие расходы.
- 1 Реакция электролиза
- 1.1 Полуклеточные реакции
- 2 Процедура
- 3 Техники
- 3.1 Электролиз щелочной водой
- 3.2 Электролиз с полимерной электролитической мембраной
- 3.3 Электролиз с твердыми оксидами
- 4 Какая польза от электролиза воды??
- 4.1 Производство водорода и его использование
- 4.2 Как метод отладки
- 4.3 Как поставка кислорода
- 5 Домашний эксперимент
- 5.1 Домашние переменные
- 6 Ссылки
- Реакция электролиза
- Полуклеточные реакции
- процесс
- методы
- Электролиз щелочной водой
- Электролиз с полимерной электролитической мембраной
- Электролиз с твердыми оксидами
- Какая польза от электролиза воды?
- Производство водорода и его использование
- Как метод отладки
- В качестве источника кислорода
- Домашний эксперимент
- Домашние переменные
- Электролиз воды
- Что такое электролиз
- Электролиз воды
- Что мы узнали?
- НИЗКОАМПЕРНЫЙ ЭЛЕКТРОЛИЗ ВОДЫ
- Инструменты и оборудование, использованные при эксперименте
- Результаты эксперимента
- ЗАКЛЮЧЕНИЕ
- ЛИТЕРАТУРА
Реакция электролиза
Электролиз воды включает в себя много сложных аспектов. Однако в общих чертах его основа лежит в простой глобальной реакции:
Как видно из уравнения, вмешиваются две молекулы воды: одну обычно нужно уменьшить или получить электроны, а другую — окислить или потерять электроны..
H2 Это продукт восстановления воды, потому что усиление электронов способствует протонов H + может быть ковалентно связан, и кислород превращается в ОН — . Поэтому Н2 происходит на катоде, который является электродом, где происходит восстановление.
В то время как O2 происходит от окисления воды, потому что она теряет электроны, которые позволяют ей связываться с водородом, и, следовательно, высвобождает протоны H + . O2 происходит на аноде, электроде, где происходит окисление; и в отличие от другого электрода, pH вокруг анода является кислым, а не основным.
Полуклеточные реакции
Вышеизложенное можно обобщить следующими химическими уравнениями для полуклеточных реакций:
2H2O + 2e — => H2 + 2OH — (Катод, основной)
2H2O => O2 + 4H + + 4e — (Анод, кислота)
Однако вода не может потерять больше электронов (4e — ) из которых другая молекула воды побеждает на катоде (2e — ); следовательно, первое уравнение должно быть умножено на 2, а затем вычтено со вторым уравнением, чтобы получить чистое уравнение:
Но 4Н + и 4OH — они образуют 4H2Или, таким образом, они устраняют четыре из шести молекул H2Или оставив два; и в результате глобальная реакция только что изложил.
Реакции полуэлемента изменяются в зависимости от значений рН, методов, а также имеют потенциальные потенциалы восстановления или окисления, которые определяют, какой ток необходимо подавать, чтобы электролитический процесс воды происходил самопроизвольно..
процесс
На верхнем изображении показан вольтметр Хоффмана. Цилиндры заполняются водой и выделенными электролитами через среднее сопло. Роль этих электролитов заключается в повышении проводимости воды, потому что в нормальных условиях очень мало ионов H3О + и ОН — продукты вашего авто ионизации.
Два электрода обычно платиновые, хотя на изображении они были заменены угольными электродами. Оба связаны с батареей, с которой применена разность потенциалов (ΔV), которая способствует окислению воды (образование O).2).
Электроны перемещаются по всему контуру, пока вы не достигнете другого электрода, где вода выигрывает и становится Н2 и ОН — . На данный момент анод и катод уже определены, которые могут быть дифференцированы по высоте водяных столбов; тот, который имеет меньшую высоту, соответствует катоду, где образуется Н2.
В верхней части цилиндров есть несколько клавиш, позволяющих выпускать образующиеся газы. Вы можете тщательно проверить наличие H2 заставляя его реагировать с пламенем, сгорание которого дает газообразную воду.
методы
Методы электролиза воды варьируются в зависимости от количества Н2 и O2 что предлагается генерировать. Оба газа очень опасны, если их смешивать друг с другом, и поэтому электролизеры имеют сложную конструкцию, чтобы минимизировать увеличение газовых давлений и их диффузию через водную среду..
Кроме того, методы колеблются в зависимости от элемента, электролита, добавляемого в воду, и самих электродов. С другой стороны, некоторые подразумевают, что реакция проводится при более высоких температурах, уменьшая потребление электроэнергии, а другие используют огромные давления для поддержания H.2 хранится.
Среди всех методов можно упомянуть следующие три:
Электролиз щелочной водой
Электролиз проводят с основными растворами щелочных металлов (КОН или NaOH). С помощью этой техники происходят реакции:
Как видно, как на катоде, так и на аноде вода имеет основной pH; и кроме того, ОН — мигрировать на анод, где они окисляются до O2.
Электролиз с полимерной электролитической мембраной
В этой технике используется твердый полимер, который служит проницаемой мембраной для H + , но водонепроницаемый для газов. Это гарантирует большую безопасность при электролизе.
Полуклеточные реакции для этого случая:
Ионы Н + они мигрируют от анода к катоду, где они уменьшаются, чтобы стать H2.
Электролиз с твердыми оксидами
Очень отличающийся от других методов, он использует оксиды в качестве электролитов, которые при высоких температурах (600-900ºC) функционируют в качестве среды переноса анионов. 2- .
Обратите внимание, что на этот раз оксидные анионы, или 2- , те, кто путешествует на анод.
Какая польза от электролиза воды?
Электролиз воды дает H2 (г) и О2 (G). Приблизительно 5% газообразного водорода, производимого в мире, образуется в результате электролиза воды..
H2 это побочный продукт электролиза водных растворов NaCl. Присутствие соли облегчает электролиз за счет увеличения электропроводности воды.
Глобальная реакция, которая имеет место:
Чтобы понять огромную важность этой реакции, будут упомянуты некоторые виды использования газообразных продуктов; потому что, в конце концов, именно они стимулируют разработку новых методов для достижения электролиза воды более эффективным и экологичным способом..
Из всех них наиболее желательным является использование ячеек, которые энергетически заменяют использование сжигания ископаемого топлива..
Производство водорода и его использование
-Водород, получаемый при электролизе, может быть использован в химической промышленности, действующей в реакциях зависимости, в процессах гидрирования или в качестве восстановителя в процессах восстановления..
-Кроме того, это важно в некоторых действиях, имеющих коммерческое значение, таких как: производство соляной кислоты, перекиси водорода, гидроксиламинов и т. Д. Участвует в синтезе аммиака по каталитической реакции с азотом.
-В сочетании с кислородом он производит пламя с высокой калорийностью, с температурами в диапазоне от 3000 до 3500 К. Эти температуры могут использоваться для резки и сварных швов в металлургической промышленности, для роста синтетических кристаллов, производства кварца и т. Д..
-Обработка воды: слишком высокое содержание нитратов в воде может быть уменьшено путем их удаления в биореакторах, в которых бактерии используют водород в качестве источника энергии
-Водород вмешивается в синтез пластмасс, полиэстера и нейлона. Кроме того, он является частью производства стекла, увеличивая сгорание во время выпекания.
-Реагирует с оксидами и хлоридом многих металлов, в том числе серебра, меди, свинца, висмута и ртути с образованием чистых металлов.
-И, кроме того, он используется в качестве топлива в хроматографических анализах с детектором пламени..
Как метод отладки
Электролиз растворов хлорида натрия используется для очистки воды бассейна. Во время электролиза водород образуется в катоде и хлоре (Cl2) на аноде. Говорят об электролизе в этом случае как хлоратор соли.
Хлор растворяется в воде с образованием хлорноватистой кислоты и гипохлорита натрия. Хлорноватистую кислоту и гипохлорит натрия стерилизуют водой.
В качестве источника кислорода
Электролиз воды также используется для генерации кислорода на Международной космической станции, которая служит для поддержания кислородной атмосферы на станции..
Водород можно использовать в топливном элементе, способе накопления энергии и использовать воду, которая генерируется в элементе для потребления астронавтами..
Домашний эксперимент
Эксперименты по электролизу воды проводились на лабораторных весах с помощью вольтметров Хоффмана или другой сборки, которая позволяет вместить все необходимые элементы электрохимической ячейки..
Из всех возможных сборок и оборудования самым простым может быть большой прозрачный контейнер для воды, который будет служить ячейкой. Кроме того, вы должны иметь под рукой любую металлическую или электропроводящую поверхность, которая будет выполнять функцию электродов; один для катода, а другой для анода.
Для этой цели могут быть полезны даже карандаши с острыми точками на обоих концах. И, наконец, небольшой аккумулятор и несколько кабелей, которые соединяют его с импровизированными электродами..
Если не сделать в прозрачном контейнере, образование пузырьков газа не может быть оценено.
Домашние переменные
Хотя электролиз воды является предметом, который содержит много интригующих и обнадеживающих аспектов для тех, кто ищет альтернативные источники энергии, домашний эксперимент может быть скучным для детей и других зрителей..
Следовательно, достаточное напряжение может быть приложено для формирования H-образования2 и O2 чередуя определенные переменные и отмечая изменения.
Первый — это изменение pH воды с использованием уксуса для подкисления воды или Na.2Колорадо3 немного подвести Изменение количества наблюдаемых пузырьков должно произойти.
Кроме того, тот же эксперимент можно повторить с холодной и горячей водой. Таким образом, влияние температуры на реакцию будет затем рассматриваться.
Наконец, чтобы сделать сбор данных немного менее бесцветным, вы можете прибегнуть к очень разбавленному раствору сока фиолетовой капусты. Этот сок является основным кислотным индикатором природного происхождения..
Добавляя его в емкость с введенными электродами, можно заметить, что на аноде вода станет розовой (кислотной), а на катоде окраска будет желтой (основной).
Электролиз воды

Средняя оценка: 4.4
Всего получено оценок: 198.
Средняя оценка: 4.4
Всего получено оценок: 198.
Процесс электролиза – это окислительно-восстановительная реакция, возможная только под действием электричества. Электролиз протекает в расплавах и растворах. В лабораториях для получения чистых газов – водорода и кислорода – проводят электролиз воды.
Что такое электролиз
Для осуществления процесса электролиза в раствор или в расплав помещают два электрода, подключённых к противоположным полюсам источника тока. В качестве электродов чаще всего используется металл или графит, так как эти материалы пропускают электрический ток.

Под действием электричества электрод, подключенный к отрицательному полюсу, становится катодом, а электрод, соединённый с положительным полюсом, превращается в анод. Катод и анод притягивают противоположные ионы: к катоду направляются положительно заряженные катионы, к аноду – отрицательно заряженные анионы.
Катод является окислителем, на нём происходит процесс восстановления катионов. На аноде протекает процесс окисления: анод восстанавливает анионы и окисляется.
Процесс электролиза можно разделить на два этапа. Сначала происходит диссоциация – распад электролита (раствора или расплава) на ионы. Затем протекают реакции на электродах.
Электролиз воды
Если пропустить через воду электрический ток, жидкость начнёт диссоциироваться на составляющие молекулу воды атомы. В результате процесса электролиза воды получают кислород и водород. Однако в зависимости от природы электродов можно получить озон и перекись водорода.
Схема электролиза воды:
Вода – слабый электролит, поэтому электролиз чистой, дистиллированной воды протекает медленно или не идёт вовсе. Для ускорения процесса в воду добавляют сильный электролит, увеличивающий проводимость электрического тока.
Электролит выбирается так, чтобы исключить конкуренцию между катионами электролита и катионами воды (H + ). В противном случае водород не будет произведён. Чтобы исключить конкуренцию, необходимо подобрать электролит, катионы которого будут иметь меньший электродный потенциал, чем H + воды. На роль катиона электролита подходят:
Для исключения конкуренции анионов, наоборот, подбирают электролит с анионами большего электродного потенциала, чем анион OH – воды. В качестве такого электролита применяется щелочь для образования гидроксильного иона OH – .
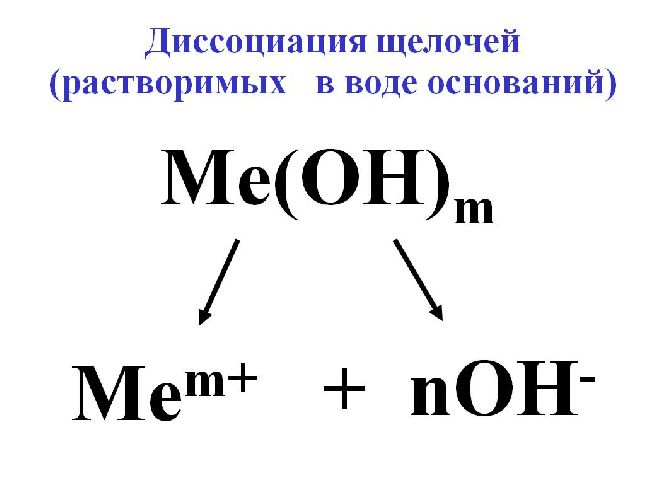
Для электролиза воды используются сильные щелочи: гидроксид калия (KOH) или натрия (NaOH). В некоторых случаях применяется сильная кислота, например, H2SO4.
Что мы узнали?
Электролиз – процесс образования и оседания на электродах ионов вещества под действием электрического тока. Вода разделяется на катионы водорода и анионы кислорода. Положительные катионы движутся к катоду, отрицательные анионы – к аноду. В некоторых случаях вода диссоциируется на озон и перекись водорода. Из-за низкой способности к диссоциации в воду добавляется сильный электролит, не мешающий образованию водорода и кислорода. Чаще всего добавляется щёлочь или сильная кислота.
НИЗКОАМПЕРНЫЙ ЭЛЕКТРОЛИЗ ВОДЫ
Аннотация: показана возможность реализации процесса электролиза воды, протекающего при фотосинтезе, в технических устройствах. При этом затраты энергии на разложение молекул воды на водород и кислород уменьшаются примерно в 2000 раз.
В последние годы растёт интерес к водородной энергетике. Объясняется это тем, что водород является неисчерпаемым и экологически чистым энергоносителем. Однако реализация этих качеств сдерживается большими затратами энергии на получение его из воды. Самые современные электролизёры расходуют 4,0 кВтч на кубический метр этого газа. Процесс электролиза идет при напряжении 1,6-2,0 Вольта и силе тока в десятки и сотни Ампер. При сжигании кубического метра водорода выделяется 3,55 кВтч энергии [1], [2].
Проблему уменьшения затрат энергии на получение водорода из воды решают многие лаборатории мира, но существенных результатов нет. Между тем в Природе существует экономный процесс разложения молекул воды на водород и кислород. Протекает он при фотосинтезе. При этом атомы водорода отделяются от молекул воды и используются в качестве соединительных звеньев при формировании органических молекул, а кислород уходит в атмосферу. Возникает вопрос: а нельзя ли смоделировать электролитический процесс разложения воды на водород и кислород, который идет при фотосинтезе?
Поиск ответа на поставленный выше вопрос привел к простой конструкции ячейки (рис. 1), в которой процесс идет при напряжении 1,5-2,0 Вольта (по показаниям вольтметра) между анодом и катодом, и силе тока 0,02 Ампера (по показаниям амперметра и осциллографа) [1], [2], [3], [4].
Рис. 1. Лабораторная модель низкоамперной ячейки электролизёра (в стадии патентования)
Электроды ячейки изготовлены из стали, что исключает явления, присущие гальваническому элементу. Тем не менее на электродах ячейки появляется разность потенциалов около 0,1В при полном отсутствии электролитического раствора в ней. После заливки раствора разность потенциалов увеличивается. При этом положительный знак заряда всегда появляется на верхнем электроде, а отрицательный – на нижнем. Если источник постоянного тока генерирует импульсы, то выход газов увеличивается.
Поскольку лабораторная модель ячейки низкоамперного электролизёра генерирует небольшое количество газов, то самым надёжным методом определения их количества
является метод определения изменения массы раствора за время опыта и последующего расчета выделившегося водорода и кислорода.
Известно, что грамм-атом численно равен атомной массе вещества, а грамм-молекула – молекулярной массе вещества. Например, грамм-молекула водорода в молекуле воды равна двум граммам, а грамм-атом атома кислорода – 16 граммам. Грамм-молекула воды равна 18 граммам. Так как масса водорода в молекуле воды составляет 2х100/18=11,11%, а масса кислорода – 16х100/18=88,89%, то это же соотношение водорода и кислорода содержится в одном литре воды. Это означает, что в 1000 граммах воды содержится 111,11 грамм водорода и 888,89 грамм кислорода.
Один литр водорода весит 0,09 гр., а один литр кислорода -1,47 гр. Это означает, что из одного литра воды можно получить 111,11/0,09=1234,44 литра водорода и 888,89/1,47=604,69 литра кислорода. Из этого следует, что один грамм воды содержит 1,23 литра водорода [1].
Затраты электроэнергии на получение 1000 литров водорода сейчас составляют 4 кВтч, а на один литр – 4 Втч. Поскольку из одного грамма воды можно получить 1,234 литра водорода, то на получение водорода из одного грамма воды сейчас расходуется 1,234х4=4,94 Втч. Результаты эксперимента представлены на рис. 2-11 и в таблице.
Инструменты и оборудование, использованные при эксперименте
Специальный экспериментальный низкоамперный электролизер (рис. 1); вольтметр класса точности 0,2 (ГОСТ 8711-78); амперметр класса точности 0,2 (ГОСТ 8711-60); электронные весы с ценой деления 0,1 и 0,01 грамма; секундомер с ценой деления 0,1с, электронный осциллограф АСК-2022. Осциллограф был настроен на режим работы с открытым входом.
Результаты эксперимента
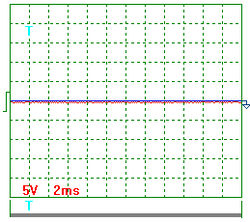
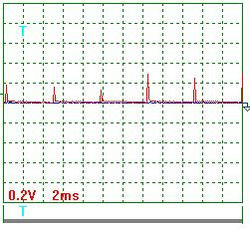
На рис. 2-11 показаны осциллограммы напряжения и тока на входе в электролизёр
Рис. 2. Напряжение
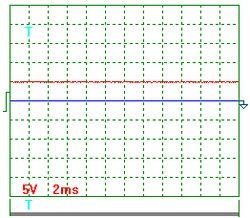
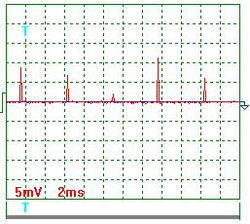
Рис. 3. Напряжение
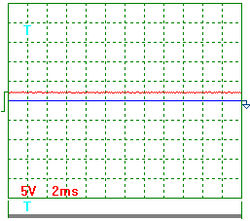
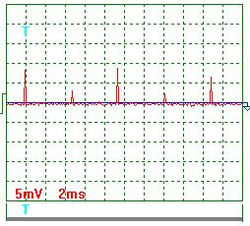
Рис. 4. Напряжение
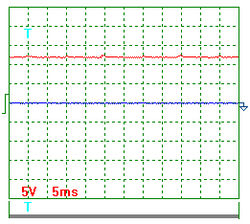
На рис. 2 показана осциллограмма напряжения при частоте импульсов около 200Гц. Масштаб записи один к одному. Импульсы не видны, так как их амплитуда ничтожно мала. Измерения показывают, что на осциллограмме зафиксировано напряжение около 11,5 Вольт. Вольтметр показывал в это время 11,4 Вольта.
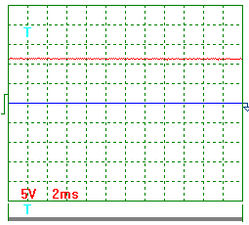
На рис. 3. показана осциллограмма напряжения на входе в электролизёр через 1 секунду после отключения его от сети. На рис. 4 показана осциллограмма напряжения на входе в электролизёр через 3 секунды после отключения его от сети. Осциллограммы на рис. 3 и 4 показывают, что после отключения электролизёра от сети идет процесс его разрядки. Отметим особо, что напряжение, постепенно уменьшаясь, не становится равным нулю. Это указывает на то, что электролизёр является не только конденсатором, но и источником энергии.
Рис. 5. Напряжение
Рис. 6. Напряжение
Рис. 7. Напряжение
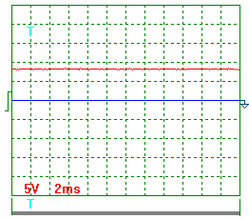
На рис. 5. осциллограмма напряжения на входе в электролизёр при замкнутых контактах (короткое замыкание). На рис. 6. осциллограмма напряжения на входе в электролизёр через 1 сек. после снятия короткого замыкания. На рис. 7. осциллограмма напряжения на входе в электролизёр через 3 минуты после снятия короткого замыкания.
Как видно, в начальный момент после отключения электролизёра от сети (рис. 3) у него остаётся потенциал близкий к потенциалу сети, который образовался при зарядке электролизёра в процессе включения его в сеть и настройки на заданный режим работы. Особо подчеркнём, что ток в процессе зарядки был в несколько раз больше его рабочей величины 0,02А.
Через 3 секунды после отключения сети (рис. 4) потенциал на входе в электролизёр уменьшается с 11,4 В до 8 В примерно.
В момент короткого замыкания контактов электролизёра (рис. 5) напряжение на его входе становится равным нулю. Через 1 сек. после снятия короткого замыкания (рис. 6), потенциал на входе в электролизёр восстанавливается до 5 В. Через 3 минуты он уменьшается до 2 Вольт. До нулевого значения потенциал на входе в электролизёр вообще не опускается.
На осциллограмме (рис. 2) не видны импульсы потому, что их амплитуда ничтожно мала. Если увеличить масштаб, то импульсы выглядят так (рис. 8 и 9).
Рис. 8. Напряжение
Рис. 9. Напряжение
Результаты обработки осциллограмм напряжения (рис. 8 и 9).
Учитывая масштабный коэффициент, равный 10, найдём среднее значение амплитуды импульсов напряжения
=[(0,20+0,24+0,12+0,10+0,30+0,18+0,16+0,12+0,30+ 0,24+0,30)/11] x10=2,05 В.
Период импульсов Т=(24х2)/10=4,8 мс.
Длительность импульсов =(2х1,45)/10=0,29мс.
Частота импульсов =(1/0,001×4,8)=208,3 Гц.
Скважность импульсов =4,8/0,29=16,55.
Коэффициент заполнения =0,5/16,55=0,0302
Эквивалентная средняя составляющая импульсов напряжения, рассчитанная по показаниям осциллографа =2,05х0,0302=0,062 В. Вольтметр в это время показывал 11,4 В.
Таким образом, есть основания полагать, что низкоамперный электролизёр обладает свойствами конденсатора и источника электричества одновременно. Зарядившись в начале, он постепенно разряжается под действием электролитических процессов, протекающих в нём. Количество генерируемой им электрической энергии оказывается недостаточным, чтобы поддерживать процесс электролиза, и он постепенно разряжается. Если его подзаряжать импульсами напряжения, компенсирующими расход энергии, то заряд электролизёра, как конденсатора, будет оставаться постоянным, а процесс электролиза -стабильным.
Величина потенциала необходимого для компенсации разрядки электролизёра зафиксирована на осциллограммах 8 и 9. Эту величину и надо использовать при расчете затрат энергии на получение водорода из воды при её низкоамперном электролизе.
Итак, по показаниям вольтметра и амперметра мощность источника питания лабораторной модели низкоамперного электролизёра составляет Однако, анализ осциллограмм показывает, что эта мощность необходима только для запуска электролизера в работу. После запуска, когда он зарядится, мощность для его подзарядки составляет , то есть в 190 раз меньше (табл. 1).
Наличие постоянной составляющей электрического потенциала на входе в электролизёр показывает, что для расчета затрат энергии на процесс электролиза надо использовать не показания вольтметра, а показания осциллографа, регистрирующие потенциал подзарядки электролизёра, следующий из осциллограмм, представленных на рис. 8 и 9.
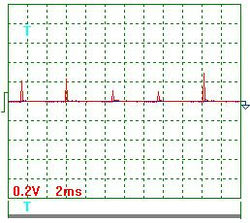
На рис. 10 и 11 показаны осциллограммы тока, когда источник питания электролизёра генерировал импульсы с частотой около 200Гц.
Результаты обработки осциллограмм тока (рис. 10 и 11).
Учитывая масштабный коэффициент, равный 10, и сопротивление резистора 0,1 Ом, найдём среднее значение амплитуды импульсов тока.
Средний ток в цепи питания электролизёра =0,655х0,0302=0,01978А=0,02А. Показания амперметра – 0,02А.
Показатели процесса низкоамперного электролиза воды
1 – продолжительность работы электролизера, включенного в сеть, в шести циклах t, мин
2 – показания вольтметра V, Вольт;
2’ – показания осциллографа V’, Вольт;
3 – показания амперметра I, Ампер;
3’ – показания осциллографа, I’, Ампер;
4 – расход энергии по вольтметру и амперметру (P=VxIx /60), Втч;
4’ – расход энергии по показаниям осциллографа (P’=V’xI’x /60) Втч;
5 – продолжительность работы электролизёра, отключенного от сети, за шесть циклов, мин
6 – изменение массы раствора m, грамм
7 – масса испарившейся воды m’, грамм
8 – масса воды, перешедшей в газы, m’’=m-m’, грамм
9 – расход энергии на грамм воды, перешедшей в газы, по показаниям вольтметра и амперметра E=P/m’’, Втч/грамм воды;
9’ – расход энергии на грамм воды, перешедшей в газы, по показаниям осциллографа E’=P’/m’’, Втч/грамм воды;
10 –существующий расход энергии на грамм воды, переходящей в газы E’’, Втч/гр. воды
11 – уменьшение расхода энергии на получение водорода из воды по показаниям вольтметра и амперметра K=E’’/P, раз;
11’ – уменьшение расхода энергии на получение водорода из воды по показаниям осциллографа K’=E’’/P’, раз;
12количество выделившегося водорода М=0,54×1,23×0,09=0,06, грамм
13 — энергосодержание полученного водорода (W=0,06х142/3,6) =2,36, Втч
14-энергетическая эффективность процесса электролиза воды по показаниям вольтметра и амперметра (Wх100/P), %;
14’ — энергетическая эффективность процесса электролиза воды по показаниям осциллографа (Wх100/P’), %;
Таким образом, вольтметр показывает величину напряжения заряженного электролизёра, как конденсатора, который постепенно разряжается, а импульсы напряжения, фиксируемые осциллографом – величину его подзарядки, которая и характеризует энергию, потребляемую электролизером из сети. Из этого следует, что для расчета расхода энергии, потребляемой низкоамперным электролизером из сети, надо использовать напряжение, регистрируемое не вольтметром, а осциллографом. В результате, затраты энергии на получение водорода из воды при низкоамперном электролизе уменьшаются не в 12 раз, а почти в 2000 раз.
Небольшая величина тока 0,02А и небольшая величина, соответствующего напряжения 0,062В, дают нам основание предполагать, что в низкоамперном электролизёре процесс электролиза воды аналогичен тому, который идет при фотосинтезе.
Соответствие процесса электролиза воды при низкоамперном электролизе процессу её электролиза, протекающему при фотосинтезе, подтверждается также интенсивным выходом пузырьков газов в течение нескольких часов после отключения электролизера от сети.
ЗАКЛЮЧЕНИЕ
Уменьшение затрат энергии на получение водорода из воды примерно в 2000 раз даёт веские основания полагать, что низкоамперный электролиз воды аналогичен её электролизу, протекающему при фотосинтезе.
ЛИТЕРАТУРА
1. Канарёв Ф.М. Начала физхимии микромира. Третье издание. Краснодар 2003. Kanarev.innoplaza.net (In Russian, Part 1, Part 2).
2. Kanarev Ph.M. The Foundation of Physchemistry of Micro World. The second edition.
(In English). Kanarev.innoplaza.net
3. Канарёв Ф.М. Низкоамперный электролиз воды. Kanarev.innoplaza.net Article 18.
4. Канарёв Ф.М. Водоэлектрические генераторы тепла. Kanarev.innoplaza.net
Ну и где это чудо? Кто из потомков отъявленного турецкого янычара, эдаких остапов — бендеров — кулибиных наладило подпольное изготовление и сбыт с целью быстрого и сказочного обогащения? На каком птичьем рынке вам, озираясь по сторонам в поисках агентов мировой нефтяной индустрии вам предложат из под полы запретное устройство? Или оно уже выпускается легально, невзирая на все физические законы? Тогда в каком магазине за ним выстроилась очередь? Судя по количеству одноимённых патентов данного автора на эту тему, он промышляет на ниве патентотворчества, но отнюдь не практического применения. Может потому, что знает истинную эффективность всей этой чудо — техники нетрадиционной ориентации»
Желаю искренно Профессору Канареву здоровья и научных успехов. Надо что бы у профессора было как можно больше учеников последователей. Информация должна уходить простым людям мелким Кулибиным. Что бы технологию нельзя было остановить.
С юрием несоглашусь, простота дело не всегда хорошее, а дак для таких технологий, не простота нужна а контроль, так как простота в наше время влечёт за собой большие беды. Напри мер, простодушее и доверчивость, дадут как раз распростронение сея технологий далеко не простым, а наоборот бездушным поедателям энергии которые для общего дела шевельнуться нежелают вообще. А потом бум и на земле вечная мерзлота, что то вдруг настала. Этот вопрос особого характера, который должен служить на благо, а не на зло. А это пример, что на первый взгляд показалось комуто, при детальном разложении данного вопроса, «простым людям», как раз таки доверять не льзя. Несущий свет, не всегда может быть светлым, иначе свет разгораеться так ярко что, радиоактивность повышаеться.
Люди слышать должны друг друга, независимо от света их душ, чтоб гармония в этом была, должны политики этим заниматься, в наше время.
Мейер, Конарёв и . на ютубе, все секретнариане для делания денег для себя. Агенты.
Если при сжигании полученного водорода выделяется 3, 55 кВтч энергии на куб, то по закону сохранения энергии никак нельзя затратить на процесс обратный сжиганию ни в 12 раз ни тем более в 2000 раз энергии меньше чем 4кВтч на упомянутых самых современных электролизерах. Иначе можно создать вечный двигатель, который будет разлагать воду и сжигать ее по кругу.
Я тоже ищу методы разложения воды на водород и кислород не дорогим способом ,но чем больше ищу инфу тем более разочаровываюсь в этом так как проект заряд публикует лживую информацию на своем сайте , например метод смешивание структурированной воды с добавлением салярки
С обычной водой — это чистая лапша на уши , его разоблачение было показано в передача где он «обосрался » пытаясь продемонстрировать свое «ноу х. » но был разоблочен физиком присутсвующим в качестве жюри на передаче. Все это ставит под сомнениевсе что публикуют те кто пытается выдать желаемое за действительное, якобы они имеют такие тенологии . Только не понятно зачем тратить свое время на снятие видео потом выкладывать его в интернет заведомо зная его неэфективность под видом эдокого борца за распространение свободной и доступной энергии . Все это подрывает всяческое доверие к авторам этих статей ,хотя кто знает ,может в этом тоже есть чьито интересы? Но с другой стороны на сегодня нет ни одного сверх единичного устройства вырабатывающего дешовую энергию кроме подделок в нете в виде киношек и роликов снятыми «самоделкиными недоучками» . Срамота и позор всем кто это делает !
работает ли именно этот вариант я не знаю, но ребята пора уже продвигаться вперёд и отступить от нынешнего положения дел. мыслите шире господа: всё возможно, верьте в чудеса. ибо когдато считали что земля на черепахах стоит, а позже что атом самый маленький. и тд и тп
Экспериментируйте . повторюсь всё возможно☺
Вода — уникальное природное , экологически чистое , энергетически эффективное , возобновляемое топливо. Воде содержится водород . кислород и немного (0, 15%) дейтерия.
Это значит — мы можем получать синтетическое топливо из воды на соединении (синтезе) из таких же высокомолекулярных полимеров , как сама вода, на основе кремнийорганических полимеров , заменяя углерод на кремний , тем более таблица Менделеева это позволяет. Результаты просто ошеломляющие!
Но , друзья мои , любая вода , тем более водопроводная , для этого не подходит , нужна вода модифицированная по нескольким параметрам рН и ОВП , насыщенная растворенными нейтральными и активными газами , неорганическими солями и кислотами.
Так как воде содержится немного дейтерия , на воде можно с помощью катализаторов получать низкоэнергетический холодный ядерный синтез , но этого вполне достаточно для отопления и обеспечения автономной электроэнергией жилого дома площадью до 1000 м2.
Не унывайте друзья , прогресс научно-технологический идет , хотим мы этого или нет , с нами или без нас. Матушку Землю спасите от загрязнения !
Может быть, двигатель внутреннего сгорания это ошибочная версия нашей цивилизации? Был другой путь, без использования углеводородов, пластиков и прочей ядовитой массы. Где человечество свернуло на гибельную для себя дорожку, отравляя все вокруг.? И нельзя ли создать безопасную систему получения энергии в связке вода-ветер-солнце? Может, я рассуждаю, как дилетант, Но я не химик, не физик,
См. Таблицу и сразу находим ошибку:
4 – расход энергии по вольтметру и амперметру (P=VxIx /60), Втч = 0, 228
Остальное, соответственно, неверное.
очень интересуюсь вашими исследованиями
Прежде чем строить подобные чудо-машины прочитайте, хотя бы, «Занимательную Физику» Перельмана. В данном опыте все основано на подсчете уменьшения массы. Как было организован контроль улетучивания паров посредством обычной тепловой конвекции?
Был у меня в практике такой случай. Проводили мы одни высокоточные измерения. По всем расчетам КПД системы был больше единицы. Не на много, но больше. Стали искать приток энергии извне. Выяснили, что активное (включенное в розетку) контрольно измерительное оборудование вносило свою лепту.
Очередные «опыты с тараканами». почему — написали уже выше. Автор не шарит ни в биологии (полагая, что фотосинтез — это электролиз воды), ни в физике (полагая, что на разложение воды можно потратить меньше энергии, чем получить потом при сжигании водорода), ни в химии (учитывая изотопный состав, масса водорода не 11.11%), ни даже в арифметике начальных классов школы (111.11/0.09 не равно 1234.44). Ну и до кучи скромно умалчивает, что патент — это подтверждение не работоспособности установки или ее пригодности для заявленной цели, а лишь новизны. И то лишь в том смысле, что до него никто подобную совершенно бесполезную хрень патентовать не догадался.
Это то же , что и ячейки Меера -американца. Он и патент получил . Его ячейки проверяли ( работали автономно — без автора) 3 года — только после этого ему дали патент . Есть и подробное описание и способы применения в быту и автопроме. Изучайте , дерзайте .
Привет интернет ученные все изобретаете?
О сколько нам пткрытий чудных готовит просвищенья дух, и разум- сын ошибок трудных, и гений, парадоксов друг!
Вот как-то так)). Говорят ,гениальное все просто.
Заостряйте внимание перед сном, и вам может присниться решение проблеммы (как когда то, приснилась таблица Менделееву).
дармовой двигатель полезной энергии изобретён давно, это рычаг на одном конце которого пружина. После нажатия на другой конец рычага, пружина возвращает рычаг в исходное состояние без подвода энергии. Вот двигатель дармовой энергии. Надо подумать про цикличность этой установки.
Никто не говорит о вечных двигателях, но вспомните формулу Е=mc2. Речь о максимальной эффективности получения энергии. Сколько нужно затратить энергии, чтобы получить ядерный взрыв? И сколько энергии выделится при этом? Понимаете?
Друзья, не надо лишних эмоций! Водород, в газообразном состоянии-это Атомный вид топлива с актановым число 1000. Атомы водорода очень (мелкие )и способны проникать сквозь многие материалы! По этому опыты не всегда правдивы. При сгорании водорода(гремучая смесь) теплоемкость превышает в несколько раз теплоемкость пропана! Советую обьединиться и совмесными усилиями выгодно разложить атомы водорода и кислорода! Уже год я наблюдаю за этим (водородным) движением и к лету решил сам сделать электролизер! Не равнодушные ,пишите свои пожелания и открытия на номер 87772364860 можно ватсап.
Привет всем болельщикам ВОДОРОДА! Пол года интересуюсь этой темой. Понял что водород имеет актановое число в 10 раз больше бензина 1000! По теплоемкости ,в разы больше Пропана. Осталось правильно настроить! Летом попробую сделать)).
Итак,друзья,много чего тут сказано,написано и слова умные и про вечный двигатель и тд тп, но. такое есть ощущение что вы в школе физику прогуливали, извините за такую пикантную подробность!Есть такая интересная штука(я уж буду по простецки говорить),называется ЗАКОН СОХРАНЕНИЯ ЭНЕРГИИ,а гласит он следующее(опять же своими словами)-нельзя получить КПД процесса больше чем затрачено совокупной энергии на сам процесс,МЕНЬШЕ МОЖНО,БОЛЬШЕ НЕЛЬЗЯ. Т.Е. Нельзя от батарейки ААА запитать допустим. сварочный аппарат это же в жизни никому в голову не приходит. Но тут эта тема живёт и процветает!То что сдесь описано есть «патентованая» хрень гн-а Мейера и называется «топливная ячейка Мейера», красиво всё у него там описано но никто повторить его «подвиг» не может!А «подвиг» заключался в следующем, товарищ Мейер,взяв обычный,вобщем электролизёр и подведя к нему ток 12v 0.2 a (подавая ток импульсно)заявил что на выделяемом количестве газа может ездить автомобиль!Фактически он(Мейер) запитал автомобиль мощьностю 2-3квт(условно) напряжением 12 v 0.2 a и очень обижался когда его поднимали насмех?! Фактически гн. Мейер не генератор водорода изобрёл а обманул закон природы и не просто помелочи а КИНУЛ ПРИРОДУ ПОКРУПНЯКУ!!Это же нобилевка по физике(раз) и просто источник дармовой энергии который можно сравнить с изобретением ядерной реакции(только ещё круче)И вся эта тема с водородными генераторами любого толка ПРОТИВОРЕЧИТ ЗАКОНУ СОХРАНЕНИЯ ЭНЕРГИИ. Эти генераторы не только машину не потянут но и экономии не создадут т.к. Вы запитываете или подпитываете ввтомобиль лишь силой тока вашего аккомулятора который вырабатывается вашим генератором,для работы которого вы должны сжечь топлива больше чем получите выход газа. О какой экономии может идти речь. Проблема вечного двигателя в том и заключается что кпд процесса всегда ниже чем нужно энергии для самого процесса!А ТО ЧТО ТУТ ОПИСАНО ЭТО И ЕСТЬ ВЕЧНЫЙ ДВИГАТЕЛЬ. Удачи)))
А тот гусь который свой номер выложил предложил «объединиться и совместными усилиями выгодно разложить атомы кислорода и водорода»🤣🤣🤣-просил «писать свои пожелания» вобще «улыбает» до бесконечности! Пожелание к нему только одно — ПРОЧИТАЙ ШКОЛЬНЫЙ УЧЕБНИК ФИЗИКИ ЗА ПОСЛЕДНИЙ КЛАСС. МНОГО ДЕНЕГ СЭКОНОМИШЬ ДА И ВРЕМНИ ТОЖЕ!!)))
Многие, кто пишут про закон сохранения энергии несомненно правы. Но случается, что иногда мы не замечаем каких-то свойств вещества. И вполне возможно, что повторный цикл с отработанной водой невозможен и в таком случае это не вечный двигатель. Заряд воды, тяжёлая ли это вода, а возможно, ещё какая-нибудь фишка влияют на электролиз. Когда кто-то говорит о воровстве патента — это глупо, ведь человек не способен к творчеству он опирается на прошлый опыт, сопоставляет знания и получает, что-то новое.
Ребята АВТОР не нарушает ни чего и Меер (маер) гений т.к. использует частотные свойства воды.
Ребятки, который пишут про ТО (по энштейну) и пр. вы в курсе что Земля-то КРУГЛАЯ?, но раньше было плоская, а телегу лошадь дергала, а сейчас наоборот телега дергает лошадь🙂👽
Всем доброго времени суток! ТО ,что я прочитал в этой статье — очень интересно и дает многим умам пищу, как сделать этот мир лучше! Скептис, который источают товарищи — знатоки фундаментальной физики просто наводит улыбку на лице! Мне понятен закон СОХРАНЕНИЯ ЭНЕРГИИ и многое то, что мне преподавали в университете 15 лет назад на факультете Инженерной Физики. Но. Меня всегда поражал гений Николы Тесла, Циолковского и т.д. И сейчас в наше время мы пользуемся результатами их открытий порой до конца не понимая, что такое электричество, радиоволны и т.д. Человеку 15-го столетия оставалось только мечтать о полете к звездам и возможности передавать информацию за тысячи километров за секунды. Фантасты — огромные мечтатели, их мечты зачастую реализовываются в будущем. Так вот, как вы себе представляете теорию о карпускулярно-волновом дуализме!? Чтобы рассматривать вещество одновременно волной? Мне это кажется бредом, но это общепринятый закон! Как фотон может тогда существовать и что это такое!? Ведь в теории ни одна материальная частица не может иметь скорость света, иначе бабах и произойдет взрыв, который породит новую галактику! А медики, которые невольно стали заложниками фармацевтии, а конкретно кардиологи. Эти товарищи забыли кто такой Ланг, хотя они не забыли, они его просто не знают! Мои знакомые кардиологи просто работают по принципу — как научили так и делаем. А я физик, и эксперимент это инструмент подтверждения или опровержения теоретической базы. И вместо того, чтобы прикрываясь законом о сохранении, хаять, то что здесь изложено, проявить интерес к этому результату, как поиск не сверх единицы, а новому свойству материала. Ведь атомный взрыв никто не отменял! А откуда тогда такое огромное количество энергии? Хотя, огромное вам спасибо, товарищи скептики — агенты нефтяных монополий, благодаря вам пытливые умы рождают новые технологии и делают этот мир лучше. Так что выбрасывайте ваши чайники, микроволновые плиты и сотовые телефоны! Разводите костры, и разводите голубей для почты! А мы поддержим эти результаты в своих трудах, чтобы через несколько лет, ваши дома отапливались дешовой энергией! Спасибо за внимание, накипело!
Уважаемый Игорь. Все открытия и изобретения о которых вы пишите, включая ядерные реакции, не противоречат закону сохранения энергии. А вот в результатах опытов которые здесь проводят те которые даже и измерять не умеют можно усомниться. Ну и банальный вопрос: кто или что мешает Вам и другим Вашим коллегам изготовить действующую модель подобного изобретения кроме этого закона? нефтяные магнаты? Так они наверное и секунды своего времени не потратят на бесполезное общения с Вами. У них работают грамотные специалисты, а не малообразованные несущие чушь.
Многие, кто пишут про закон сохранения энергии несомненно правы. только забывают о чем говорится в «законе»-Зако́н сохране́ния эне́ргии — фундаментальный закон природы, установленный эмпирически и заключающийся в том, что для изолированной физической системы, изолированной, Карл!,изолированной!