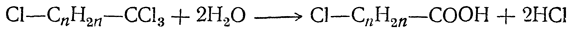Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Хлоруксусная кислота: получение и химические свойстваХлоруксусная кислота представляет собой уксусную кислоту, в которой один из атомов водорода, находящийся в метильной группе, замещен на свободный атом хлора. Ее получают в результате взаимодействия уксусной кислоты с хлором. Основным сырьем для получения является уксусная кислота. Хлоруксусная кислота также может быть получена при гидролизе трихлорэтилена. В результате гидролиза получают химически чистый продукт. Однако данный метод подразумевает использование чистой дистиллированной воды без каких-либо примесей. Хлоруксусная кислота применяется для получения различного рода красителей, лекарственных препаратов, витаминов и всевозможных пестицидов. Ее также используют в качестве поверхностно-активного вещества (ПАВ). При хлорировании уксусной кислоты в среде неорганических катализаторов (а именно уксусного ангидрида, серы и фосфора) получается хлоруксусная кислота, формула которой CH2Cl-COOH: Хлоруксусная кислота представляет собой гигроскопические, прозрачные кристаллы с температурой плавления 61,2°С и температурой кипения 189,5°С. Вещество легкорастворимое (как в спирту, так и в водной среде, а также в ацетоне, бензоле и четыреххлористом углероде). Монохлоруксусная кислота – ядовитое и чрезвычайно опасное вещество, при проглатывании которого довольно часто наблюдается летальный исход. При попадании на кожные покровы хлоруксусная кислота вызывает сильнейшие ожоги, которые длительное время не заживают. При вдыхании паров кислоты могут наблюдаться воспалительные изменения в легких, а также в верхних и нижних дыхательных путях. Рабочие производственных цехов по производству монохлоруксусной кислоты страдают нарушением обоняния, хроническими ринофарингитами, шелушением и сухостью кожи. Также при длительном взаимодействии с агрессивным веществом наблюдаются поражения эпидермиса кожи, выраженные дерматитами в области лица, шеи, верхних и нижних конечностей, в редких случаях — туловища. Хлоруксусная кислота в человеческом организме превращается в тиодиуксусную кислоту, которая выводиться из организма с калом и мочой. Основные методы предосторожности при эксплуатации: — категорически запрещается вдыхать пары, газ, дым и пыль; — обязательно использовать средства индивидуальной защиты при выполнении работ, связанных с любым контактом с кислотой (непроницаемый комбинезон, защитные очки, резиновые сапоги и перчатки); — в случае вдыхании паров или попадании кислоты на кожу следует незамедлительно обратиться за квалифицированной помощью в ближайшее медицинское учреждение. Предельно допустимая и теоретически безопасная концентрация хлоруксусной кислоты в воздухе производственного помещения составляет около одного мг/м 3 . При транспортировке кислоты ее упаковывают в полимерную тару (контейнера или бочки), картонные барабаны, а также стальные емкости. Допускается транспортировка любым видом крытого транспорта. Следует помнить, что монохлоруксусная кислота пожаро- и взрывоопасна. Это вещество легко воспламеняется. Хлоруксусные кислотыВо втором случае при избытке воды сразу получается кислота. Монохлоруксусная кислота образует расплывающиеся на воздухе кристаллы с т. пл. 61,5° С и т. кип. 189° С (существует также неустойчивая полиморфная разность с т. пл. 56,3°С). Эта кислота вырабатывается в больших количествах и используется в различных отраслях химической промышленности, в том числе для получения важного поверхностно-активного вещества — карбоксиметилцеллюлозы, в синтезе гербицидов — производных феноксиуксусной кислоты, широко применяемых для химической прополки зерновых и некоторых технических культур, а также как промежуточный продукт при синтезе индиго. Трихлоруксусная кислота ССl3—СООН получается окислением хлораля азотной кислотой. Это — гигроскопические кристаллы с т. пл. 52° С и т. кип. 197° С. Она находит применение в медицине как средство для прижигания; ее соли — ценные гербициды для овощных культур. β-Хлорпропионовая кислота СН2Сl—СН2—СООН — кристаллы с т. пл. 41° С. Она перегоняется при 204° С, частично отщепляя хлористый водород и превращаясь в акриловую кислоту. β-Хлорпропионовая кислота получается присоединением хлористого водорода к акролеину с последующим окислением азотной кислотой. Интересный новый путь получения некоторых галоидзамещенных кислот представляет реакция теломеризации, приводящая к образованию тетрахлорпроизводных типа ССl3—СnН2n—СН2Сl. Омылением таких тетрахлорпроизводных получаются галоидзамещенные кислоты: Из этилена этим путем могут быть получены β-хлорпропионовая, δ-хлорвалериановая и другие подобные кислоты. β-Иодпропионовая кислота CH2J—СН2—СООН — кристаллы с т. пл. 82° С — и ее этиловый эфир находят некоторое применение для синтезов. Получить ее можно присоединением иодистого водорода к акриловой кислоте. Однако обычно ее готовят, действуя иодом и фосфором на водные растворы глицериновой кислоты СН2ОН—СНОН—СООН; при действии образующейся иодистоводородной кислоты один гидроксил глицериновой кислоты замещается на иод, а другой восстанавливается. |