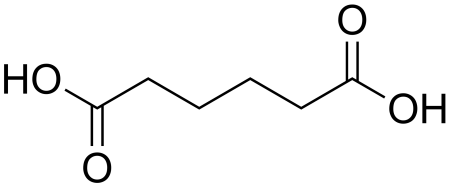
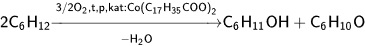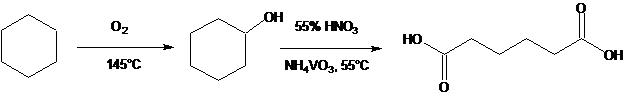| Адипиновая кислота | |
|---|---|
 | |
| Систематическое наименование | гександиовая кислота |
| Традиционные названия | адипиновая кислота, 1,4-бутандикарбоновая кислота |
| Хим. формула | C₆H₁₀O₄ |
| Рац. формула | HO2C(CH2)4CO2H |
| Состояние | кристаллическое |
| Молярная масса | 146,14 г/моль |
| Плотность | 1,36 г/см³ |
| Динамическая вязкость | 4,54 МПа·с (160 °C) |
| Т. плав. | 153 °C |
| Т. кип. | 265 (при 100 мм рт. ст.) °C |
| Т. разл. | 210-240 °C |
| Энтальпия сгорания | −2800 кДж/моль |
| Энтальпия плавления | 16,7 кДж/моль |
| Энтальпия кипения | |
| pKa | K1 3,7⋅10 −5 ; K2 0,53⋅10 −5 |
| Растворимость в воде | 1,44 г/100 г (15 °C); 5,12 г/100 г (40 °C); 34,1 г/100 г (70 °C) |
| Дипольный момент | 13,47⋅10 −30 Кл·м |
| ГОСТ | ГОСТ 10558-80 |
| Рег. номер CAS | 124-04-9 |
| PubChem | 196 |
| Рег. номер EINECS | 204-673-3 |
| SMILES | |
| Кодекс Алиментариус | E355 |
| RTECS | AU8400000 |
| ChEBI | 30832 |
| ChemSpider | 191 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Адипиновая кислота (гександиовая кислота) HOOC(CH2)4COOH — двухосновная предельная карбоновая кислота. Обладает всеми химическими свойствами, характерными для карбоновых кислот.
Образует соли, большинство из которых растворимо в воде.
Легко этерифицируется в моно- и диэфиры. С гликолями образует полиэфиры. Соли адипиновой кислоты — адипинаты. При взаимодействии с NH3 и аминами даёт аммонийные соли, при дегидратации превращающиеся в адипамиды. С диаминами образует полиамиды, с NH3 в присутствии катализатора при 500—600 °C — адиподинитрил.
Содержание
- 1 Получение
- 1.1 Промышленное получение
- 1.2 Лабораторные методики синтеза
- 1.3 Другие возможные способы получения
- 2 Свойства
- 3 Применение
- 4 Мировое производство
Получение
Промышленное получение
В промышленности адипиновую кислоту получают главным образом двухстадийным окислением циклогексана. На первой стадии (жидкофазное окисление воздухом при 142—145 °C и 0,7 МПа) получают смесь циклогексанона и циклогексанола:
которая разделяется ректификацией. Циклогексанон используют для производства капролактама. Циклогексанол окисляют 40—60%-ной HNO3 при 55 °C (катализатор — NH4VO3); выход адипиновой кислоты при этом способе производства составляет
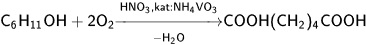
Перспективным способом производства адипиновой кислоты является гидрокарбонилирование бутадиена.
Лабораторные методики синтеза
Адипиновую кислоту с неплохим выходом можно получить, окисляя циклогексанол или циклогексанон оксидом хрома (VI), дихроматом калия или дихроматом натрия в присутствии серной кислоты:
Дихромат калия использовать неудобно из-за его малой растворимости — в растворе окислителя много воды, в которой адипиновая кислота растворяется.
Органическое вещество следует приливать к окислителю по каплям, поскольку при этой реакции выделяется много тепла.
Другие возможные способы получения
Адипиновую кислоту можно получить также следующими способами:
- Окислением циклогексана 50-70%-ной HNO3 при 100—200 °C и 0,2-1,96 МПа или N2O4 при 50 °C:
- Окислением циклогексанона озоном или HNO3:
- Карбонилированием ТГФ в ангидрид адипиновой кислоты, из которого действием H2O получают кислоту:
Свойства
Декарбоксилируется при 300—320 °C. Энтальпия сгорания (ΔH 0 сгор) −2800 кДж/моль.
Применение
Адипиновая кислота — сырьё в производстве полигексаметиленадипинамида (
90 % всей производимой кислоты), её эфиров, полиуретанов; пищевая добавка E355 для придания кислого вкуса пищевым продуктам (в частности, в производстве безалкогольных напитков). Является основным компонентом различных средств для химического удаления накипи.
Используется также для удаления остаточного клеящего материала после заполнения швов между керамическими облицовочными плитками.
Мировое производство
Мировое производство адипиновой кислоты — свыше 2,6 млн т/год (по состоянию на 2012 год).
Химия и технология органических веществ
| Исполнитель: | |||
| студент группы | З-2Д21 | Ковтун Е.Д. Шароглазов А. Мирзалиева А.А. | 06.06.2016 |
| Руководитель: | |||
| преподаватель | Волгина Татьяна Николаевна |
1. Изучить теоретические основы процессов получения адипиновой кислоты.
2. Получить адипиновую кислоту окислением циклогексанола.
3. Оценить факторы, влияющие на выход и чистоту адипиновую кислоты.
1. Теоретическая часть
1.1. Методы получения продукта
1.2. Области применения продукта
1.3. Физико-химические свойства исходных реагентов
2. Экспериментальная часть
2.1. Схема установки
2.3. Физико-химические методы анализа
3. Результаты и их обсуждение
3.1. Химия процесса
3.2. Экспериментальные данные
3.3. Материальный баланс
3.4. Блок-схема процесса
Адипиновая кислота HOOC(CH2)4COOH –важнейшая в техническом отношении насыщенная дикарбоновая кислота. Белый кристаллический порошок. Она вырабатывается в крупных заводских масштабах и применяется в производстве полиамидных, полиэфирных и полиуретановых смол, для синтеза пластификаторов и ряда других продуктов.
Растворима в этаноле; в эфире и воде- ограниченно. Адипиновая кислота обладает всеми химическими свойствами, характерными для карбоновых кислот. Образует соли, большинство из которых растворимы в воде. Легко этерифицируется в моно- и диэфиры. С гликолями образует полиэфиры. Соли и эфиры адипиновой кислоты называют адипинатами. При взаимодействии с NH3 и аминами адипиновая кислота дает аммонийные соли, которые при дегидратации превращаются в адипамиды. С диаминами адипиновая кислота образует полиамиды, с NH3 в присутствии катализатора при 300-400 °С — адиподинитрил.
1. ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
1.1. МЕТОДЫ ПОЛУЧЕНИЯ ПРОДУКТА
Наиболее экономичными из всех существующих методов производства адипиновой кислоты являются окислительные методы, так как в их основе лежит использование более дешевого сырья. Исходным сырьем выступает циклогексанон, циклогексанол, их смесь или циклогексан:
· Синтез адипиновой кислоты окислением циклогексанона или циклогексанола.
Наибольшее применение нашел метод окисления циклогексанона или циклогексанола 50-60% -ной азотной кислотой, что позволяет получить адипиновую кислоту с наибольшим выходом. Реакция протекает при 60-80 0 С, а на заключительном этапе температуру повышают до 105 0 С под давлением 0,2-1,0 МПа в присутствии медно-ванадатного катализатора:
Циклогексанон Адипиновая кислота
Циклогексанол Адипиновая кислота
· Синтез адипиновой кислоты окислением циклогексана.
Процесс можно проводить в одну или две стадии. Двухстадийный процесс оказался наиболее целесообразным. На первой стадии происходит жидкофазное окисление циклогексана воздухом в присутствии катализаторов при 120-160 0 С, образуется смесь циклогексанона и циклогексанола с выходом 60-80%. После отделения не превращённого циклогексана полученную смесь либо разделяют на чистые компоненты, либо подвергают доокислению воздухом в уксусной кислоте или 50-60% -ной азотной кислотой.
Так же существуют способы получения адипиновой кислоты из других исходных реагентов:
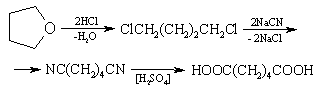
· Синтез адипиновой кислоты из бутадиена-1,3 через адиподинтрил.
Процесс, осуществляемый в США, в крупном промышленном масштабе состоит в хлорировании бутадиена, замещении хлора на циангруппу, гидрировании С=С- связи и гидролизе полученного адиподинитрила:
· Синтез адипиновой кислоты электрохимической гидромеризацией акрилонитрила.
Электрохимическая гидромеризация акрилонитрила с образованием адипонитрила, который при гидролизе дет адипиновую кислоту:
· Синтез адипиновой кислоты из фурфурола.
Декарбонилирование фурфурола, гидрирование полученного при этом фурана и взаимодействие полученного тетрагидрофурана с оксидом углерода и водой
· Синтез адипиновой кислоты из ацетилена.
Процесс состоит в конденсации ацетилена с формальдегидом, при этом образуется бутиндиол-1,4, который гидрируется до бутандиола-1,4. Дегидратацией последнего получают тетрагидрофуран, который при взаимодействии с оксидом углерода и водой образует адипиновую кислоту
1.2. ОБЛАСТИ ПРИМЕНЕНИЯ ПРОДУКТА
Адипиновая кислота — сырье в производстве полигексаметиленадипинмида (
90% производимой кислоты), её эфиров, полиуретанов; пищевая добавка (придает кислый вкус, в частности, в производстве безалкогольных напитков).
Увеличивается использование адипиновой кислоты в производстве полиуретанов. Сейчас темпы роста производства и потребления полиуретанов превышают темпы роста производства и потребления полиамидов, особенно полиамидных волокон. К примеру, спрос на адипиновую кислоту со стороны западноевропейских продуцентов полиуретана постоянно повышается, и сегодня темпы его роста составляют примерно 12-15 % в год. Тем не менее, спрос на полиамид (нейлон) для производства пластмасс тоже возрастает, особенно в азиатском регионе. Объясняется это тем, что для производства полиуретанов в странах АТР чаще используют простые полиэфиры, в синтезе которых не принимает участия адипиновая кислота, поэтому до 85 % адипиновой кислоты здесь используется в производстве полиамидов. Эта особенность оказывает волновой эффект на спрос адипиновой кислоты в регионе, поэтому среднегодовые темпы прироста мирового спроса на этот продукт прогнозируются на уровне 3-3,5%. В России собственное производство адипиновой кислоты пока отсутствует, хотя имеются весьма благоприятные для этого условия: развита сырьевая база (циклогексанол, циклогексанон, азотная кислота), имеются крупные потребители конечной продукции (пластификаторов, мономеров). Перспективная потребность в адипиновой кислоте для России оценивается величиной в несколько десятков тысяч тонн в год. В Российской Федерации адипиновая кислота используется для производства пластификаторов, полиамидов, фармацевтических препаратов, полиуретанов.
Адипиновая кислота как пищевой подкислитель уступает лимонной и фумаровой кислотам и имеет ограниченное применение. Она, например, конкурирует с лимонной кислотой в производстве желатиновых десертов, джемов и желе. В этих продуктах способность адипиновой кислоты усиливать желеобразование позволяет снизить расход желатина и др. белковых ингредиентов. На десерты желатинового типа, выпускаемые в США фирмой «General Foods Corp.» расходуется основная часть пищевой адипиновой кислоты в стране. Некоторое её количество используется в сыроварении и производстве сухих основ напитков. Потребление адипиновой кислоты в пищевой промышленности за последние два десятилетия не изменилось, оставаясь на уровне 1-3 тыс. т. в год. Адипиновую кислоту пищевого сорта производят в США фирмы nDu Pont» и nMonsanto»
Применение адипиновой кислоты в пищевой промышленности стран Западной Европы не разрешено законодательством.
1.3. ФИЗИКО-ХИМИЧЕСКИЕСВОЙСТВА ИСХОДНЫХ РЕАГЕНТОВ
Молярная масса= 100,16 г/моль; маслянистая бесцветная жидкость; в чистом виде — гигроскопические кристаллы с запахом камфоры и сивушного масла; tпл =25,1 °С; tкип= 161,1 °С; ΔH пл 0 =1,783 кДж/моль; ΔHисп 0 = 60,2 кДж/моль (25-450 °С); ΔHвозгонки =60,8 кДж/моль (0-25 °С); ΔH сгор 0 =-3517 кДж/моль; ΔH образ 0 -294,5 кДж/моль; теплопроводность =0,136 Вт (м x град) (20 °С). Растворимость циклогексанола в воде 4,3% по массе, воды в циклогексаноле 12,6%, неограниченно смешивается с СО2 при 21-26 °С и 6,4 МПа, растворим в большинстве органических растворителей.
Циклогексанол образует азеотропные смеси: вода (97,9; 21), фенол (128,9; 11), фурфурол (156,4; 45),кумол (150,0; 28), о-ксилол (142,8; 13), м-ксилол (138,7; 5), п-ксилол (137,8; 30), анизол (152,4; 30), циклогексанон (119,6; 12 и 91; 17 при давлении соответственно 300 и 100 мм рт. ст.).
По химическим свойствам обладает всеми характерными свойствами вторичных спиртов. При окислении (напр., HNO3, KMnO4) превращается в адипиновую кислоту, циклогексанон и низшие моно- и дикарбоновые кислоты; при дегидрировании дает циклогексанон.
Азот в азотной кислоте четырёхвалентен, степень окисления +5. Азотная кислота — бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения +82,6 °C ( при нормальном атмосферном давлении) с частичным разложением. Азотная кислота смешивается с водой во всех соотношениях. Водные растворы HNO3 с массовой долей 0,95-0,98 называют «дымящей азотной кислотой», с массовой долей 0,6-0,7 — концентрированной азотной кислотой. С водой образует азеотропную смесь (массовая доля 68,4 %, d2 0 = 1,41 г/см, tкип = 120,7 °C)
При кристаллизации из водных растворов азотная кислота образует кристаллогидраты:
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
2.1. СХЕМА УСТАНОВКИ
1 — Электроплитка; 2 – Баня; 3 – Круглодонная колба; 4 – Термометр; 5 – Капельная воронка; 6 – Мешалка.
В круглодонную трёхгорлую колбу, снабжённую механической мешалкой, обратным
холодильником, термометром и капельной воронкой, вливают 20мл 51,7%-ной
азотной кислоты, добавляют 0,01г ванадата аммония. Колбу помещают в водяную
баню и нагревают до 55°С и при энергичном перемешивании приливают из капельной
воронки несколько капель циклогексанола. Реакция начинается только после короткого (до 5 минут) периода индукции и сопровождается выделением бурых
оксидов азота. Температуру в колбе поддерживают 55-60°С путём охлаждения в бане
со льдом и приливают с соответствующей скоростью остальное количество циклогексанола (обычно в течение 1-1,5часа). К концу реакции после добавления почти всего количества циклогексанола охлаждение снимают и в случае необходимости слегка подогревают колбу на водяной бане для поддержания
температуры 55-60°С до окончания прибавления остатка циклогексанола. После
прибавления всего количества циклогексанола нагревание смеси при непрерывном
перемешивании продолжают на кипящей водяной бане до прекращения выделения
оксидов азота. Горячую жидкость переливают в стакан и оставляют в прохладном
месте кристаллизоваться. Выпавший кристаллический осадок адипиновой кислоты
отфильтровывают на воронке Шотта, промывают 10-12 мл очень холодной воды
и сушат на воздухе. Определяют массу и температуру плавления полученной
адипиновой кислоты и составляют материальный баланс. Полученные кристаллы
2.3. ФИЗИКО-ХИМИЧЕСКИЕ МЕТОДЫ АНАЛИЗА
3. РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1. ХИМИЯ ПРОЦЕССА
| C6H12O | HNO3 | C6H10O4 | N2O3 | H2O |
| Молярная масса М, г/моль | ||||
| Количество ν, моль | ||||
| Масса m, г |
Взято для опыта:
| Масса, г | Объем, мл | |
| C6H12O | 5,00 | 5,30 |
| HNO3 (ρ=0,94г/мл) | 26,20 | 19,90 |
| Ванадат аммония | 0,01 | — |
Теоретический выход адипиновой кислоты:
Справочное значение температуры плавления:
3.2. ЭКСПЕРИМЕНТАЛЬНЫЕ ДАННЫЕ
В ходе лабораторной работы было получено mпракт=3,34г адипиновой кислоты, температура плавления составила 153 0 С, что соответствует справочному значению.
3.3. МАТЕРИАЛЬНЫЙ БАЛАНС
Расчёт компонентов расхода:
| Приход | Расход | ||||
| Компонент | г | % | Компонент | г | % |
| C6H12O | 5,00 | C6H10O4 | 3,34 | ||
| HNO3 | 26,20 | N2O3 | 3,48 | ||
| H2O | 1,24 | ||||
| C6H12O(непрореаг) | 2,72 | ||||
| HNO3(непрореаг) | 20,44 | ||||
| ∑ | 31,20 | ∑ | 31,22 |
3.4. 

СИНТЕЗ АДИПИНОВОЙ КИСЛОТЫ И ЕЕ ДИЭТИЛОВОГО ЭФИРА
Адипиновая кислота относится к двухосновным предельным карбоновым кислотам алифатического ряда. Она является продуктом промышленного синтеза, но может также быть синтезирована в лаборатории. Поэтому ее можно использовать как доступный шестиуглеродный синтон в построении сложных молекул. С точки зрения стратегии синтеза адипиновая кислота является n-гексильным эквивалентом [1, с. 289]. Например, из нее можно получить 1,6-гександиол. В свою очередь α,ω-диолы широко примененяются в синтезе веществ биогенного происхождения, половых феромонов некоторых видов насекомых отряда L epidoptera [2, с. 1199]. На основе половых феромонов разрабатываются видоспецифичные средства защиты растений [3, с. 3].
В промышленности адипиновую кислоту обычно синтезируют двухстадийным окислением циклогексана (рис. 1).
Реакции промышленного синтеза адипиновой кислоты
На первой стадии окислением кислородом воздуха получают смесь циклогексанона и циклогесанола. Продукты разделяют ректификацией. Циклогексанон идет на синтез капролактама, а циклогексанол подвергают дальнейшему окислению азотной кислотой в присутствии катализатора, NH4VO3-ванадата аммония.
В лаборатории синтез начинают сразу из циклогексанола. В качестве окислителей также можно использовать оксид хрома (VI), дихромат калия или натрия в присутствии серной кислоты. Реакции идут по уравнениям, представленным на рис. 2.
Реакции лабораторного синтеза адипиновой кислоты
Хотя на выбор экспериментатора предоставлены различные окислители, метод с азотной кислотой является экономически и практически приемлемым для осуществления в лаборатории. Работу необходимо выполнять в хорошо действующем вытяжном шкафу, так как при реакции выделяются ядовитые окислы азота.
За основу синтеза была взята методика окисления циклогексанола азотной кислотой [4, c. 18]. Выполнение самого окисления не представляет особых трудностей. Но на стадии выделения адипиновую кислоту необходимо очистить от янтарной и глутаровой кислот, которых особенно много присутствует во второй кристаллизационной порции адипиновой кислоты (см. представленную ниже методику синтеза адипиновой кислоты из циклогексанола). Авторы литературной методики использовали перекристаллизацию из концентрированной азотной кислоты. Это приводит к частичной потере адипиновой кислоты и полной потере янтарной и глутаровой кислот.
Литературные константы янтарной (С4), глутаровой (С5) и адипиновой (С6) кислот представлены в таблице 1. Из представленных данных наглядно видно, что ректификация смеси карбоновых кислот имеет ряд технических затруднений. Прежде всего, это связано с их высокими температурами плавления.
Таблица 1.
Физико-химические константы кислот
| Название кислоты | Химическая формула | Tпл., °С | Ткип., °С/ P, torr |
| янтарная | HOOCCH2CH2COOH | 184-186 | 100/760 |
| глутарова | HOOCCH2CH2CH2COOH | 95-98 | 200/20 |
| адипиновая | HOOCCH2CH2CH2CH2COOH | 151-154 | 265/100 |
Мы применили альтернативную очистку сырой адипиновой кислоты. Решение состояло в синтезе диэтилового эфира и последующей фракционной вакуумной ректификации. Наряду с диэтиладипатом удается выделить небольшие количества диэтилсукцината и диэтилглутарата, которые также могут найти применение в синтезе половых феромонов насекомых. Константы для полученных эфиров представлены в таблице 2. Чистота сложных эфиров была подтверждена методом ГЖХ на капиллярной колонке.
Таблица 2.
Физико-химические константы сложных эфиров кислот
| Название эфира | Химическая формула | Ткип., °С/ P, torr | nd 20 |
| диэтилсукцинат | H5C2OOC(CH2)2COOС2H5 | 121-126/20 | 1,42 |
| диэтилглутарат | H5C2OOC(CH2)3COOС2H5 | 133-138/20 | 1,423 |
| диэтиладипат | H5C2OOC(CH2)4COOС2H5 | 142-147/20 | 1,427 |
Сложные эфиры в сравнении с карбоновыми кислотами являются жидкостями, которые хорошо смешиваются с диэтиловым эфиром и легче восстанавливаются алюмогидридом лития в соответствующий ɑ,ω-диолы. Затраты на этиловый спирт (можно напрямую восстанавливать карбоксильные группы) окупаются использованием меньших количеств алюмогидрида лития и растворителя в реакции восстановления [5, с. 214]. Таким образом, мы не применяли перекристаллизацию сырой адипиновой кислоты, а сразу получали ее диэтиловый эфир.
Выбор этилового спирта для проведения реакции этерификации адипиновой кислоты обусловлен его относительной доступностью и низкой молекулярной массой. Проведение реакции в отсутствии катализатора не представляет практического интереса вследствие малой скорости протекания процесса. Чаще всего для синтеза метиловых и этиловых эфиров в качестве кислых катализаторов применяют серную кислоту, толуолсульфокислоту и хлористый водород (метод Фишера) [6, с. 4196].
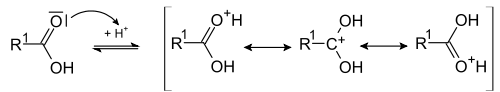
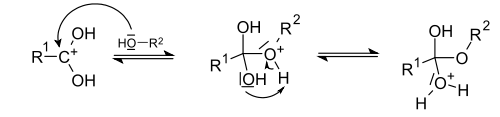
Реакция этерификации проходит по механизму бимолекулярного нуклеофильного замещения (SN2-тип реакций). На первой стадии происходит протонирование атома кислорода карбонильной группы карбоновой кислоты с образованием резонансностабилизированного карбкатиона:
Схема образования стабилизированного карбкатиона
После этого происходит нуклеофильная атака атома кислорода гидроксильной группы спирта на карбониевый центр с образованием алкилоксониевого иона. Эта стадия является лимитирующей. Затем происходит миграция протона на один из гидроксилов бывшей карбоксильной группы:
Нуклеофильное взаимодействие спирта с карбкатионом
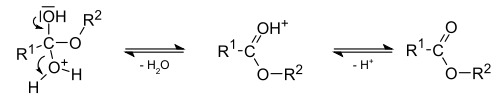
Завершающей стадией является отщепление промежуточного продукта присоединения воды и протона-катализатора с образованием сложного эфира:
Завершающая стадия образования сложного эфира
Интересно, что в реакциях этерификации кислород отщепляется от карбоксильной группы, а водород от спиртовой.
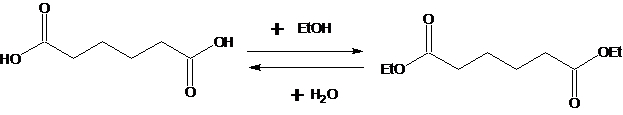
Реакция этерификации является обратимой и подчиняется принципу Ле Шетелье (рис. 5).
Общая схема синтеза диэтилового эфира адипиновой кислоты
Поэтому для увеличения выхода сложного эфира мы использовали избыток абсолютного спирта (99.5%-ный), который был получен ректификацией 95.6%-ного спирта-ректификата с бензолом (см. представленную ниже методику получения абсолютного (99.5%-ного) спирта).
Еще один подход для увеличения выхода сложного эфира состоит в выборе такого растворителя, который образует азеотропную смесь с водой. Реакцию проводят в прямом или обратном аппарате Дина и Старка. Это позволяет с помощью азеотропной отгонки удалять воду из зоны реакции [7, c. 1].
В качестве растворителя был выбран хлороформ [8, с. 153]. В сравнении с толуолом реакция идет при более низкой температуре и требует меньших количеств этанола [9, с. 178-180].
Лабораторный синтез адипиновой кислоты из циклогексанола.
В 5 л круглодонную колбу, оборудованную механической мешалкой, термометром и 1 л делительной воронкой помещают 2100 г (16.6 молей) 50 % азотной кислоты (ρ = 1.32 г/мл). Кислоту нагревают до начала кипения и вносят 1 г ванадата аммония. Далее включают перемешивание и прикапывают 530 мл (5 молей) циклогексанола. После первых 40-50 капель необходимо выждать некоторое время до начала реакции, что заметно по изменению цвета и началу выделения бурых окислов азота. Затем колбу помещают в баню со смесью льда и воды и охлаждают так, чтобы поддерживать температуру окисления в районе 55-60°С. Циклогексанол приливают с максимально возможной скоростью, при которой удается поддерживать заданную температуру. Чтобы предотвратить возможную кристаллизацию адипиновой кислоты, после прибавления 500 мл циклогексанола охлаждение убирают и проводят синтез при повышенной температуре реакционной массы.
После прибавления всего циклогексанола перемешивание продолжают в течение одного часа на кипящей водяной бане. Затем смесь охлаждают до 0°С и фильтруют выпавшую адипиновую кислоту. Фильтрат промывают 500 мл ледяной воды и высушивают на воздухе до постоянной массы. Выход 395-410 г белых кристаллов, которые плавятся при 146-149°С. Выпариванием азотной кислоты были получены дополнительные 30-40 г вещества, плавящегося при 141-144°С. Данная порция адипиновой кислоты сильно загрязнена янтарной и глутаровой кислотами. Общий выход сырой адипиновой кислоты составил 425-440 г (58-60% от теоретического количества). Адипиновая кислота может быть перекристаллизована из 700 мл концентрированной азотной кислоты. Такая кислота плавится при 151-152°С. Потери на перекристаллизацию составляют около 5% по массе. Удовлетворительных результатов перекристаллизации можно добиться использованием в 2.5 раза большего по массе количества 50% этилового спирта.
Получение абсолютного (99.5%-ного) этилового спирта.
1.1 л промышленного 95.6%-ного спирта-ректификата подвергают ректификации при нормальном давлении. Головную и кубовую фракции отбрасывают, получая около 1 л чистого спирта-ректификата, который кипит при 78.2°С. Отдельно, отбрасывая головную фракцию, получают безводный бензол, который кипит при 80°С.
В 2 л колбе смешивают 1000 мл этанола с 600 мл бензола и осторожно ректифицируют смесь. При этом отгоняется тройная азеотропная смесь, которая кипит при 64.9°С и содержит 18.5% спирта, 74.1% бензола и 7.4% воды. Далее при 68.2°С отгоняется двойная азеотропная смесь, которая содержит 32% спирта и 68% бензола. После чего при 78.3°С перегоняется фракция достаточно чистого 99.5%-ного этилового спирта. Данный реагент был использован в следующем шаге. Поучено около 730 мл абсолютного спирта.
Получение диэтилового эфира адипиновой кислоты.
Смесь 73.1 г (0.50 моль) адипиновой кислоты, 80.5 г (1.75 моль) этанола (99.5%), 5.00 г моногидрата п-толуолсульфокислоты и 100 мл хлороформа кипятят с насадкой Дина-Старка (обратный холодильник и водоотделитель; для случая. Когда органический растворитель тяжелее воды) примерно 8 часов.
Затем отгоняют под вакуумом хлороформ и избыток EtOH, а остаток перегоняют под вакуумом водоструйного насоса, получая 91.7 г (91%) диэтилового эфира адипиновой кислоты в виде бесцветной жидкости с т. кип. 137-138°С/20 мм.рт.ст. и nd 20 1.4278.
Список литературы: