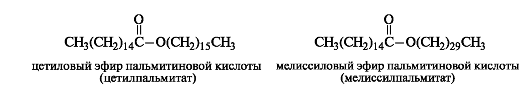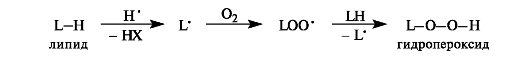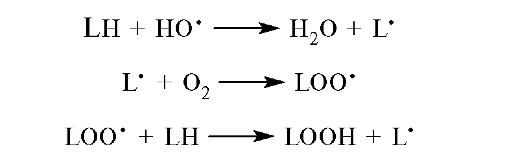— сложные эфиры трехатомного спирта глицерина и высших карбоновых кислот (в состав некоторых жиров входят остатки и низших карбоновых кислот)
- Общая формула
- Классификация, агрегатное состояние
- Получение жиров (реакция Бертло)
- Химические свойства
- Биологическая роль жиров
- Номенклатура жиров
- Физические свойства жиров
- Химические свойства жиров
- 1.1. Кислотный гидролиз
- 1.2. Щелочной гидролиз — омыление жиров
- 2. Гидрирование (гидрогенизация) ненасыщенных жиров
- 3. Мыло и синтетические моющие средства
- Присоединения, окисления. Понятие о йодном числе.
Общая формула
Классификация, агрегатное состояние
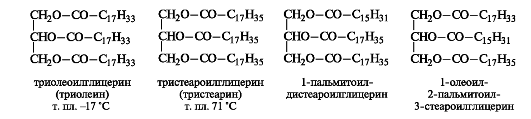
I. По однородности ацильных остатков:
(содержат остатки одной кислоты); например:
(содержат остатки разных кислот); например:
II. По агрегатному состоянию:
содержащие остатки насыщенных карбоновых кислот (чаще всего пальмитиновой и стеариновой); например:
Остатки насыщенных кислот преобладают в жирах животного происхождения (бараний жир, сливочное масло и др.)
, содержащие остатки ненасыщенных карбоновых кислот (чаще всего олеиновой, линолевой и линоленовой); например:
Остатки ненасыщенных кислот преобладают в жирах растительного происхождения (растительные масла: подсолнечное, оливковое и др.).
Получение жиров (реакция Бертло)
Реакция этерификации глицерина высшими карбоновыми кислотами:
Химические свойства
1. Кислотный гидролиз
2. Щелочной гидролиз (реакция Шевреля)
Образующиеся в результате щелочного гидролиза натриевые или калиевые соли ВКК представляют собой мыла (соответственно — твердые и жидкие); поэтому эти реакции часто называют омылением жиров.
3. Ферментативный гидролиз
В организмах человека и животных жиры, поступающие в составе пищи, подвергаются гидролитическому расщеплению с участием специальных ферментов — липаз (уравнение аналогично уравнению кислотного гидролиза).
4. Водный гидролиз
Промышленный метод гидролиза жиров заключается в обработке их водяным паром при температуре Т ≈ 200°С под давлением (уравнение аналогично уравнению кислотного гидролиза).
5. Гидрогенизация (гидрирование) жидких жиров
(1 моль данного жира может максимально присоединить 5 моль Н2, так как в радикале -C17H33 содержится 1 двойная связь, а в каждом радикале -С17Н31: — по 2 двойные связи; итого 5 двойных связей).
Таким путем из растительных масел в промышленности получают твердые жиры, являющиеся основой для производства маргарина.
6. Присоединение галогенов жидкими жирами
Растительные масла обесцвечивают бромную воду:
Биологическая роль жиров
Жиры (триглицериды) — важный компонент пищи человека и многих животных. Они служат резервным источником энергии (при сгорании 1 г жира выделяется примерно 39 кДж теплоты).
У растений триглицериды встречаются в основном в семенах и плодах, а у животных и человека — в подкожном слое, между мышечными волокнами и в брюшной полости. Жиры предохраняют организм от тепловых потерь, так как являются плохим проводником тепла.
Номенклатура жиров
Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой. Все животные жиры, кроме рыбьего – твёрдые. | Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими. Все растительные жиры, кроме пальмового масла – жидкие. |
Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
| Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия . |
2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
| Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина: |
| Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира. |
3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca 2+ и Mg 2+ дают с высшими кислотами нерастворимые в воде соли.
| Например, тристеарат глицерина взаимодействует с сульфатом кальция |
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата .
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Присоединения, окисления. Понятие о йодном числе.
Воски — сложные эфиры высших жирных кислот и высших одноатомных спиртов.
Воски образуют защитную смазку на коже человека и животных и предохраняют растения от высыхания. Они применяются в фармацевтической и парфюмерной промышленности при изготовлении кремов и мазей. Примером служит цетиловый эфир пальмитиновой кислоты (цетин) — главный компонент спермацета. Спермацет выделяется из жира, содержащегося в полостях черепной коробки кашалотов. Другим примером является мелиссиловый эфир пальмитиновой кислоты — компонент пчелиного воска.
Жиры и масла — самая распространенная группа липидов. Большинство из них принадлежит к триацилглицеринам — полным эфирам глицерина и ВЖК, хотя также встречаются и принимают участие в обмене веществ моно- и диацилглицерины.
Жиры и масла (триацилглицерины) — сложные эфиры глицерина и высших жирных кислот.
В организме человека триацилглицерины играют роль структурного компонента клеток или запасного вещества («жировое депо»). Их энергетическая ценность примерно вдвое больше, чем белков
или углеводов. Однако повышенный уровень триацилглицеринов в крови является одним из дополнительных факторов риска развития ишемической болезни сердца.
Твердые триацилглицерины называют жирами, жидкие — маслами. Простые триацилглицерины содержат остатки одинаковых кислот, смешанные — различных.
В составе триацилглицеринов животного происхождения обычно преобладают остатки насыщенных кислот. Такие триацилглицерины, как правило, твердые вещества. Напротив, растительные масла содержат в основном остатки ненасыщенных кислот и имеют жидкую консистенцию.
Особенностью сложных липидов является их бифильность, обусловленная неполярными гидрофобными и высокополярными ионизированными гидрофильными группировками. В фосфатидилхолинах, например, углеводородные радикалы жирных кислот образуют два неполярных «хвоста», а карбоксильная, фосфатная и холиновая группы — полярную часть.
На границе раздела фаз такие соединения действуют, как превосходные эмульгаторы. В составе клеточных мембран липид- ные компоненты обеспечивают высокое электрическое сопротивление мембраны, ее непроницаемость для ионов и полярных молекул и проницаемость для неполярных веществ. В частности, большинство анестезирующих препаратов хорошо растворяются в липидах, что позволяет им проникать через мембраны нервных клеток.
Жирные кислоты — слабые электролиты (pKa
4,8). Они в малой степени диссоциированы в водных растворах. При pH pKa, т. е. в физиологических условиях, преобладает ионизированная форма RCOO-. Растворимые соли высших жирных кислот называются мылами. Натриевые соли высших жирных кислот твердые, калиевые — жидкие. Как соли слабых кислот и сильных оснований мыла частично гидролизуются в воде, их растворы имеют щелочную реакцию.
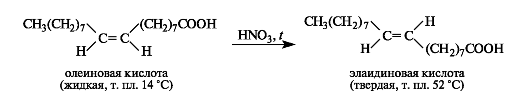
Природные ненасыщенные жирные кислоты, имеющие цис-конфигурацию двойной связи, обладают большим запасом внутренней энергии и, следовательно, по сравнению с транс-изомерами термодинамически менее стабильны. Их цис-транс-изомеризация легко проходит при нагревании, особенно в присутствии инициаторов радикальных реакций. В лабораторных условиях это превращение можно осуществить действием оксидов азота, образующихся при разложении азотной кислоты при нагревании.
Высшие жирные кислоты проявляют общие химические свойства карбоновых кислот. В частности, они легко образуют соответствующие функциональные производные. Жирные кислоты с двойными связями проявляют свойства ненасыщенных соединений — присоединяют по двойной связи водород, галогеноводороды и другие реагенты.
С помощью реакции гидролиза устанавливают строение липидов, а также получают ценные продукты (мыла). Гидролиз — первая стадия утилизации и метаболизма пищевых жиров в организме.
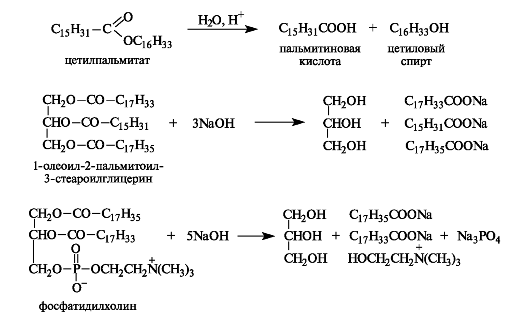
Гидролиз триацилглицеринов осуществляют либо воздействием перегретого пара (в промышленности), либо нагреванием с водой в присутствии минеральных кислот или щелочей (омыление). В организме гидролиз липидов проходит под действием ферментов липаз. Некоторые примеры реакций гидролиза приведены ниже.
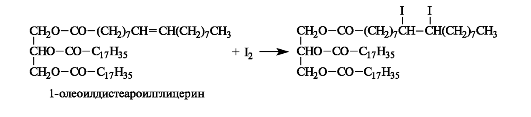
Липиды, содержащие в структуре остатки ненасыщенных кислот, присоединяют по двойным связям водород, галогены, галогеноводороды, воду в кислой среде. Иодное число — это мера ненасыщенности триацилглицеринов. Оно соответствует числу граммов иода, которое может присоединиться к 100 г вещества. Состав природных жиров и масел и их иодные числа варьируют в достаточно широких пределах. В качестве примера приводим взаимодействие 1-олеоил- дистеароилглицерина с иодом (иодное число этого триацилглицерина равно 30).
Каталитическое гидрирование (гидрогенизация) ненасыщенных растительных масел — важный промышленный процесс. В этом случае водород насыщает двойные связи и жидкие масла превращаются в твердые жиры.
Окислительные процессы с участием липидов и их структурных компонентов достаточно разнообразны. В частности, окисление кис- лородом воздуха ненасыщенных триацилглицеринов при хранении , сопровождаемое гидролизом, является частью процесса, известного как прогоркание масла.
Первичными продуктами взаимодействия липидов с молекулярным кислородом являются гидропероксиды, образующиеся в резуль- тате цепного свободнорадикального процесса
Пероксидное окисление липидов — один из наиболее важных окислительных процессов в организме. Он является основной причиной повреждения клеточных мембран (например, при лучевой болезни).
Структурные фрагменты ненасыщенных высших жирных кислот в фосфолипидах служат мишенью для атаки активными формами кис- лорода
ри атаке, в частности, гидроксильным радикалом HO’, наиболее активным из АФК, молекулы липида LH происходит гомолитический разрыв связи С-Н в аллильном положении, как показано на примере модели пероксидного окисления липидов. Образующийся радикал аллильного типа L’ мгновенно реагирует с находящимся в среде окисления молекулярным кислородом с образованием липидпероксильного радикала LOO’. С этого момента начинается цепной каскад реакций пероксидации липидов, поскольку происходит постоянное образование аллильных липидных радикалов L’, возобнов- ляющих этот процесс.
Липидные пероксиды LOOH — неустойчивые соединения и могут спонтанно или при участии ионов металлов переменной валентности (см. 3.2.1) разлагаться с образованием липидоксильных радикалов LO’, способных инициировать дальнейшее окисление липидного субстрата. Такой лавинообразный процесс пероксидного окисления липидов представляет собой опасность разрушения мембранных структур клеток.
Промежуточно образующийся радикал аллильного типа имеет мезомерное строение и может далее подвергаться превращениям по двум направлениям (см. схему пути а и б), приводящим к промежуточным гидропероксидам. Гидропероксиды нестабильны и уже при обычной температуре распадаются с образованием альдегидов, которые далее окисляются в кислоты — конечные продукты реакции. В результате получаются в общем случае две монокарбоновые и две дикарбоновые кислоты с более короткими углеродными цепями.
Ненасыщенные кислоты и липиды с остатками ненасыщенных кислот в мягких условиях окисляются водным раствором перманга- ната калия, образуя гликоли, а в более жестких (с разрывом углеродуглеродных связей) — соответствующие кислоты.