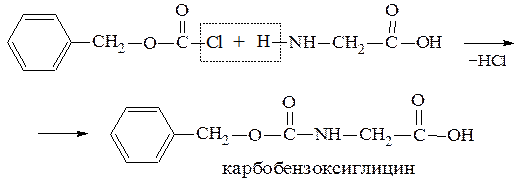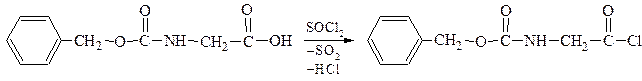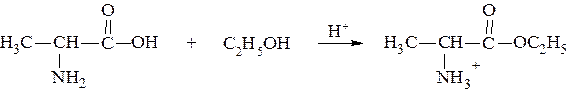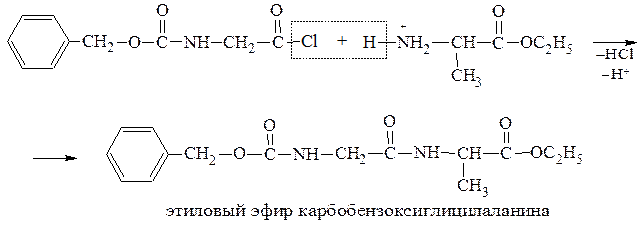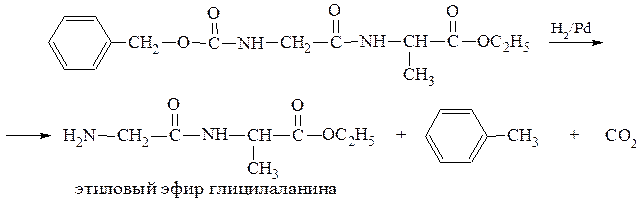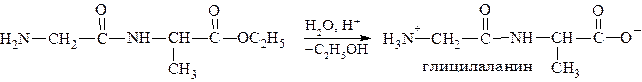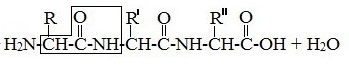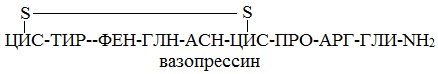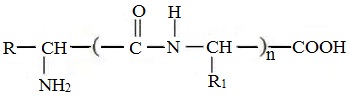Основная проблема при синтезе пептидов — проблема защиты аминогруппы. При взаимодействии карбоксильной группы одной аминокислоты с аминогруппой другой кислоты необходимо исключить возможность протекания реакции между карбоксильной группой и аминогруппой молекул одной и той же аминокислоты.
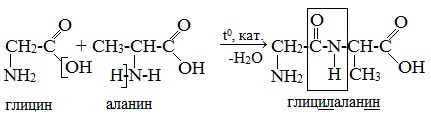
Например, при получении дипептида гли — ала необходимо предотвращать одновременное образование глицилглицина и аланилаланина. Реакцию можно направить в нужную сторону, если в одну из аминогрупп ввести заместитель, который сделает эту аминогруппу нереакционноспособной. Этот процесс называется защитой аминогруппы. Как уже было отмечено выше, защищать аминогруппу можно реакциями взаимодействия с ангидридом и хлорангидридом уксусной кислоты, с бензоилхлоридом (см. стр.60).
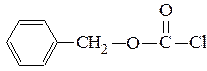
является карбобензоксихлорид , который
одновременно является и хлорангидридом и сложным эфиром. И как любой хлорангидрид он может превращать амин в амид.
Подобные амиды, однако, отличаются от большинства амидов в одном отношении, которое очень существенно для синтеза пептидов: карбобензоксигруппу можно отщеплять действием реагентов, не затрагивающих пептидные связи, (каталитическим гидрогенолизом).
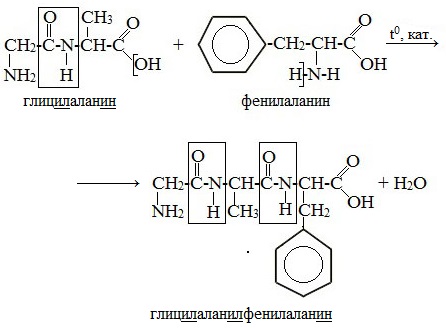
Рассмотрим подробно синтез дипептида глицилаланина. Процесс складывается из следующих стадий:
1) защита аминогруппы глицина:
2) активация карбоксильной группы глицина (получение хлорангидрида):
3) защита карбоксильной группы аланина (взаимодействие ала-нина с этиловым спиртом с образованием сложноэфирной группы):
4) образование пептидной связи:
5) снятие защиты с аминогруппы:
6) гидролиз сложноэфирной группы:
Открытые и изученные в настоящее время пептиды можно разделить на следующие группы по их физиологическому действию:
1) регулирующие процессы пищеварения;
2) обладающие гормональной активностью;
3) регулирующие тонус сосудов и артериальное давление;
4) обладающие обезболивающим действием;
5) регулирующие аппетит;
6) участвующие в регуляции высшей нервной деятельности.
БЕЛКИ
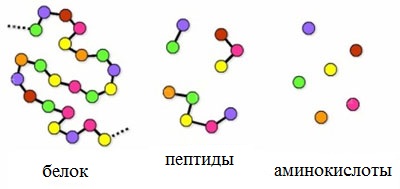
Как уже было отмечено ранее, трудно провести четкую границу между пептидами и белками. Обычно к белкам относят, как правило, высокомолекулярные пептиды, выполняющие основные биологичес-кие функции.
- Постройте дипептид лей — вал?
- Составьте уравнения : Дипептид — — — > ; аминоуксусная кислота?
- Сколько различных дипептидов может быть образовано тремя аминокислотами : глицином, аланином, лейцином?
- Напишите уравнение химической реакции образования дипептида лизина?
- При нагревании дипептида с водным раствором NaOH была получена только одна соль с массовой долей Na 12?
- За счёт чего происходит образование дипептидов?
- Получить из карбида кальция дипептид?
- Напишите уравнение реакции образования дипептида из валина и серина?
- Дипептиды, органика?
- Какая молекулярная формула дипептида аминоуксусной кислоты?
- Биосинтез лей вал фен глуДНК — ?
- Уравнение образование дипептида гли вал выделите обведите пептидную связь
- Образование дипептидов
- Образование трипептидов
- Номенклатура
- Биологическое значение
- Химические свойства
Постройте дипептид лей — вал?
Химия | 10 — 11 классы
Постройте дипептид лей — вал.
HOOC — CH(NH2) — CH2 — CH(CH3) — CH3 + СH3 — CH(CH3) — Ch(NH2) — COOH =
СH3 — CH(CH3) — CH2 — CH(NH2) — CO — NH — CH(CH(CH3)2 — COOH + H2O.
Составьте уравнения : Дипептид — — — > ; аминоуксусная кислота?
Составьте уравнения : Дипептид — — — > ; аминоуксусная кислота.
Сколько различных дипептидов может быть образовано тремя аминокислотами : глицином, аланином, лейцином?
Сколько различных дипептидов может быть образовано тремя аминокислотами : глицином, аланином, лейцином.
Запишите названия этих дипептидов.
Напишите уравнение химической реакции образования дипептида лизина?
Напишите уравнение химической реакции образования дипептида лизина.
При нагревании дипептида с водным раствором NaOH была получена только одна соль с массовой долей Na 12?
При нагревании дипептида с водным раствором NaOH была получена только одна соль с массовой долей Na 12.
29%. Установите строение дипептида.
За счёт чего происходит образование дипептидов?
За счёт чего происходит образование дипептидов?
Получить из карбида кальция дипептид?
Получить из карбида кальция дипептид.
Напишите уравнение реакции образования дипептида из валина и серина?
Напишите уравнение реакции образования дипептида из валина и серина.
Дипептиды, органика?
Какая молекулярная формула дипептида аминоуксусной кислоты?
Какая молекулярная формула дипептида аминоуксусной кислоты?
Биосинтез лей вал фен глуДНК — ?
Биосинтез лей вал фен глу
Если вам необходимо получить ответ на вопрос Постройте дипептид лей — вал?, относящийся к уровню подготовки учащихся 10 — 11 классов, вы открыли нужную страницу. В категории Химия вы также найдете ответы на похожие вопросы по интересующей теме, с помощью автоматического «умного» поиска. Если после ознакомления со всеми вариантами ответа у вас остались сомнения, или полученная информация не полностью освещает тематику, создайте свой вопрос с помощью кнопки, которая находится вверху страницы, или обсудите вопрос с посетителями этой страницы.
Вот такая формула : C5H12.
1) С + O2 = СO2 2)CO2 + H2 = H2CO2 3) H2CO3 + Ca(OH)2 = CaCO3 + 2H20 4) CaCO3 + 2HCl = CaCl2 + H2O + CO2 C — УГЛЕРОД O — кислород H — водород CA — кальций Cl — ХЛОР.
А) 2HNO3 + CuO — Cu(NO3)2 + H2O б) H2SO4 + 2NaOH — Na2SO4 + 2H2O в) 2HCl + K2CO3 — 2KCl + H2CO3.
Последнее не знаю точно.
2) и 6) если 2 варианта надо, если один то только 6).
Найдем сперва сколько грамм весит 1 моль. D(метан) = х / 16 Делим х на 16, так как метан весит 16. И вот подставим значения. 2, 5 = х / 16 Х = 40 Нашли что вещество весит 40 грамм. Напишем реакцию горения для сгорания 10 грамм этого вещетва , то ..
Ca + 2H₂O = Ca(OH)₂ + H₂↑ Ca + SiO₂(t) = CaO + Si CaO + SiO₂ (t) = CaSiO₃ 5Ca + 2CO₂(t) = CaC₂ + 4CaO Ca + 2HCl = CaCl₂ + H₂↑ 3Ca + N₂(t) = Ca₃N₂ Ca + H₂(t) = CaH₂.
N = m / M = 5, 34 / 132, 5 = 0, 04г / моль 3 — 2 х — 0, 04 это пропорция х = 0, 06г / моль V = n * Vm = 0, 06 * 22, 4 = 1, 344л.
2Mg + H2O — MgO + H2 Cu + HCl = = = > CuCl2 + H2(протекает при 600 — 700 гр Цельсия, реакция идет с HCl в газовом состоянии, а не с жидким HCl) 4Li + O2 = 2Li2O Cu + CI₂ = CuCI₂ Mg + CuCl2 — > MgCl2 = Cu 2Al + 3Fe2SO4 = Al2(SO4)3 + 6Fe Na2O + H2O = 2..
Налить воды и размешать. Сахар растворится в воде и опустится на дно, бензин поднимется наверх. Вставляем трубочку и. . Если это, конечно, не бак автомобиля.
Уравнение образование дипептида гли вал выделите обведите пептидную связь
Пептиды – семейство веществ, молекулы которых построены из двух и более остатков аминокислот, соединенных в цепь пептидными (амидными) связями —С(О)NН- .
Пептиды можно рассматривать как продукты конденсации двух или более молекул аминокислот.
Число пептидов, которые могут быть построены из 20 природных аминокислот, огромно.
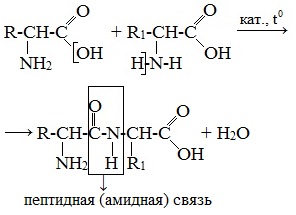
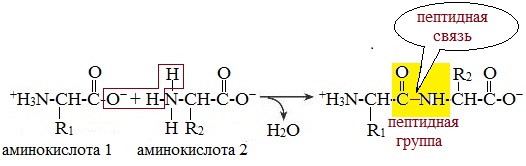
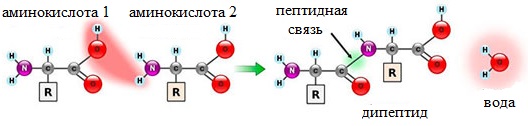
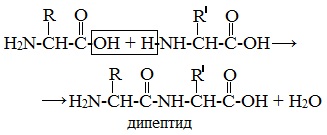
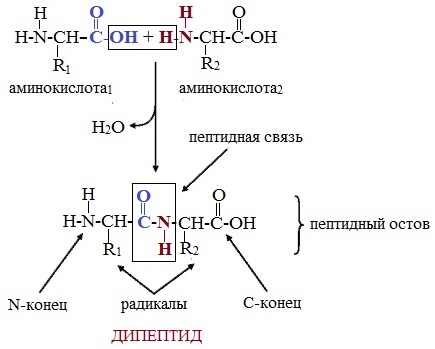
Две молекулы аминокислоты могут реагировать друг с другом с отщеплением молекулы воды и образованием продукта, в котором фрагменты связаны пептидной связью –СО-NH- .
Образование дипептидов
Две аминокислоты образуют дипептид:
Образование трипептидов
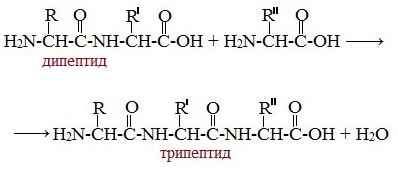
Молекула дипептида, подобно аминокислотам, содержит аминогруппу и карбоксильную группу и может реагировать еще с одной молекулой аминокислоты:
Полученное соединение называется трипептидом.
Процесс наращивания пептидной цепи может продолжаться неограниченно и приводит к веществам с очень высокой молекулярной массой (белкам).
Формулы пептидов обычно записываются так, что свободная аминогруппа находится слева, а свободная карбоксильная группа – справа. Основная часть пептидной цепи построена из повторяющихся участков –СН-СО-NН- и боковых групп R, R’ и т.д.
Структуру пептидов, содержащих большое число остатков аминокислот, записывают в сокращенном виде с использованием обозначений.
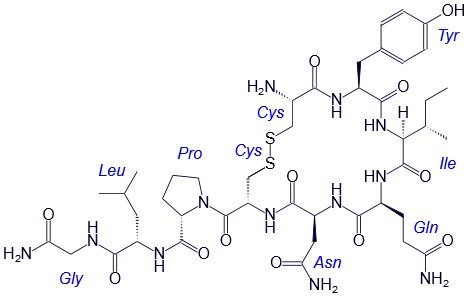
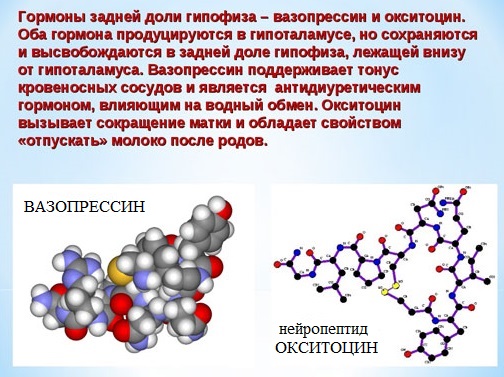
Например, строение молекулы вазопрессина – пептида, построенного из 9 аминокислотных остатков, можно изобразить следующим образом:
Структурная формула вазопрессина
Эту же структуру можно изобразить в сокращенном виде с использованием трехбуквенных и однобуквенных обозначений аминокислот:
В этом пептиде остатки цистеина связаны дисульфидными мостиками. Правый конец цепи содержит амидную группу –СО-NН2 вместо карбоксильной.
Номенклатура
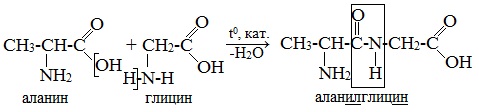
При составлении названия дипептида сначала называют аминокислоту, у которой в образовании дипептида участвует группа –СООН. В тривиальном названии этой кислоты последняя буква «н» заменяется буквой «л». Затем прибавляют без изменений тривиальное название аминокислоты, у которой в образовании дипептида участвует группа –NH2.
Любой дипептид имеет свободные амино- и карбоксильную группы и поэтому может взаимодействовать еще с одной молекулой аминокислоты, образуя трипептид. Таким же путем получают тетрапептиды и т.д.
Биологическое значение
Многие пептиды проявляют биологическую активность. Простейший из них – трипептид глутатион, который относится к классу гормонов – веществ, регулирующих процессы жизнедеятельности. Этот гормон построен из остатков глицина, цистеина и глутаминовой кислоты.
Некоторые пептиды (окситоцин, вазопрессин, инсулин) имеют огромное биологическое значение, являются важными гормонами.
Вазапрессин и окситоцин содержат 9 аминокислотных остатков.
Вазопрессин вырабатывается гипофизом и стимулирует сокращение кровеносных сосудов, повышает кровяное давление, а окситоцин стимулирует выделение молока молочными железами.
Инсулин – биологически важный пептид, который построен из двух цепей, состоящих из 21 и 30 α-аминокислотных остатков, которые связаны между собой дисульфидными мостиками. Вырабатывается поджелудочной железой и снижает содержание сахара в крови.
Химические свойства
Основное свойство пептидов – способность к гидролизу. При гидролизе происходит полное или частичное расщепление пептидной цепи и образуются более короткие пептиды с меньшей молекулярной массой или α-аминокислоты, составляющие цепь.
Анализ продуктов полного гидролиза позволяет установить аминокислотный состав пептида. Полный гидролиз происходит при длительном нагревании пептида с концентрированной соляной кислотой.
Последовательность аминокислот в цепи может быть установлена путем частичного гидролиза пептида. Для этого необходимо последовательно, одну за другой, отщеплять аминокислоты от одного из концов цепи и устанавливать их структуру.
Гидролиз пептидов может происходить в кислой или щелочной среде, а также под действием ферментов. В кислой и щелочной средах образуются соли аминокислот.
Ферментативный гидролиз важен тем, что протекает селективно, т.е. позволяет расщеплять строго определенный участки пептидной цепи. Селективный гидролиз может протекать и под действием неорганических реагентов. Так, бромистый циан (BrCN) расщепляет полипептидную цепь только по пептидной связи, образованной карбоксильной группой метионина.