| Нитрат хрома III | |
|---|---|
 | |
| Систематическое наименование | Нитрат хрома III |
| Хим. формула | Cr(NO3)3 |
| Состояние | твёрдое |
| Молярная масса | 238.011 г/моль |
| Плотность | 1,85 г/см³ |
| Температура | |
| • плавления | 60,06 °C |
| • разложения | 125 °C |
| Растворимость | |
| • в воде | 81 г/100 мл |
| Рег. номер CAS | 13548-38-4 |
| PubChem | 24598 |
| Рег. номер EINECS | 236-921-1 |
| SMILES | |
| RTECS | GB6300000 |
| ChEBI | 86204 |
| Номер ООН | 2720 |
| ChemSpider | 23000 |
| ЛД50 | 3250 мг/кг |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
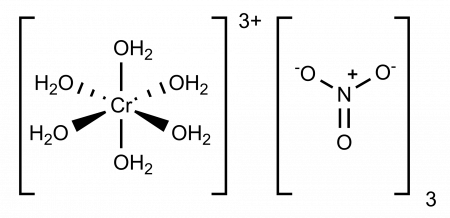
Нитрат хрома III — неорганическое вещество, соль металла хрома и азотной кислоты с формулой Cr(NO3)3, в безводном состоянии кристаллическое вещество зелёного цвета, образует несколько кристаллогидратов, самый устойчивый из которых нонагидрат [Cr(H2O)6](NO3)3•3H2O.
Содержание
- 1 Получение
- 2 Физические свойства
- 3 Химические свойства
- 4 Применение
Получение
- Взаимодействием азотной кислоты с оксидом и гидроксидом хрома:
Cr2O3 + 6 HNO3 → 2 Cr(NO3)3 + 3 H2O Cr(OH)3 + 3 HNO3 → Cr(NO3)3 + 3 H2O
- Обменными реакциями:
CrCl3 + 3 NH4NO3 → 100oC Cr(NO3)3 + 3 NH3 ↑ + 3 HCl ↑
- Безводный нитрат хрома III получают сушкой кристаллогидрата:
[Cr(H2O)6](NO3)3 ⋅ 3 H2O → 100oC Cr(NO3)3 + 9 H2O
- В промышленности нитрат хрома III получают реакцией гидроксида хрома с азотной кислотой.
Физические свойства
Нитрат хрома III в безводном состоянии представляет собой зелёный гигроскопичный порошок, который разлагается при 125°С. Образует несколько кристаллогидратов, наиболее изученный из которых — нонагидрат [Cr(H2O)6](NO3)3•3H2O, который при стандартных условиях является кристаллическим веществом пурпурного или тёмно-фиолетового цвета. Шесть молекул воды сконцентрированы вокруг атома хрома, остальные три молекулы располагаются в кристаллической решетке.
Нитрат, как и его нонанагидрат, хорошо растворяется в воде, а также этаноле и ацетоне.
Гидролиз нитрата хрома (III)
Cr(NO3)3 — соль образованная слабым основанием и сильной кислотой, поэтому реакция гидролиза протекает по катиону.
Первая стадия (ступень) гидролиза
Полное ионное уравнение
Cr 3+ + 3NO3 — + HOH ⇄ CrOH 2+ + 2NO3 — + H + + NO3 —
Сокращенное (краткое) ионное уравнение
Cr 3+ + HOH ⇄ CrOH 2+ + H +
Вторая стадия (ступень) гидролиза
Полное ионное уравнение
CrOH 2+ + 2NO3 — + HOH ⇄ Cr(OH)2 + + NO3 — + H + + NO3 —
Сокращенное (краткое) ионное уравнение
CrOH 2+ + HOH ⇄ Cr(OH)2 + + H +
Третья стадия (ступень) гидролиза
Сокращенное (краткое) ионное уравнение
Cr(OH)2 + + HOH ⇄ Cr(OH)3 + H +
Среда и pH раствора нитрата хрома (III)
В результате гидролиза образовались ионы водорода (H + ), поэтому раствор имеет кислую среду (pH
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. |


