Метан CH4 – это предельный углеводород, содержащий один атом углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, легче воды, нерастворим в воде и не смешивается с ней.
- Гомологический ряд метана
- Строение метана
- Изомерия метана
- Химические свойства метана
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование метана
- 2. Реакции разложения метана (д егидрирование, пиролиз)
- 3. Окисление метана
- 3.1. Полное окисление – горение
- 3.2. Каталитическое окисление
- Получение метана
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Водный или кислотный гидролиз карбида алюминия
- 3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 4. Синтез Фишера-Тропша
- 5. Получение метана в промышленности
- Расчеты горения
- Глава 8. Характеристики горения газов
- Глава 8. Характеристики горения газов
- 8.1. РЕАКЦИИ ГОРЕНИЯ
- 8.2. РАСЧЕТЫ ГОРЕНИЯ
- 8.3. ТЕМПЕРАТУРА ГОРЕНИЯ
- 8.4. ТЕМПЕРАТУРА САМОВОСПЛАМЕНЕНИЯ
- 8.5. ПРЕДЕЛЫ ВОСПЛАМЕНЯЕМОСТИ И ВЗРЫВАЕМОСТИ
- 8.6. ГОРЕНИЕ В НЕПОДВИЖНОЙ СРЕДЕ
- 8.7. ГОРЕНИЕ В ЛАМИНАРНОМ И турбулентном ПОТОКах
- 8.8. УСТОЙЧИВОСТЬ ГОРЕНИЯ
- 8.9. СХЕМЫ ОГНЕПРЕГРАДИТЕЛЕЙ
- 8.10. ПРИНЦИПЫ СЖИГАНИЯ
- 8.11. УСЛОВИЯ ОБРАЗОВАНИЯ ПРОДУКТОВ НЕПОЛНОГО СГОРАНИЯ И СНИЖЕНИЕ В НИХ КОНЦЕНТРАЦИИ ВРЕДНЫХ ВЕЩЕСТВ
Гомологический ряд метана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4, или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение метана
В молекуле метана встречаются связи C–H. Связь C–H ковалентная слабополярная. Это одинарная σ-связь. Атом углерода в метане образует четыре σ-связи. Следовательно, гибридизация атома углерода в молекуле метана– sp 3 :
При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:
Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода |
Изомерия метана
Для метана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Химические свойства метана
Метан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для метана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для метана характерны только радикальные реакции.
Метан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
Для метана характерны реакции радикального замещение.
1.1. Галогенирование
Метан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании метана сначала образуется хлорметан:
Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:
| Химическая активность хлора выше, чем активность брома, поэтому хлорирование протекает быстро и неизбирательно. |
Бромирование протекает более медленно.
Реакции замещения в алканах протекают по свободнорадикальному механизму.
Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат неспаренный электрон.
Первая стадия. Инициирование цепи.
Под действием кванта света или при нагревании молекула галогена разрывается на два радикала:
Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом.
Вторая стадия. Развитие цепи.
Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород.
При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с новой нераспавшейся молекулой хлора:
Третья стадия. Обрыв цепи.
При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами, образуя молекулы, радикальный процесс обрывается.
Могут столкнуться как одинаковые, так и разные радикалы, в том числе два метильных радикала:
1.2. Нитрование метана
Метан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании до 140 о С и под давлением. Атом водорода в метане замещается на нитрогруппу NO2.
Например. При нитровании метана образуется преимущественно нитрометан:2. Реакции разложения метана (д егидрирование, пиролиз)При медленном и длительном нагревании до 1500 о С метан разлагается до простых веществ: Если процесс нагревания метана проводить очень быстро (примерно 0,01 с), то происходит межмолекулярное дегидрирование и образуется ацетилен: Пиролиз метана – промышленный способ получения ацетилена. 3. Окисление метанаАлканы – малополярные соединения, поэтому при обычных условиях они не окисляются даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.). 3.1. Полное окисление – горениеАлканы горят с образованием углекислого газа и воды. Реакция горения алканов сопровождается выделением большого количества теплоты. Уравнение сгорания алканов в общем виде: При горении алканов в недостатке кислорода может образоваться угарный газ СО или сажа С. Промышленное значение имеет реакция окисления метана кислородом до простого вещества – углерода: Эта реакция используется для получения сажи. 3.2. Каталитическое окисление
Продукт реакции – так называемый «синтез-газ». Получение метана1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета. Реакция больше подходит для получения симметричных алканов. Получить таким образом метан нельзя. 2. Водный или кислотный гидролиз карбида алюминияЭтот способ получения используется в лаборатории для получения метана. 3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении. R–COONa + NaOH → R–H + Na2CO3 Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты. При взаимодействии ацетата натрия с гидроксидом натрия при сплавлении образуется метан и карбонат натрия: 4. Синтез Фишера-ТропшаИз синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды: Это промышленный процесс получения алканов. Синтезом Фишера-Тропша можно получить метан: 5. Получение метана в промышленностиВ промышленности метан получают из нефти, каменного угля, природного и попутного газа . При переработке нефти используют ректификацию, крекинг и другие способы. Расчеты горенияРасчеты горения ведут по химическим уравнениям реакций, используя законы газового состояния: Бойля – Мариотта Рассмотрим реакцию горения водорода в кислороде: Рассмотрим реакцию горения метана в кислороде: В практических условиях сжигание газа осуществляется в воздухе. Примем состав сухого воздуха: О2 – 21 %, N2 – 79%. Следовательно, 1 м 3 кислорода содержится в 100/21 = 4,76 м 3 воздуха. Или на 1 м 3 кислорода приходится 3,76 м 3 азота. Отсюда условная формула воздуха: (О2 + 3,76N2). Запишем реакцию горения водорода в воздухе: Из уравнения следует, что при нормальных условиях для полного сгорания 1 м 3 водорода требуется 0,5 × 4,76 = 2,38 м 3 воздуха. Таким образом, для сгорания 1 м 3 водорода требуется 2,38 м 3 воздуха. В результате образуются продукты сгорания: 1 м 3 воды в виде пара и 1,88 м 3 азота. Запишем реакцию горения метана в воздухе: Из уравнения следует, что для полного сгорания 1 м 3 метана необходимо 2 × 4,76 = 9,52 м 3 воздуха. Таким образом, при нормальных условиях для сгорания 1 м 3 метана требуется 9,52 м 3 сухого воздуха. Продукты сгорания содержат 1 м 3 диоксида углерода, 2 м 3 паров воды и 7,52 м 3 азота. Запишем реакцию горения пропана в воздухе: Из уравнения видно, что для полного сгорания 1 м 3 пропана необходимо 5 × 4,76 = 23,8 м 3 воздуха. Таким образом, при нормальных условиях для сгорания 1 м 3 пропана требуется 23,8 м 3 сухого воздуха. Приведенные расчеты выполнены для стехиометрических уравнений и полученные соотношения воздуха и газа называются стехиометрическими. Например, для горения метана в воздухе стехиометрическое соотношение – 9,52. В реальных условиях воздуха может не хватать для полного сгорания газа или, напротив, воздух подается в избыточном количестве. Для характеристики реальных соотношений воздуха и газа в процессе горения введена безразмерная величина: коэффициент избытка воздуха (окислителя) – коэффициент α. Для стехиометрического соотношения α = 1. Если имеет место недостаток воздуха, то α 1. Например, в процессе горения израсходовано 23 м 3 воздуха и 2 м 3 метана. Подсчитываем коэффициент α. Реальное соотношение воздуха и газа 23/2 = 11,5. Отсюда α = 11,5/9,52 = 1,2. Выше показано, как можно подсчитывать необходимое количество воздуха для сгорания и определять объем продуктов сгорания для индивидуальных газов. Но обычно используемый газ – смесь различных газов. В этом случае расчет теоретически необходимого объема воздуха (воздуха сухого) ведется по формуле: где Используемый для сжигания атмосферный воздух содержит влагу, поэтому расчет объема влажного воздуха производят по формуле: где 0,00124 – объем 1 г водяного пара. И, наконец, определяется объем воздуха действительный с учетом величины коэффициента α по формуле: Пример. Имеется газ состава СН4 – 95%, С3Н8 – 5%. Определить объем воздуха действительного для сжигания данного газа при α = 1,1 и Объем продуктов сгорания газовой смеси определяется по следующим формулам. Объем диоксида углерода Объем водяных паров где N2 – процентное содержание азота в газовой смеси. Суммарный объем продуктов сгорания Дата добавления: 2015-06-22 ; просмотров: 8060 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ Глава 8. Характеристики горения газовГлава 8. Характеристики горения газов8.1. РЕАКЦИИ ГОРЕНИЯГ о р е н и е — быстропротекающая химическая реакция соединения горючих компонентов с кислородом, сопровождающаяся интенсивным выделением теплоты и резким повышением температуры продуктов сгорания. Реакции горения описываются т.н. стехиометрическими уравнениями, характеризующими качественно и количественно вступающие в реакцию и образующиеся в результате ее вещества (Стехиометрический состав горючей смеси (от греч. stoicheion — основа, элемент и греч. metreo — измеряю) — состав смеси, в которой окислителя ровно столько, сколько необходимо для полного окисления топлива) . Общее уравнение реакции горения любого углеводорода где m, n — число атомов углерода и водорода в молекуле; Q — тепловой эффект реакции, или теплота сгорания. Реакции горения некоторых газов приведены в табл. 8.1. Эти уравнения являются балансовыми, и по ним нельзя судить ни о скорости реакций, ни о механизме химических превращений. Таблица 8.1. Реакции горения и теплота сгорания сухих газов (при 0°С и 101,3 кПа)
Т е п л о в о й э ф ф е к т (теплота сгорания) Q — количество теплоты, выделяющееся при полном сгорании 1 кмоля, 1 кг или 1 м 3 газа при нормальных физических условиях. Различают высшую Qв и низшую Qн теплоту сгорания: высшая теплота сгорания включает в себя теплоту конденсации водяных паров в процессе горения (в реальности при сжигании газа водяные пары не конденсируются, а удаляются вместе с другими продуктами сгорания). Обычно технические расчеты обычно ведут по низшей теплоте сгорания, без учета теплоты конденсации водяных паров (≈2400 кДж/кг). КПД, рассчитанный по низшей теплоте сгорания, формально выше, но теплота конденсации водяных паров достаточно велика, и ее использование более чем целесообразно. Подтверждение этому — активное применение в отопительной технике контактных теплообменников, весьма разнообразных по конструкции. Для смеси горючих газов высшая (и низшая) теплота сгорания газов определяется по соотношению где r1, r2, …, rn — объемные (молярные, массовые) доли компонентов, входящих в смесь; Q1, Q2, …, Qn — теплота сгорания компонентов. Воспользовавшись табл. 8.1, высшую и низшую теплоту сгорания, кДж/м 3 , сложного газа можно определять по следующим формулам: где H2, CO, CH4 и т.д. — содержание отдельных составляющих в газовом топливе, об. %. Процесс горения протекает гораздо сложнее, чем по формуле (8.1), так как наряду с разветвлением цепей происходит их обрыв за счет образования промежуточных стабильных соединений, которые при высокой температуре претерпевают дальнейшие преобразования. При достаточной концентрации кислорода образуются конечные продукты: водяной пар Н2О и двуокись углерода СО2. При недостатке окислителя, а также при охлаждении зоны реакции, промежуточные соединения могут стабилизироваться и попадать в окружающую среду. Интенсивность тепловыделения и рост температуры приводят к увеличению в реагирующей системе активных частиц. Такая взаимосвязь цепного реагирования и температуры, свойственная практически всем процессам горения, привела к введению понятия цепочечно-теплового взрыва — сами химические реакции горения имеют цепной характер, а их ускорение происходит за счет выделения теплоты и роста температуры в реагирующей системе. Скорость химической реакции в однородной смеси пропорциональна произведению концентраций реагирующих веществ: где С1 и С2 — концентрации реагирующих компонентов, кмоль/м 3 ; k — константа скорости реакции, зависящая от природы реагирующих веществ и температуры. При сжигании газа концентрации реагирующих веществ можно условно считать неизменными, так как в зоне горения происходит непрерывный приток свежих компонентов однозначного состава. Константа скорости реакции (по уравнению Аррениуса): где К0 — предэкспоненциальный множитель, принимаемый для биометрических гомогенных смесей, ≈1,0; Е — энергия активации, кДж/кмоль; R — универсальная газовая постоянная, Дж/(кг•К); Т — абсолютная температура, К (°С); е — основание натуральных логарифмов. Предэкспоненциальный множитель К0 можно истолковать как константу, отражающую полноту столкновения молекул, а Е — как минимальную энергию разрыва связей молекул и образования активных частиц, обеспечивающих эффективность столкновений. Для распространенных горючих смесей она укладывается в пределах (80÷150)•10 3 кДж/кмоль. Уравнение (8.6) показывает, что скорость химических реакций резко возрастает с увеличением температуры: например, повышение температуры с 500 до 1000 К влечет повышение скорости реакции горения в 2•10 4 ÷5•10 8 раз (в зависимости от энергии активации). На скорость реакций горения влияет их цепной характер. Первоначально генерируемый реакцией атомы и радикалы вступают в соединения с исходными веществами и между собой, образуя конечные продукты и новые частицы, повторяющие ту же цепь реакций. Нарастающее генерирование таких частиц приводит к «разгону» химических реакций — фактически взрыву всей смеси. Высокотемпературное горение углеводородов имеет сложный характер и связано с образованием активных частиц в виде атомов и радикалов, а также промежуточных молекулярных соединений. В качестве примера приводятся реакции горения простейшего углеводорода — метана: Итог единичного цикла: 8.2. РАСЧЕТЫ ГОРЕНИЯКислород для горения поступает из воздуха как его составная часть. Для расчетов принимается, что объемный состав сухого воздуха следующий: кислород — 21,0%, азот — 79,0%. Согласно приведенным сведениям, 1 м 3 кислорода содержится в 100/21 = 4,76 м 3 воздуха, или на 1 м 3 кислорода приходится 79/21 = 3,76 м 3 азота. Учитывая, что 1 кмоль газа при нормальных условиях занимает объем 22,4 л, реакцию горения (см. уравнение 8.1) любого углеводорода в воздухе можно записать в обобщенном виде: Потребности в кислороде и воздухе при горении различных газов, подсчитанные по приведенным реакциям горения, представлены в табл. 8.2. Таблица 8.2. Теоретическая потребность в сухом кислороде и воздухе, м 3 , и объем продуктов сгорания газа при сжигании 1 м 3 газа
Для сложного газа расход сухого воздуха Vc, м 3 /м 3 , подсчитывается по формуле, учитывающей потребность в кислороде отдельных компонентов смеси: Теоретический расход влажного воздуха Vвл, м 3 /м 3 , больше определяемого по формуле (8.7) на объем содержащихся водяных паров: где dв — влажность воздуха, г/м 3 . При неизвестном химическом составе газов, но известной низшей теплоте сгорания Qн, кДж/м 3 , теоретический расход воздуха V т , м 3 /м 3 , Реальный расход воздуха Vдв, м 3 /м 3 , принимается всегда несколько большим: где α — коэффициент избытка воздуха, соответствующий требованиям ГОСТ. Для полного сгорания топлива значение α должно быть больше 1. Состав и объем продуктов сгорания, подсчитанный по реакциям горения некоторых газов в сухом воздухе, приведен в табл. 8.2. 8.3. ТЕМПЕРАТУРА ГОРЕНИЯВ теплотехнике различаются следующие температуры горения газов: жаропроизводительность, калориметрическую, теоретическую и действительную (расчетную). Жаропроизводительность tж — максимальная температура продуктов полного сгорания газа в адиабатических условиях с коэффициентом избытка воздуха α = 1,0 и при температуре газа и воздуха, равной 0°C: где Qн — низшая теплота сгорания газа, кДж/м 3 ; ∑Vcp — сумма произведений объемов диоксида углерода, водяного пара и азота, образовавшихся при сгорании 1 м 3 газа (м 3 /м 3 ), и их средних объемных теплоемкостей при постоянном давлении в пределах температур от 0°С до tж (кДж/(м 3 o°С). В силу непостоянства теплоемкости газов жаропроизводительность определяется методом последовательных приближений. В качестве начального параметра берется ее значение для природного газа (≈2000°С), при α = 1,0 определяются объемы компонентов продуктов сгорания, по табл. 8.3 находится их средняя теплоемкость и затем по формуле (8.11) считается жаропроизводительность газа. Если в результате подсчета она окажется ниже или выше принятой, то задается другая температура и расчет повторяется. Таблица 8.3. Средняя объемная теплоемкость газов, кДж/(м 3 •°С) | CO2 | N2 | O2 | CO | CH4 | H2 | H2O (водяные пары) | воздух | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| сухой | влажный на 1 м 3 сухого газа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 0 | 1,5981 | 1,2970 | 1,3087 | 1,3062 | 1,5708 | 1,2852 | 1,4990 | 1,2991 | 1,3230 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 100 | 1,7186 | 1,2991 | 1,3209 | 1,3062 | 1,6590 | 1,2978 | 1,5103 | 1,3045 | 1,3285 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 200 | 1,8018 | 1,3045 | 1,3398 | 1,3146 | 1,7724 | 1,3020 | 1,5267 | 1,3142 | 1,3360 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 300 | 1,8770 | 1,3112 | 1,3608 | 1,3230 | 1,8984 | 1,3062 | 1,5473 | 1,3217 | 1,3465 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 400 | 1,9858 | 1,3213 | 1,3822 | 1,3356 | 2,0286 | 1,3104 | 1,5704 | 1,3335 | 1,3587 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 500 | 2,0030 | 1,3327 | 1,4024 | 1,3482 | 2,1504 | 1,3104 | 1,5943 | 1,3469 | 1,3787 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 600 | 2,0559 | 1,3453 | 1,4217 | 1,3650 | 2,2764 | 1,3146 | 1,6195 | 1,3612 | 1,3873 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 700 | 2,1034 | 1,3587 | 1,3549 | 1,3776 | 2,3898 | 1,3188 | 1,6464 | 1,3755 | 1,4020 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 800 | 2,1462 | 1,3717 | 1,4549 | 1,3944 | 2,5032 | 1,3230 | 1,6737 | 1,3889 | 1,4158 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 900 | 2,1857 | 1,3857 | 1,4692 | 1,4070 | 2,6040 | 1,3314 | 1,7010 | 1,4020 | 1,4293 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1000 | 2,2210 | 1,3965 | 1,4822 | 1,4196 | 2,7048 | 1,3356 | 1,7283 | 1,4141 | 1,4419 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1100 | 2,2525 | 1,4087 | 1,4902 | 1,4322 | 2,7930 | 1,3398 | 1,7556 | 1,4263 | 1,4545 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1200 | 2,2819 | 1,4196 | 1,5063 | 1,4448 | 2,8812 | 1,3482 | 1,7825 | 1,4372 | 1,4658 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1300 | 2,3079 | 1,4305 | 1,5154 | 1,4532 | – | 1,3566 | 1,8085 | 1,4482 | 1,4771 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1400 | 2,3323 | 1,4406 | 1,5250 | 1,4658 | – | 1,3650 | 1,8341 | 1,4582 | 1,4876 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1500 | 2,3545 | 1,4503 | 1,5343 | 1,4742 | – | 1,3818 | 1,8585 | 1,4675 | 1,4973 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1600 | 2,3751 | 1,4587 | 1,5427 | – | – | – | 1,8824 | 1,4763 | 1,5065 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1700 | 2,3944 | 1,4671 | 1,5511 | – | – | – | 1,9055 | 1,4843 | 1,5149 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1800 | 2,4125 | 1,4746 | 1,5590 | – | – | – | 1,9278 | 1,4918 | 1,5225 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1900 | 2,4289 | 1,4822 | 1,5666 | – | – | – | 1,9698 | 1,4994 | 1,5305 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2000 | 2,4494 | 1,4889 | 1,5737 | 1,5078 | – | – | 1,9694 | 1,5376 | 1,5376 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2100 | 2,4591 | 1,4952 | 1,5809 | – | – | – | 1,9891 | – | – | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2200 | 2,4725 | 1,5011 | 1,5943 | – | – | – | 2,0252 | – | – | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2300 | 2,4860 | 1,5070 | 1,5943 | – | – | – | 2,0252 | – | – | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2400 | 2,4977 | 1,5166 | 1,6002 | – | – | – | 2,0389 | – | – | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2500 | 2,5091 | 1,5175 | 1,6045 | – | – | – | 2,0593 | – | – | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Жаропроизводительность распространенных простых и сложных газов при их горении в сухом воздухе приведена в табл. 8.4. При сжигании газа в атмосферном воздухе, содержащем около 1 вес. % влаги, жаропроизводительность снижается на 25–30°С.
Таблица 8.4. Жаропроизводительность газов в сухом воздухе
| Простой газ | Жаропроизводительность, °С | Сложный газ усредненного состава | Приближенная жаропроизводительность, °С | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Водород | 2235 | 2040 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Оксид углерода | 2370 | 2080 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Метан | 2043 | 2120 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Этан | 2097 | 1980 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Пропан | 2110 | 2050 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Бутан | 2118 | 1750 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Пентан | 2119 | 1670 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Этилен | 2284 | 2115 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ацетилен | 2620 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Коэффициент избытка воздуха α | Калориметрическая температура горения tк, °С | Теоретическая температура горения tт, °С | Коэффициент избытка воздуха α | Калориметрическая температура горения tк, °С |
|---|---|---|---|---|
| 1,0 | 2010 | 1920 | 1,33 | 1620 |
| 1,02 | 1990 | 1900 | 1,36 | 1600 |
| 1,03 | 1970 | 1880 | 1,40 | 1570 |
| 1,05 | 1940 | 1870 | 1,43 | 1540 |
| 1,06 | 1920 | 1860 | 1,46 | 1510 |
| 1,08 | 1900 | 1850 | 1,50 | 1470 |
| 1,10 | 1880 | 1840 | 1,53 | 1440 |
| 1,12 | 1850 | 1820 | 1,57 | 1410 |
| 1,14 | 1820 | 1790 | 1,61 | 1380 |
| 1,16 | 1800 | 1770 | 1,66 | 1350 |
| 1,18 | 1780 | 1760 | 1,71 | 1320 |
| 1,20 | 1760 | 1750 | 1,76 | 1290 |
| 1,22 | 1730 | – | 1,82 | 1260 |
| 1,25 | 1700 | – | 1,87 | 1230 |
| 1,28 | 1670 | – | 1,94 | 1200 |
| 1,30 | 1650 | – | 2,00 | 1170 |
Таблица 8.6. Калориметрическая температура горения природного газа tк, °С, в зависимости от коэффициента избытка сухого воздуха и его температуры (округленные значения)
| Коэффициент избытка воздуха α | Температура сухого воздуха, °С | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 20 | 100 | 200 | 300 | 400 | 500 | 600 | 700 | 800 | |
| 0,5 | 1380 | 1430 | 1500 | 1545 | 1680 | 1680 | 1740 | 1810 | 1860 |
| 0,6 | 1610 | 1650 | 1715 | 1780 | 1840 | 1900 | 1960 | 2015 | 2150 |
| 0,7 | 1730 | 1780 | 1840 | 1915 | 1970 | 2040 | 2100 | 2200 | 2250 |
| 0,8 | 1880 | 1940 | 2010 | 2060 | 2130 | 2200 | 2260 | 2330 | 2390 |
| 0,9 | 1980 | 2030 | 2090 | 2150 | 2220 | 2290 | 2360 | 2420 | 2500 |
| 1,0 | 2050 | 2120 | 2200 | 2250 | 2320 | 2385 | 2450 | 2510 | 2560 |
| 1,2 | 1810 | 1860 | 1930 | 2000 | 2070 | 2140 | 2200 | 2280 | 2350 |
| 1,4 | 1610 | 1660 | 1740 | 1800 | 2870 | 1950 | 2030 | 2100 | 2160 |
| 1,6 | 1450 | 1510 | 1560 | 1640 | 1730 | 1800 | 1860 | 1950 | 2030 |
| 1,8 | 1320 | 1370 | 1460 | 1520 | 1590 | 1670 | 1740 | 1830 | 1920 |
| 2,0 | 1220 | 1270 | 1360 | 1420 | 1490 | 1570 | 1640 | 1720 | 1820 |
Таблица 8.7. Калориметрическая температура горения tк технического пропана в сухом воздухе с t = 0°С в зависимости от коэффициента избытка воздуха α
| Коэффициент избытка воздуха α | Калориметрическая температура горения tк, °С | Коэффициент избытка воздуха α | Калориметрическая температура горения tк, °С |
|---|---|---|---|
| 1,0 | 2110 | 1,45 | 1580 |
| 1,02 | 2080 | 1,48 | 1560 |
| 1,04 | 2050 | 1,50 | 1540 |
| 1,05 | 2030 | 1,55 | 1500 |
| 1,07 | 2010 | 1,60 | 1470 |
| 1,10 | 1970 | 1,65 | 1430 |
| 1,12 | 1950 | 1,70 | 1390 |
| 1,15 | 1910 | 1,75 | 1360 |
| 1,20 | 1840 | 1,80 | 1340 |
| 1,25 | 1780 | 1,85 | 1300 |
| 1,27 | 1750 | 1,90 | 1270 |
| 1,30 | 1730 | 1,95 | 1240 |
| 1,35 | 1670 | 2,00 | 1210 |
| 1,40 | 1630 | 2,10 | 1170 |
Теоретическая температура горения tT — максимальная температура, определяемая аналогично калориметрической tк, но с поправкой на эндотермические (требующие теплоты) реакции диссоциации диоксида углерода и водяного пара, идущие с увеличением объема:
При высоких температурах диссоциация может привести к образованию атомарного водорода, кислорода и гидроксильных групп ОН. Кроме того, при сжигании газа всегда образуется некоторое количество оксида азота. Все эти реакции эндотермичны и приводят к снижению температуры горения.
Теоретическая температура горения может быть определена по следующей формуле:
где qдис — суммарные затраты теплоты на диссоциацию СО2 и Н2О в продуктах сгорания, кДж/м 3 ; ΣVcp — сумма произведения объема и средней теплоемкости продуктов сгорания с учетом диссоциации на 1 м 3 газа.
Таблица 8.8. Степень диссоциации водяного пара H2O и диоксида углерода CO2 в зависимости от парциального давления
| Температура, °С | Парциальное давление, МПа | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 0,004 | 0,006 | 0,008 | 0,010 | 0,012 | 0,014 | 0,016 | 0,018 | 0,020 | 0,025 | 0,030 | 0,040 | |
| Водяной пар H2O | ||||||||||||
| 1600 | 0,85 | 0,75 | 0,65 | 0,60 | 0,58 | 0,56 | 0,54 | 0,52 | 0,50 | 0,48 | 0,46 | 0,42 |
| 1700 | 1,45 | 1,27 | 1,16 | 1,08 | 1,02 | 0,95 | 0,90 | 0,85 | 0,8 | 0,76 | 0,73 | 0,67 |
| 1800 | 2,40 | 2,10 | 1,90 | 1,80 | 1,70 | 1,60 | 1,53 | 1,46 | 1,40 | 1,30 | 1,25 | 1,15 |
| 1900 | 4,05 | 3,60 | 3,25 | 3,0 | 2,85 | 2,70 | 2,65 | 2,50 | 2,40 | 2,20 | 2,10 | 1,9 |
| 2000 | 5,75 | 5,05 | 4,60 | 4,30 | 4,0 | 3,80 | 3,55 | 3,50 | 3,40 | 3,15 | 2,95 | 2,65 |
| 2100 | 8,55 | 7,50 | 6,80 | 6,35 | 6,0 | 5,70 | 5,45 | 5,25 | 5,10 | 4,80 | 4,55 | 4,10 |
| 2200 | 12,3 | 10,8 | 9,90 | 9,90 | 8,80 | 8,35 | 7,95 | 7,65 | 7,40 | 6,90 | 6,50 | 5,90 |
| 2300 | 16,0 | 15,0 | 13,7 | 12,9 | 12,2 | 11,6 | 11,1 | 10,7 | 10,4 | 9,6 | 9,1 | 8,4 |
| 2400 | 22,5 | 20,0 | 18,4 | 17,2 | 16,3 | 15,6 | 15,0 | 14,4 | 13,9 | 13,0 | 12,2 | 11,2 |
| 2500 | 28,5 | 25,6 | 23,5 | 22,1 | 20,9 | 20,0 | 19,3 | 18,6 | 18,0 | 16,8 | 15,9 | 14,6 |
| 3000 | 70,6 | 66,7 | 63,8 | 61,6 | 59,6 | 58,0 | 56,5 | 55,4 | 54,3 | 51,9 | 50,0 | 47,0 |
| Диоксид углерода CO2 | ||||||||||||
| 1500 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,5 | 0,4 | 0,4 | 0,4 | 0,4 | 0,4 | – |
| 1600 | 2,0 | 1,8 | 1,6 | 1,5 | 1,45 | 1,4 | 1,35 | 1,3 | 1,25 | 1,2 | 1,1 | |
| 1700 | 3,8 | 3,3 | 3,0 | 2,8 | 2,6 | 2,5 | 2,4 | 2,3 | 2,2 | 2,0 | 1,9 | |
| 1800 | 6,3 | 5,5 | 5,0 | 4,6 | 4,4 | 4,2 | 4,0 | 3,8 | 3,7 | 3,5 | 3,3 | |
| 1900 | 10,1 | 8,9 | 8,1 | 7,6 | 7,2 | 6,8 | 6,5 | 6,3 | 6,1 | 5,6 | 5,3 | |
| 2000 | 16,5 | 14,6 | 13,4 | 12,5 | 11,8 | 11,2 | 10,8 | 10,4 | 10,0 | 9,4 | 8,8 | |
| 2100 | 23,9 | 21,3 | 19,6 | 18,3 | 17,3 | 16,5 | 15,9 | 15,3 | 14,9 | 13,9 | 13,1 | |
| 2200 | 35,1 | 31,5 | 29,2 | 27,5 | 26,1 | 25,0 | 24,1 | 23,3 | 22,6 | 21,2 | 20,1 | |
| 2300 | 44,7 | 40,7 | 37,9 | 35,9 | 34,3 | 32,9 | 31,8 | 30,9 | 30,0 | 28,2 | 26,9 | |
| 2400 | 56,0 | 51,8 | 48,8 | 46,5 | 44,6 | 43,1 | 41,8 | 40,6 | 39,6 | 37,5 | 35,8 | |
| 2500 | 66,3 | 62,2 | 59,3 | 56,9 | 55,0 | 53,4 | 52,0 | 50,7 | 49,7 | 47,3 | 45,4 | |
| 3000 | 94,9 | 93,9 | 93,1 | 92,3 | 91,7 | 90,6 | 90,1 | 89,6 | 88,5 | 87,6 | 86,8 | |
Как видно из табл. 8.8, при температуре до 1600°С степень диссоциации может не учитываться, и теоретическую температуру горения может принять равной калориметрической. При более высокой температуре степень диссоциации может существенно снижать температуру в рабочем пространстве. На практике особой необходимости в этом нет, теоретическую температуру горения необходимо определять только для высокотемпературных печей, работающих на предварительно нагретом воздухе (например, мартеновских). Для котельных установок в этом нужды нет.
Таблица 8.9. Максимальные
температуры, возникающие
в свободном пламени, °С
Действительная (расчетная) температура продуктов сгорания tд — температура, которая достигается в реальных условиях в самой горячей точке факела. Она ниже теоретической и зависит от потерь теплоты в окружающую среду, степени отдачи теплоты из зоны горения излучением, растянутости процесса горения во времени и др. Действительные усредненные температуры в топках печей и котлов определяются по тепловому балансу или приближенно по теоретической или калориметрической температуре горения в зависимости от температуры в топках с введением в них экспериментально установленных поправочных коэффициентов:
где η— т.н. пирометрический коэффициент, укладывающийся в пределах:
- для качественно выполненных термических и нагревательных печей с теплоизоляцией — 0,75–0,85;
- для герметичных печей без теплоизоляции — 0,70–0,75;
- для экранированных топок котлов — 0,60–0,75.
В практике надо знать не только приведенные выше адиабатные температуры горения, но и максимальные температуры, возникающие в пламени. Их приближенные значения обычно устанавливают экспериментально методами спектрографии. Максимальные температуры, возникающие в свободном пламени на расстоянии 5–10 мм от вершины конусного фронта горения, приведены в табл. 8.9. Анализ приведенных данных показывает, что максимальные температуры в пламени меньше жаропроизводительности (за счет затрат тепла на диссоциацию Н2О и СО2 и отвода теплоты из пламенной зоны).
8.4. ТЕМПЕРАТУРА САМОВОСПЛАМЕНЕНИЯ
Для инициирования реакций горения нужны условия воспламенения смеси топлива с окислителем. Воспламенение может быть самопроизвольным и вынужденным (зажигание).
Температура самовоспламенения — минимальная температура, при которой в нагретой газовоздушной смеси начинается самопроизвольный (т.е. без внешнего подвода теплоты) процесс горения, за счет выделения теплоты горящими частицами газа.
Температура самовоспламенения не является фиксированной для данного газа и зависит от многих параметров: его содержания в газовоздушной смеси, степени однородности смеси, формы и размеров сосуда, в котором смесь нагревается, быстроты и способа ее нагрева, каталитического влияния стенок сосуда, давления, под которым находится смесь. Точный учет перечисленных факторов весьма сложен, поэтому на практике, например, при оценке взрывоопасности, пользуются экспериментальными данными (см. табл. 8.10).
Таблица 8.10. Наименьшие измеренные температуры самовоспламенения некоторых газов и паров в смеси с воздухом при атмосферном давлении
| Газ | Температура самовоспламенения, °С | Газ | Температура самовоспламенения, °С | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Водород | 530 | 455 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Оксид углерода | 610 | 455 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Метан | 650 | 455 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Этан | 510 | 335 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Пропан | 500 | 290 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Бутан | 429 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Газ | Содержание газа в газовоздушной смеси, об. % | Коэффициент избытка воздуха α при пределах воспламенения | |||||
|---|---|---|---|---|---|---|---|
| При пределах воспламеняемости | При стехиометрическом составе смеси | При составе смеси, дающем максимальное давление взрыва | |||||
| нижнем | верхнем | нижнем | верхнем | ||||
| Водород | 4,0 | 75,0 | 29,5 | 32,3 | 0,739 | 9,8 | 0,15 |
| Оксид углерода | 12,5 | 74,0 | 29,5 | – | – | 2,9 | 0,15 |
| Метан | 5,0 | 15,0 | 9,5 | 9,8 | 0,717 | 1,8 | 0,65 |
| Этан | 3,2 | 12,5 | 5,68 | 6,28 | 0,725 | 1,9 | 0,42 |
| Пропан | 2,3 | 9,5 | 4,04 | 4,60 | 0,858 | 1,7 | 0,40 |
| н-Бутан | 1,7 | 8,5 | 3,14 | 3,6 | 0,858 | 1,7 | 0,35 |
| Изобутан | 1,8 | 8,4 | 3,14 | – | – | 1,8 | 0,35 |
| н-Пентан | 1,4 | 7,8 | 2,56 | 3,0 | 0,865 | 1,8 | 0,31 |
| Этилен | 3,0 | 16,0 | 6,5 | 8,0 | 0,886 | 2,2 | 0,17 |
| Пропилен | 2,4 | 10,0 | 4,5 | 1,9 | 0,37 | ||
| Бутилен | 1,7 | 9,0 | 3,4 | 1,7 | 0,35 | ||
| Ацетилен | 2,5 | 80,0 | 7,75 | 14,5 | 1,03 | 3,3 | 0,019 |
Таблица 8.12. Пределы воспламеняемости газов в смеси с кислородом (при t = 20°C и p = 101,3 кПа)
| Газ | Содержание газа в газокислородной смеси, об. %, при пределах воспламеняемости | |
|---|---|---|
| нижнем | верхнем | |
| Водород | 4,0 | 94,0 |
| Оксид углерода | 12,5 | 94,0 |
| Метан | 5,0 | 6,0 |
| Этан | 3,0 | 56,0 |
| Пропан | 2,2 | 55,0 |
| н-Бутан | 1,7 | 49,0 |
| Изобутан | 1,7 | 49,0 |
| Этилен | 3,0 | 80,0 |
| Пропилен | 2,0 | 53,0 |
| Бутилен | 1,47 | 50,0 |
| Ацетилен | 2,5 | 89,0 |
Пределы воспламеняемости для распространенных газов в смесях с воздухом и кислородом приведены в табл. 8.11–8.12. С увеличением температуры смеси пределы воспламеняемости расширяются, а при температуре, превышающей температуру самовоспламенения, смеси газа с воздухом или кислородом горят при любом объемном соотношении.
Пределы воспламеняемости зависят не только от видов горючих газов, но и от условий проведения экспериментов (вместимости сосуда, тепловой мощности источника зажигания, температуры смеси, распространения пламени вверх, вниз, горизонтально и др.). Этим объясняются несколько отличающиеся друг от друга значения этих пределов в различных литературных источниках. В табл. 8.11–8.12 приведены сравнительно достоверные данные, полученные при комнатной температуре и атмосферном давлении при распространении пламени снизу вверх в трубке диаметром 50 мм и более. При распространении пламени сверху вниз или горизонтально нижние пределы несколько возрастают, а верхние снижаются. Пределы воспламеняемости сложных горючих газов, не содержащих балластных примесей, определяются по правилу аддитивности:
где Lг — нижний или верхний предел воспламеняемости сложного газа в газовоздушной или газокислородной смеси, об. %; r1, r2, …, rn — содержание отдельных компонентов в сложном газе, об. %; r1 + r2 + … + rn = 100%; l1, l2, …, ln — нижние или верхние пределы воспламеняемости отдельных компонентов в газовоздушной или газокислородной смеси по данным табл. 8.11 или 8.12, об. %.
При наличии в газе балластных примесей пределы воспламеняемости могут быть определены по формуле:
где Lб — верхний и нижний пределы воспламеняемости смеси с балластными примесями, об. %; Lг — верхний и нижний пределы воспламеняемости горючей смеси, об. %; Б — количество балластных примесей, доли единицы.
При расчетах часто необходимо знать коэффициент избытка воздуха α при разных пределах воспламеняемости (см. табл. 8.11), а также давление, возникающее при взрыве газовоздушной смеси. Коэффициент избытка воздуха, соответствующий верхнему или нижнему пределам воспламеняемости, можно определить по формуле
Давление, возникающее при взрыве газовоздушных смесей, можно определить с достаточным приближением по следующим формулам:
для стехиометрического соотношения простого газа с воздухом:
для любого соотношения сложного газа с воздухом:
где Рвз — давление, возникающее при взрыве, МПа; рн — начальное давление (до взрыва), МПа; β — коэффициент объемного расширения газов, численно равный коэффициенту давления (1/273); tK — калориметрическая температура горения, °С; m — число молей после взрыва, определяемое по реакции горения газа в воздухе; п — число молей до взрыва, участвующих в реакции горения; Vвлпс — объем влажных продуктов сгорания на 1 м 3 газа, м 3 ; Vт — теоретический расход воздуха, м 3 /м 3 .
Таблица 8.13. Давление, возникающее при взрыве пропанововоздушной смеси, в зависимости от коэффициента сброса kсб и вида защитного устройства
| Вид защитного устройства | Коэффициент сброса kсб, м 2 /м 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 0,063 | 0,033 | 0,019 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Одинарное глухое остекление с наружным креплением стекла толщиной 3 мм | 0,005 | 0,009 | 0,019 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Двойное глухое остекление с наружным креплением стекла толщиной 3 мм | 0,007 | 0,015 | 0,029 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Поворотный одинарный оконный переплет с большим шарниром и пружинным замком на нагрузку 5 МПа/м 2 | 0,002 | – | – | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Поворотный одинарный оконный переплет с верхним шарниром и пружинным замком на нагрузку 5 МПа/м 2 | 0,003 | – | – | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Свободно лежащие на перекрытии плиты массой, кг/ м 2 : | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Газ | Смесь с максимальной нормальной скоростью распространения пламени | Стехиометрическая смесь | ||||
|---|---|---|---|---|---|---|
| Содержание в смеси, об. % | Максимальная нормальная скорость распространения | Содержание в смеси, об. % | Нормальная скорость распространения пламени | |||
| газа | воздуха | газа | воздуха | |||
| Водород | 42,0 | 58,0 | 2,67 | 29,5 | 70,5 | 1,6 |
| Оксид углерода | 43,0 | 57,0 | 0,42 | 29,5 | 70,5 | 0,30 |
| Метан | 10,5 | 89,0 | 0,37 | 9,5 | 90,5 | 0,28 |
| Этан | 6,3 | 93,7 | 0,40 | 5,7 | 94,3 | 0,32 |
| Пропан | 4,3 | 95,7 | 0,38 | 4,04 | 95,96 | 0,31 |
| н-Бутан | 3,3 | 96,7 | 0,37 | 3,14 | 96,86 | 0,30 |
| Этилен | 7,0 | 93,0 | 0,63 | 6,5 | 93,5 | 0,5 |
| Пропилен | 4,8 | 95,2 | 0,44 | 4,5 | 95,5 | 0,37 |
| Бутилен | 3,7 | 96,3 | 0,43 | 3,4 | 96,6 | 0,38 |
| Ацетилен | 10,0 | 90,0 | 1,35 | 7,75 | 92,25 | 1,0 |
Как видно из данных табл. 8.14, максимальная скорость распространения пламени соответствует смесям газа и воздуха с недостатком окислителя (не стехиометрическим). При избытке горючего повышается эффективность столкновения реагирующих частиц и скорость химических реакций возрастает.
Скорости распространения пламени для газокислородных смесей на порядок выше, чем для газовоздушных. Так, максимальная нормальная скорость распространения пламени метано-кислородной смеси — 3,3 м/с, а для смеси пропана и бутана с кислородом — 3,5–3,6 м/с.
Максимальная нормальная скорость распространения пламени в смеси сложного газа с воздухом, м/с, определяется по формуле:
где r1, r2,…rn — содержание отдельных компонентов в сложном газе, об. %; u1, u2. un — максимальные нормальные скорости распространения пламени компонентов сложного газа в смеси с воздухом, м/с.
Приведенные соотношения пригодны для газов, обладающих близкими нормальными скоростями распространения пламени, например, для природных и сжиженных углеводородных газов. Для смесей газов, обладающих резко различными скоростями распространения пламени (например, для смесей природных и искусственных газов, смесей с высоким содержанием водорода), они дают только приближенные значения.
Если же в смеси присутствуют балластные примеси (азот и диоксид углерода), то для приближенного расчета скорости распространения пламени следует воспользоваться формулой:
Значительно повышает скорость распространения пламени подогрев газовоздушной смеси:
где и‘н — скорости распространения пламени в нагретой смеси с абсолютной температурой Т‘, К; ин — то же, в холодной смеси с температурой Т, К.
Предварительный нагрев смеси изменяет ее плотность обратно пропорционально абсолютной температуре, поэтому и скорости распространения пламени растут пропорционально этой температуре. Этот факт надо учитывать при расчетах, особенно в тех случаях, когда огневые каналы горелок располагаются в нагретой кладке или когда на них воздействует излучение топки, раскаленных газов и т.п.
Равномерность распространения пламени возможна при выполнении следующих условий:
- огневая трубка имеет небольшую длину;
- горение распространяется при постоянном давлении, близком к атмосферному.
Если длина трубки значительна, то равномерное распространение пламени для некоторых смесей может перейти в вибрационное, а затем — и в детонационное со сверхзвуковой скоростью горения (2000 м/с и более), когда воспламенение смеси происходит за счет ударной волны, нагревающей смесь до температур, превышающих температуру самовоспламенения. Детонация возникает в смесях, обладающих высокими скоростями распространения пламени. Пределы концентрации детонации уже пределов воспламеняемости газовоздушных и газокислородных смесей, об. %: пропан — 3,2–37, изобутан — 2,8–31, водород — 15–90. Давление, возникающее при детонационном горении, может превышать начальное в десятки раз и приводить к разрушению труб и других сосудов, рассчитанных на высокие давления.
8.7. ГОРЕНИЕ В ЛАМИНАРНОМ И турбулентном ПОТОКах
Рис. 8.3. Фронт горения
газовоздушной смеси в
ламинарном режиме движения
Фронт пламени может быть остановлен, если создать встречное движение горючей смеси со скоростью, равной нормальной скорости распространения пламени. Наглядный пример — поверхность внутреннего конуса бунзеновской горелки. За счет регулирования состава газовоздушной смеси, вытекающей из горелки при ламинарном режиме движения, можно добиться появления устойчивого и резко очерченного конуса горения (рис. 8.3). Боковая поверхность конуса (фронт пламени), неподвижная относительно огневой кромки канала горелки, движется по направлению к вытекающей газовоздушной смеси, а пламя в этом случае распространяется по нормали к поверхности воспламенения в каждой ее точке. На поверхности конусного фронта пламени сохраняется равенство скоростей — проекции скорости потока газовоздушной смеси на нормаль wн к образующей конуса и нормальной скорости распространения пламени uн подчиняются закону Михельсона:
где φ — угол между направлением потока и нормалью к поверхности конусного фронта пламени; wпот — средняя скорость потока газовоздушной смеси, проходящей через горелку за единицу времени, м/с.
Постоянство нормальной скорости распространения пламени справедливо только для основной части боковой поверхности конусного фронта пламени. В вершине конуса скорость увеличивается благодаря прогреву газовоздушной смеси близко расположенными участками конусной поверхности фронта пламени, а у основания конуса — снижается за счет охлаждающего воздействия торцевой части огневого канала горелки.
Для практических расчетов обычно пренебрегают этой разницей и принимают скорость прохождения смеси через фронт пламени постоянной по всей поверхности конуса и равной uн.
Усредненная нормальная скорость распространения пламени равна
где Vсм — объем проходящей через горелку газовоздушной смеси, S — площадь поверхности конусного фронта пламени.
На практике конусный фронт пламени не имеет правильной геометрической формы, поэтому для точного определения S пламя фотографируют, фронт пламени разбивается на ряд усеченных конусов. Сумма боковых поверхностей и есть общая поверхность конусного фронта пламени. Значения нормальных скоростей распространения пламени, определенные как методом бунзеновской горелки, так и другими методами, одинаковы и равны нормальным скоростям, приведенным в табл. 8.14.
Высота конусного фронта пламени зависит в основном от размера огневого канала горелки. Уменьшение высоты пламени может достигаться дроблением крупных огневых каналов на несколько мелких. Для одинаковых по составу газовоздушных смесей высота конусных фронтов пламени малых каналов h может быть приближенно определена по высоте фронта пламени одиночного канала Н:
где n — число малых каналов.
Для горелок с высокой тепловой мощностью (горелки промышленных котлов, печей и т.п.) горение, как правило, происходит в турбулентном потоке — гладкий конусный фронт пламени из-за вихревого движения и пульсаций размывается и теряет четкие конусные очертания. При этом наблюдаются два характерных вида горения, соответствующие мелкои крупномасштабной турбулентности.
При масштабах турбулентности, не превышающих толщину зоны ламинарного горения, конусный фронт пламени сохраняет свою форму и остается гладким, хотя зона горения увеличивается. Если же масштаб турбулентности превышает толщину зоны нормального горения, поверхность конусного фронта пламени становится неровной. Это ведет к увеличению суммарной поверхности фронта горения и сжиганию большего количества горючей смеси на единицу поперечного сечения потока.
При крупномасштабной турбулентности, значительно превышающей толщину зоны ламинарного горения, волнение поверхности фронта пламени приводит к отрыву отдельных частиц горячей смеси, дробящихся последующими пульсациями. Фронт пламени теряет свою целостность и превращается в систему отдельных очагов горения в виде равных, расчленяющихся и сгорающих в потоке частиц горючей смеси.
Рис. 8.4. Изменение относительной скорости
распространения пламени коксового газа
в смеси с воздухом в зависимости от числа
Рейнольдса и режима движения смеси
При крупномасштабной турбулентности поверхность фронта пламени, слагаясь из поверхностей всех горящих частиц, увеличивается, приводя к резкому росту скорости распространения пламени (рис. 8.4). В этом случае может происходить не только фронтовое горение, распространяющееся с нормальной скоростью vn, но и объемное, возникающее за счет турбулентных пульсаций раскаленных продуктов горения в свежую смесь. Следовательно, суммарная скорость распространения пламени при крупномасштабной турбулентности определяется тем или иным сочетанием элементов фронтового и объемного горения.
При отсутствии пульсаций турбулентная скорость горения становится равной нормальной скорости распространения пламени. Наоборот, если пульсационная скорость значительно превышает нормальную, турбулентная скорость горения становится мало зависящей от физико-химических свойств горючей смеси. Эксперименты показали малую зависимость скорости сгорания различных гомогенных газовоздушных смесей с α>1 в промышленных топках от нормальной скорости распространения пламени.
8.8. УСТОЙЧИВОСТЬ ГОРЕНИЯ
Рис. 8.5. Схема прямой компенсации
uн=wпот при ламинарном движении
газовоздушной смеси
1 – стенка горелки;
2 – фронт пламени
Основные факторы, влияющие на устойчивость горения, — скорости истечения газовоздушной смеси и распространения пламени. При горении газовоздушных смесей в ламинарном потоке устойчивой частью конусного фронта пламени является его нижняя часть. В этом месте фронт пламени за счет расширения вытекающей в атмосферу газовоздушной смеси и тормозящего действия стенки канала развернут на горизонталь и приподнят над кромкой канала на толщину фронта пламени (рис. 8.5).
На данном участке фронта происходит полная компенсация скорости газовоздушного потока скоростью распространения пламени uн = wпот . На всем остальном конусном участке фронта пламени компенсация имеет частичный характер и осуществляется только в направлении, нормальном к фронту горения: uн = wпот cosφ . Cоставляющая wпот sinφ остается неуравновешенной и сносит точку воспламенения от основания конуса к его вершине. Cтабильность конусного фронта пламени объясняется тем, кольцевой пояс у основания служит источником зажигания, без которого остальная часть фронта была бы снесена потоком газовоздушной смеси.
Если скорость истечения смеси превышает скорость распространения пламени, ширина зажигающего пояска уменьшается, пока не станет ничтожно малой. В этом случае устойчивость фронта пламени нарушается, и происходит отрыв от горелки. Если же скорость распространения пламени в кольцевой пристенной области (не на стенке) превысит скорость истечения газовоздушной смеси, пламя втягивается внутрь смесителя горелки (проскок).
При отрыве наблюдаются:
- срыв пламени с горелки и его погасание;
- отрыв от кромки огневого канала, когда пламя достигает нового достаточно устойчивого положения в потоке над горелкой;
- срыв поднятого пламени и его погасание;
- отброс приподнятого факела к кромке огневого канала горелки;
- создание взвешенного пламени при поджигании струи на некотором расстоянии от горелки.
Все эти явления недопустимы, так как приводят к накоплению в окружающей атмосфере или в топке несгоревшего газа.
На рис. 8.6 показаны экспериментальные кривые отрыва пламени от кромок огневых каналов инжекционных однофакельных горелок, работающих на смеси холодного газа с воздухом. На границе и выше указанных кривых начинается отрыв пламени, а ниже кривых — устойчивое горение.
В практике широко распространены многофакельные инжекционные горелки с огневыми каналами диаметром 2–6 мм (рис. 8.7). Установление скоростей отрыва пламени wотр для таких горелок может производиться по следующей формуле:
где dk — диаметр огневых каналов, м; α1 — коэффициент избытка первичного воздуха; T — абсолютная температура газовоздушной смеси, К.
По формуле видно, что стабильность горения растет с увеличением диаметров огневых каналов и температуры и снижается с увеличением коэффициента избытка первичного воздуха. Стабильность горения повышается также за счет взаимного влияния пламени.
Отрыв пламени от огневых каналов может происходить и в силу других причин. При неправильном расположении горелки и каналов отвода продуктов сгорания они могут попасть в инжектор горелки и привести к отрыву пламени (за счет снижения скорости распространения пламени в газовоздушной смеси, разбавленной инертными газами). Также причиной отрыва может быть высокая скорость вторичного воздуха, сдувающего пламя с огневых каналов.
Таблица 8.15. Скорость гомогенной смеси природного
газа с воздухом, при которой происходит проскок
пламени, м/с (температура смеси 20°С)
| Диаметры огневых каналов | Коэффициент избытка первичного воздуха | |||||
|---|---|---|---|---|---|---|
| 0,6 | 0,7 | 0,8 | 0,9 | 1,0 | 1,1 | |
| 3,5 | 0,05 | 0,10 | 0,18 | 0,22 | 0,23 | 0,21 |
| 4,0 | 0,08 | 0,12 | 0,22 | 0,25 | 0,26 | 0,20 |
| 5,0 | 0,09 | 0,16 | 0,27 | 0,31 | 0,31 | 2,23 |
| 6,0 | 0,11 | 0,18 | 0,32 | 0,38 | 0,39 | 0,26 |
| 7,0 | 0,13 | 0,22 | 0,38 | 0,44 | 0,45 | 0,30 |
| 8,0 | 0,15 | 0,25 | 0,43 | 0,50 | 0,52 | 0,35 |
| 9,0 | 0,17 | 0,28 | 0,48 | 0,57 | 0,58 | 0,39 |
| 10,0 | 0,20 | 0,30 | 0,54 | 0,64 | 0,65 | 0,43 |
Недопустим также и проскок пламени внутрь смесителя горелки, обычно сопровождающийся хлопком. Проскок приводит либо к погасанию пламени и выбросу несгоревшей смеси в помещение или топку, либо к горению смеси внутри горелки. Тенденция пламени к проскоку зависит от вида газа, нормальной скорости распространения пламени, содержания первично го воздуха в газовоздушной смеси, размеров огневых каналов, температур смеси или стенок каналов. Влияние на проскок пламени оказывают также коэффициент теплопроводности материалов, из которых выполнены огневые каналы, их форма, глубина и качество изготовления, наличие заусениц, обломов краев и т. п.
Приведенные в табл. 8.15 значения скоростей гомогенных смесей природных газов с воздухом, при которых происходит проскок, можно использовать и для других газов с учетом поправок:
где w‘пр — скорость проскока пламени для другого газа, м/с; wпр — скорость проскока для природного газа (по табл. 8.15), м/с; u‘н — нормальная скорость распространения пламени для другого газа, м/с; uн — скорость распространения пламени в метане, м/с.
Максимальная же скорость проскока может быть рассчитана по приближенной формуле:
Этой же формулой с достаточным для практики приближением можно руководствоваться и для других газов с введением поправки на изменение нормальной скорости pacпpocтранения пламени. На основании многочисленных экспериментов можно сделать следующий вывод: пределы устойчивой работы горелок ограничены скоростями отрыва и проскока пламени.
На рис. 8.8 приведены кривые, характеризующие скорости потока смеси природного газа с воздухом, при которых происходят отрыв и проскок пламени. Характер кривых свидетельствует о резком снижении устойчивости пламени по мере увеличения содержания в смеси первичного воздуха. Повышение устойчивости пламени происходит при снижении содержания первичного воздуха и достигает максимума при его уменьшении до нуля (диффузионное горение). Однако такое сжигание углеводородных газов во многих случаях недопустимо, так как приводит к появлению желтых язычков пламени, характеризующих появление в нем сажистых частиц.
Рис. 8.9. Распространенные стабилизаторы горения
а – цилиндрический туннель с внезапным расширением сечения;
б – то же, при закрученом потоке;
в – конический туннель при закрученном потоке;
г – стабилизатор в виде конического тела;
д – то же, в виде круглого стержня;
е – то же, в виде устойчивого кольцевого пламени
1 – огневой насадок горелки; 2 – туннель; 3 – боковое отверстие;
4 – кольцевой канал; 5 – кольцевое пламя;
6 – пламя основного потока газовоздушной смеси
В практике для расширения диапазона устойчивости горения любых горючих газовоздушных смесей скорость потока принимается в несколько раз большей, чем скорость отрыва. Предотвращение отрыва пламени достигается применением стабилизаторов горения (рис. 8.9).
Для стабилизации пламени инжекционных и других горелок, выдающих осесимметричные газовоздушные струи, применяются огнеупорные цилиндрические туннели с внезапным расширением их сечения. Действие такого туннеля основано на периферийной циркуляции части раскаленных продуктов горения, возникающей за счет создаваемого струей разрежения.
Для стабилизации пламени горелок, выдающих закрученную газовоздушную смесь, применяются как цилиндрические, так и конические туннели с углом раскрытия 30–60°. При закрученном потоке на периферии туннеля возникает большее давление, чем в его центральной части. Это приводит к приосевой рециркуляции части раскаленных продуктов горения и поджиганию втекающей в туннель холодной газовоздушной смеси изнутри.
Когда установка туннелей невозможна, для стабилизации пламени применяют тела плохо обтекаемой формы, размещаемые в потоке газовоздушной смеси на выходе ее из огневого канала горелки. Воспламенение смеси при этом происходит на периферии стабилизатора, за которым возникает частичная рециркуляция раскаленных газов, поджигающих горючую смесь изнутри. Стабилизирующее действие таких устройств ниже, чем туннелей.
В инжекционных однои многофакельных горелках широко используются стабилизаторы горения в виде специальной огневой насадки. Стабилизирующее действие этого устройства основано на предотвращении разбавления основного потока в корне факела избыточным воздухом, сужающим пределы его устойчивости, а также на подогреве и поджигании кольцевым пламенем основного потока по всей его периферии. Устойчивость кольцевого пламени при отрыве достигается за счет такого соотношения сечений огневого кольца и боковых отверстий, при котором скорость газовоздушной смеси в кольцевой полости не превышает нормальной скорости распространения пламени. Для предотвращения проскока пламени в смеситель горелки размеры боковых отверстий, формирующих кольцевое пламя, принимаются меньшими критических.
8.9. СХЕМЫ ОГНЕПРЕГРАДИТЕЛЕЙ
Воздух или кислород, попав в газопровод, может образовать взрывчатую смесь, поэтому необходимо обязательно предохранять трубопроводы от проникновения в него воздуха или кислорода. На всех взрывоопасных производствах должны быть созданы условия, исключающие возможность возникновения поджигающих импульсов. Источниками воспламенения, приводящими газовоздушные смеси к взрыву, являются:
- открытое пламя;
- электрические разряды действующего электрооборудования;
- короткое замыкание в электрических проводах;
- искрение в электрических приборах;
- перегорание открытых предохранителей;
- разряды статического электричества.
Взрывобезопасность обеспечивается различными огнепреградителями. устанавливаемыми в трубопроводах, на резервуарах, на продувочных газопроводах, свечах и других системах, где существует опасность взрыва.
Погасание пламени в канале, заполненном горючей смесью, происходит лишь при минимальном диаметре канала, зависящем от химического состава и давления смеси, и объясняется потерями теплоты из зоны реакции к стенкам канала. При уменьшении диаметра канала увеличивается его поверхность на единицу массы реагирующей смеси, т.е. возрастают теплопотери. Когда они достигают критического значения, скорость реакции горения уменьшается настолько, что дальнейшее распространение пламени становится невозможным.
Пламегасящая способность огнепреградителя зависит в основном от диаметра гасящих каналов и гораздо меньше — от их длины, а возможность проникновения пламени через гасящие каналы зависит в основном от свойств и состава горючей смеси и давления. Нормальная скорость распространения пламени является основной величиной, определяющей размер гасящих каналов и выбор типа огнепреградителя: чем она больше, тем меньшего размера канал требуется для гашения пламени. Также размеры гасящих каналов зависят от начального давления горючей смеси. Для оценки пламегасящей способности огнепреградителей применяется т.н. критерий Пекле Ре:
В пределе гашения пламени формула критерий Пекле принимает вид:
где wсм— нормальная скорость распространения пламени; d — диаметр гасящего канала; dкp — критический диаметр гасящего канала; ср — удельная теплоемкость газа при 0°С и постоянном давлении; р — давление газа; ркр — критическое давление газа; R — универсальная газовая постоянная; Т0 — абсолютная температура газа; λ0 — теплопроводность исходной смеси.
Таким образом, для расчета пламегасящей способности огнепреградителей необходимы следующие исходные данные:
- нормальные скорости распространения пламени горючих газовых смесей;
- фактический размер максимальных гасящих каналов данного огнепреградителя.
Если полученное значение больше Рекр = 65, огнепреградитель не задержит распространения пламени данной горючей смеси, и наоборот, если Ре 2,0 (8.34)
Использовав факт постоянства Рекр на пределе гашения пламени, можно вычислить ориентировочный критический диаметр каналов для любой горючей смеси, если известны скорость распространения пламени, а также теплоемкость и теплопроводность газовой системы. Рекомендуются следующие критические диаметры гасящего канала, мм:
- при сжигании газовоздушной смеси — 2,9 для метана и 2,2 для пропана и этана;
- при сжигании кислородных смесей в трубах (при абсолютном давлении 0,1 МПа в условиях свободного расширения продуктов сгорания) — 1,66 для метана и 0,39 для пропана и этана.
Конструктивно огнепреградители делятся на четыре типа (рис. 8.10):
- с насадкой из гранулированных материалов;
- с прямыми каналами;
- из металлокерамики или металловолокна;
- сетчатые.
По способу установки — на три типа: на трубах для выброса газов в атмосферу или на факел; на коммуникациях; перед газогорелочными устройствами.
В корпусе насадочного огнепреградителя между решетками находится насадка с наполнителем (стеклянные или фарфоровые шарики, гравий, корунд и другие гранулы из прочного материала). Кассетный огнепреградитель представляет собой корпус, в который вмонтирована огнепреграждающая кассета из гофрированной и плоской металлических лент, плотно свитых в рулон. В корпусе пластинчатого огнепреградителя — пакет из плоскопараллельных металлических пластин со строго определенным расстоянием между ними. У сетчатого огнепреградителя в корпусе размещен пакет из плотно сжатых металлических сеток. Металлокерамический огнепреградитель представляет собой корпус, внутри которого установлена пористая металлокерамическая пластина в виде плоского диска или трубки.
Чаще всего применяются сетчатые огнепреградители (их начали устанавливать еще в начале XIX века в шахтерских лампах (лампах Деви) для предотвращения взрывов рудничного газа). Эти огнепреградители рекомендуются для защиты установок, в которых сжигается газовое топливо. Огнепреграждающий элемент состоит из нескольких слоев латунной сетки с размером ячеек 0,25 мм, зажатых между двумя перфорированными пластинами. Пакет сеток укреплен в съемной обойме.
Корпус огнепреградителя изготовлен из чугунного или алюминиевого сплава и состоит из двух одинаковых частей, соединенных болтами с расположенной между ними съемной обоймой. Кроме рассмотренных сухих огнепреградителей, широко применяются жидкостные предохранительные затворы, предохраняющие газопроводы от попадания взрывной волны и пламени при газопламенной обработке металлов, а также трубопроводы и аппараты, заполненные газом, от проникновения в них кислорода и воздуха.
Жидкостные затворы должны:
- препятствовать распространению взрывной волны при обратных ударах и при воспламенении газов;
- предохранять газопровод от попадания в него кислорода и воздуха;
- обеспечивать минимальное гидравлическое сопротивление прохождению потока газа. Кроме того, жидкость из затвора не должна уноситься в виде капель в заметных количествах.
8.10. ПРИНЦИПЫ СЖИГАНИЯ
В основе процессов сжигания газа — принципы, условно называемые кинетическим и диффузионным. При к и н е т и ч е с к о м принципе до начала горения создается однородная смесь с некоторым избытком воздуха. Сгорание такой смеси происходит в коротком прозрачном факеле без образования в пламени частиц сажи. Для сжигания газа по кинетическому принципу применяются специальные смесители или инжекционные горелки, подготавливающие гомогенную газовоздушную смесь с коэффициентом избытка первичного воздуха α1 = 1,02:1,05.
При меньшем содержании первичного воздуха по кинетическому принципу протекает только начальная стадия горения, до использования кислорода, находящегося в смеси с газом. Оставшиеся газы и продукты неполного сгорания сжигают за счет внешней диффузии кислорода (вторичного воздуха), т.е. по д и ф ф у з и о н н о м у принципу. При α1 а – ламинарное пламя; б – турбулентное пламя
Диффузионное горение может быть переведено в кинетическое или промежуточное, если смешение будет опережать процессы горения. На практике этого можно добиться принудительной подачей воздуха, приводящей к образованию квазигомогенной газовоздушной смеси с α1 > 1,0, сгорающей в прозрачном факеле.
Для иллюстрации принципов сжигания на рис. 8.11. приведены схемы свободных факелов: ламинарного и турбулентного. Ламинарный факел возникает за счет взаимной молекулярной диффузии газа и воздуха. Внутри конусного ядра 1 — чистый газ, вытекающий из трубки при ламинарном режиме течения. В зоне 2 — смесь из газа и продуктов сгорания, в зоне 3 — смесь из продуктов сгорания и воздуха. Граница 4 представляет собой гладкий конусный фронт пламени, к которому снаружи диффундируют молекулы воздуха, а изнутри — молекулы газа. Продукты сгорания частично диффундируют навстречу газу, интенсивно нагревая его в предпламенной зоне. Это приводит к пиролизу углеводородов и образованию сажистых частиц, придающих пламени яркую светимость.
Интенсифицировать горение можно за счет турбулизации смешивающихся потоков. У турбулентного факела нет четкого конусного фронта горения, он «размыт» и раздроблен пульсациями на отдельные частицы.
Структура пламени состоит из ядра чистого газа 1, зоны сравнительно медленного горения 2, размытой зоны наиболее интенсивного горения 3 с высоким содержанием продуктов сгорания и зоны горения 4 с преобладанием в ней воздуха. Четко выраженных границ между зонами нет, они непрерывно смещаются в зависимости от степени турбулизации потока. Особенностями турбулентного факела являются:
- протекание процесса горения почти по всему объему;
- повышение интенсивности горения;
- большая прозрачность пламени;
- меньшая его устойчивость по отношению к отрыву.
Турбулентное сжигание газа широко используется в топках различных котлов и печей. Для интенсификации процесса горения применяют как естественную (за счет повышения скоростей), так и искусственную, турбулизацию потоков, например, закруткой воздушного потока и подачей в него под различными углами тонких струй газа.
8.11. УСЛОВИЯ ОБРАЗОВАНИЯ ПРОДУКТОВ НЕПОЛНОГО СГОРАНИЯ И СНИЖЕНИЕ В НИХ КОНЦЕНТРАЦИИ ВРЕДНЫХ ВЕЩЕСТВ
При сжигании горючих газов в продуктах сгорания могут содержаться компоненты как полного (диоксид углерода и водяной пар), так и неполного сгорания (оксид углерода, водород, ненасыщенные, насыщенные, ароматические углеводороды и сажистые частицы). Кроме того, в продуктах сгорания всегда обнаруживаются и оксиды азота. Наличие продуктов неполного сгорания в значительных концентрациях недопустимо, так как приводит к загрязнению атмосферы токсическими веществами и к снижению КПД установок, работающих на газовом топливе.
Основные причины их большого содержания:
- сжигание газов с недостаточным количеством воздуха;
- плохое смешение горючих газов и воздуха до и в процессе горения;
- чрезмерное охлаждение пламени до завершения реакций горения.
Для метана реакции горения (в зависимости от концентрации кислорода в реагирующей смеси) могут быть описаны следующими уравнениями:
при стехиометрическом соотношении или при избытке окислителя;
при недостатке окислителя.
Рис. 8.12. Промежуточные продукты сгорания
Рис. 8.13. Содержание первичного воздуха,
при котором предотвращается образование
желтых языков в пламени
Газ: 1 – коксовый;
2 – природный газовых месторождений;
3 – нефтяных месторождений;
4 – пропан; 5 – бутан
На рис. 8.12 показан приближенный усредненный состав некоторых промежуточных соединений — водорода, оксида углерода, этилена, ацетилена и сравнительно небольшое число насыщенных и простейших ароматических соединений — и диоксида углерода, возникающих в пламени при диффузионном горении природного газа (97%). Сжигание газа производилось в ламинарном факеле, газ вытекал из трубки диаметром 12 мм. Общая высота пламени 130–140 мм.
Максимальная концентрация водорода и ацетилена достигается примерно на одной высоте пламени, они исчезают почти одновременно в вершине светящейся зоны пламени. Из всех образующихся в пламени промежуточных соединений (исключая сажистые частицы) оксид углерода исчезает последним. Это дает основание судить по его индексу о полноте сгорания газа. В продуктах сгорания всегда присутствуют оксиды азота, максимальная концентрация которых возникает в зонах интенсивного выгорания оксида углерода и водорода.
Горение углеводородных газов с недостатком окислителя приводит к образованию частиц сажи, придающих пламени желтую окраску. Процесс выгорания сажи протекает стадийно и сравнительно медленно. Иногда выгорание образовавшихся частиц сажи затягивается и может прекратиться полностью при входе в низкотемпературную область факела или при омывании пламенем теплообменных поверхностей. Таким образом, наличие светящегося пламени всегда свидетельствует о протекании пиролитических процессов и о возможности химической неполноты сгорания, в особенности в малогабаритных экранированных топках котлов.
Предотвращение образования сажистых частиц достигается предварительным смешением углеводородных газов с достаточным количеством окислителя. Содержание первичного воздуха в смеси, при котором возникает прозрачное пламя, зависит не только от вида углеводородов, но и от условий смешения с вторичным воздухом (диаметра огневых каналов горелок) (рис. 8.13). На границе и выше кривых пламя прозрачно, а ниже кривых имеет желтые язычки. Кривые показывают, что содержание первичного воздуха в смеси возрастает при увеличении числа углеродных атомов в молекуле и диаметра огневых каналов горелок. Коэффициент избытка первичного воздуха α1 в смеси, при котором исчезают желтые язычки пламени, в зависимости от указанных факторов может быть определен для малых огневых каналов горелок:
где m и n — число углеродных и водородных атомов в молекуле или среднее их число для сложного газа; dk — диаметр огневых каналов горелки, мм; d0 — эталонный диаметр канала горелки (1 мм).
Обеспечение полноты сгорания в практических условиях — задача достаточно сложная, зависящая не только от принципа сжигания газа, но и от условий развития пламени в топочном объеме. Наиболее высокие требования по полноте сгорания предъявляются к бытовым аппаратам и другим установкам, сбрасывающим продукты сгорания в атмосферу. Сгорание газа в таких установках является наиболее трудным, так как связано с омыванием пламенем холодных теплообменных поверхностей. Для сжигания газа в бытовых плитах применяют инжекционные многофакельные горелки, образующие гомогенную смесь с коэффициентом избытка первичного воздуха α1 а – горелка с периферийной подачей вторичного воздуха;
б – с центральной и периферийной подачей вторичного воздуха
1 – природный газ, горелка с периферийным подводом
вторичного воздуха, расстояние до дна посуды 25 мм;
2–4 – природный газ, горелка с перифейрийным и
центральным подводом вторичного воздуха, расстояние
до дна посуды, мм: 2 – 25, 3 – 18, 4 – 10;
5 – сжиженный газ, горелка с центральным и периферийным
подводом вторичного воздуха, расстояние до дна посуды 25 мм;
6 – сжиженный газ, горелка с периферийным подводом
На рис. 8.14 приведены схемы 2-конфорочных горелок для бытовых газовых плит и усредненная концентрация оксида углерода СО в продуктах сгорания природного метана (95 об. %) и пропана (93 об. %) при работе горелок с номинальной тепловой мощностью. Различие горелок заключается в том, что к одной из них вторичный воздух подводится только с периферии, а к другой — как с периферии, так и из центрального канала.
Полнота сгорания газа зависит от коэффициента избытка первичного воздуха в смеси, расстояния от огневых каналов горелки до дна посуды, вида горючего газа, способа подвода вторичного воздуха. При этом увеличение содержания первичного воздуха в смеси, а также увеличение расстояния от горелки до дна посуды приводят к снижению концентрации оксида углерода в продуктах сгорания. Минимальная концентрация оксида углерода соответствует коэффициенту избытка первичного воздуха α1 = 0,6 и выше и расстоянию от горелки до дна посуды 25 мм, а максимальная — α1 = 0,3 и ниже и расстоянию от горелки до дна посуды 10 мм. Кроме того, увеличение тепловой мощности горелок на 15–20% за счет повышения давления газа приводит к росту концентрации оксида углерода в продук тах сгорания в 1,2–1,3 раза, а за счет теплоты сгорания газа — в 1,5–2 раза.
На появление в процессе горения ароматических соединений — бензола, полициклических бензпирена, безантрацена и др. — следует обратить особое внимание, так как некоторые из них канцерогенны. Процесс их образования весьма сложен и протекает стадийно. На первом этапе появляется ацетилен и его производные. В пламенной зоне эти вещества претерпевают процессы удлинения цепи с перестройкой тройных углеродных связей на двойные. В результате циклизации и дегидратации приводят к появлению различных ароматических соединений, включая полициклические.
Таблица 8.16. Средняя концентрация в продуктах сгорания оксида углерода и бенз(а)пирена в зависимости от вида газа, типа горелки и коэффициента избытка первичного воздуха (тепловая нагрузка горелки — 1600 ккал/ч, расстояние от горелки до дна посуды — 24–26 мм)
















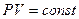 , Гей-Люссака
, Гей-Люссака 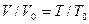 , Шарля
, Шарля 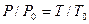 и Клапейрона – Менделеева
и Клапейрона – Менделеева 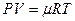 . Используется также закон Авогадро, согласно которому один грамм-моль любого газа при нормальных условиях (Т = 273 К, Р = 760 мм рт. ст.) занимает одинаковый объём – 22,4 дм 3 . Соответственно один кг-моль – 22,4 м 3 .
. Используется также закон Авогадро, согласно которому один грамм-моль любого газа при нормальных условиях (Т = 273 К, Р = 760 мм рт. ст.) занимает одинаковый объём – 22,4 дм 3 . Соответственно один кг-моль – 22,4 м 3 .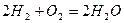 . Из уравнения следует, что при нормальных условиях для полного сгорания 2 × 22,4 = 44,8 м 3 водорода требуется 22,4 м 3 кислорода. Обычно для простоты и удобства расчеты ведут на один кубометр сжигаемого газа, т.е. для сгорания 1 м 3 водорода требуется 0,5 м 3 кислорода.
. Из уравнения следует, что при нормальных условиях для полного сгорания 2 × 22,4 = 44,8 м 3 водорода требуется 22,4 м 3 кислорода. Обычно для простоты и удобства расчеты ведут на один кубометр сжигаемого газа, т.е. для сгорания 1 м 3 водорода требуется 0,5 м 3 кислорода.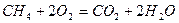 . Из уравнения следует, что для полного сгорания 22,4 м 3 метана требуется 2 × 22,4 = 44,8 м 3 кислорода. Следовательно, для сгорания 1 м 3 метана необходимо 2 м 3 кислорода.
. Из уравнения следует, что для полного сгорания 22,4 м 3 метана требуется 2 × 22,4 = 44,8 м 3 кислорода. Следовательно, для сгорания 1 м 3 метана необходимо 2 м 3 кислорода.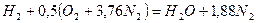 .
.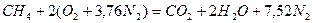 .
.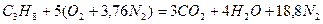 .
.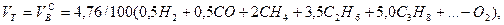 нм 3 /нм 3 , (10.4)
нм 3 /нм 3 , (10.4)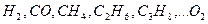 – соответственно объемное процентное содержание данных газов в исходной смеси.
– соответственно объемное процентное содержание данных газов в исходной смеси.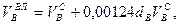 нм 3 /нм 3 , (10.5)
нм 3 /нм 3 , (10.5)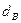 – влагосодержание воздуха, г/нм 3 ;
– влагосодержание воздуха, г/нм 3 ;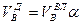 . (10.6)
. (10.6) , нм 3 /нм 3 ,
, нм 3 /нм 3 ,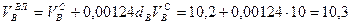 , нм 3 /нм 3 ,
, нм 3 /нм 3 ,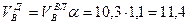 , нм 3 /нм 3 .
, нм 3 /нм 3 .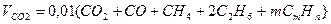 , нм 3 /нм 3 . (10.7)
, нм 3 /нм 3 . (10.7)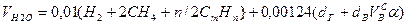 , нм 3 /нм 3 . (10.8)
, нм 3 /нм 3 . (10.8)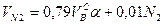 , нм 3 /нм 3 . (10.9)
, нм 3 /нм 3 . (10.9)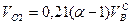 , нм 3 /нм 3 . (10.10)
, нм 3 /нм 3 . (10.10) , нм 3 /нм 3 . (10.11)
, нм 3 /нм 3 . (10.11)





