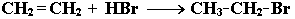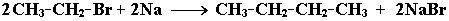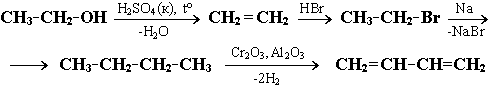закрепить, обобщить и систематизировать знания по кислородсодержащим органическим соединениям, в том числе и на основе генетической связи между классами этих веществ.
- Просмотр содержимого документа «Генетическая связь предельных одноатомных спиртов с углеводородами.»
- Please wait.
- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Урок химии в 11 классе: Генетическая связь между углеводородами,спиртами,альдегидами,спиртами,карбоновыми кислотами.
Просмотр содержимого документа
«Генетическая связь предельных одноатомных спиртов с углеводородами.»
УМК.Химия.10 класс Учеб.для общеобразва.организаций:базовый
уровень/Г.Е.Рудзитиис, Ф.Г.Фельдман-2 издание-М.:Просвещение, 2012г.
Тема урока: Генетическая связь предельных одноатомных спиртов с углеводородами.
Общее количество часов, отведенное на изучение темы, 6 часов.
Место урока- 4 урок по теме
Тип урока: урок обобщения знаний.
Цели урока: закрепить, обобщить и систематизировать знания по кислородсодержащим органическим соединениям, в том числе и на основе генетической связи между классами этих веществ.
образовательные: повторить основные термины и понятия по теме, закрепить знания о составе, строении и свойствах спиртов;
развивающие: умение анализировать, сравнивать, устанавливать связь между строением и свойствами соединений, развивать творческие способности и познавательный интерес учащихся к химии;
воспитательные: уделять особое внимание тем вещам, которые мы используем в жизни.
Методы: словесный, наглядный, , проблемно-поисковый, контроль знаний.
Оборудование: компьютер, экран, проектор, таблица «Классификация кислородсодержащих органических веществ», опорный конспект «Функциональная группа определяет свойства вещества».
Планируемые результаты обучения
Предметные. Знать зависимость между составом, строением и свойствами веществ. Уметь приводить примеры и составлять уравнения химических реакций, раскрывающих
генетические связи между спиртами и углеводородами. Отрабатывать умение производить расчёты по химическим уравнениям, если одно из реагирующих веществ взято в избытке.
Метапредметные. Уметь организовывать учебное сотрудничество и совместную деятельность с учителем и сверстниками, работать индивидуально и в группе (находить общее решение и разрешать конфликты на основе согласования позиций и учёта интересов), формулировать, аргументировать и отстаивать своё мнение.
Личностные. Формировать целостное мировоззрение, соответствующее современному уровню развития науки, на основе представлений о генетической связи между разными
классами органических веществ. Развивать коммуникативную компетентность.
I. Организационный момент.
II. Ребята, сегодня на уроке мы будем решать генетические задачи, на которых закрепим полученные знания в ходе изучения тем.
Свойства углеводородов зависят от химического, пространственного, электронного строения молекул и характера химических связей.
Изучение строения, химических свойств и способов получения углеводородов различных групп показывает, что все они генетически связаны между собой, т.е. возможны превращения одних углеводородов в другие:
Это позволяет осуществлять целенаправленный синтез заданных соединений, используя ряд необходимых химических реакций (цепь превращений).
Задача 1. Назвать промежуточные продукты в схеме превращений:

Решение. В данной цепи превращений, включающей 4 реакции, из этилового спирта С2Н5ОН должен быть получен бутадиен-1,3 СН2=СН–СН=СН2.
1. При нагревании спиртов с концентрированной серной кислотой
H2SO4 (водоотнимающее средство) происходит их дегидратация с образованием алкена Отщепление воды от этилового спирта приводит к образованию этилена:
2. Этилен – представитель алкенов. Являясь ненасыщенным соединением, он способен вступать в реакции присоединения . В результате гидробромирования этилена:
3.При нагревании бромэтана в присутствии металлического натрия (реакция Вюрца, образуется н-бутан (вещество Z):
4.Дегидрирование н-бутана в присутствии катализатора – один из способов получения бутадиена-1,3 СН2=СН–СН=СН2
(раздел 5.4. Получение алкадиенов).
Ответ:
1. Осуществите превращения:
Выполнение упражнений на закрепление знаний.
Учащиеся выполняют задания в рабочих тетрадях.
Пользуясь схемой генетической связи, укажите из каких веществ, формулы которых приведены в задании в одну стадию можно получить спирты? Запишите уравнения соответствующих реакций. Назовите исходные вещества и продукты реакции. Суффиксы в названиях углеводородов и галогенпроизводных углеводородов подчеркните соответственно кратности связи.
Назовите класс веществ и установите генетическую связь (покажите это с помощью стрелок).
Теперь немного усложним наше задание.. Составьте цепочку превращений из предложенных соединений. Среди формул веществ есть «лишние». Каким это задание является по отношению к предыдущему?
Закрепление свойств углеводородов в форме игры «Нет –да»
1. Можно получить спирт из этена? (да)
2. Этанол содержится в листьях растений? (нет)
3. Брожениям сахаристых веществ получают метанол? (нет)
4. Из древесной стружки сбраживанием можно получить этанол? (нет)
5. Если картофель заморозить , то можно получить этиловый спирт? (да)
.Рефлексивный тест:
1. Мне это пригодится в жизни.
2. На уроке было над чем подумать.
3. На все возникшие у меня вопросы я получил(а) ответы.
4. На уроке я поработал(а) добросовестно.
Дом.задание. Пов.§20-21, схемы превращений упр.14,15*,
Осуществите превращения:
C2H5OH-C2H5CL-C2H5OH-C2H5OC2H5
/
CO2
Список литературы
Химия .Органическая химия .10 класс: учеб. для общеобразоват. учреждений: базовый уровень Г.Е. Рудзитис, Ф.Г. Фельдман. – 13е изд.-М.: Просвещение, 2009.
Химия 8-11 класс (тематическое планирование по учебнику Г.Е.Рудзитиса, Ф.Г.Фельдмана)/ сост. Брейгер Л.М.-Волгоград:Учитель-АСТ,1999
Химия . Большой справочник для подготовки к ЕГЭ: учебно- методическое пособие/ Под редакцией В.Н. Доронькина.- изд.2-е, перераб.- Ростов н/ Д: Легион, 2016.
Суровцева Р.П. и др. Химия.10-11 классы: Методическое пособие.-М.: Дрофа,2000.
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e29263dfcc27a40 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Урок химии в 11 классе: Генетическая связь между углеводородами,спиртами,альдегидами,спиртами,карбоновыми кислотами.
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Урок химии в 11 классе
Тема урока: Генетическая связь между углеводородами,спиртами,альдегидами,спиртами,карбоновыми кислотами.
Тип урока: урок обобщения знаний.
Цели урока: закрепить, обобщить и систематизировать знания по кислородсодержащим органическим соединениям, в том числе и на основе генетической связи между классами этих веществ. Закрепить умения предсказывать химические свойства незнакомых органических веществ, опираясь на знание функциональных групп. Развивать у учащихся доказательную речь, умения использовать химическую терминологию, проводить, наблюдать и описывать химический эксперимент. Воспитывать потребности в знаниях о тех веществах, с которыми мы соприкасаемся в жизни.
Методы: словесный, наглядный, практический, проблемно-поисковый, контроль знаний.
Реактивы: ацетилсалициловая кислота (аспирин), вода, хлорид железа(III), раствор глюкозы, универсальный индикатор, раствор сульфата меди (II), раствор гидроксида натрия, яичный белок, этанол, бутанол-1, уксусная кислота, стеариновая кислота.
Оборудование: компьютер, экран, проектор, таблица «Классификация кислородсодержащих органических веществ», опорный конспект «Функциональная группа определяет свойства вещества», ступка с пестиком, стеклянная палочка, спиртовка, пробиркодержатель, воронка, фильтр, стаканы, штатив с пробирками, пипетка, мерный цилиндр на 10 мл.
I. Организационный момент.
СЕГОДНЯ НА УРОКЕ:
1) Вы закрепите умения предсказывать химические свойства незнакомых органических веществ, опираясь на знание функциональных групп.
2) Вы узнаете, какие известные вам функциональные группы входят в состав самого знаменитого жаропонижающего средства.
3)Вы обнаружите функциональные группы в веществе сладкого вкуса, который применяют в медицине как питательное вещество и компонент кровозамещающих жидкостей.
4) Вы увидите, как можно получить чистое серебро.
5) Мы поговорим о физиологическом воздействии этилового спирта.
6) Мы обсудим последствия употребления алкогольных напитков беременными женщинами.
7) Вы приятно удивитесь: оказывается, вы знаете уже так много!
II. Повторение и обобщение полученных знаний учащихся.
1. КЛАССИФИКАЦИЯ КИСЛОРОДСОДЕРЖАЩИХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ.
Обобщение материала начинаем с классификации кислородсодержащих органических веществ. Для этого мы воспользуемся таблицей «Классификация кислородсодержащих органических соединений». В ходе фронтальной работы повторим кислородсодержащие функциональные группы.
В органической химии существуют три важнейшие функциональные группы, включающие атомы кислорода: гидроксильная, карбонильная и карбоксильная. Последнюю можно рассматривать как сочетание двух предыдущих. В зависимости от того, с какими атомами или группами атомов связаны данные функциональные группы, кислородсодержащие вещества делятся на спирты, фенолы, альдегиды, кетоны и карбоновые кислоты.
Рассмотрим эти функциональные группы и их влияние на физические и химические свойства веществ.
Вы уже знаете, что это не единственно возможный признак классификации. Одинаковых функциональных групп в молекуле может быть несколько, и обратите внимание к соответствующей строке таблицы.
Следующая строка отражает классификацию веществ по типу радикала, связанного с функциональной группой. Хочется обратить внимание на то, что в отличие от спиртов, альдегидов, кетонов и карбоновых кислот гидроксиарены выделяют в отдельный класс соединений – фенолы.
Число функциональных групп и строение радикала определяют общую молекулярную формулу веществ. В данной таблице они приведены только для предельных представителей классов с одной функциональной группой.
Все классы соединений, «уместившиеся» в таблицу, являются монофункциональными, т. е. несут только одну кислородсодержащую функцию.
Для закрепления материала по классификации и номенклатуре кислородсодержащих веществ привожу несколько формул соединений и прошу учащихся определить «их место» в приведенной классификации и дать название.
Непредельная, одноосновная кислота
Предельный, двухатомный спирт
Предельный, одноатомный спирт
ВЗАИМОСВЯЗЬ СТРОЕНИЯ И СВОЙСТВ КИСЛОРОДСОДЕРЖАЩИХ СОЕДИНЕНИЙ.
Природа функциональной группы оказывает существенное влияние на физические свойства веществ данного класса и во многом определяет его химические свойства.
В понятие «физические свойства» входит агрегатное состояние веществ.
Агрегатное состояние линейных соединений разных классов:
Гомологический ряд альдегидов начинается с газообразного при комнатной температуре вещества — формальдегида, а среди одноатомных спиртов и карбоновых кислот газов нет. С чем это связано?
Молекулы спиртов и кислот дополнительно связаны друг с другом водородными связями.
Учитель просит учащихся сформулировать определение «водородная связь» (это межмолекулярная связь между кислородом одной молекулы и гидроксильным водородом другой молекулы) , корректирует его и при необходимости диктует для записи: химическая связь между электронодефицитным атомом водорода и электроноизбыточным атомом элемента с большой электроотрицательностью (F, O , N ) называется водородной.
А сейчас сравните температуры кипения (°C) первых пяти гомологов веществ трех классов.
Что можно сказать после рассмотрения таблиц?
В гомологических рядах спиртов и карбоновых кислот отсутствуют газообразные вещества и температуры кипения веществ высокие. Это связано с наличием водородных связей между молекулами. За счет водородных связей молекулы оказываются ассоциированными (как бы сшитыми), поэтому, чтобы молекулы стали свободными и приобрели летучесть, необходимо затратить дополнительную энергию на разрыв этих связей.
Что можно сказать о растворимости спиртов, альдегидов и карбоновых кислот в воде? (Демонстрация растворимости в воде спиртов – этилового, пропилового, бутилового и кислот – муравьиной, уксусной, пропионовой, масляной и стеариновой. Демонстрируется также раствор муравьиного альдегида в воде.)
При ответе используется схема образования водородных связей между молекулами кислоты и воды, спиртов, кислот.
Необходимо отметить, что с увеличением молекулярной массы растворимость в воде спиртов и кислот уменьшается. Чем больше углеводородный радикал в молекуле спирта или кислоты, тем труднее группе OH держать молекулу в растворе за счет образования слабых водородных связей.
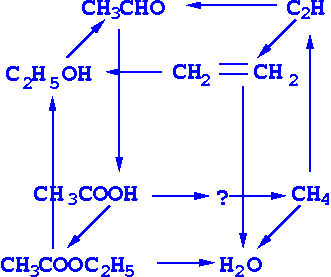
3. ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ РАЗЛИЧНЫМИ КЛАССАМИ КИСЛОРОДСОДЕРЖАЩИХ СОЕДИНЕНИЙ.
Изображаю на доске формулы ряда соединений, содержащих по одному атому углерода:
Почему именно в такой последовательности они изучаются в курсе органической химии?
Как изменяется степень окисления атома углерода?
Учащиеся диктуют строчку: -4, -2, 0, +2, +4
Теперь становится ясно, что каждое последующее соединение является все более окисленной формой предыдущего. Отсюда очевидно, что продвигаться по генетическому ряду слева направо следует с помощью реакций окисления, а в обратном направлении – с использованием процессов восстановления.
Не выпадают ли кетоны из этого «круга родственников»? Конечно, нет. Их предшественники – вторичные спирты.
Химические свойства каждого класса веществ были подробно рассмотрены на соответствующих уроках. Для обобщения этого материала я предложила в качестве домашней работы задания по взаимопревращениям в несколько необычной форме.
1. Соединение с молекулярной формулой C3H8O подвергли дегидрированию, в результате чего получили продукт состава C3H6O . Это вещество вступает в реакцию «серебряного зеркала», образуя соединение C3H6O2 . При действии на последнее вещество гидроксидом кальция получили вещество, используемое в качестве пищевой добавки под кодом E 282. Оно препятствует росту плесени в хлебобулочных и кондитерских изделиях и, кроме того, содержится в таких продуктах, как швецарский сыр. Определите формулу добавки E 282, напишите уравнения упомянутых реакций и назовите все органические вещества.
CH3 – CH2 – COH + Ag2O → CH3 – CH2 – COOH + 2Ag (упрощенный вид уравнения, аммиачный раствор оксида серебра)
Ответ: пропионат кальция.
2. Соединение состава C4H8Cl2 с неразветленным углеродным скелетом нагрели с водным растворомNaOH и получили органическое вещество, которое при окислении Cu(OH)2 превратилось в C4H8O2 . Определите строение исходного соединения.
Решение: если 2 атома хлора находятся у разных атомов углерода, то при обработке щелочью мы получили бы двухатомный спирт, который не окислялся бы Cu(OH)2 . Если 2 атома хлора находились бы при одном атоме углерода в середине цепи, то при обработке щелочью получили бы кетон, который не окисляется Cu(OH)2. Тогда, искомое соединение – 1,1-дихлорбутан.
3. При нагревании 19,2 г натриевой соли предельной одноосновной кислоты с гидроксидом натрия образовалось 21,2 г карбоната натрия. Назовите кислоту.
При нагревании происходит декарбоксилирование:
В соответствии с общей формулой предельных одноосновных карбоновых кислот для определения количества атомов углерода надо решить уравнение:
Ответ: пропионовая кислота.
Для закрепления знаний о химических свойствах кислородсодержащих органических веществ, выполним тест.
2. В ней — сочетанье двух начал,
Одно – в рождении зеркал.
Конечно, не для созерцанья,
А для науки пониманья.
…И в царстве леса встречается она,
Меньшие братья здесь ее друзья,
Им сердце отдано сполна…
варианты:
А) пикриновая кислота
Б) муравьиная кислота
В) уксусная кислота
Г) карбоксильная группа
Д) бензойная кислота
5. Этаналь реагирует с веществами
А) метанолом
Б) водородом
В) аммиачным раствором оксида серебра
Г) гидроксидом меди (II)
Д) хлороводородом
1. Альдегиды можно получить
А) окислением алкенов
Б) окислением спиртов
В) гидратацией алкинов
Г) при нагревании кальциевых солей карбоновых кислот
Д) гидратацией алкенов
3. 2-метилбутанол-2
А) непредельный спирт
Б) предельный спирт
В) одноатомный спирт
Г) третичный спирт
Д) альдегид
4. Вы наблюдали реакцию
А) на многоатомные спирты
Б) окисление спирта
В) взаимодействие фенола с хлоридом железа (III)
Г) «серебряного зеркала»
Д) «медного зеркала»
5. Уксусная кислота реагирует с веществами
А) водородом
Б) хлором
В) пропанолом
Г) гидроксидом натрия
Д) метаналем
ОТВЕТЫ УЧАЩИЕСЯ ОФОРМЛЯЮТ В ТАБЛИЦЕ:
Если соединить правильные ответы сплошной линией, получается цифра «5».
Групповая работа учащихся.
ЗАДАНИЕ ДЛЯ 1 ГРУППЫ
1. Рассмотрите структурные формулы двух веществ, назовите функциональные группы.
ацетилсалициловая кислота (аспирин)
2. Проведите лабораторную работу «Обнаружение функциональных групп в молекуле ацетилсалициловой кислоты».
Цели: закрепить знания учащихся о качественных реакциях органических соединений, отработать навыки экспериментального определения функциональных групп.
Реактивы и оборудование: ацетилсалициловая кислота (аспирин), вода, хлорид железа(III); ступка с пестиком, стеклянная палочка, спиртовка, пробиркодержатель, воронка, фильтр, стаканы, штатив с пробирками, пипетка, мерный цилиндр на 10 мл.
Опыт 1. Доказательство отсутствия фенольного гидроксила в ацетилсалициловой кислоте (аспирине).
В пробирку помещают 2-3 крупинки ацетилсалициловой кислоты, добавляют 1 мл воды и энергично встряхивают. К полученному раствору прибавляют 1-2 капли раствора хлорида железа(III). Что наблюдаете? Сделайте выводы.
Фиолетовое окрашивание не появляется. Следовательно, в ацетилсалициловой кислоте НООС-С6Н4-О-СО-СН3 отсутствует свободная фенольная группа, так как это вещество – сложный эфир, образованный уксусной и салициловой кислотами.
Опыт 2. Гидролиз ацетилсалициловой кислоты.
В пробирку помещают измельченную таблетку ацетилсалициловой кислоты и добавляют 10 мл воды. Доводят содержимое пробирки до кипения и кипятят в течение 0,5-1 мин. Профильтруйте раствор. Затем к полученному фильтрату прибавляют 1-2 капли раствора хлорида железа(III). Что наблюдаете? Сделайте выводы.
Запишите уравнение реакции:
Оформите работу, заполнив таблицу, в которой есть следующие графы: выполняемая операция, реактив, наблюдения, вывод.
Появляется фиолетовое окрашивание, что указывает на выделение салициловой кислоты, содержащей свободную фенольную группу. Как сложный эфир ацетилсалициловая кислота легко гидролизуется при кипячении с водой.
Задание для 2 группы
1. 1. Рассмотрите структурные формулы веществ, назовите функциональные группы.
2. Проведите лабораторную работу «Обнаружение функциональных групп в молекуле глюкозы».
Цели: закрепить знания учащихся о качественных реакциях органических соединений, отработать навыки экспериментального определения функциональных групп.
Реактивы и оборудование: раствор глюкозы, универсальный индикатор, раствор сульфата меди (II), раствор гидроксида натрия, спиртовка, пробиркодержатель, спички, мерный цилиндр на 10 мл.
2.1. Налейте в пробирку 2 мл раствора глюкозы. С помощью универсального индикатора сделайте вывод о наличии или отсутствии карбоксильной группы.
2.2. Получите гидроксид меди (II): влейте в пробирку 1 мл сульфата меди (II) и добавьте к нему гидроксид натрия. К полученному осадку прилейте 1 мл глюкозы, встряхните. Что наблюдаете? Для каких функциональных групп характерна данная реакция?
2.3. Полученную в опыте № 2 смесь нагрейте. Отметьте изменения. Для какой функциональной группы характерна данная реакция?
2.4. Оформите работу, заполнив таблицу, в которой есть следующие графы: выполняемая операция, реактив, наблюдения, вывод.
Демонстрационный опыт. Взаимодействие раствора глюкозы с аммиачным раствором оксида серебра.
— карбоксильная группа отсутствует, т.к. раствор имеет нейтральную реакцию на индикатор;
— осадок гидроксида меди (II) растворяется и появляется ярко-синее окрашивание, характерное для многоатомных спиртов;
— при нагревании этого раствора выпадает желтый осадок гидроксида меди (I), который при дальнейшем нагревании краснеет, что показывает наличие альдегидной группы.
Вывод. Таким образом, молекула глюкозы содержит карбонильную и несколько гидроксильных групп и представляет собой альдегидоспирт.
Задание для 3 группы
Физиологическое действие этанола
1. Каково действие этанола на живые организмы?
2. Используя имеющиеся на столе оборудование и реактивы, продемонстрируйте влияние этанола на живые организмы. Прокомментируйте увиденное.
Цель опыта: убедить учащихся, что спирт денатурирует белки, необратимо нарушает их структуру и свойства.
Оборудование и реактивы: штатив с пробирками, пипетка, мерный цилиндр на 10 мл, яичный белок, этанол, вода.
Ход опыта: в 2 пробирки налейте по 2 мл яичного белка. В одну добавить 8 мл воды, в другую – столько же этанола.
В первой пробирке белок растворяется, хорошо усваивается организмом. Во второй пробирке образуется плотный белый осадок – в спирте белки не растворяются, спирт отнимает у белков воду. В результате этого нарушаются структура и свойства белка, его функции.
3. Расскажите о влиянии этилового спирта на различные органы и системы органов человека.
Расскажите о последствиях употребления алкогольных напитков беременным женщинам.
Издревле человеку известно большое число ядовитых веществ, все они отличаются пи силе воздействия на организм. Среди них выделяется вещество, которое известно в медицине как сильный протоплазматический яд, – это этиловый спирт. Смертность от алкоголизма превышает число смертельных случаев, вызываемых всеми инфекционными заболеваниями вместе взятыми.
Обжигая слизистую оболочку полости рта, глотки, пищевода, он поступает в желудочно-кишечный тракт. В отличие от многих других веществ спирт быстро и полностью всасывается в желудке. Легко преодолевая биологические мембраны, примерно через час он достигает максимальной концентрации в крови.
Молекулы спирта быстро проникают через биологические мембраны в кровь по сравнению с молекулами воды. Беспрепятственно преодолеть биологические мембраны молекулам этилового спирта позволяют их малый размер, слабая поляризация, образование водородных связей с молекулами воды, хорошая растворимость спирта в жирах.
Быстро всасываясь в кровь, хорошо растворяясь в межклеточной жидкости, спирт поступает во все клетки организма. Учеными установлено, что, нарушая функции клеток, он вызывает их гибель: при употреблении 100 г пива погибает около 3000 клеток мозга, 100 г вина – 500, 100 г водки – 7500, соприкосновение эритроцитов с молекулами спирта приводит к свертыванию кровяных клеток.
В печени происходит обезвреживание ядовитых веществ, поступивших в кровь. Этот орган врачи называют мишенью для алкоголя, так как 90 % этанола обезвреживается именно в нем. В печени происходят химические процессы окисления этилового спирта.
Вспоминаем с учащимися этапы процесса окисления спирта:
Этиловый спирт окисляется до конечных продуктов распада только в том случае, если суточное потребление этанола не превышает 20 г. Если же доза превышена, то в организме накапливаются промежуточные продукты распада.
Это приводит к целому ряду побочных отрицательных эффектов: повышенному образованию жира и накоплению его в клетках печени; накоплению пероксидных соединений, способных разрушать клеточные мембраны, в результате чего содержимое клеток вытекает через образовавшиеся поры; весьма нежелательным явлениям, совокупность которых приводит к разрушению печени — циррозу.
Уксусный альдегид в 30 раз токсичнее этилового спирта. Кроме того, в результате различных биохимических реакций в тканях и органах, в том числе в головном мозге, возможно образование тетрагидропапаверолина, структура и свойства которого напоминают широко известные наркотики психотропного действия – морфин и канабинол. Врачи доказали, что возникновение мутаций и различных уродств у эмбрионов вызывает именно уксусный альдегид.
Уксусная кислота усиливает синтез жирных кислот и приводит к жировому перерождению печени.
Изучая физические свойства спиртов, мы затрагивали вопрос изменения их токсичности в гомологическом ряду одноатомных спиртов. С увеличением молекулярной массы молекул веществ возрастают их наркотические свойства. Если сравнить этиловый и пентиловый спирты, то молекулярная масса последнего больше в 2 раза, а токсичность – в 20 раз. Спирты, содержащие три- пять атомов углерода, образуют так называемые сивушные масла, наличие которых в спиртных напитках увеличивает их ядовитые свойства.
В этом ряду исключение составляет метанол — сильнейший яд. При попадании в организм 1-2 чайных ложек его поражается зрительный нерв, что приводит к полной слепоте, а употребление 30-100 мл приводит к смертельному исходу. Опасность усиливается из-за сходства метилового спирта с этиловым спиртом по свойствам, внешнему виду, запаху.
Вместе с учащимися пробуем найти причину этого явления. Они выдвигают различные гипотезы. Останавливаемся на том, что к факторам, увеличивающим токсичность метилового спирта, можно отнести малый размер молекул (высокая скорость распространения), а также то, что промежуточные продукты его окисления — муравьиный альдегид и муравьиная кислота – сильные яды.
Не обезвреженный печенью спирт и ядовитые продукты его распада вновь поступают в кровь и разносятся по всему организму, надолго оставаясь в нем. Например, в головном мозге спирт обнаруживается в неизменном виде после 20 дней после его принятия.
Обращаем внимание учащихся на то, как спирт и продукты его распада выводятся из организма.
10% в неизменном виде через легкие, почки и кожу
К сожалению, в последнее время потребление спиртного, как и курение, распространено среди женщин. Влияние алкоголя на потомство идет по двум направлениям.
Во-первых, употребление алкоголя сопровождается глубокими изменениями в половой сфере как мужчин, так и женщин. Алкоголь и продукты его разложения могут подействовать как на женские, так и на мужские половые клетки еще до оплодотворения – изменяется их генетическая информация (см. рис. «Здоровые (1) и патологические (2) сперматозоиды»).
Если употребление алкоголя длительное, нарушается деятельность половой системы, она начинает производить неполноценные половые клетки.
Во-вторых, алкоголь непосредственно воздействует на зародыш. Постоянное употребление 75—80 г водки, коньяка или 120—150 г более слабых алкогольных напитков (пива) может вызвать алкогольный синдром плода. Через плаценту в воды, окружающие плод, попадают не только алкоголь, но и продукты его разложения, в частности уксусный альдегид , который в десятикратном размере опаснее самого алкоголя.
Алкогольная интоксикация пагубно воздействует на плод, потому что его печень, куда прежде всего попадает кровь из плаценты, еще не имеет специального фермента, разлагающего алкоголь, и он, не обезвреженный, разносится по всему организму и вызывает необратимые изменения. Особенно алкоголь опасен на 7—11-й неделе беременности, когда начинают развиваться внутренние органы. Он отрицательно воздействует на их развитие, вызывая нарушения и изменения. Особенно страдает головной мозг. Из-за воздействия алкоголя могут развиться слабоумие, эпилепсия, неврозы, сердечные и почечные нарушения, повреждаются внешние и внутренние половые органы.
Иногда повреждения психики и интеллекта наблюдаются уже в раннем детстве, но чаще всего они выявляются, когда дети начинают учиться. Такой ребенок интеллектуально ослаблен, агрессивен. Алкоголь действует на организм ребенка намного сильнее, чем на организм взрослого человека. Особенно чувствительны и легкоранимы нервная система и мозг ребенка.
Итак, посмотрим на таблицу «Влияние алкоголя на наследственность и здоровье детей» и сделаем выводы .
В семьях пьющих родителей
В семьях непьющих родителей
Умерли в первые месяцы жизни
Оказались неполноценными, больными
Здоровы физически и душевно
Длительное употребление спиртных напитков приводит к размягчению коркового слоя. Наблюдаются многочисленные точечные кровоизлияния; нарушается передача возбуждения от одной нервной клетки на другую. Не забывайте лаконичных предостерегающих слов В. В. Маяковского:
Не пейте спиртных напитков.
Пьющим – яд, окружающим – пытка.
Таким образом, вы закрепили умения предсказывать химические свойства незнакомых органических веществ, опираясь на знание функциональных групп, повторили физические и химические свойства кислородсодержащих органических веществ, закрепили умения определять принадлежность органических соединений к классам веществ.
III. Домашнее задание.
1. Осуществите превращения:
2. Изучите возможные причины загрязнения окружающей среды вблизи производства: метанола, фенола, формальдегида, уксусной кислоты. Проанализируйте влияние этих веществ на природные объекты: атмосферу, водные источники, почву, растения, животных и человека. Опишите меры оказания первой помощи при отравлении