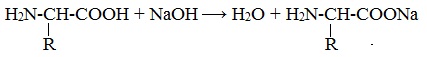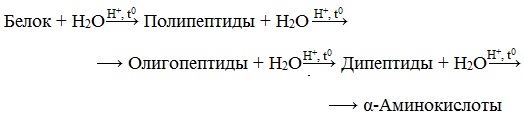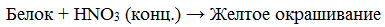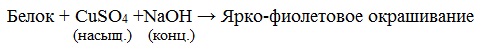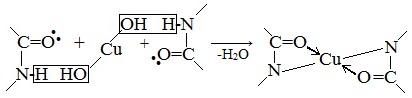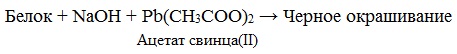По химическому составу белки делятся на две группы:
а) простые белки – протеины, которые при гидролизе распадаются только на аминокислоты;
б) сложные белки или протеиды, образующие при гидролизе аминокислоты и вещества небелковой природы (углеводы, нуклеиновые кислоты и др.) — соединения белковых веществ с небелковыми.
1. Амфотерные свойства белков
Как и аминокислоты, белки являются амфотерными соединениями, так как молекула любого белка содержит на одном конце группу -NH2, а на другом конце – группу -СООН.
Так, при действии щелочей белок реагирует в форме аниона – соединяется с катионом щелочи:
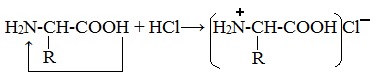
При действии же кислот он выступает в форме катиона:
Если в молекуле белка преобладают карбоксильные группы, то он проявляет свойства кислот, если же преобладают аминогруппы, — свойства оснований.
Очень важным для жизнедеятельности живых организмов является буферное свойство белков, т.е. способность связывать как кислоты, так и основания, и поддерживать постоянное значение рН различных систем живого организма.
Белки обладают и специфическими физико-химическими свойствами.
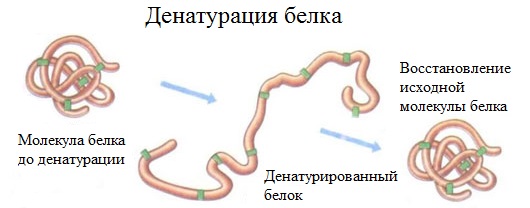
2. Денатурация белка (необратимое осаждение, свертывание)
Денатурация – это разрушение вторичной и третичной структуры белка (полное или частичное) и изменение его природных свойств с сохранением первичной структуры белка.
Сущность денатурации белка сводится к разрушению связей, обусловливающих вторичную и третичную структуры молекулы (водородных, солевых и других мостиков). А это приводит к дезориентации конфигурации белковой молекулы.
Денатурация бывает обратимой и необратимой.
Обратимая денатурация белка происходит при употреблении алкоголя, солёной пищи.
Необратимая денатурация может быть вызвана при действии таких реагентов, как концентрированные кислоты и щелочи, спирты, в результате воздействия высокой температуры, радиации, при отравлении организма солями тяжелых металлов (Hg 2+ , Pb 2+ , Си 2+ ).
Например, яичный белок альбумин осаждается из раствора (свертывается) при варке яиц (при температуре 60-70 0 С), теряя способность растворяться в воде.
Видеоопыт «Свертывание белков при нагревании»
Видеоопыт «Осаждение белков солями тяжелых металлов»
Видеоопыт «Осаждение белков спиртом»
3. Гидролиз белков
Гидролиз белков – это необратимое разрушение первичной структуры в кислом или щелочном растворе с образованием аминокислот.
Анализируя продукты гидролиза, можно установить количественный состав белков.
Переваривание белков в организме по своей сути представляет ферментативный гидролиз белковых молекул.
В лабораторных условиях и в промышленности проводится кислотный гидролиз.
В ходе гидролиза белков происходит разрушение пептидных связей. Гидролиз белка имеет ступенчатый характер:
4. Цветные (качественные) реакции на белки
Для белков известно несколько качественных реакций.
а) Ксантопротеиновая реакция (на остатки аминокислот, содержащих бензольные кольца)
Белки, содержащие остатки ароматических аминокислот (фенилаланина, тирозина), дают желтое окрашивание при действии концентрированной азотной кислоты.
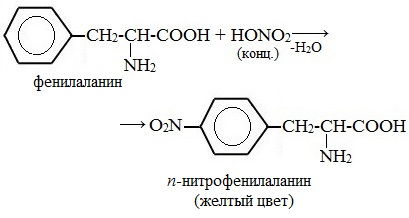
Причина появления окраски – образование нитропроизводных ароматических аминокислот, например, фенилаланина:
Видеоопыт «Ксантопротеиновая реакция на белки»
б) Биуретовая реакция (на пептидные связи)
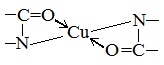
Все соединения, содержащие пептидную связь, дают фиолетовое окрашивание при действии на них солей меди (II) в щелочном растворе.
Причина появления окраски – образование комплексных соединений с координационным узлом:
Видеоопыт «Биуретовая реакция белков»
Видеоопыт «Качественные реакции на белки: биуретовая и ксантопротеиновая»
в) Цистеиновая реакция (на остатки аминокислот, содержащих серу)
Причина появления окраски – образование черного осадка сульфида серебра (II) PbS.
Видеоопыт «Качественное определение азота в органических соединениях»
Денатурация белков при нагревании
Белки денатурируют и выпадают в осадок при нагревании их растворов выше 50-60 0 С. Свернувшиеся белки не могут быть снова переведены в раствор, т.к. при нагревании нарушаются связи, стабилизирующие четвертичную, третичную и вторичную структуры белковых молекул, изменяются их физико-химические свойства, также снижается и гидратационная способность.
В изоэлектрическом состоянии при нагревании степень денатурации увеличивается, т.к. изоэлектрическая точка для большинства белков находится в слабокислой среде, то небольшое подкисление раствора белка способствует более полной его коагуляции.
Устойчивость белковых мицелл наблюдается в сильнокислой или щелочной среде даже при кипячении, так как молекулы белка, заряжаясь одноименно, отталкиваются друг от друга.
Добавление к сильнокислому раствору белков нейтральных солей при нагревании способствует осаждению белков вследствие дегидратирования их частиц.
Ход работы: 1)В пять пробирок вносят по 2 мл раствора яичного альбумина.
2) Белок в первой пробирке нагревают до кипения. Появляется осадок белка.
3) Во вторую пробирку добавляют одну каплю 1%-ного раствора уксусной кислоты и нагревают. Осадок выпадает быстрее, так как белок находится ближе к изоэлектрическому состоянию.
4) Добавляют в третью пробирку 0,5 мл 10%-ного раствора уксусной кислоты и нагревают. Осадок не образуется даже при кипячении.
5) В четвертую пробирку прибавляют 0,5 мл 10%-ного раствора уксусной кислоты, несколько капель насыщенного раствора хлористого натрия и нагревают. Образуется осадок белка.
6) В пятую пробирку прибавляют 0,5 мл 10%-ного раствора едкого натра и нагревают. Осадок белка не образуется и при кипячении.
Результаты наблюдений заносят в таблицу 2.
Осаждение белков концентрированными минеральными кислотами
Концентрированные минеральные кислоты (Н2SO4, НСl, НNО3 и др.) вызывают необратимую денатурацию белков, следствием чего является агрегация белковых молекул и их осаждение.
Денатурирующее действие минеральных кислот объясняется их воздействием на функциональные группы белка. Минеральные кислоты, например, превращают отрицательно заряженную группу –СОО — в незаряженную –СООН, что приводит к нарушению ионных связей (солевых мостиков) и, как следствие, к разворачиванию полипептидных цепей. При длительном воздействии концентрированными минеральными кислотами могут произойти гидролиз белка, а также реакции нитрования, окисления, сульфирования и т.д.
Ход работы. К 1 мл концентрированной Н2SO4 осторожно, под тягой, по стенке пробирки добавляют 1 мл раствора яичного альбумина так, чтобы не смешивать жидкости.
На границе соприкосновения двух жидкостей образуется белое кольцо выпавшего в осадок белка. При осторожном смешивании жидкостей осадок не исчезает.
Результаты заносят в таблицу 2.
Осаждение белков органическими кислотами
Белки из растворов необратимо осаждаются органическими кислотами. Трихлоруксусная кислота (ТХУ) ССl3СООН и сульфосалициловая кислота С6Н3ОНСООНSО3Н являются очень чувствительными, специфическими реактивами на белок и широко применяются с этой целью.
Осаждение белков ТХУ часто применяют для полного удаления (осаждения) белков из биологических жидкостей.
Ход работы. В одну пробирку вносят 1 мл раствора белка и добавляют несколько капель 10%-ного раствора ТХУ. Выпадает осадок.
В другую пробирку вносят 1-2 мл раствора белка и добавляют несколько капель сульфосалициловой кислоты. Выпадает осадок белка.
Результаты вносят в таблицу 2.
Осаждение белков солями тяжелых металлов
При действии небольших концентраций солей тяжелых металлов (Рb +2 , Аg +1 , Аs +3 , Нg +2 , Сd +2 , Вi +3 и т.д.) на растворы белка происходит денатурация белковых молекул. Осаждение денатурированного белка обусловлено адсорбцией иона тяжелого металла на поверхности белковой молекулы и образованием не растворимых в воде комплексных соединений. Кроме того, тяжелые металлы нейтрализуют электрический заряд и изменяют четвертичную, третичную и вторичную структуры макромолекул белка, образуя связи между функциональными группами молекул.
Существуют определенные границы концентраций солей тяжелых металлов, при которых комплекс белка с солью тяжелого металла переходит в осадок либо находится в растворимом состоянии.
Ход работы. К 2 мл раствора яичного альбумина добавляют 5 капель 1%-ного раствора сульфата меди. Выпадает осадок, который растворяется в избытке (7-10 мл) раствора этой соли.
Результаты наблюдений заносят в таблицу 2.
Таблица 2 — Результаты наблюдений
| Исследуемый материал | Денатурирующий фактор и его воздействие | Наблюдения |
Материалы и реактивы: раствор яичного альбумина 1% (см. приложение Б, п.4); 10%-ный раствор уксусной кислоты; 10%-ный раствор NаОН; 96%-ный этиловый спирт; 80%-ный ацетон; концентрированные кислоты Н2SO4, НСl, НNО3; 1%-ный раствор сульфата меди; 10%-ный раствор ТХУ; насыщенный раствор NаСI.
Оборудование: пробирки обыкновенные; пипетки на 1–2 мл; спиртовка.
Контрольные вопросы
1.Что такое денатурация белка?
2. Какие Вы знаете денатурирующие факторы и каков механизм их действия?
3. Какие структуры белковых молекул изменяются при денатурации?
4. Является ли денатурация обратимым процессом?
Уравнение денатурации белка при нагревании
16 лет успешной работы в сфере подготовки к ЕГЭ и ОГЭ!
1602 поступивших (100%) в лучшие вузы Москвы
Подготовка к ЕГЭ, ОГЭ и предметным Олимпиадам в Москве
| До окончания записи осталось: | |||||||
| Записаться на экспресс-курс! | |||||||
- home
- map
У Вас возникли вопросы?
Мы обязательно Вам перезвоним:
Свертывание белков нагреванием
Описание.
Возьмем для опыта раствор белка куриных яиц. Попробуем нагреть пробу белка. При нагревании белка происходит денатурация. Молекулы белка меняют свою структуру, свернувшийся белок выпадает в виде мелких частиц и хлопьев. Свертывание белков при нагревании – необратимый процесс.