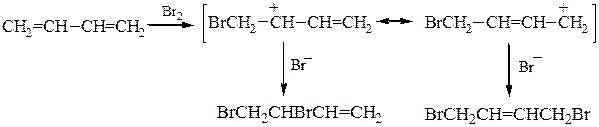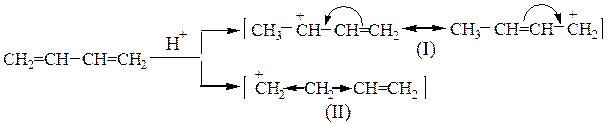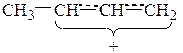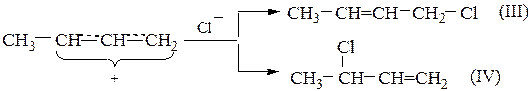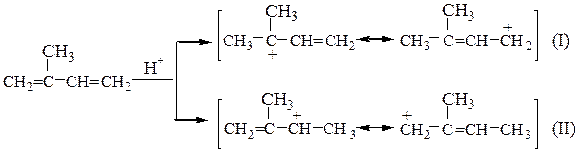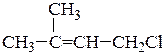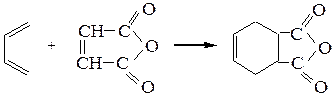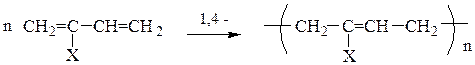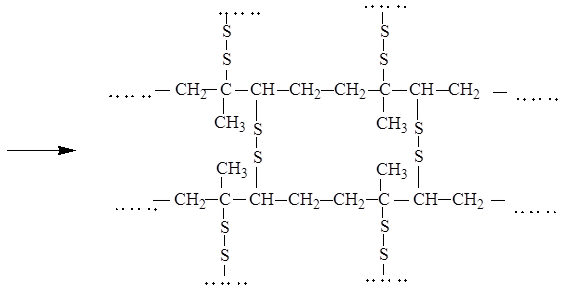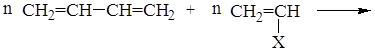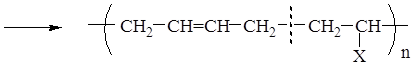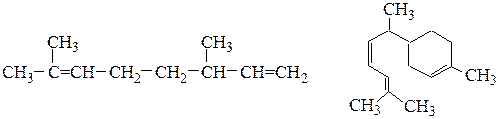Алкадиены – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствуют две двойные связи между атомами углерода С=С.
Общая формула алкадиенов CnH2n-2 (как у алкинов, а также циклоалкенов), где n ≥ 3.
Наличие двух двойных связей между атомами углерода очень сильно влияет на свойства углеводородов. В этой статье мы подробно остановимся на свойствах, способах получения и особенностях строения алкадиенов.
- Химические свойства сопряженных алкадиенов
- 1. Реакции присоединения
- 1.1. Гидрирование
- 1.2. Галогенирование алкадиенов
- 1.3. Гидрогалогенирование алкадиенов
- 1.5. Полимеризация
- 2. Окисление алкадиенов
- 2.1. Мягкое окисление алкадиенов
- 2.2. Жесткое окисление
- 2.3. Горение алкадиенов
- И 1,4-присоединение реагентов.
- Acetyl
- 🔥 Видео
Видео:4.1. Алкадиены (диены): Строение, номенклатура, изомерия. ЕГЭ по химииСкачать

Химические свойства сопряженных алкадиенов
Сопряженные алкадиены – непредельные нециклические углеводороды, в молекулах которых две двойные связи образуют сопряженную систему.
Химические свойства алкадиенов похожи на свойства алкенов. Алкадиены также легко вступают в реакции присоединения и окисления.
| Химические свойства сопряженных алкадиенов отличаются от алкенов некоторыми особенностями, которые обусловлены делокализацией электронной плотности π-связей. |
Видео:ЭТО ПОМОЖЕТ разобраться в Органической Химии — Алкены, Урок ХимииСкачать

1. Реакции присоединения
Для алкадиенов характерны реакции присоединения по одной из двойных связей С=С, либо по обоим связям. Реакции с водой, галогенами и галогеноводородами протекают по механизму электрофильного присоединения. При присоединении одной молекулы реагента к алкадиену рвется только одна двойная связь. При присоединении двух молекул реагента к алкадиену разрываются обе двойные связи.
| Помимо присоединения по одной из двух двойных связей (1,2-присоединение), для сопряженных диенов характерно так называемое 1,4-присоединение, когда в реакции участвует вся делокализованная система из двух двойных связей, реагент присоединяется к 1 и 4 атому углерода сопряженной системы, а двойная связь образуется между 2 и 3 атомами углерода. |
1.1. Гидрирование
Гидрирование алкадиенов протекает в присутствии металлических катализаторов, при нагревании и под давлением.
При присоединении одной молекулы водорода к дивинилу образуется смесь продуктов (бутен-1 и бутен-2):
Соотношение продуктов 1,2- и 1,4- присоединения зависит от условий реакции.
| При комнатной и повышенной температуре основным продуктом реакции является 1,4-продукт (бутен-2). |
При полном гидрировании дивинила образуется бутан:
1.2. Галогенирование алкадиенов
Присоединение галогенов к алкадиенам происходит даже при комнатной температуре в растворе (растворители — вода, CCl4).
| При взаимодействии с алкадиенами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на двойную связь. |
| Например, при взаимодействии бутадиена-1,3 с бромной водой преимущественно протекает 1,4 присоединение и образуется 1,4-дибромбутен-2: |
Побочным продуктом бромирования дивинила является 3,4-дибромбутен-1:
При полном бромировании дивинила образуется 1,2,3,4-тетрабромбутан:
1.3. Гидрогалогенирование алкадиенов
Алкадиены взаимодействуют с галогеноводородами. При присоединении хлороводорода к бутадиену-1,3 преимущественно образуется 1-хлорбутен-2:
3-Хлорбутен-1 образуется в небольшом количестве.
При присоединении полярных молекул к алкадиенам образуется смесь изомеров. При этом выполняется правило Марковникова.
| Правило Марковникова: при присоединении полярных молекул типа НХ к алкадиенам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода при двойной связи. |
1.5. Полимеризация
Полимеризация — это процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
nM → Mn (M – это молекула мономера)
| Полимеризация алкадиенов протекает преимущественно по 1,4-механизму, при этом образуется полимер с кратными связями, называемый каучуком. |
Продукт полимеризации дивинила (бутадиена) называется искусственным каучуком:
При полимеризации изопрена образуется природный (натуральный) каучук:
Видео:Каучуки: бутадиеновый, изопреновый, хлоропреновый. ЕГЭ по химииСкачать

2. Окисление алкадиенов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на мягкое и жесткое.
2.1. Мягкое окисление алкадиенов
Мягкое окисление алкадиенов протекает при низкой температуре в присутствии перманганата калия. При этом раствор перманганата обесцвечивается.
В молекуле алкадиена разрываются только π-связи и окисляются атомы углерода при двойных связях. При этом образуются четырехатомные спирты.
| Обесцвечивание алкадиенами водного раствора перманганата калия, как и в случае алкенов – качественная реакция на двойную связь. |
2.2. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) происходит полный разрыв двойных связей С=С и связей С-Н у атомов углерода при двойных связях. При этом у окисляемых атомов углерода образуются связи с атомами кислорода.
Так, если у атома углерода окисляется одна связь, то образуется группа С-О-Н (спирт). При окислении двух связей образуется двойная связь с атомом углерода: С=О, при окислении трех связей — карбоксильная группа СООН, четырех — углекислый газ СО2.
Можно составить таблицу соответствия окисляемого фрагмента молекулы и продукта:
| Окисляемый фрагмент | KMnO4, кислая среда | KMnO4, H2O, t |
| >C= | >C=O | >C=O |
| -CH= | -COOH | -COOK |
| CH2= | CO2 | K2CO3 |
При окислении бутадиена-1,3 перманганатом калия в среде серной кислоты возможно образование щавелевой кислоты и углекислого газа:
2.3. Горение алкадиенов
Алкадиены, как и прочие углеводороды, горят в присутствии кислорода с образованием углекислого газа и воды.
В общем виде уравнение сгорания алкадиенов выглядит так:
Видео:ТИПОВЫЕ ЗАДАЧИ ПО ХИМИИ: Химическое Количество Вещества, Моль, Молярная Масса и Молярный ОбъемСкачать

И 1,4-присоединение реагентов.
Гидрирование и галогенирование. Двойные связи дивинила реагируют не каждая сама по себе, а как единая p-система; атака мезомерного катиона нуклеофилом Вr — приводит к продуктам 1,2- и 1,4-присоединения, поскольку именно второй и четвертый атомы углерода сопряженной системы двойных связей несут в этом катионе положительный заряд:
Присоединение второй молекулы реагента дает один насыщенный продукт – 1,2,3,4-тетрабромбутан.
Аналогично, ступенчатое гидрирование бутадиена-1,3 протекает через образование бутена-1 (продукт 1,2-присоединения) и бутена-2 (продукт 1,4-присоединения), а полное гидрирование приводит к бутану.
Взаимодействие бутадиена-1,3 с хлороводородом происходит по механизму электрофильного присоединения (АЕ). При разрыве единой p-электронной системы сопряженного диена могут образовываться два карбкатиона:
Катион (I) представляет собой мезомерный катион, так как p-электроны двойной связи взаимодействуют с образующимся положительным центром, в результате чего происходит перераспределение электронной плотности:
Образовавшийся ион более устойчив, чем ион (II), в котором л-связь непосредственно не участвует во взаимодействии с карбкатионным центром и, кроме того, индуктивный эффект соседнего насыщенного атома углерода уменьшен под влиянием ненасыщенной винильной группы. Поэтому преимущественно образуется карбкатион (I), который на втором этапе реакции может связаться с хлорид-анионом через один из двух атомов углерода (центральный атом аллильного катиона не может образовывать новую связь):
Соотношение количеств изомеров (III) и (IV) зависит от условий проведения процесса. При обычных условиях преобладает продукт (III). Согласно общему механизму реакций присоединения анион хлора должен атаковать карбкатионный центр с противоположной стороны по отношению к той, где образовалась связь С-Н, поэтому более доступным для атаки оказывается самый удаленный концевой атом углерода аллильного иона.
2-метилбутадиена-1,3 гидрохлорирование эквимолярным количеством HCl
преимущественно дает 4-хлор-2-метилбутен-2.
Гибридный катион (I) имеет положительный заряд частично на третичном атоме углерода; в гибридном катионе (II) положительный заряд распределен между вторичным и первичным С-атомами. Таким образом гибрид (I) более стабилен и будет промежуточно образующимся в реакции карбкатионом. 1,4-Присоединение хлороводорода к изопрену дает
Электрофильное и радикальное присоединение к сопряженным диенам протекает легче, чем у алкенов. Это объясняется тем, что из диенов легче образуются карбкатионы или радикалы аллильного типа, которые стабильнее насыщенных карбкатионов или радикалов.
Диеновая конденсация (реакция Дильса-Альдера).При наличии у диенов цис-сопряженной системы двойных связей происходит их взаимодействие с непредельными соединениями (диенофилами) по типу 1,4-циклоприсоеди-нения, причем образующиеся с высокими выходами вещества (аддукты) содержат шестичленный цикл.
бутадиен-1,3 малеиновый аддукт
Полимеризация и сополимеризация. Сопряженные диены более склонны к полимеризации, чем алкены. В зависимости от строения исходного сопряженного диена, условий реакции, катализатора возможно образование полимерной цепи как за счет 1,4-, так и 1,2-присоединения. Практическое значение имеют полимеры, полученные в результате 1,4-присоединения.
Натуральный каучук является полимером 2-метилбутадиена-1,3 (Х = СН3) и по строению он представляет собой цис-полиизопрен.
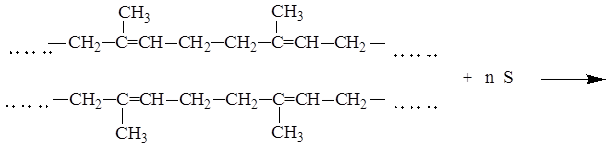
При сшивании линейных макромолекул каучука, как правило, сульфидными мостиками, он превращается в резину, теряет пластичность и приобретает упругость. Процесс превращения каучука в резину называется вулканизацией:
В настоящее время налажено производство различных видов каучуков, основанные на сополимеризации сопряженных диенов с прочими мономерами:
сополимер (например: Х = С6Н5 – бутадиен-стирольный каучук;
CN – бутадиен-нитрильный каучук и др.)
Контрольные вопросы к главе 3 «Диеновые углеводороды»
№ 1. Почему в случае присоединения хлороводорода к бутадиену-1,3 образуется смесь 3-хлорбутена-1 и 1-хлорбутена-2, в которой преобладает второе из названных соединений.
№ 2. При 1,4-присоединении хлороводорода к 2-метилбутадиену-1,3 (изопрену) в качестве основного продукта образуется 1-хлор-3-метилбутен-2, а не 1-хлор-2-метилбутен-2. Почему ?
№ 3. Какой из диенов – бутадиен-1,3 , изопрен (2-метилбутадиен-1,3) или пиперилен (пентадиен-1,3) при взаимодействии с 1 моль бромоводорода при 25 0 С дает только один продукт?
№ 4. Изобразите конфигурации цепей полимеров, полученных из бута-диена-1,3 в результате: (а) цис-1,4-присоединения; (б) транс-1,4-присоединения.
Что образуется в результате озонолиза полученных полимерных продуктов?
№ 5. При термической полимеризации бутадиена-1,3 в качестве побочного продукта образуется циклический димер, не склонный к дальнейшей полимеризации. Это вещество при гидрировании дает этилциклогексан; способно присоединять 2 моль брома; в результате деструктивного окисления образует 3-карбоксигександиовую кислоту. Какое строение имеет молекула димера бутадиена-1,3?
№ 6.Напишите уравнения реакций диеновой конденсации: (а) бутадиена-1,3 с тетрацианоэтиленом; (б)1-винилциклопентена с акролеином СH2=CH-CN; (в) 2-метилпентадиена-2,4 с малеиновым ангидридом; (г) 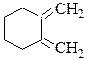
№ 7. Из каких реагентов можно получить следующие соединения по реакции Дильса—Альдера: 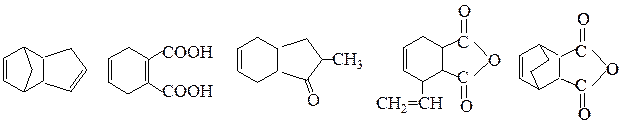
(в) мирцена (выделен из листьев лавра) (г) цингиберена
№ 9.Установите строение углеводородаС11Н20, если при окисление его хромовой смесью приводит к смеси бутанона-2, бутандиовой кислоты и пропионовой кислоты.
№ 10. Витамин D2 представляет собой непредельный спирт С28Н44О, в котором нет тройных связей. При каталитическом гидрировании он дает соединение С28Н52О. Сколько двойных связей содержит молекула витамина D2 ?
АЛКИНЫ
Определение.Алкины – ненасыщенные углеводороды, содержащие тройную связь и образующие гомологический ряд общей формулы СnH2n-2.
Изомерия.Обусловлена как разветвлением углеродного скелета (а), так и положением тройной связи (б); межклассовая изомерия с диенами (в).
Видео:Окисление органических соединений перманганатом калияСкачать

Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. 🔥 ВидеоТеория МО бутадиенаСкачать  4.3. Алкадиены (диены): Химические свойства. ЕГЭ по химииСкачать  73,2 g каучука, полученного при сополимеризации бутадиена-1,3 и стирола, обесцвечивает 400 g 8-ойСкачать  Химия ЕГЭ 2022 / Задание 32Скачать  ЭТОТ метод поможет на уроках ХИМИИ / Химия 9 классСкачать  Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать  Урок 173. Задачи на 1-й закон термодинамики - 1Скачать  Составление уравнений химических реакций. 1 часть. 8 класс.Скачать  Тепловой эффект хим. реакции. Энтальпия. Закон Гесса. Капучинка ^-^Скачать  Урок 133. Закон Бернулли. Уравнение БернуллиСкачать  Составление уравнений реакций. 1 часть. 10 класс.Скачать  Решение задач по уравнениям реакций, если одно из реагирующих веществ взято в избытке. 1 ч. 9 класс.Скачать  Опыты по химии. Получение этилена и опыты с нимСкачать  Окислительно-восстановительные реакции. 3 часть. 9 класс.Скачать  7.1. Спирты: Номенклатура, классификация, изомерия. ЕГЭ по химииСкачать  |