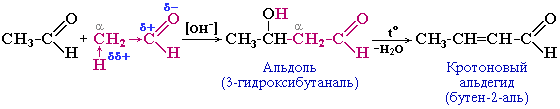Вы будете перенаправлены на Автор24
Альдегиды в щелочной среде вступают в реакции альдольной конденсации (А. Бородин, Ж. Вурц, 1872):
Сначала под действием основного катализатора — гидроксид-аниона или этоксид-аниона $C_2H_5O^-$ из альдегида образуется сопряженный анион — сильный нуклеофил, который атакует электрофильный центр карбонильной группы следующей молекулы альдегида. Полученный в результате такого взаимодействия алкоголятний анион быстро превращается в альдоль.
Так, например, две молекулы пропаналя в реакции с водными растворами гидроксидов при 0-5 $^circ$С образуют 3-гидрокси-2-метилпентаналь с 55-60% выходом, а две молекулы уксусного альдегида дают альдоль с 50%-ным выходом:
Видео:Альдольная конденсацияСкачать

Механизм альдольной конденсации катализируемой основаниями
Механизм реакций альдольной конденсации, катализируемых основаниями, включает три стадии:
На первой стадии образуются енолят-ионы. Равновесные концентрации енолят-ионов очень малы и редко превышают 1-3%, поскольку $pK_a$ альдегидов примерно равны 17-18, а для воды значение $pK_a$ равно 15,7. Присоединение енолят-ионов к карбонильным группам неионизированных молекул альдегидов на второй стадии определяет скорость всего процесса.
Готовые работы на аналогичную тему
Видео:АЛЬДОЛЬНАЯ КОНДЕНСАЦИЯСкачать

Дегидратация альдолей
Синтезированные альдоли при нагревании, как правило, легко отщепляют воду с образованием ненасыщенных карбонильных соединений. Процесс получения ненасыщенного альдегида или кетона из альдолей называют кротоновой конденсацией, по названию альдегида, впервые полученного таким методом:
Дегидратация альдолей в $alpha, beta$-ненасыщенные альдегиды также катализируется основаниями и протекает с промежуточным образованием енолят-ионов альдолей:
Видео:Альдольно кротоновая конденсацияСкачать

Механизм альдольной конденсации катализируемой кислотами
Альдегиды способны вступать в альдольную конденсацию и в кислой сред, но остановить реакцию на стадии альдолей при этом достаточно трудно, и часто получается продукт кротоновой конденсации.
В кислых средах определяющей скорость всего процесса стадией является присоединение енолов к карбонильным группам.
В отличие от щелочного катализатора, который действует только на метиленовую компонента, при кислотном катализе наблюдается действие как на метиленовый, так и на карбонильный компонент с протонизацией атомов кислорода:
В кислых средах практически невозможно остановить процесс на стадии образования альдолей и конечными продуктами оказываются $alpha, beta$-ненасыщенные альдегиды — продукты их дегидратации.
Для протонованой метиленовой компоненты характерно отщепление $H+$ от группы $OH$ с образованием исходной карбонильной молекулы или от $alpha$-углеродного атома с образованием енола. В еноле же под влиянием $+M$-эффекта атома кислорода и $-I$-эффекта вицильной группы электронная плотность $pi$-связи смещена отгидроксильной группы, в результате чего енол реагирует далее с активированной карбонильной компонентой.
В сильнокислой среде для альдолей обычно характерна дегидратация с образованием оксида мезитила. В условиях реакции оксид мезитила реагирует с последующей молекулой карбонильного соединенния и конечным продуктом, в отличие от реакции в щелочной среде, является форон (в присутствия газообразной кислоты) или мезитилен (в присутствии концентрированной жидкой кислоты).
Видео:10.1. Альдегиды и кетоны: Строение, номенклатура, изомерия. ЕГЭ по химииСкачать

Уравнение альдольной конденсации для этаналя
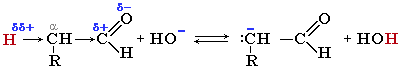
В молекуле альдегида или кетона на a -атоме углерода (соседнем с карбонильной группой) под влиянием карбонила понижена электронная плотность. Это вызывает поляризацию связи С a -Н и способствует отщеплению атома водорода в форме протона (H + ). В частности, происходящий под действием оснований отрыв протона от a -углеродного атома, приводит к образованию соответствующего карбаниона.
Такие карбанионы могут играть роль нуклеофилов по отношению к карбонильной группе другой молекулы альдегида или кетона. Поэтому оказываются возможными реакции, в которых одна молекула карбонильного соединения (в форме карбаниона) присоединяется к C=O-группе другого карбонильного соединения.
Например, уксусный альдегид на холоду при действии разбавленных растворов щелочей превращается в альдоль; при проведении реакции в более жестких условиях (при нагревании) альдоль дегидратируется с образованием кротонового альдегида.
Легкое отщепление воды от альдоля объясняется подвижностью водородного атома в a -звене, на которое действуют —I-эффекты двух групп (ОН и С=О).
Конденсацию альдегидов или кетонов, протекающую по первому типу, называют альдольной конденсацией, или альдольным присоединением, а по второму типу — кротоновой конденсацией.
Впервые эти реакции осуществили одновременно (1872 г.) и независимо друг от друга А.П. Бородин и Ш.А. Вюрц.
Видео:№ 82. Органическая химия. Тема 16. Альдегиды. Часть 7. Реакции конденсации, полимеризации альдегидовСкачать

Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. 🌟 ВидеоЧ-1 АЛЬДОЛЬНАЯ И АЛЬДОЛЬНО-кротоновая конденсацииСкачать  10.3. Альдегиды и кетоны: Химические свойства. ЕГЭ по химииСкачать  ЭТО ПОМОЖЕТ разобраться в Органической Химии — Алкены, Урок ХимииСкачать  Реакции окисления, нуклеофильного присоединения альдегидов и кетонов. 11 класс.Скачать  карбонильные соединения. часть 4Скачать  Химия. Альдегиды и кетоныСкачать  Лекция 18Скачать  Химия с нуля — АЛКИНЫ, Тройная связь, Типы Гибридизации // Органическая ХимияСкачать  Альдегиды строение, свойства | Химия 10 класс #28 | ИнфоурокСкачать  Конденсат Бозе - Эйнштейна: пятое агрегатное состояние веществаСкачать  Парообразование и конденсация. 8 класс.Скачать  10.2. Альдегиды и кетоны: Способы получения. ЕГЭ по химииСкачать  Химические свойства альдегидов и кетонов. 11 класс.Скачать  Органическая Химия — Алканы и Цепь из АтомовСкачать  Получение альдегидов и кетонов. 11 класс.Скачать  |