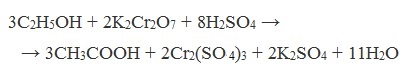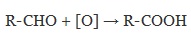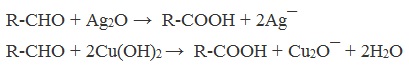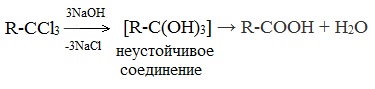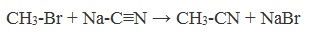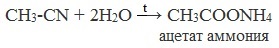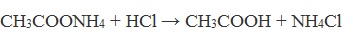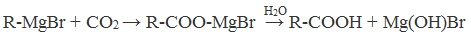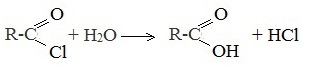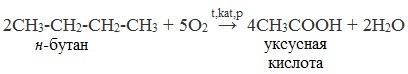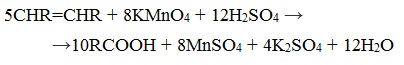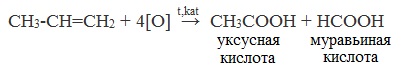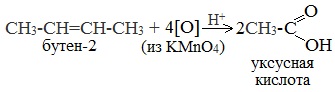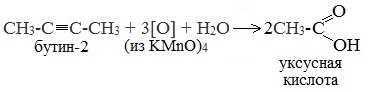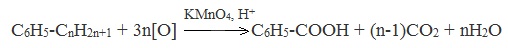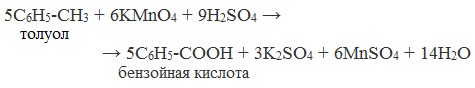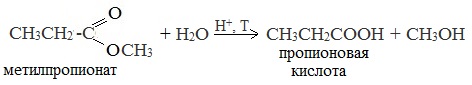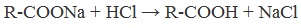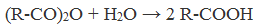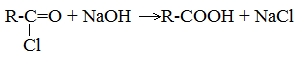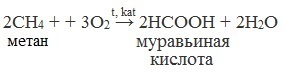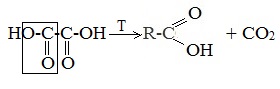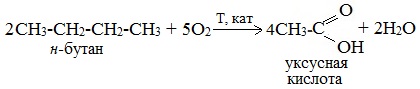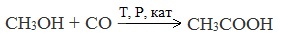Ввиду очень высокой реакционной способности вещества, оно является очень важным исходным материалом для выполнения синтеза целого ряда различных органических соединений, включая и синтез уксусной кислоты. Производство уксусной кислоты синтетического типа из ацетилена, получило очень широкое развитие и уверено вошло в промышленность тяжелого органического синтеза. А некоторые страны для производства уксусной кислоты используют исключительно ацетилен. В основе данного процесса лежит реакция гидратации ацетилена в вещество ацетальдегид, который после окисляют в знакомую нам уксусную кислоту, купить которую можно в любом магазине. Раньше сам ацетилен получали только из карбида кальция. Но на сегодняшний день в большинстве стран карбид кальция – это один из главнейших исходных материалов для получения ацетилена. Реакция воды с карбидом протекает при стандартной температуре с определенным количественным выходом ацетилена. Его концентрация в сыром газе составляет почти 99%.
Существуют специальные заводы, которые занимаются производством карбида кальция. Но на многих химических заводах включая и заводы синтетического каучука и уксусной кислоты, имеются специальные карбидные цехи, а также цехи по получению ацетилена, и растворителя 647, цена производства которого таким методом достаточно высока. Существующий сегодня метод производства ацетилена из карбида кальция имеет некоторые недостатки, главный из которых – это громоздкое оборудование и затруднение использования шлама-отхода, который накапливается в очень больших количествах. По этой причине, до сегодняшнего времени в связи с большой потребностью в ацетилене как исходном сырьевом материале для выполнения синтеза. Во многих странах ведутся интенсивные исследовательские работы по получению его из метана, пропана, этана, бутана, которые содержаться в промышленных и естественных нефтяных газах, и даже из растворителя р5, купить который для этого — достаточно нерациональный шаг. Также ведутся работы по получению ацетилена из нескольких типов жидких углеводородов (керосина, бензина, мазута и др.). Но самый большой интерес вызывает получения данного вещества из природного газа. Сейчас данный метод только внедряется в промышленность и очень интенсивно совершенствуется.
- Свойства алкинов
- Физические свойства алкинов
- Химические свойства алкинов
- Реакции электрофильного присоединения (реакции тройной углерод-углеродной связи)
- Реакции замещения водородных атомов ацетилена
- Уксусная кислота из ацетилена уравнение
- Общие способы получения карбоновых кислот
- В промышленности
- В лаборатории
- Специфические способы получения важнейших кислот
Свойства алкинов
Свойства алкинов – физические и химические похожи на свойства алкенов и алкадиенов. Однако кислотные свойства алкинов создают ряд отличительных химических свойств.
Физические свойства алкинов
Алкины, за исключением ацетилена, не имеют цвета и запаха. При нормальных условиях первые 4 члена ряда являются газами, с 5 по 15 – жидкостями, более 15 – твердыми веществами.
Растворимость алкинов
Алкины являются относительно полярными молекулами, поэтому хорошо растворимы в полярных растворителях или растворителях с низкой полярностью. В воде алкины растворяются незначительно, но лучше, чем алканы и алкены.
Точки плавления и кипения алкинов
Как правило, алкины плавятся и кипят при более высоких температурах, по сравнению соответствующих алканов и алкенов. Температуры плавления и кипения алкинов, увеличиваются пропорционально их молекулярной массе.
В таблице приведены физические постоянные некоторых алкинов:
Химические свойства алкинов
В общем алкины более реакционноспособны, чем алканы и алкены. Большинство реакций, в которых они участвуют являются реакциями электрофильного присоединения. Однако терминальные алкины (тройная связь находится в конце цепи) также подвергаются и реакциям замещения. Атомы водорода при sp-гибридизованном атоме углерода способны подвергаться протонизации, вследствие чего алкины имеют относительно кислую природу.
Реакции электрофильного присоединения (реакции тройной углерод-углеродной связи)
1) Гидрирование алкинов. В присутствии активных катализаторов (никель, платина) восстанавление алкинов водородом происходит сразу до алканов. При использовании менее активных катализаторов (Pd, железо Ренея) реакция протекает через стадию образования алкена:
При гидрировании гомологов ацетилена на первой стадии получаются цис-олефины.
2) Галогенирование алкинов протекает в две легко разделимые стадии, из которых первая стадия протекает более энергично. При недостатке галогена реакция идет в одну стадию, при избытке – две стадии:
3) Гидрогалогенирование алкинов также протекает в две разделимые стадии. При гидрохлорировании ацетилена на первоначальном этапе образуется важный в промышленности продукт – хлористый винил, далее происходит образование 1,1-дихлорэтан:
Присоединение молекулы HCl к хлористому винилу происходит по правилу Марковникова. Аналогичным образом присоединяется молекула HBr.
4) Гидратация алкинов происходит согласно правилу Марковникова с участием Hg 2+ в качестве катализатора (реакция Кучерова). В ходе такой реакции, из ацетилена образуется ацетальдегид, а из его гомологов — кетоны: 5) Присоединение спиртов и меркаптанов. При воздействии едкого кали ацетилен и монозамещенные ацетилены под давлением присоединяют спирты, образуя акрилвиниловые эфиры (Реппе, Фаворский А.Е., М.Ф. Шоствковский):
Подобным образом происходит присоединение меркаптанов.
6) Присоединение кислот.
Присоединение уксусной кислоты к ацетилену происходит в условиях гетерогенного катализа (H3PO4 или B2O3) с образованием винилацетата:
Винилацетат хорошо полимеризуется с образованием поливинилацетата (ПВА):
Присоединение синильной кислоты к ацетилену происходит с образованием акрилонитрила:
Акрилонитрил используют для получения полиакрилонитрила: 7) Присоединение хлоридов некоторых металлов к ацетилену:
8) Реакции полимеризации
Димеризация ацетилена происходит в присутствии солей Cu (I) с образованием винилацетилена. Дальнейшее его взаимодействие с соляной кислотой приводит к образованию хлоропрена, который используют при получении хлоропреновых каучуков:
А.Д. Петров путем кросс-димеризации ацетилена получил изобутилен. В качестве катализаторов выступает никель в присутствии хлорида цинка:
Тримеризация ацетилена в присутствии активного угля и при температуре около 600°С ведет к образованию такого важного продукта, как бензол (реакция Зелинского):
Ученый Шеффер в 1966 г обнаружил, что при пропускании над хлоридом алюминия раствора диметилацетилена в бензоле, последний тримеризуется. Продуктом реакции является гексаметилбицикло[2,2,0]гексадиен (гексаметилдьюаровский бензол), который далее при при воздействии температуры подвергается изомеризации в гексаметилбензолПри использовании в качестве катализатора димезитиленкобальта гексаметилбензол получается непосредственно из диметилацетилена:
Тетрамеризация ацетилена под действием комплексных солей никеля ведет к образованию циклоокта-1,3,5,7-тетраена (синтез Реппе):
10) Окисление алкинов концентрированным раствором перманганата калия (KMnO4) в кислой среде протекает с образованием карбоновых кислот. Розовый раствор KMnO4 в ходе реакции обесцвечивается:
Окисление алкинов в мягких условиях, т.е. разбавленный раствор KMnO4, комнатная температура, происходит без разрыва связей. При окислении ацетилена продуктом реакции является щавелевая кислота, при окислении его гомологов в нейтральной среде реакцию можно остановить на стадии образования дикетонов:
При горении алкинов происходит их полное окисление до углекислого газа и воды. Реакция экзотермическая и протекает с выделением 1300 кДж/моль тепла:
Реакции замещения водородных атомов ацетилена
1) Взаимодействие с солями тяжелых металлов (качественная реакция). При взаимодействии ацетилена и монозамещенных гомологов с аммиачными растворами окиси серебра или полухлористой меди обрадуются нерастворимые осадки ацетиленидов:
Ацетилинид серебра Ag-C≡C-Ag – бесцветный и R-C≡C-Ag — белый
Ацетилинид меди Cu-C≡C-Cu – вишнево-бурый и R-C≡C-Cu – желто-бурый
Ацетилениды – взрывчатые вещества. Под действием кислот разлагаются с образованием ацетилена и соответствующих солей металлов.
2) Взаимодействие ацетилена и его гомологов с щелочными и щелочноземельными металлами в жидком аммиаке также приводит к образованию ацетилинидов:
Действие производных Na и Mg, известных как реактив Иоцича, подобно реактиву Греньяра, поэтому широко используются в органическом синтезе.
3) Взаимодействие ацетилена и его гомологов с кетонами в присутствии едкого кали, под небольшим давлением (А.Е. Фаворский): 4) Взаимодействие ацетилена и его гомологов с альдегидами в присутствии ацетилинида меди (Реппе):
5) Ацетилен-аллен-диеновая перегруппировка Фаворского происходит при нагревании ацетиленов с металлическим натрием. При этом расположенная «внутри» соединения тройная связь перемещается в конец. А при нагревании ацетиленов с расположенной в конце тройной связью со спиртовым раствором щелочи происходит перемещение тройной связи к центру молекулы:
Уксусная кислота из ацетилена уравнение
Некоторые карбоновые кислоты встречаются в природе в свободном состоянии (муравьиная, уксусная, масляная, валериановая и др.). Однако, основным источником карбоновых кислот является органический синтез. Рассмотрим основные способы получения карбоновых кислот
Общие способы получения карбоновых кислот
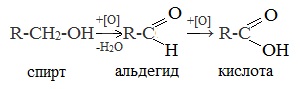
1. Окисление первичных спиртов и альдегидов под действием различных окислителей
В качестве окислителей применяют KMnO4 и K2Cr2O7.
Например:
Для окисления альдегидов используются те же реагенты, что и для спиртов.
При окислении перманганатом калия происходит обесцвечивание фиолетово-розового раствора.
При окислении дихроматом калия — цвет меняется с оранжевого на зеленый.
А также для них характерны реакции «серебряного зеркала» и окисление гидроксидом меди (II) – качественные реакции альдегидов:
2. Гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода
В результате реакции образуются спирты, содержащие три группы ОН у одного атома углерода. Такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты:
3. Получение карбоновых кислот из цианидов (нитрилов)
Этот способ позволяет наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия:
Образующийся нитрил уксусной кислоты CH3-CN (ацетонитрил, метилцианид) при нагревании гидролизуется с образованием ацетата аммония:
При подкислении раствора выделяется кислота:
4. Использование реактива Гриньяра (по схеме)
5. Гидролиз галогенангидридов кислот
С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту:
В промышленности
1. Выделяют из природных продуктов
(жиров, восков, эфирных и растительных масел)
2. Окисление алканов кислородом воздуха ( в присутствии катализаторов – солей марганца или при нагревании под давлением)
Обычно образуется смесь кислот. При окислении бутана единственным продуктом является уксусная кислота:
3. Окисление алкенов и алкинов
При жестком окислении алкенов кипящим раствором KMnO4 в кислой среде происходит полный разрыв двойной связи:
При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты:
4. Окисление гомологов бензола (получение бензойной кислоты)
Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия:
В лаборатории
1. Гидролиз сложных эфиров
При кислотном гидролизе получают карбоновые кислоты и спирты (реакция обратная этерификации):
2. Из солей карбоновых кислот
3. Гидролиз ангидридов кислот
При легком нагревании с водой ангидриды образуют соответствующие карбоновые кислоты:
4. Щелочной гидролиз галоген производных карбоновых кислот
Специфические способы получения важнейших кислот
Способы получения НСООН
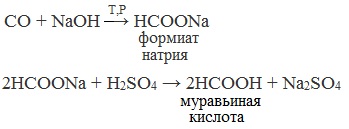
1. Взаимодействие оксида углерода (II) с гидроксидом натрия
Муравьиную кислоту получают нагреванием под давлением гидроксида натрия и оксида углерода (II) под давлением и обработкой полученного формиата натрия серной кислотой:
2. Каталитическое окисление метана
3. Декарбоксилирование щавелевой кислоты
Муравьиную кислоту можно получить при нагревании щавелевой кислоты:
Способы получения СН3СООН
Получение уксусной кислоты для химических целей
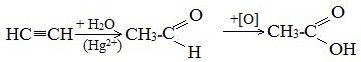
1. Синтез из ацетилена
Данный способ получения уксусной кислоты основан на окислении уксусного альдегида, который в свою очередь получают из ацетилена по реакции Кучерова (ацетилен получают из очень доступного сырья — метана):
2. Каталитическое окисление бутана
Большое значение имеет способ получения уксусной кислоты, основанный на окислении бутана кислородом воздуха:
Процесс получения уксусной кислоты из метана является многостадийным (метан – ацетилен – уксусный альдегид – уксусная кислота). Ее получение окислениям будана сокращает число стадий, что дает большой экономический эффект.
3. Каталитическое карбонилирование метанола
Получение уксусной кислоты для пищевых целей
4. Уксуснокислое брожение этанола
Уксусную кислоту для пищевых целей получают уксуснокислым брожением жидкостей, содержащих спирт (вино. пиво):