Гидроксид бериллия Be(OH)2 — неорганическое соединение. Белый, при нагревании разлагается. Не растворяется в воде. Проявляет амфотерные свойства.
Относительная молекулярная масса Mr = 43,03; относительная плотность для тв. и ж. состояния d = 1,92.
- Способы получения
- Качественная реакция
- Химические свойства
- Гидроксид бериллия (Be (OH) 2) химическое строение, свойства и применение
- Химическая структура
- Бериллий гидроокись альфа
- Бета-гидроксид бериллия
- Гидроксид бериллия в минералах
- Паровая гидроокись бериллия
- свойства
- внешний вид
- Термохимические свойства
- растворимость
- Риски подверженности
- приложений
- получение
- Получение металлического бериллия
- Гидроксид бериллия (Be (OH) 2): структура, свойства и применение
- Содержание:
- Химическая структура
- Альфа-гидроксид бериллия
- Бета-гидроксид бериллия
- Гидроксид бериллия в минералах
- Пары гидроксида бериллия
- Свойства
- вид
- Термохимические свойства
- Растворимость
- Риски воздействия
- Приложения
- Получение
- Получение металлического бериллия
- Ссылки
Способы получения
1. Гидроксид бериллия получают в результате взаимодействия хлорида бериллия и разбавленного раствора гидроксида натрия , на выходе образуется хлорид натрия и гидроксид бериллия :
BeCl2 + 2NaOH = Be(OH)2↓ + 2NaCl
При избытке раствора щелочи образуется комплексная соль:
2 . При взаимодействии бериллия с водой в состоянии кипения образуется гидроксид бериллия или оксид бериллия и водород:
3. Хлорид бериллия при взаимодействии с концентрированным гидратом аммиака образует хлорид аммония и гидроксид бериллия:
4. Сульфат бериллия взаимодействует с разбавленным раствором гидроксида натрия, образуя гидроксид бериллия и сульфат натрия:
5. В результате реакции между сульфатом бериллия и концентрированным гидратом аммиака образуется гидроксид бериллия и сульфат аммония:
Качественная реакция
Качественная реакция на гидроксид бериллия — окрашивание фенолфталеина в малиновый цвет .
Химические свойства
1. Гидроксид бериллия взаимодействует со сложными веществами :
1.1. Гидроксид бериллия реагирует с кислотами:
1.1.1. В результате реакции между гидроксидом бериллия и разбавленной соляной кислотой образуется хлорид бериллия и вода:
1.1.2. С разбавленной плавиковой кислотой гидроксид бериллия также может взаимодействовать. При этом образуются фторид бериллия и вода:
1.1.3. Гидроксид бериллия вступает в реакцию с концентрированной плавиковой кислотой, образуя на выходе тетрафторобериллат водорода и воду:
1.2. Гидроксид бериллия взаимодействует с оксидами:
1.2.1. В результате взаимодействия гидроксида бериллия и углекислого газа образуется дигидроксокарбонат бериллия и вода:
1.3. Гидроксид бериллия вступает в реакцию с основаниями :
1.3.1. Гидроксид бериллия взаимодействует с концентрированным раствором гидроксида натрия образуя тетрагидроксобериллат натрия:
1.3.2. При взаимодействии гидроксида бериллия и гидроксида натрия при 200 — 300º С с образованием бериллата натрия и воды:
2. Гидроксид бериллия разлагается при температуре 200 — 800º С, образуя на выходе оксид бериллия и воду:
Гидроксид бериллия (Be (OH) 2) химическое строение, свойства и применение
гидроксид бериллия представляет собой химическое соединение, состоящее из двух молекул гидроксида (ОН) и молекулы бериллия (Ве). Его химическая формула Be (OH)2 и он характеризуется как амфотерный вид. Как правило, он может быть получен в результате реакции между моноксидом бериллия и водой в соответствии со следующей химической реакцией: BeO + H2O → Be (OH)2
С другой стороны, это амфотерное вещество имеет молекулярную конфигурацию линейного типа. Однако могут быть получены различные структуры гидроксида бериллия: альфа и бета форма, как минеральная, так и в паровой фазе, в зависимости от используемого метода..
- 1 Химическая структура
- 1.1 Бериллий гидроксид альфа
- 1.2 Бета-бериллиевый гидроксид
- 1.3 Гидроксид бериллия в минералах
- 1.4 Пар бериллиевого гидроксида
- 2 свойства
- 2.1 Внешний вид
- 2.2 Термохимические свойства
- 2.3 Растворимость
- 2.4 Риски, связанные с воздействием
- 3 использования
- 4 Получение
- 4.1 Получение металлического бериллия
- 5 ссылок
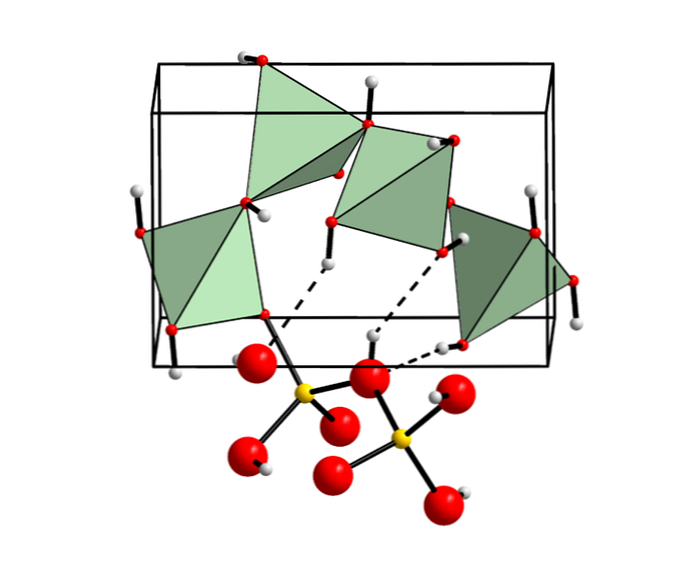
Химическая структура
Это химическое соединение может быть найдено четырьмя различными способами:
Бериллий гидроокись альфа
При добавлении любого основного реагента, такого как гидроксид натрия (NaOH), к раствору соли бериллия, получается альфа (α) форма гидроксида бериллия. Пример показан ниже:
2NaOH (разбавленный) + BeCl2 → Be (OH)2↓ + 2NaCl
Бета-гидроксид бериллия
Вырождение этого альфа-продукта формирует метастабильную тетрагональную кристаллическую структуру, которая через длительный период времени превращается в ромбическую структуру, называемую бета-гидроксидом бериллия (β).
Эта бета-форма также получается в виде осадка из раствора бериллия натрия гидролизом в условиях, близких к температуре плавления..
Гидроксид бериллия в минералах
Хотя это не обычно, гидроксид бериллия встречается как кристаллический минерал, известный как бехоит (называемый таким образом в связи с его химическим составом).
Встречается в гранитных пегматитах, образующихся при превращении гадолинита (минералов группы силикатов) в вулканические фумаролы..
Этот относительно новый минерал был впервые обнаружен в 1964 году и в настоящее время обнаружен только в гранитных пегматитах, расположенных в штатах Техас и Юта в Соединенных Штатах..
Паровая гидроокись бериллия
При температуре выше 1200 ° C (2190 ° C) в паровой фазе существует гидроксид бериллия. Получается в результате реакции между водяным паром и оксидом бериллия (BeO).
Аналогично, полученный пар имеет парциальное давление 73 Па, измеренное при температуре 1500 ° С..
свойства
Гидроксид бериллия имеет молярную массу или приблизительную молекулярную массу 43,0268 г / моль и плотность 1,92 г / см. 3 . Его температура плавления находится при температуре 1000 ° С, при которой начинается его разложение..
В качестве минерала, Be (OH)2 (Behoita) имеет твердость 4, а его плотность составляет 1,91 г / см. 3 и 1,93 г / см 3 .
внешний вид
Гидроксид бериллия представляет собой белое твердое вещество, которое в своей альфа-форме имеет желатиновый и аморфный вид. С другой стороны, бета-форма этого соединения имеет четко выраженную орторомбическую и стабильную кристаллическую структуру..
Можно сказать, что морфология минерала Be (OH)2 он разнообразен, потому что его можно найти в виде ретикулярных кристаллов, древесных или сферических агрегатов. Точно так же это прибывает в белый, розовый, голубоватый и даже бесцветный и с жирным стекловидным блеском.
Термохимические свойства
Энтальпия образования: -902,5 кДж / моль
Энергия Гиббса: -815,0 кДж / моль
Энтропия образования: 45,5 Дж / моль
Теплоемкость: 62,1 Дж / моль
Удельная теплоемкость: 1443 Дж / К
Стандартная энтальпия образования: -20,98 кДж / г
растворимость
Гидроксид бериллия по своей природе амфотерный, поэтому он способен отдавать или принимать протоны и растворять как кислые, так и щелочные среды в кислотно-щелочной реакции с образованием соли и воды..
В этом смысле растворимость Be (OH)2 в воде ограничен продуктом растворимости Kps(H 2 O), что равно 6,92 × 10 -22 .
Риски подверженности
Законно допустимый предел воздействия на человека (PEL или OSHA) вещества, содержащего гидроксид бериллия, установлен для максимальной концентрации от 0,002 мг / м. 3 и 0,005 мг / м 3 составляет 8 часов, а для концентрации 0,0225 мг / м 3 максимум 30 минут.
Эти ограничения связаны с тем, что бериллий классифицируется как канцерогенный агент типа А1 (канцерогенный агент у людей, на основании количества данных эпидемиологических исследований).
приложений
Использование гидроксида бериллия в качестве сырья для обработки какого-либо продукта очень ограничено (и необычно). Однако это соединение используется в качестве основного реагента для синтеза других соединений и получения металлического бериллия..
получение
Оксид бериллия (BeO) — химическое соединение высокочистого бериллия, наиболее используемое в промышленности. Он характеризуется как бесцветное твердое вещество со свойствами электрической изоляции и высокой теплопроводностью..
В этом смысле процесс его синтеза (по техническому качеству) в первичной промышленности осуществляется следующим образом:
- Гидроксид бериллия растворяют в серной кислоте (Н2SW4).
- Когда реакцию проводят, раствор фильтруют, так что нерастворимые примеси оксида или сульфата удаляются таким образом..
- Фильтрат подвергают выпариванию для концентрирования продукта, который охлаждают до получения кристаллов сульфата бериллия BeSO4.
- БеСО4 кальцинируют при определенной температуре от 1100 ° C до 1400 ° C.
Конечный продукт (BeO) используется для изготовления специальных керамических изделий промышленного назначения..
Получение металлического бериллия
При добыче и переработке бериллиевых минералов образуются примеси, такие как оксид бериллия и гидроксид бериллия. Последний подвергается серии превращений до получения металлического бериллия.
Be (OH) реагирует2 с раствором бифторида аммония:
(NH4)2BeF4 он подвергается повышению температуры, подвергаясь термическому разложению:
Наконец, восстановление фторида бериллия при температуре 1300 ° C магнием (Mg) приводит к металлическому бериллию:
Бериллий используется в металлических сплавах, производстве электронных компонентов, производстве радиационных экранов и окон, используемых в рентгеновских аппаратах..
Гидроксид бериллия (Be (OH) 2): структура, свойства и применение
Гидроксид бериллия (Be (OH) 2): структура, свойства и применение — Наука
Содержание:
В гидроксид бериллия Это химическое соединение, состоящее из двух молекул гидроксида (ОН) и одной молекулы бериллия (Ве). Его химическая формула — Be (OH).2 и он характеризуется тем, что является амфотерным видом. Обычно его можно получить в результате реакции между монооксидом бериллия и водой в соответствии со следующей химической реакцией: BeO + H2О → Ве (ОН)2
С другой стороны, это амфотерное вещество имеет линейную молекулярную конфигурацию. Однако из гидроксида бериллия можно получить различные структуры: альфа- и бета-формы, в виде минерала и в паровой фазе, в зависимости от используемого метода.
Химическая структура
Это химическое соединение можно найти в четырех различных формах:
Альфа-гидроксид бериллия
Добавление любого основного реагента, такого как гидроксид натрия (NaOH), к раствору соли бериллия дает альфа (α) форму гидроксида бериллия. Пример показан ниже:
2NaOH (разбавленный) + BeCl2 → Be (ОН)2↓ + 2NaCl
Бета-гидроксид бериллия
Вырождение этого альфа-продукта формирует метастабильную тетрагональную кристаллическую структуру, которая по прошествии длительного периода времени превращается в ромбическую структуру, называемую бета (β) гидроксидом бериллия.
Эта бета-форма также получается в виде осадка из раствора бериллия натрия путем гидролиза в условиях, близких к температуре плавления.
Гидроксид бериллия в минералах
Хотя это необычно, гидроксид бериллия встречается в виде кристаллического минерала, известного как бегоит (названный в честь его химического состава).
Он образуется в гранитных пегматитах, образованных преобразованием гадолинита (минералы из группы силикатов) в вулканические фумаролы.
Этот относительно новый минерал был впервые обнаружен в 1964 году, а в настоящее время они обнаружены только в гранитных пегматитах, расположенных в штатах Техас и Юта в США.
Пары гидроксида бериллия
При температурах выше 1200 ° C (2190 ° C) гидроксид бериллия находится в паровой фазе. Его получают в результате реакции водяного пара с оксидом бериллия (BeO).
Точно так же образующийся пар имеет парциальное давление 73 Па, измеренное при температуре 1500 ° C.
Свойства
Гидроксид бериллия имеет приблизительную молярную массу или молекулярную массу 43,0268 г / моль и плотность 1,92 г / см. 3 . Его точка плавления находится при температуре 1000 ° C, при которой начинается его разложение.
Как минерал Be (OH)2 (бегоит) имеет твердость 4, а его плотность составляет 1,91 г / см 3 и 1,93 г / см 3 .
вид
Гидроксид бериллия представляет собой белое твердое вещество, которое в альфа-форме имеет студенистый и аморфный вид. С другой стороны, бета-форма этого соединения состоит из четко определенной, ромбической и стабильной кристаллической структуры.
Можно сказать, что морфология минерала Be (OH)2 он разнообразен, поскольку может быть найден в виде сетчатых, древовидных кристаллов или сферических агрегатов. Точно так же он бывает белого, розового, голубоватого и даже бесцветного цвета и с жирным стекловидным блеском.
Термохимические свойства
Энтальпия образования: -902,5 кДж / моль
Энергия Гиббса: -815,0 кДж / моль.
Энтропия образования: 45,5 Дж / моль
Теплоемкость: 62,1 Дж / моль
Удельная теплоемкость: 1,443 Дж / К
Стандартная энтальпия образования: -20,98 кДж / г
Растворимость
Гидроксид бериллия является амфотерным по своему характеру, поэтому он способен отдавать или принимать протоны и растворяется как в кислой, так и в основной среде в кислотно-щелочной реакции с образованием соли и воды.
В этом смысле растворимость Be (OH)2 в воде он ограничен произведением растворимости Kps(H2O), что равно 6,92 × 10 -22 .
Риски воздействия
Законный допустимый предел воздействия на человека (PEL или OSHA) гидроксида бериллия, установленный для максимальной концентрации в пределах 0,002 мг / м 3 и 0,005 мг / м 3 составляет 8 часов, а для концентрации 0,0225 мг / м 3 максимальное время 30 минут.
Эти ограничения связаны с тем, что бериллий классифицируется как канцероген типа A1 (канцероген для человека, исходя из количества данных эпидемиологических исследований).
Приложения
Использование гидроксида бериллия в качестве сырья для обработки некоторых продуктов очень ограничено (и необычно). Однако это соединение, используемое в качестве основного реагента для синтеза других соединений и получения металлического бериллия.
Получение
Оксид бериллия (BeO) — наиболее широко используемое химическое соединение бериллия высокой чистоты в промышленности. Он характеризуется как бесцветное твердое вещество с электроизоляционными свойствами и высокой теплопроводностью.
В этом смысле процесс его синтеза (по техническому качеству) в первичной промышленности осуществляется следующим образом:
- Гидроксид бериллия растворяется в серной кислоте (H2ЮЗ4).
- После проведения реакции раствор фильтруют, чтобы таким образом удалить нерастворимые оксидные или сульфатные примеси.
- Фильтрат упаривают для концентрирования продукта, который охлаждают с получением кристаллов сульфата бериллия BeSO.4.
- Поцелуй4 его прокаливают при определенной температуре от 1100 ° C до 1400 ° C.
Конечный продукт (BeO) используется для изготовления специальных керамических изделий промышленного назначения.
Получение металлического бериллия
Во время добычи и обработки минералов бериллия образуются примеси, такие как оксид бериллия и гидроксид бериллия. Последний подвергают серии превращений до получения металлического бериллия.
Be (OH) реагирует2 с раствором бифторида аммония:
(NH4)2BeF4 подвергается повышению температуры, подвергаясь термическому разложению:
Наконец, восстановление фторида бериллия при температуре 1300 ° C магнием (Mg) приводит к металлическому бериллию:
Бериллий используется в металлических сплавах, производстве электронных компонентов, производстве экранов и радиационных окон, используемых в рентгеновских аппаратах.
Ссылки
- Википедия. (н.д.). Гидроксид бериллия. Восстановлено с en.wikipedia.org
- Холлеман, А. Ф .; Виберг, Э. и Виберг, Н. (2001). Гидроксид бериллия. Получено с books.google.co.ve
- Издательство, М. Д. (н.э.). Бехойте. Получено с сайта handbookofmineralogy.org
- Все реакции. (н.д.). Гидроксид бериллия Be (OH)2. Получено с allreactions.com
- PubChem. (н.д.). Гидроксид бериллия. Получено с pubchem.ncbi.nlm.nih.gov
- Уолш, К. А., Видаль, Э. Э. (2009). Химия и переработка бериллия. Получено с books.google.co.ve
15 основных характеристик живых существ
Дрок: характеристика, систематика, среда обитания, свойства, уход.