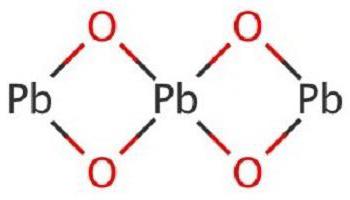
| Оксид свинца II | |
|---|---|
 | |
| Систематическое наименование | Оксид свинца |
| Традиционные названия | Окись свинца |
| Хим. формула | PbO |
| Рац. формула | PbO |
| Состояние | α-красные, β-жёлтые кристаллы |
| Молярная масса | 223,20 г/моль |
| Плотность | α 9,13; 9,40 β 9,45; 9,63 г/см³ |
| Т. плав. | 886 °C |
| Т. кип. | 1535 °C |
| Мол. теплоёмк. | 46,41 Дж/(моль·К) |
| Энтальпия образования | -218,6 кДж/моль |
| Растворимость в воде | α 0,279 22 β 0,513 22 г/100 мл |
| ГОСТ | ГОСТ 9199-77 ГОСТ 5539-73 |
| Рег. номер CAS | 1317-36-8 |
| PubChem | 14827 |
| Рег. номер EINECS | 215-267-0 |
| SMILES | |
| RTECS | OG1750000 |
| ChEBI | 81045 |
| Номер ООН | 3288 |
| ChemSpider | 14141 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Оксид свинца II — бинарное неорганическое соединение металла свинца и кислорода с формулой PbO, красные или жёлтые кристаллы, плохо растворимые в воде.
- Содержание
- Получение
- Физические свойства
- Химические свойства
- Применение
- Физиологическое действие
- Оксид свинца: формула, свойства, метод получения
- Способы его получения
- Физические характеристики
- Химические особенности и свойства
- Оксид свинца II
- Оксид свинца IV
- Применение
- №82 Свинец
- История открытия:
- Нахождение в природе, получение:
- Физические свойства:
- Химические свойства:
- Важнейшие соединения:
- Применение:
Содержание
- 1 Получение
- 2 Физические свойства
- 3 Химические свойства
- 4 Применение
- 5 Физиологическое действие
Получение
- В природе встречаются минералы свинцовый глёт и массикот — оксид свинца PbO с различными примесями.
- Пропуская воздух через расплавленный свинец:
2Pb + O2 → 600oC 2PbO
- Нагревание гидроксида свинца:
Pb(OH)2 → 100−145oC PbO + H2O
- Нагревание карбоната свинца:
PbCO3 → 315oC PbO + CO2
- Разложение нитрата свинца:
2Pb(NO3)2 → 200−470oC 2PbO + 4NO2 + O2
- Разложение диоксида свинца:
2PbO2 → 600oC 2PbO + O2
- Окисление сульфида свинца:
2PbS + 3O2 → 1200oC 2PbO + 2SO2
Физические свойства
Оксид свинца II образует кристаллы двух модификаций:
- α-модификация, свинцовый глёт, устойчивый до температуры 489°С, красные кристаллы тетрагональной сингонии, пространственная группа P 4/nmm, параметры ячейки a = 0,396 нм, c = 0,500 нм, Z = 4.
- β-модификация, массикот, устойчивый при температуре выше 489°С, при комнатной температуре метастабилен, жёлтые кристаллы ромбической сингонии, пространственная группа P bcm, параметры ячейки a = 0,5492 нм, b = 0,4497 нм, c = 0,5891 нм, Z = 4.
Диамагнитен, обладает полупроводниковыми свойствами, тип проводимости зависит от состава.
Химические свойства
- Проявляет амфотерные свойства, реагирует с кислотами:
PbO + 2HCl → PbCl2 + H2O
- и щелочами:
PbO + 2NaOH → 400oC Na2PbO2 + H2O
- Во влажном состоянии поглощает углекислоту с образованием основной соли:
2PbO + CO2 + H2O → Pb2(OH)2CO3
- Окисляется кислородом:
6PbO + O2 → 445−480oC 2Pb3O4
- Бромом в водной суспензии окисляется до диоксида свинца:
PbO + Br2 + H2O → PbO2 + 2HBr
- Восстанавливается до металлического свинца водородом, оксидом углерода, алюминием (со взрывом):
PbO + H2 → 200−350oC Pb + H2O PbO + CO → 3 00−400oC Pb + CO2 3PbO + 2Al → T 3Pb + Al2O3
Применение
- В производстве сурика и других соединений свинца.
- Как компонент свинцово-кислотных аккумуляторов.
- В производстве свинцовых стёкол (хрусталь, флинтглас) и глазурей.
- При производстве олиф (сиккатив).
Как и все соединения свинца, оксид свинца(II) токсичен.
Физиологическое действие
Оксид свинца ядовит, как и все его соединения. Относится ко 2-му классу опасности.
Оксид свинца: формула, свойства, метод получения
В этой статье мы разберемся с тем, что собой представляет оксид свинца, покажем его формулу, рассмотрим химические и физические характеристики, а также не забудем рассказать о способах его получения. В общем, эта статья понравится тем, кто хочет или уже разбирается в химии. Ведь свинец встречается повсеместно. Если вы до сих пор не знаете область его применения, то прочитайте статью, чтобы понять весь потенциал этого химического элемента таблицы Менделеева.
Способы его получения
Изначально разберемся, как называется оксид свинца. Он традиционно именуется окисью свинца и представляют собой группу бинарных веществ, образованных элементами металла свинца и неметалла кислорода. Существует шесть основных форм PbO: PbO2, PbO, Pb12O19, Pb12O17, Pb3O4. Каждая из них имеет свои особенности строения молекулы, способы получения и область применения. Самые распространенные формы — это оксид свинца (II) и (IV).
Физические характеристики
Оксид свинца, формула которого PbO, может находиться в двухвидовых модификациях: высоко- и низкотемпературных. Переходы от высокотемпературной формы к низкотемпературной происходят медленнее, чем в обратном порядке. Вследствие этого элемент может пребывать в метастабильности при комнатной температуре, а в процессе растирания изменять модификационную форму.
Испарение протекает конгруэнтно, чаще всего в формах Pb2O2 и Pb4O4. Также данная группа оксидов является полупроводником. По типу проводимости, в зависимости от состава, но не превышая пределы гомогенности, оксиды бывают дырочными и электронными. По цвету они обычно бывают желтыми, красными и черными.
Химические особенности и свойства
Растворение хорошо протекает в азотной и кислородной кислотах, ухудшается растворимость в серной и соляной кислоте, так как образуются PbC12 и PbSO4, которые слаборастворимы. При растворении в щелочной среде образуются гексагидроксоплюмбаты (Na2[Pb(OH)4]). Они являются сильными окислителями, некоторые из них могут проявлять свойства амфотеров — окисляться и поглощать другие вещества. Все они способны окисляться до различных состояний, например, на открытом воздухе PbO при температуре 370 градусов перейдет в состояние молекулы Pb12O17, при 540 градусах образуется Pb3O4, а в водородной (H2) и монооксид углеродной (СО) среде вновь образуется металл путем восстановления.
Оксид свинца II
PbO является неорганическим соединением, которое в воде растворяется плохо. Это бинарное вещество в виде кристаллов красного или желтого цвета. В данном соединении свинец проявляет вторую валентность, соответствуя постоянной валентности кислорода. Встречается в природе с примесями, например, в массикоте или свинцовом глёте.
Как получить оксид свинца в промышленности? Его получают путем пропускания кислорода через свинец, нагретый до температуры 600 градусов (2Pb+O2—2PbO), путем нагревания гидроксида свинца при температурах около 100-145 градусов (Pb(OH)2—PbO+CO2), разложением нитратов (2Pb(NO3)2—2Pb+4NO2+O2), прогреванием карбоната свинца (PbCO3—PbO+CO2), разложением диоксидов свинца (2PbO2—PbO+O2) и окислением сульфидов свинца (2PbS+3O2—2PbO+2SO2).
По своим свойствам PbO (II) способен образовать кристаллы в двух модификационных вариантах, которые устойчивы при 489 градусах и выше.
Альфа модификация (свинцовый углет) представляет собой кристаллы красного цвета тетрагональной сингонии, имеют пространственную группу P 4/nmm. Показатель растворимости в воде — α 0,279 22 . Бета модификация (массикот) проявляет метастабильность при комнатных температурах, имеет желтый цвет, кристаллическую форму, ромбическую сингонию, пространственную группу P bcm. Показатель растворимости в воде — β 0,513 22 г/100 мл.
Оксид свинца может проявлять свойства амфотеров при взаимодействии с кислотами (PbO+2HCl—PbCl2+H2O), щелочами (PbO+2NaOH—(400градусов)Na2PbO2+H2O). Способен окисляться, взаимодействуя с кислородом до Pb3O4, а в водной суспензии бромом окисляется до диоксида свинца PbO2. Восстановление до металла происходит при участии оксида углерода, водорода и алюминия. В состоянии влажности поглощает диоксид углерода, образуя при этом основные соли.
Оксид свинца IV
Оксид свинца 4, он же диоксид свинца, имеет формулу PbO2. Является оксидом высших степеней. Как и другие соединения свинца с кислородом является бинарным веществом. Это порошок тёмно-коричневого цвета, довольно тяжелый, которому присущ запах озона. Раньше его можно было встретить под названием пероксид, или перекись свинца.
Добывают PbO2 в промышленности при помощи обработки азотной кислотой сурика свинца, после чего проводится промывка, помещение в вакуум и сушка: Pb3O4+4HNO3—PbO2+2Pb(NO3)2+2H2O.
Температура плавления данного соединения равна 290 градусов, плотность составляет 9.38г/ см³, молярная масса — 239,1988г/моль. Диоксид свинца 4 является очень сильным окислителем, способен вытеснять из концентрированной соляной кислоты хлор в результате нагревания (PbO2+4HCl—PbCl2+Cl2+2H2O). Соли марганца (II) также поддаются окислению до перманганата (5PbO2+2MnSO4+3H2SO4—5PbSO4+2HMnO4+2H2O). Является весьма токсичным веществом.
Применение
Области применения диоксидов свинца самые разнообразные. Оксид свинца 4 находит свое применение, выполняя функцию сиккативов (маслянистых веществ, необходимых для ускорения процесса засыхания красок), катализатора (вещества, необходимого для ускорения протекания химических реакций между соединениями, которые при этом не входят в конечный состав продуктов любых протекающих реакций) и окислителя (вещества, в состав которого входят атомы, способные присоединять к себе свободные электроны в процессе химической реакции, окислитель также можно назвать акцептором).
PbO2 широко используется в свинцово-сернокислотных аккумуляторах, в роли положительных электронных масс в гальванических элементах. Часто, но в малых количествах может применяться как покрытие для электродов, чтобы улучшить электролизный процесс. Диоксид свинца 2 используют при изготовлении суриков, PbO2 можно встретить в аккумуляторах. Оксид свинца широко используется в области изготовления свинцовых стёкол и глазурей. Pb3O4 можно встретить в свинцовых аккумуляторах в качестве замазки и как пигмент для красок против коррозии. Большинство оксидов свинца используют при изготовлении радиотехники, резинотехнической продукции. Также незаменимы они в процессе добычи свинцовых солей при химическом синтезе.
№82 Свинец
История открытия:
Свинец известен с III — II тысячелетия до н.э. в Месопотамии, Египте и других древних странах, где из него изготовляли большие кирпичи (чушки), статуи богов и царей, печати и различные предметы быта. Из свинца делали бронзу, а также таблички для письма острым твердым предметом. В более позднее время римляне стали изготовлять из свинца трубы для водопроводов. В древности свинец сопоставлялся с планетой Сатурн и часто именовался сатурном. В средние века благодаря своему тяжелому весу свинец играл особую роль в алхимических операциях, ему приписывали способность легко превращаться в золото.
Нахождение в природе, получение:
Содержание в земной коре 1,6·10 -3 % по массе. Самородный свинец встречается редко, круг пород, в которых он установлен, достаточно широк: от осадочных пород до ультраосновных интрузивных пород. В основном встречается в виде сульфидов (PbS — свинцовый блеск).
Получение свинца из свинцового блеска проводят путем обжигательно-реакционной плавки: сначала подвергают шихту неполному обжигу (при 500-600°С), при котором часть сульфида переходит в оксид и сульфат:
2PbS + 3О2 = 2РbО + 2SO2 PbS + 2О2 = РbSO4
Затем, продолжая нагревание, прекращают доступ воздуха; при этом оставшийся сульфид регирует с оксидом и сульфатом, образуя металлический свинец:
PbS + 2РbО = 3Рb + SO2 PbS + РbSO4 = 2Рb +2SO2
Физические свойства:
Один из самых мягких металлов, легко режется ножом. Обычно покрыт более или менее толстой плёнкой оксидов грязно-серого цвета, при разрезании открывается блестящая поверхность, которая на воздухе со временем тускнеет. Плотность — 11,3415 г/см 3 (при 20°C). Температура плавления — 327,4°C, температура кипения — 1740°C
Химические свойства:
При большой температуре свинец образует с галогенами соединения вида РbХ2, с азотом прямо не реагирует, при нагревании с серой образует сульфид PbS, кислородом окисляется до PbO.
В отсутствии кислорода свинец не реагирует с водой при комнатной температуре, но при действии горячего водяного пара образует оксиды свинца и водород. В ряду напряжений свинец стоит левее водорода, но он не вытесняет водород из разбавленных HCl и H2SO4, из-за перенапряжения выделения Н2 на свинце, а также из-за образования на поверхности металла плёнки труднорастворимых солей, защищающих металл от дальнейшего действия кислот.
В концентрированных серной и соляной кислотах при нагревании свинец растворяется, образуя соответственно и Н2[РbCl4]. Азотная, а также некоторые органические кислоты (например, лимонная) растворяют свинец с получением солей Рb(II). Реагирует свинец и с концентрированными растворами щелочей:
Pb + 8HNO3 (разб.,гор.) = 3Pb(NO3)2 + 2NO + 4H2O.
Pb + 3H2SO4 (>80%) = Pb(HSO4)2 + SO2 + 2H2O
Pb + 2NаOН (конц.) + 2H2O = Nа2[Pb(OН)4] + Н2
Для свинца наиболее характерны соединения со степенью окисления: +2 и +4.
Важнейшие соединения:
Оксиды свинца — с кислородом свинец образует ряд соединений Рb2О, РbО, Рb2О3, Рb3О4, РbО2, преимущественно амфотерного характера. Многие из них окрашены в красные, жёлтые, чёрные, коричневые цвета.
Оксид свинца (II) — РbО. Красный (низкотемпературная a-модификация, глет) или желтый (высокотемпературная b-модификация, массикот). Термически устойчив. Очень плохо реагируют с водой, раствором аммиака. Проявляет амфотерные свойства, реагирует с кислотами и щелочами. Окисляется кислородом, восстанавливается водородом и монооксидом углерода.
Оксид свинца (IV) — РbО2. Платтнерит. Темно-коричневый, тяжелый порошок, при слабом нагревании разлагается без плавления. Не реагирует с водой, разбавленными кислотами и щелочами, раствором аммиака. Разлагается концентрированными кислотами, концентрированными щелочами при кипячении медленно переводится в раствор с образованием .
Сильный окислитель в кислой и щелочной среде.
Оксидам РbО и РbО2 соответствуют амфотерные гидрооксиды Рb(ОН)2 и Рb(ОН)4. Получение . Свойства .
Рb3О4 — свинцовый сурик. Рассматривается как смешаный оксид или орто-плюмбат свинца(II) — Рb2PbО4. Оранжево-красный порошок. При сильном нагревании разлагается, плавится только под избыточном давлением О2. Не реагирует с водой, гидратом аммиака. Разлагается конц. кислотами и щелочами. Сильный окислитель.
Соли свинца(II) . Как правило бесцветны, по растворимости в воде делятся на нерастворимые (например, сульфат, карбонат, хромат, фосфат, молибдат и сульфид), малорастворимые (йодид, хлорид и фторид) и растворимые (к примеру, ацетат, нитрат и хлорат свинца). Ацетат свинца, или свинцовый сахар, Pb(CH3COO)2·3H2O, бесцветные кристаллы или белй порошок сладкого вкуса, медленно выветривается с потерей гидратной воды, относится к очень ядовитым веществам.
Халькогениды свинца — PbS, PbSe, и PbTe — кристаллы чёрного цвета, узкозонные полупроводники.
Соли свинца(IV) могут быть получены электролизом сильно подкисленных серной кислотой растворов солей свинца(II). Свойства .
Гидрид свинца(IV) — PbH4 — газообразное вещество без запаха, которое очень легко разлагается на свинец и водород. Получается в небольших количествах при реакции Mg2Pb и разбавленной HCl.
Применение:
Свинец хорошо экранирует радиацию и рентгеновские лучи, применяется в качестве защитного материала, в частности, в рентгеновских кабинетах, в лабораториях, где существует опасность облучения радиацией. Также используют для изготовления пластин аккумуляторов (около 30% выплавляемого свинца), оболочек электрических кабелей, защиты от гамма-излучения (стенки из свинцовых кирпичей), как компонент типографских и антифрикционных сплавов, полупроводниковых материалов.
Свинец и его соединения, особенно органические, токсичны. Попадая в клетки, свинец дезактивирует ферменты, тем самым нарушая обмен веществ, вызывая умственную отсталость у детей, заболевания мозга. Свинец может заменять кальций в костях, становясь постоянным источником отравления. ПДК в атмосферном воздухе соединений свинца 0,003 мг/м 3 , в воде 0,03 мг/л, почве 20,0мг/кг.
Барсукова М. Петрова М.
ХФ ТюмГУ, 571 группа.