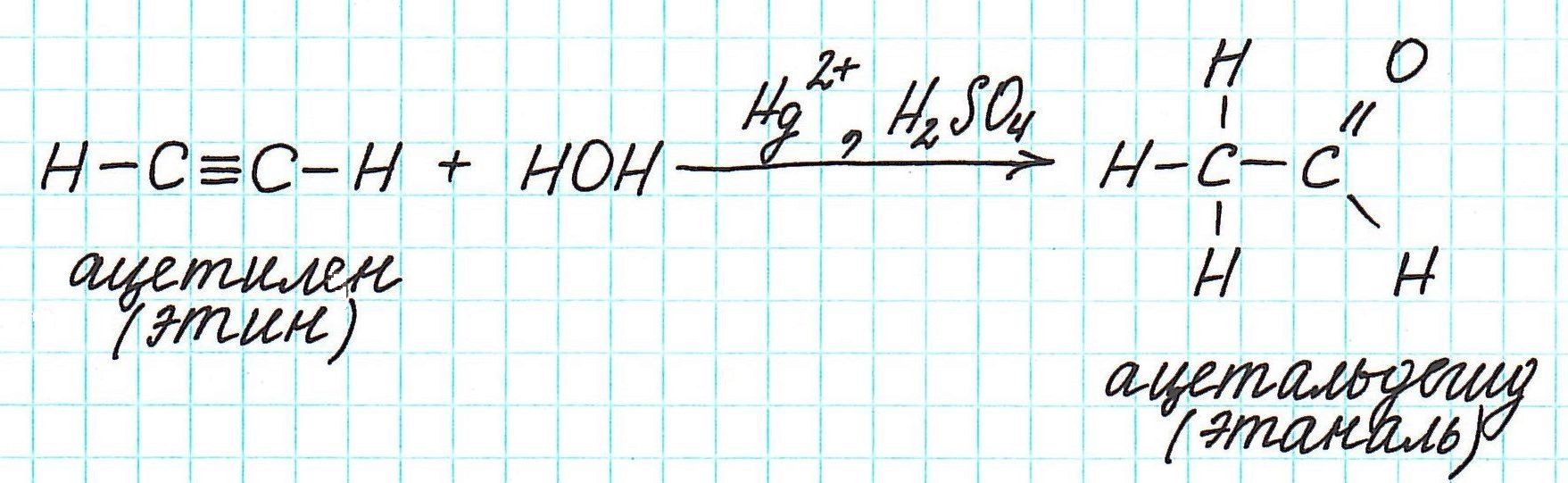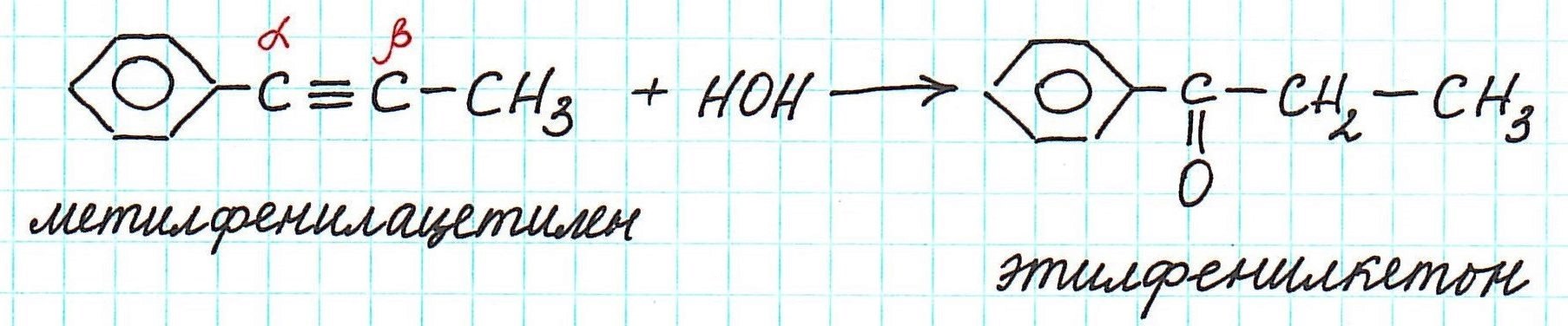Реакция Кучерова для ацетилена (1881 г) стала основой промышленного получения уксусного альдегида как исходного сырья в синтезе многих органических соединений.
Кучеров Михаил Григорьевич (1850 – 1911) – российский химик-органик, внесший значительный вклад в развитие органического синтеза.
Взаимодействие ацетилена с водой (гидратация) приводит к образованию уксусного альдегида (ацетальдегида):
Обязательным условием протекания реакции является присутствие в качестве катализатора раствора (5%) соли ртути (II) в сернокислой (10%) среде. Катализаторами могут быть также соли Au + , Cu + , Ag + и Ru 3+ . Однако доказана лучшая эффективность солей Hg 2+ (чаще HgSO4).
Механизм реакции Кучерова для ацетилена
Несмотря на кажущуюся простоту процесса, механизм его до сих пор не совсем ясен.
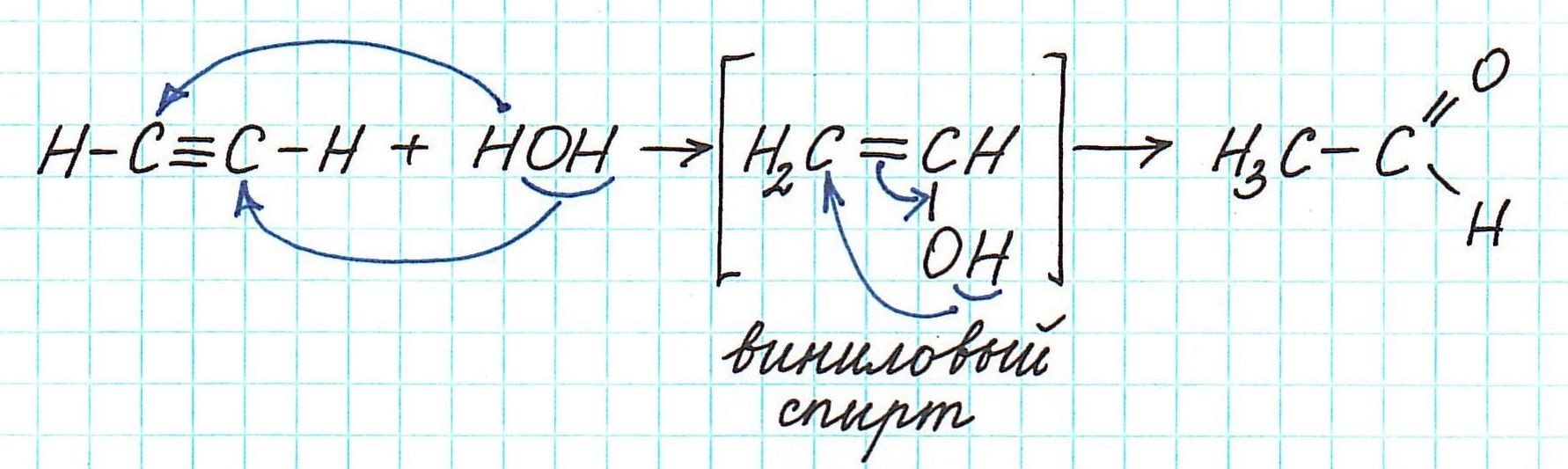
Однако достоверно известно, что одной из промежуточных стадий является образование неустойчивых непредельных спиртов (енолей). Их молекулы содержат гидроксильную группу –ОН у атома углерода с двойной связью.
Например, реакция Кучерова для ацетилена проходит следующим образом:
Механизм реакции Кучерова для гомологов ацетилена
При гидратации гомологов ацетилена образуются не альдегиды, а кетоны . Причем присоединение воды происходит по правилу Марковникова:
Алкины ряда R ̶ C≡CH при гидратации всегда образуют метилкетоны: R ̶ C(O) ̶ CH3. Реакция получения ацетона (диметилкетона) как раз является таким примером.
Алкины ряда R1 ̶ C≡C ̶ R2 при гидратации в зависимости от строения R1 и R2 могут давать смесь кетонов с явным преобладанием одного из них:
Как определить, какой кетон будет преобладать?
Молекула 4-метилпентина-2 содержит третичный атом углерода. Ближний к нему атом углерода с тройной связью находится в α-положении к нему, следующий – в β-положении. Образование карбонильной группы, характерной для кетонов, происходит в основном у углерода в α-положении.
Еще пример:
Итак, реакция Кучерова для ацетилена приводит к образованию ацетальдегида; реакция Кучерова для гомологов ацетилена приводит к образованию кетонов.
Видео:8 класс. Химия. Как расставить коэффициенты в уравнении?Скачать

Контрольная работа по теме «Спирты. Альдегиды. Карбоновые кислоты»
Разработано 4 варианта заданий. Работа рассчитана на 40 минут, содержит два типа заданий:
- задания с выбором одного правильного ответа из предложенного списка
- задания со свободным ответом
Видео:Как расставлять коэффициенты в уравнении реакции? Химия с нуля 7-8 класс | TutorOnlineСкачать

Скачать:
| Вложение | Размер |
|---|---|
| variant_1.doc | 47.5 КБ |
| variant_2.doc | 55.5 КБ |
| variant3.doc | 49 КБ |
| variant_4.doc | 50.5 КБ |
Видео:Расстановка Коэффициентов в Химических Реакциях // Подготовка к ЕГЭ по ХимииСкачать

Предварительный просмотр:
Контрольная работа по разделу «Спирты. Альдегиды. Карбоновые кислоты»
Инструкция по выполнению работы
Работа состоит из двух частей и включает 14 заданий. Часть А включает 10 заданий (А1-А10). К каждому заданию дается 4 варианта ответа, из которых — только один правильный.
Часть В (В1-В4) состоит из четырех заданий, для которых нужно дать ответ в виде числа или в виде набора цифр, записав их последовательно, без пробелов. В задании В4 решите задачи.
За выполнение различных по сложности заданий дается один (часть А), два (часть В) балла, которые затем суммируются. Постарайтесь набрать как можно больше баллов.
А1. Общая формула предельных одноатомных спиртов
1) СnH 2n+1 OH 2) СnH 2n O 3) СnH 2n+2 4) СnH 2n (OH) 2
А 2. Функциональной группой карбоновых кислот является
1) гидроксогруппа 2) карбонильная группа 3) карбоксильная группа 4) аминогруппа
А 3. Название вещества, формула которого СН 3 ─СOOH
1) ацетальдегид 2) уксусная кислота 3) этанол 4) муравьиная кислота
А 4. Вещества СН 3 – СН 2 –СООН и СН 3 –СООН являются
1) структурными изомерами 2) изомерами по положению функциональной группы
3) гомологами 4) альдегидами
А 5. Сумма коэффициентов в уравнении реакции горения метанола
1) 9 2) 6 3) 8 4) 11
А 6. Этанол взаимодействует с
1) уксусной кислотой 2) метаном 3) водородом 4) лакмусом
А 7. Уксусная кислота может реагировать с
1) серебром 2) магнием 3) метаном 4) медью
А 8. При взаимодействии альдегидов с водородом в присутствии катализатора при нагревании образуются
1) углеводороды 2) карбоновые кислоты 3) арены 4) спирты
А 9. В схеме С 2 Н 6 → Х → С 2 Н 5 ОН веществом «Х» является
1) С 2 Н 5 ─ O ─ C 2 H 5 2) С 2 Н 2 3) С 2 Н 5 Br 4) СН 3 ОН
А 10. Реакция с аммиачным раствором оксида серебра (I ) характерна для
1) пропанола -1 3) пропионовой кислоты
2) прапаналя 4) этандиола
В 1.Установите соответствие между формулой вещества и его названием
2) пропионовая кислота
В) CH 3 — CH 2 -COOH
3) этановая кислота
4) этиловый спирт
Ответ (набор цифр без пробелов): ________________
В 2. Установите соответствие между названием вещества и классом (группой) органических соединений, к которому оно принадлежит (цифры могут повторяться):
КЛАСС (ГРУППА) ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
А) этиловый спирт
2) предельные одноатомные спирты
4) сложные эфиры
5) карбоновые кислоты
6) многоатомные спирты
Ответ (набор цифр без пробелов): ________________
В 3. Для предельных одноатомных спиртов характерны реакции
2) взаимодействие с активными металлами
В 4. Решите задачи
Задача №1. Объем водорода, который выделится при взаимодействии 4,6 г натрия с этиловым спиртом, равен _____________ л. (Ответ записать в виде целого числа с точностью до сотых).
Задача №2. В двух пробирках находятся вещества: глицерин и ацетальдегид. Как распознать каждое из веществ? Напишите уравнения реакций.
Видео:Расстановка коэффициентов в химических реакциях: как просто это сделатьСкачать

Предварительный просмотр:
Контрольная работа по разделу ««Спирты. Альдегиды. Карбоновые кислоты»
Инструкция по выполнению работы
На выполнение данной работы отводится 40 мин. Работа состоит из двух частей и включает 14 заданий. Часть А включает 10 заданий (А1-А10). К каждому заданию дается 4 варианта ответа, из которых — только один правильный.
Часть В (В1-В4) состоит из четырех заданий, для которых нужно дать ответ в виде числа или в виде набора цифр, записав их последовательно, без пробелов. В задании В4 решите одну из задач.
Внимательно прочитайте каждое задание и предлагаемые варианты ответа. Отвечайте только после того, как вы поняли вопрос и проанализировали все варианты ответа.
За выполнение различных по сложности заданий дается один (часть А), два (часть В) балла, которые затем суммируются. Постарайтесь набрать как можно больше баллов. Желаем успеха!
При выполнении заданий этой части (А1-А10) выберите только один из четырёх предложенных вариантов ответа. В бланке ответов выполняемого вами задания
поставьте знак « Х » в клеточку, номер которой соответствует номеру выбранного вами ответа.
А1. Общая формула одноосновных карбоновых кислот
1) R -COOH 2) R — OH 3) RCHO 4) R- O — R
А 2. Функциональной группой спиртов является
1) гидроксогруппа 2) карбонильная группа 3) карбоксильная группа 4) аминогруппа
А 3. Название вещества, формула которого НСOOH
1) ацетальдегид 2) уксусная кислота 3) этанол 4) муравьиная кислота
А 4. Вещества СН 3 – СН 2 –ОН и СН 3 –ОН являются
1) структурными изомерами 2) изомерами по положению функциональной группы
3) гомологами 4) альдегидами
А 5. Сумма коэффициентов в уравнении реакции гидратации ацетилена в присутствии солей ртути (реакции Кучерова)
1) 4 2) 3 3) 8 4) 2
А 6. Альдегиды не взаимодействуют с
1) водородом 2) гидроксидом меди (II)
3) аммиачным раствором оксида серебра (I) 4) метаном
А 7. Многоатомным спиртом является
1) этанол 2) этилен 3) этиленгликоль 4) этилацетат
А 8.Верны ли следующие суждения о свойствах веществ?
А.Уксусная кислота – слабая кислота.
Б.При окислении альдегидов получаются карбоновые кислоты.
1) верно только суждение А 2) верно только суждение Б
3) оба суждения верны 4) оба суждения неверны
А 9. В схеме С 2 Н 2 → Х → СН 3 СООН веществом «Х» является
1) метан 2) бензол 3) уксусный альдегид 4) масляная кислота
А 10. Этанол можно получить из этилена в результате реакции
1) гидратации 3) галогенирования
2) гидрирования 4) гидрогалогенирования
Ответом к заданиям части В является набор цифр или число, которые следует записать в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки.
В заданиях В1-В3 на установление соответствия к каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами. Затем получившуюся последовательность цифр перенесите в бланк ответов № 1 без пробелов и других символов. (Цифры в ответе могут повторяться).
В задании В4: решите одну из задач. Ответом в задаче 1 является число, запишите его в бланк ответов. Если вы выбрали задачу 2, то напишите уравнения соответствующих реакций на отдельном листе.
В 1.Установите соответствие между формулой вещества и его названием
Видео:Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

КУ́ЧЕРОВА РЕА́КЦИЯ
В книжной версии
Том 16. Москва, 2010, стр. 482
Скопировать библиографическую ссылку:
КУ́ЧЕРОВА РЕА́КЦИЯ, катализируемая солями $ce$ гидратация алкинов, приводящая к образованию карбонильных соединений : $ce RC(O)CH2R′>$ или $ce$ , где $ce$ , $ce$ – атом $ce$ , углеводородный радикал. Реакция открыта М. Г. Кучеровым в 1881.
🌟 Видео
Расстановка коэффициентов в химических реакциях: как просто это сделатьСкачать
Как расставить коэффициенты? Как превратить схему химической реакции в уравнение химической реакции.Скачать

СУММА КОЭФФИЦИЕНТОВ: Как решать Квадратные Уравнения по МАТЕМАТИКЕ 8 классСкачать

8 класс. Составление уравнений химических реакций.Скачать

Расстановка коэффициентов в окислительно-восстановительных реакцияхСкачать

Как УРАВНИВАТЬ химические уравнения | Расстановка коэффициентов в химических реакцияхСкачать

Коэффициенты в уравнениях химических реакцийСкачать

Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Типы Химических Реакций — Химия // Урок Химии 8 КлассСкачать

Как расставить коэффициенты в органических ОВР? | Екатерина СтрогановаСкачать

Химические уравнения 8 класс - как расставить коэффициенты ?Скачать

89. Как расставить коэффициенты реакции методом электронного баланса (закрепление)Скачать

ХИМИЧЕСКИЕ УРАВНЕНИЯ | Как составлять уравнения реакций | Химия 8 классСкачать

54. Реакция КучероваСкачать

Как уравнивать коэффициенты (химия)Скачать