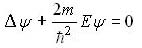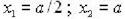Планетарная модель водородоподобного атома, сформулированная Бором, не является ни классической (поскольку допускает квантование), ни квантовой (поскольку квантование не объясняет). Объяснить квантование можно с помощью уравнения Шредингера.
Однако описание атомов и молекул с помощью уравнения Шредингера является сложной задачей. Это касается даже простейшего атома водорода и водородоподобных ионов. Поэтому ограничимся здесь качественным рассмотрением задачи, которая сводится к анализу движения электрона в кулоновском иоле ядра. Потенциальная энергия взаимодействия электрона с ядром заряда Ze задается формулой
Здесь г — расстояние между электроном и ядром. Необходимо учитывать, что атом принципиально является трехмерной системой, и одномерным приближением для его описания обойтись нельзя. Поэтому стационарное уравнение Шредингера для водородоподобного атома записывается следующим образом:
Масса ядра на несколько порядков больше массы электрона, поэтому систему центра масс обычно можно считать привязанной к ядру. Поле, в котором движется электрон, является в этой системе центрально-симметричным.
Задачи такой геометрии удобно решать в сферической системе координат (рис. 37.1). В ней для точки М выбраны координаты г, 0, ср. Расстояние до начала координат г равно ОМ. Полярный (зенитный) угол 0 — это угол между осью Oz и радиус- вектором г, который меняется в пределах от 0 до к. Азимутальный угол ф — это угол между осью Ох и проекцией радиус-вектора г на плоскость Оху, ко- Рис.37.1 торый меняется в пределах от 0 до 2л. Переход
к сферической системе от декартовой и обратно осуществляется по следующим из геометрии правилам:
После перехода к сферической системе координат решение уравнения Шредингера ищется в виде произведения трех составляющих, каждая из которых зависит от одной из сферических координат:
Решение уравнения Шредингера с трехмерным кулоновским потенциалом оказывается еще более сложным, чем в предыдущей задаче с одномерным потенциалом гармонического осциллятора. Аналогично предыдущим квантовым задачам поиск собственных волновых функций (с учетом естественных ограничений) приводит к получению дискретных собственных энергетических состояний. И каждая из составляющих волновой функции дает набор решений, характеризующийся своим квантовым числом: главным п, орбитальным / и магнитным т,.
- Стационарным уравнением шредингера для электрона в водородоподобном ионе уравнение
- 4.1. Уравнение Шредингера
- Уравнение Шредингера
- 4.2. Частица в одномерной прямоугольной яме с бесконечными стенками
- 4.3. Гармонический осциллятор
- Частица в одномерной потенциальной яме
- 4.4. Частица в поле с центральной симметрией
- 4.5. Орбитальный момент количества движения
- 4.6. Спин
- 4.7. Полный момент количества движения
- 4.8. Квантовые числа
- Таблица квантовых чисел
- Задачи
- Уравнение Шредингера (конкретные ситуации)
Стационарным уравнением шредингера для электрона в водородоподобном ионе уравнение
Аналог классического волнового уравнения был предложен Э. Шредингером в 1925 г. Как и классическое уравнение, уравнение Шредингера связывает производные волновой функции по времени и координате. Уравнение Шредингера описывает поведение любых нерелятивистских систем. На примерах частицы, находящейся в бесконечно глубокой яме, и гармонического осциллятора рассмотрены простейшие квантовые системы, получены дискретные спектры состояний. Возможности описания динамики данных систем ограничены набором квантовых чисел, отражающих универсальные и внутренние симметрии квантовых систем.
4.1. Уравнение Шредингера
В квантовой физике изменение состояния частицы описывается уравнением Шредингера
 | (4.1) |
где 
в которой 







х → 


 | (4.2) |
Уравнение Шредингера
Зависящее от времени уравнение Шредингера:
где 
Разделение переменных. Запишем Ψ(




Левая часть является функцией только координат, а правая не зависит от переменной x. Поэтому обе части последнего уравнения должны быть равны одной и той же постоянной, которую обозначим E
θ(t) = exp(−iEt/ћ), 




Уравнение 



Для трехмерной системы с массой m в поле с потенциалом U(
−(ћ 2 /2m)Δψ(



где Δ – лапласиан.
Так как уравнение Шредингера является линейным уравнением первого порядка по времени, то с его помощью по заданному значению волновой функции Ψ(x, y, z, 0) в момент времени t = 0 можно найти её значение в произвольный момент времени t − Ψ(x, y, z, t).
Уравнение Шредингера для стационарного состояния, когда потенциальная энергия частицы не зависит от времени, имеет вид
 ψ( ψ( ) = Eψ( ) = Eψ( ). ). | (4.3) |
Это уравнение называют стационарным уравнением Шредингера.
Так как в стационарном состоянии
Ψ( ,t) = ψ( ,t) = ψ( )exp(−iEt/ћ) )exp(−iEt/ћ) | (4.4) |
и вероятность найти частицу в момент t в точке x, y, z пропорциональна |Ψ(
|ψ(x,y,z)| 2 , т.е. не зависит от времени. Аналогично, вероятность обнаружить значение физической величины, характеризующей систему, также не изменяется со временем, поскольку выражается через квадрат модуля волновой функции.
4.2. Частица в одномерной прямоугольной яме с бесконечными стенками
Потенциальная энергия U(x) в прямоугольной яме удовлетворяет следующим условиям:
 | (4.5) |

Рис.4.1. Прямоугольная яма с бесконечными стенками
Частица находится в области 0 ≤ x ≤ L. Вне этой области ψ(x) = 0. Уравнение Шредингера для частицы, находящейся в области 0 ≤ x ≤ L
 | (4.6) |
Волновая функция, являющаяся решением уравнения (4.9), имеет вид
| ψ(x)= Аsin kx + Bcos kx, | (4.7) |
где k = (2mE/ћ 2 ) 1/2 . Из граничных условий ψ(0) = 0, ψ(L) = 0 и условий непрерывности волновой функции следует
| Аsin kL = 0. | (4.8) |
kL = nπ, n = 1, 2, 3, … , то есть внутри потенциальной ямы с бесконечно высокими стенками устанавливаются стоячие волны, а энергия состояния частиц имеет дискретный спектр значений En
 n = 1, 2, 3, … n = 1, 2, 3, … | (4.9) |
Частица может находиться в каком-то одном из множества дискретных состояний, доступных для неё.
Каждому значению энергии En соответствует волновая функция ψn(x), которая с учетом условия нормировки
 | (4.10) |
В отличие от классической, квантовая частица в прямоугольной яме не может иметь энергию
E 2 π 2 /(2mL 2 ). Состояния частицы ψn в одномерном поле бесконечной потенциальной ямы полностью описывается с помощью одного квантового числа n. Спектр энергий дискретный.
Рис. 4.2. Уровни энергии и волновые функции частицы Ψ в бесконечной прямоугольной яме. Квадрат модуля волновой функции |Ψ| 2 определяет вероятность нахождения частицы в различных точках потенциальной ямы.
4.3. Гармонический осциллятор
Положение уровней частицы в потенциальной яме зависит от вида потенциальной ямы. В одномерной потенциальной яме гармонического осциллятора потенциальная энергия имеет вид
 | (4.11) |
В этом случае одномерное уравнение Шредингера имеет вид
 | (4.12) |
Допустимые значения полной энергии определяются формулой
| En = ћω0(n + 1/2), n = 0, 1, 2, | (4.13) |
В отличие от бесконечной прямоугольной ямы, спектр уровней гармонического осциллятора эквидистантный.
С увеличением массы частицы или размеров области ее локализации квантовое описание частицы переходит в классическое.
Частица в одномерной потенциальной яме
Одномерная прямоугольная яма шириной L:


Одномерный гармонический осциллятор:

4.4. Частица в поле с центральной симметрией
В сферических координатах стационарное уравнение Шредингера для частицы в центральном потенциале U(r) имеет вид
 | (4.14) |
Решение уравнения (4.14) записываются в виде произведения радиальной и угловой функций
| ψ(r,θ,φ) = Rnl(r)Ylm(θ,φ), | (4.15) |
где радиальная функция Rnl(r) и угловая функция Ylm(θ,φ), называемая сферической, удовлетворяют уравнениям
 2 Ylm(θ,φ) = ћ 2 l(l +1)Ylm(θ,φ) 2 Ylm(θ,φ) = ћ 2 l(l +1)Ylm(θ,φ) | (4.16) |
 Ylm(θ,φ) = ћ 2 l(l +1)Ylm(θ,φ) Ylm(θ,φ) = ћ 2 l(l +1)Ylm(θ,φ)  | (4.17) |
Уравнение (4.16) определяет возможные собственные значения l и собственные функции Ylm(θ,φ) оператора квадрата момента 
Схема уровней (последовательность и абсолютные значения энергий) зависит от радиальной функции Rnl(r), которая в свою очередь определяется потенциалом U(r), в котором находится частица.
Рис. 4.3. Радиальное распределение вероятности нахождения электрона в кулоновском поле протона (атом водорода). Расстояния даны в боровских радиусах
r0 = ћ 2 /mee 2 ≈ 0.529·10 8 cм.
| Решения уравнения |
существуют лишь при определенных значениях квантовых чисел n (радиальное квантовое число), l (орбитальное квантовое число) и m (магнитное квантовое число).
Возможные энергетические состояния системы (уровни энергии) определяются числами n и l и в случае сферически симметричных состояний не зависят от квантового числа m. Число n может быть только целым:
n = 1, 2, …, ∞. Число l может принимать значения 0, 1, 2, …, ∞.
4.5. Орбитальный момент количества движения
Собственные значения L 2 и Lz являются решением уравнений


Они имеют следующие дискретные значения
L 2 = ћ 2 l(l + 1), где l = 0, 1, 2, 3, …,
Lz = ћm, где m = 0, ± 1, ± 2, ± 3,…, ± l.
Для характеристики состояний с различными значениями орбитального момента l обычно используют следующие обозначения:
Спектроскопические названия орбитальных моментов l
| l = 0 | s-состояние |
| l = 1 | p-состояние |
| l = 2 | d-состояние |
| l = 3 | f-состояние |
| l = 4 | g-состояние |
| l = 5 | h-состояние |
| и. т. д. |
Состоянию с l = 0 отвечает сферически симметричная волновая функция. В тех случаях, когда l ≠ 0 волновая функция не имеет сферической симметрии. Симметрия волновой функции определяется симметрией сферических функций Ylm(θ,φ). Имеет место интересное квантовое явление, когда решение сферически симметричной задачи (потенциал описывает сферически симметричную систему) приводит к состояниям, не обладающим сферической симметрией. Таким образом, симметрия уравнений не обязательно должна отражаться в симметрии каждого отдельно взятого решения этих уравнений, а лишь во всей совокупности этих решений.
Для частицы, находящейся в сферически симметричном потенциале, величина орбитального момента количества движения L:
 | (4.18) |
Обычно, для упрощения, когда говорят о величине орбитального момента количества движения, называют этой величиной квантовое число l, имея в виду, что между l и L имеется однозначная связь (4.18).
Рис. 4.4 Возможные ориентации вектора 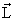
Так как величина l может принимать только целочисленные значения 0, 1, 2, 3,…, то и орбитальный момент количества движения L квантуется. Например, для частицы с l = 2 момент количества движения

= 6.58·10 -22 √6 МэВ·сек ≈ 2.6·10 — 34 Дж·сек.
Пространственное квантование. Орбитальный момент количества движения является векторной величиной. Так как величина орбитального момента количества движения квантуется, то и направление 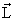
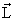
Состояние частицы, находящейся в сферически симметричном поле, полностью описывается тремя квантовыми числами: n, l и m.
Появление квантовых чисел связано со свойствами симметрии системы. Характер этой симметрии определяет возможные значения квантовых чисел. Очевидно, что система, описываемая функцией e im φ , примет прежнее значение только тогда, когда азимутальный угол φ в результате поворота вокруг оси z примет прежнее значение φ. Этому условию функция e im φ удовлетворяет только в случае, когда величина mφ кратна 2π. Т.е. величина m должна иметь целые значения. Так как необходимо учитывать вращение в двух противоположных направлениях и отсутствие вращения, единственно возможными значениями оказываются m = 0, ±1, ±2, … .
4.6. Спин
Спин − собственный момент количества движения частицы. Между значением вектора спина 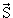
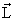
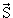 2 = ћ 2 s(s + 1) 2 = ћ 2 s(s + 1) | (4.19) |
В отличие от орбитального квантового числа l, которое может быть лишь целым числом или нулем, спиновое квантовое число s (в дальнейшем просто спин) может быть как целым (включая нуль), так и полуцелым, т. е. s = 0, 1/2, 1, 3/2, 2, 5/2, … , но при этом для каждой элементарной частицы спин может принимать единственное присущее этому типу частиц значение. Так, спины π-мезонов и К-мезонов равны 0. Спины электрона, протона, нейтрино, кварков и их античастиц равны 1/2. Спин фотона равен 1. Бозоны составляют класс частиц с целым значением спина, спин фермионов имеет полуцелое значение. Спин частицы невозможно изменить, также как её заряд или массу. Это её неизменная квантовая характеристика.
Как и в случае других квантовых векторов, проекция вектора спина 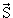
szћ = ±sћ, ±(s − 1)ћ, ±(s − 2)ћ. ±1/2ћ или 0.
Число sz − это квантовое число проекции спина. Максимальная величина sz совпадает с s. Так как спин электрона равен 1/2, то проекция этого спина может принимать лишь два значения sz = ±1/2. Если проекция +1/2, то говорят, что спин направлен вверх, если проекция -1/2, то говорят, что спин направлен вниз.
4.7. Полный момент количества движения
Полный момент количества движения частицы или системы частиц 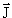
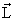
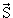
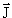
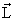
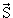
Квадрат полного момента имеет значение:
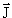
Квантовое число полного момента j, соответствующее сумме двух векторов 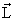
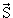
j = l + s, l + s −1. |l − s|
Проекция 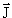
Число значений проекции Jz равно 2j + 1. Если для 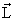
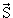
4.8. Квантовые числа
Квантовые числа – это целые или дробные числа, которые определяют все возможные значения физической величины, характеризующей различные квантовые системы – атомы, атомные ядра, кварки и другие частицы.
Таблица квантовых чисел
| n | Радиальное квантовое число. Определяет число узлов волновой функции и энергию системы. n = 1, 2, …, ∞. |
| J, j | Полный угловой момент J и его квантовое число j. Последнее никогда не бывает отрицательным и может быть целым или полуцелым в зависимости от свойств рассматриваемой системы. 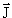 2 = ћ 2 j(j + 1). 2 = ћ 2 j(j + 1). |
| L, l | Орбитальный угловой момент L и его квантовое число l. Интерпретация l такая же, как j, но l может принимать только целые значения, включая нуль: l = 0, 1, 2,…. L 2 = ћ 2 l(l + 1). |
| m | Магнитное квантовое число. Проекция полного или орбитального углового момента на выделенную ось (обычно ось z) равна mћ. Для полного момента m = ±j, ±(j-1), …, ±1/2 или 0. Для орбитального m = ± l, ± (l-1), …, ±1, 0. |
| S, s | Спиновый угловой момент S и его квантовое число s. Оно может быть либо положительным целым (включая нуль), либо полуцелым. s – неизменная характеристика частицы определенного типа. S 2 = ћ 2 s(s + 1). |
| sz | Квантовое число проекции спинового момента частицы на выделенную ось. Эта проекция может принимать значения szћ, где sz = ± s, ± (s -1), …, ±1/2 или 0. |
| P или π | Пространственная четность. Характеризует поведение системы при пространственной инверсии  → — → —  (зеркальном отражении). Полная четность частицы Р = π(-1) l , где π – её внутренняя четность, а (-1) l – её орбитальная четность. Внутренние четности кварков положительные, антикварков — отрицательные. (зеркальном отражении). Полная четность частицы Р = π(-1) l , где π – её внутренняя четность, а (-1) l – её орбитальная четность. Внутренние четности кварков положительные, антикварков — отрицательные. |
| I | Изоспин. Характеризует свойство зарядовой инвариантности сильных взаимодействий |
Для обозначения спинового момента часто используют букву J.
Все состояния, в которых может находиться квантовая система, описываются с помощью полного набора квантовых чисел. Так в случае протона в ядре состояние протона описывается с помощью четырех квантовых чисел, соответствующих четырем степеням свободы – трем пространственным координатам и спину. Это
- Радиальное квантовое число n ( 1, 2, …, ∞),
- Орбитальное квантовое число l (0, 1, 2, …),
- Проекция орбитального момента m (± l, ± (l-1), …, ±1, 0),
- Спин протона s =1/2.
Для описания сферически-симметричных систем в квантовой физике используются различные сферически симметричные потенциалы с различной радиальной зависимостью:
- Кулоновский потенциал U = Q/r,
- Прямоугольная потенциальная яма
- Потенциал типа гармонического осциллятора U = kr 2 ,
- Потенциал Вудса-Саксона (с его помощью описываются внутриядерные взаимодействия):
где U0, а и R – положительные константы (R – радиус ядра). Во всех случаях сферически симметричные системы можно описать с помощью набора квантовых чисел n, l, j, jz, однако, в зависимости от радиального вида потенциала энергетический спектр состояний системы будет различным.
Существование сохраняющихся во времени физических величин тесно связано со свойствами симметрии гамильтониана системы. Например, в случае, если квантовая система обладает центральной симметрией U = U(r), то этой системе соответствует сохранение орбитального момента количества движения l и одной из его проекций m. При этом из-за сферической симметрии задачи энергия состояний не будет зависеть от величины m, т. е. состояния будут вырожденными по m.
Наряду с пространственными симметриями, связанными с непрерывными преобразованиями, в квантовой физике существуют и другие симметрии – дискретные. Одной из них является зеркальная симметрия волновой функции относительно инверсии координат (

Система тождественных частиц характеризуется еще одной симметрией – симметрией относительно перестановок тождественных частиц. Эта симметрия определяется свойствами частиц, образующих систему. Системы частиц с целым спином (бозонов) описываются симметричными волновыми функциями, системы частиц с полуцелым спином (фермионов) − антисимметричными волновыми функциями.
Задачи
4.1. Вычислите допустимые уровни энергии электрона, находящегося в одномерной прямоугольной потенциальной яме шириной 10 -8 см, протона, находящегося в потенциальной яме 5 Фм, и шарика массой 1 г, находящегося в потенциальной яме 1 см.
4.2. Рассчитать энергию перехода между состояниями 1s и 2s в атоме водорода.
4.3. Найти значение полного момента j для протона в d-состоянии. Каким будет результат измерения полного момента протона в состоянии 1d5/2?
4.4. Найти полный момент (квантовое число j) системы двух нуклонов в s‑состоянии (l = 0).
4.5. Какие значения может иметь полный момент системы j, если
А. Нейтрон и протон находятся в состояниях с |l,s:j>n = |1, 1 /2: 3 /2>, |l,s:j>p = |1, 1 /2: 3 /2>?
Б. Два нейтрона находятся в состояниях с |l,s:j>1 = |1, 1 /2: 3 /2> и |l,s:j>2 = |1, 1 /2: 3 /2>?
4.6. А) Нейтрон находится в p-состоянии. Найти значения полного момента j и возможные значения проекции момента jz. Каким будет результат измерения орбитального момента частицы в этом состоянии? Б) Рассмотрите задачу А) для протона в d-состоянии.
Ответ: А) j = 3/2, 1/2; jz = ±3/2, ±1/2; L = ћ√ l(l +1) = √ 2 ћ;
Б) j = 5/2, 3/2; jz = ±5/2, ±3/2, ±1/2; L = ћ√ l(l +1) = √ 6 ћ
4.7. А) Частица с собственным моментом s = 3/2 находится в состоянии с орбитальным моментом
l = 2. Найти полный момент частицы j.
Б) Частица с собственным моментом s = 1/2 находится в состоянии с орбитальным моментом
l = 3. Определите полный момент частицы j
Ответ: А) j = 7/2 ÷ 1/2; Б) j = 7/2, 5/2
4.8. Протон и нейтрон находятся в состоянии с относительным орбитальным моментом L = 1. Найти полный момент системы J.
Ответ: J = 0, 1, 2
4.9. На оболочке с квантовым числом n = 1, l = 2 находятся протон и нейтрон. Определить их суммарный полный момент J и его проекцию Jz. Изменится ли результат, если на оболочке n = 1,
l = 2 будут находиться два нейтрона?
4.10. Почему возникают вырожденные состояния?
4.11. Написать оператор Гамильтона 
4.12. Напишите стационарное уравнение Шредингера в сферической системе координат.
4.13. Какие квантовые числа характеризуют частицу в центрально-симметричной потенциальной яме?
4.14. Покажите, что волновые функции ψ = Aexp(kx −ωt) и ψ = Asin(kx −ωt) не удовлетворяют зависящему от времени уравнению Шредингера.
4.15. Покажите, что волновые функции ψ = Ae i(kx −ωt) и ψ = A(cos(kx −ωt) − sin(kx −ωt))удовлетворяют зависящему от времени уравнению Шредингера.
4.16. Частица находится в низшем состоянии n = 1 в бесконечно глубокой одномерной прямоугольной потенциальной яме размера L.
А) Рассчитайте вероятность обнаружить частицу в интервале Δx = 0.001L при x = 1 /2L, x = 2 /3L, x = L.
Б) Рассмотрите случай, когда частица находится в состоянии n = 2 при тех же значениях x.
Ответ: А) P(L/2) = 0.002; P(2L/3) = 0.0015; P(L) = 0; Б) P(L/2) = 0; P(2L/3) = 0.0015; P(L) = 0
4.17. Частица находится в состоянии n = 2 в бесконечно глубокой одномерной прямоугольной потенциальной яме размера L. Рассчитайте вероятность обнаружить частицу в интервале ( 1 /3L, 2 /3L).
Ответ: P(L/3, 2L/3) = 0.2
4.18. Электрон находится всостонии n = 5 в бесконечно глубокой одномерной прямоугольной потенциальной яме размера L. Рассчитайте вероятность обнаружить электрон в области x от 0.2L до 0.5L.
Ответ: P(0.2L, 0.5L) = 0.3
4.19. Электрон находится в бесконечно глубокой одномерной потенциальной яме. Рассчитайте ширину потенциальной ямы, если энергия состояния n = 1 равна 0.1 эВ.
Ответ: L = 1.9 нм
4.20. Рассчитайте средние значения и 2 > для состояний n = 1, 2, 3 в бесконечно глубокой прямоугольной потенциальной яме.
4.21. Что общего и в чем различие в описании атома водорода в теории Шредингера и в модели Бора?
4.22. Почему энергии атома водорода в теории Шредингера не зависят от орбитального квантового числа l?
4.23. Угловой момент характеризуется квантовым числом l = 3. Какие значения могут принимать Lz и L 2 ?
Ответ: Lz = -3ћ, -2ћ. 3ћ; L 2 = 12ћ 2
4.24. Угловой момент характеризуется квантовым числом l = 3. Какие значения могут принимать Lz и L 2 ?
Уравнение Шредингера (конкретные ситуации)
Задание 1
Стационарным уравнением Шредингера для частицы в одномерном ящике с бесконечно высокими стенками является уравнение…
Варианты ответов:
1) 
2 
3) 
4)
Задание 2
Стационарным уравнением Шредингера для частицы в трёхмерном потенциальном ящике с бесконечно высокими стенками является уравнение …
Варианты ответов:
1) 
2) 
3) 
4)
Задание 3
Стационарное уравнение Шредингера в общем случае имеет вид: 
Варианты ответов:
1) 
3) 
Задание 4
Стационарным уравнением Шредингера для электрона в водородоподобном ионе является уравнение…
Варианты ответов:
1) 
2) 
3) 
4)
Задание 5
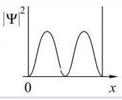
На рисунках приведены картины распределения плотности вероятности нахождения микрочастицы в потенциальной яме с бесконечно высокими стенками. Состоянию с квантовым числом n=2 соответствует распределение…
Варианты ответов:
1) 


Задание 6
На рисунке изображена плотность вероятности обнаружения микрочастицы на различных расстояниях от «стенок» ямы. Вероятность ее обнаружения в центре ямы равна…
Варианты ответов:
Задание 7
Вероятность обнаружить электрон на участке (a,b) одномерного потенциального ящика с бесконечно высокими стенками вычисляется по формуле 

Варианты ответов:
Задание 8
Вероятность обнаружить электрон на участке (a,b) одномерного потенциального ящика с бесконечно высокими стенками вычисляется по формуле 

Варианты ответов:
1) 5/8; 2) 3/8; 3) 1/2; 4) 1/4
Задание 9
Вероятность обнаружить электрон на участке (a,b) одномерного потенциального ящика с бесконечно высокими стенками вычисляется по формуле 

Варианты ответов:
1) 3/8; 2) 1/2; 3) 5/8; 4) 1/4
Задание 10
Вероятность обнаружить электрон на участке (a,b) одномерного потенциального ящика с бесконечно высокими стенками вычисляется по формуле , 
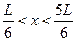
Варианты ответов:
Задание 11
Электрон находится в возбужденном состоянии (n=2) в одномерном потенциальном ящике шириной a c бесконечно высокими стенками. Плотность вероятности нахождения электрона максимальна в точках с координатами…
Варианты ответов:
1) 
2) 
3) 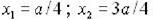
4)
Задание 12
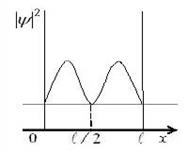
Электрон находится в первой трети прямоугольного одномерного потенциального ящика с непроницаемыми стенками на втором энергетическом уровне. Вероятность найти электрон в центре этого потенциального ящика на этом же энергетическом уровне равна …
Варианты ответов:
Задание 13
Волновая функция частицы в потенциальной яме с бесконечно высокими стенками шириной L имеет вид: 
Варианты ответов:
1) 
2) 
Задание 14
Волновая функция частицы в потенциальной яме с бесконечно высокими стенками шириной L имеет вид: 

Варианты ответов:
Задание 15
Волновая функция частицы в потенциальной яме 

Варианты ответов
1) 


Задание 16
В потенциальной яме бесконечной глубины находится электрон. Волновые функции

д) нет верного ответа.
Задание 17
Электрон, имеющий кинетическую энергию 





 |
а) 
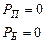

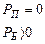
| Соответствующий случай | Буква |
Классическая теория,  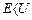 | |
Классическая теория,  | |
Квантовая теория, 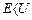 | |
Квантовая теория,  | |
| Неверный ответ |
Задание 18
Выберите правильный ответ для единиц измерения одномерной пси-функции (ψ=ψ(х))
б) 
в) 
г) 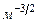
д) нет верного ответа
Задание 19
В потенциальной яме с вертикальными стенками находится электрон. Его волновая функция изображена на рисунке. В этом случае глубина потенциальной ямы
б) бесконечна слева, конечна справа;
в) бесконечна справа, конечна слева;
д) нет верного ответа.
Задание 20
Физический смысл пси-функции в том, что
а) её модуль описывает движение частицы;
б) она показывает плотность вероятности нахождения частицы в окрестности данной точки пространства;
в) квадрат её модуля показывает плотность вероятности нахождения частицы в окрестности данной точки пространства;
г) куб её модуля показывает вероятность нахождения частицы в данной точке пространства;
д) нет верного ответа.
Задание 21
Электрон находится в потенциальной яме с бесконечно высокими стенками. Для некоторых состояний в середине ямы пси-функция электрона может иметь узел, т.е. y=0. Выберите правильное высказывание:
а) пси-функция не может иметь узлов в яме с бесконечными стенками;
б) пси-функция не может иметь узел в центре ямы;
в) номера состояний кратны двум;
г) номера состояний кратны трем.
Задание 22
Частица находится в прямоугольной одномерной потенциальной яме с бесконечно высокими стенками в состоянии с главным квантовым числом n .Чему равно количество узлов пси-функции внутри ямы, не учитывая узлов (y=0) на границах ямы?
д) нет верного ответа.
Задание 23
Выберите правильное продолжение высказывания. Для макроскопических тел, например пылинки в спичечном коробке, мы не замечаем квантования уровней энергии, потому, что
а) макроскопические тела не подчиняются законам квантовой механики;
б) уровни энергии макроскопических тел расположены настолько редко, что квантование энергии не заметно;
в) уровни энергии макроскопических тел расположены настолько часто, что квантование энергии не заметно;
г) эксперименты по обнаружению квантования энергии макроскопических тел не проводились.
Задание 24
В потенциальной яме бесконечной глубины находится электрон. Волновые функции схематически представлены на рисунке. Ширину ямы уменьшили в два раза. Во сколько раз изменится при этом минимальное значение кинетической энергии электрона?
 |
Задание 25
Частица находится в одномерной бесконечно глубокой потенциальной яме прямоугольной формы. Установите соответствие между графиком зависимости 

 |
| Номер состояния | Соответствующая буква |
Задание 26
Условие нормировки пси-функции для частицы, находящейся в потенциальной яме с непроницаемыми стенками шириной l, заключается в том, что вероятность нахождения частицы внутри ямы равна:
г) 
д) нет верного ответа.
Задание 27
Выберите неверные утверждения
а) уравнение Шредингера описывает движение квантовой частицы;
б) уравнение Шредингера может быть получено уточнением законов Ньютона в классической механике;
в) квантовая теория настаивает на отказе от абсолютной определенности в задании начальных условий движения частицы;
г) в квантовой теории физический смысл имеет только вещественная часть комплексной волновой функции;
д) для макроскопических частиц предсказания квантовой и классической теории совпадают.
Задание 28
Частица находится в одномерной потенциальной яме прямоугольной формы с непроницаемыми стенками. Общее решение для стационарного уравнения Шрёдингера имеет вид:
а) 
б) 
в) 
г) 
д) правильных решений не приведено.
Задание 29
На рисунках схематично изображены зависимости от координаты плотности вероятности обнаружения частицы. Установите соответствие между формой одномерной прямоугольной потенциальной ямы и рисунком и заполните таблицу.
 |
| Форма потенциальной ямы | Соответствующая буква |
| Стенки ямы конечной высоты | |
| Обе стенки конечной высоты, правая стенка выше | |
| Обе стенки конечной высоты, левая стенка выше | |
| Левая стенка конечной высоты, правая – бесконечной | |
| Правая стенка конечной высоты, левая – бесконечной | |
| Стенки ямы бесконечной высоты |
Задание 30
Частица массы m находится в одномерной прямоугольной яме ширины l с непроницаемыми стенками в состоянии с пси-функцией Yn(x,t) и спектром энергии