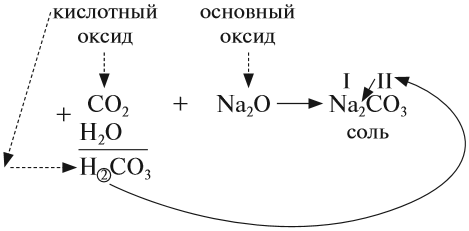
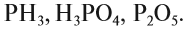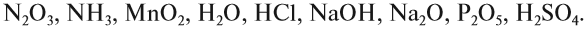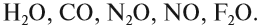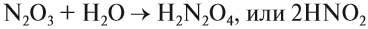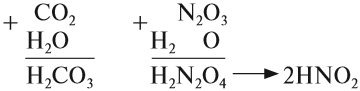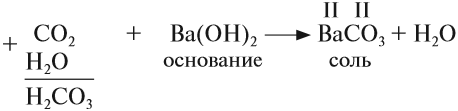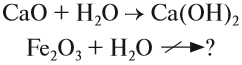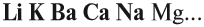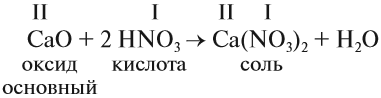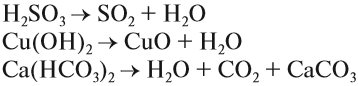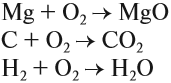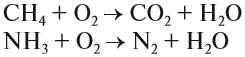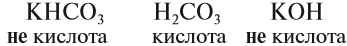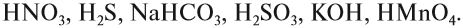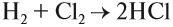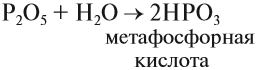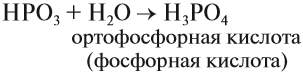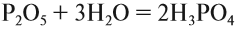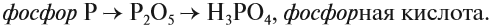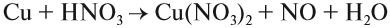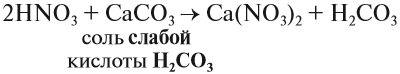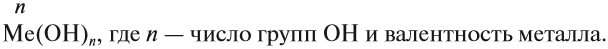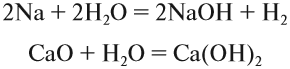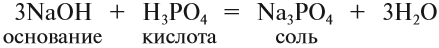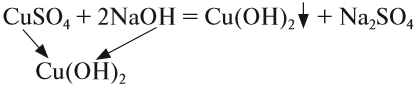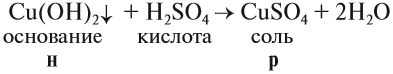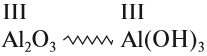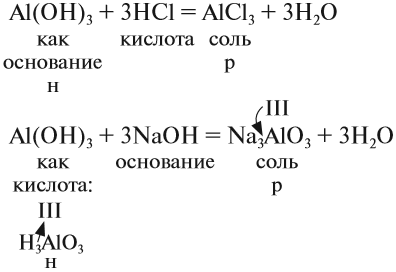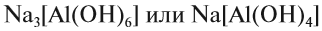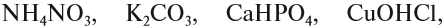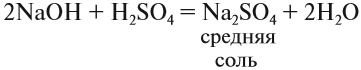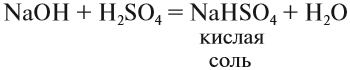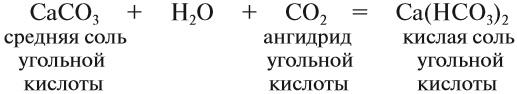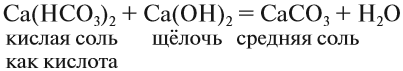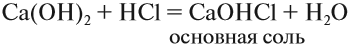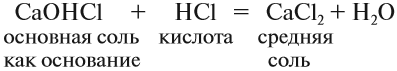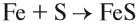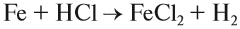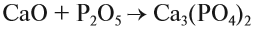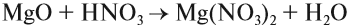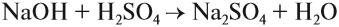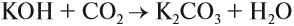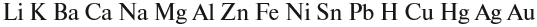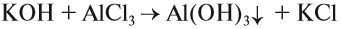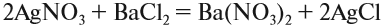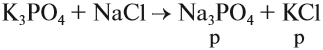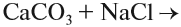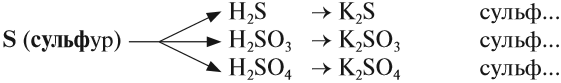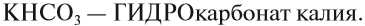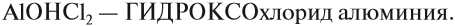Оксиды — это сложные вещества, состоящие из атомов двух элементов, один из которых — кислород со степенью окисления -2. При этом кислород связан только с менее электроотрицательным элементом.
В зависимости от второго элемента оксиды проявляют разные химические свойства. В школьном курсе оксиды традиционно делят на солеобразующие и несолеобразующие. Некоторые оксиды относят к солеобразным (двойным).
Двойные оксиды — это некоторые оксиды , образованные элементом с разными степенями окисления.
Солеобразующие оксиды делят на основные, амфотерные и кислотные.
Основные оксиды — это оксиды, обладающие характерными основными свойствами. К ним относят оксиды, образованные атомами металлов со степень окисления +1 и +2.
Кислотные оксиды — это оксиды, характеризующиеся кислотными свойствами. К ним относят оксиды, образованные атомами металлов со степенью окисления +5, +6 и +7, а также атомами неметаллов.
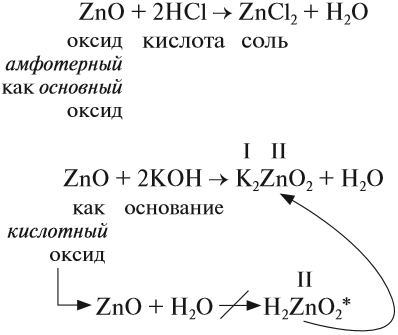
Амфотерные оксиды — это оксиды, характеризующиеся и основными, и кислотными свойствами. Это оксиды металлов со степенью окисления +3 и +4, а также четыре оксида со степенью окисления +2: ZnO, PbO, SnO и BeO.
Несолеобразующие оксиды не проявляют характерных основных или кислотных свойств, им не соответствуют гидроксиды. К несолеобразующим относят четыре оксида: CO, NO, N2O и SiO.
- Классификация оксидов
- Получение оксидов
- Химические свойства оксидов
- Химические свойства основных оксидов
- Основные способы получение оксидов
- Урок 2. Основные классы неорганических соединений
- Оксиды
- Свойства кислотных оксидов
- Свойства основных оксидов
- Свойства амфотерных оксидов
- Способы получения оксидов
- Выводы
- Кислоты
- Свойства кислот
- Выводы
- Основания
- Свойства и способы получения щелочей
- Свойства и способы получения нерастворимых в воде оснований
- Свойства амфотерных гидроксидов
- Выводы
- Способы получения солей
- Названия солей
- Выводы
Классификация оксидов
Получение оксидов
Общие способы получения оксидов:
1. Взаимодействие простых веществ с кислородом :
1.1. Окисление металлов: большинство металлов окисляются кислородом до оксидов с устойчивыми степенями окисления.
Например , алюминий взаимодействует с кислородом с образованием оксида:
Не взаимодействуют с кислородом золото, платина, палладий.
Натрий при окислении кислородом воздуха образует преимущественно пероксид Na2O2,
Калий, цезий, рубидий образуют преимущественно пероксиды состава MeO2:
Примечания : металлы с переменной степенью окисления окисляются кислородом воздуха, как правило, до промежуточной степени окисления (+3):
Железо также горит с образованием железной окалины — оксида железа (II, III):
1.2. Окисление простых веществ-неметаллов.
Как правило, при окислении неметаллов образуется оксид неметалла с высшей степенью окисления, если кислород в избытке, или оксид неметалла с промежуточной степенью окисления, если кислород в недостатке.
Например , фосфор окисляется избытком кислорода до оксида фосфора (V), а под действием недостатка кислорода до оксида фосфора (III):
Но есть некоторые исключения .
Например , сера сгорает только до оксида серы (IV):
Оксид серы (VI) можно получить только окислением оксида серы (IV) в жестких условиях в присутствии катализатора:
2SO2 + O2 = 2SO3
Азот окисляется кислородом только при очень высокой температуре (около 2000 о С), либо под действием электрического разряда, и только до оксида азота (II):
Не окисляется кислородом фтор F2 (сам фтор окисляет кислород). Не взаимодействуют с кислородом прочие галогены (хлор Cl2, бром и др.), инертные газы (гелий He, неон, аргон, криптон).
2. Окисление сложных веществ (бинарных соединений): сульфидов, гидридов, фосфидов и т.д.
При окислении кислородом сложных веществ, состоящих, как правило, из двух элементов, образуется смесь оксидов этих элементов в устойчивых степенях окисления.
Например , при сжигании пирита FeS2 образуются оксид железа (III) и оксид серы (IV):
Сероводород горит с образованием оксида серы (IV) при избытке кислорода и с образованием серы при недостатке кислорода:
А вот аммиак горит с образованием простого вещества N2, т.к. азот реагирует с кислородом только в жестких условиях:
А вот в присутствии катализатора аммиак окисляется кислородом до оксида азота (II):
3. Разложение гидроксидов. Оксиды можно получить также из гидроксидов — кислот или оснований. Некоторые гидроксиды неустойчивы, и самопроизвольную распадаются на оксид и воду; для разложения некоторых других (как правило, нерастворимых в воде) гидроксидов необходимо их нагревать (прокаливать).
гидроксид → оксид + вода
Самопроизвольно разлагаются в водном растворе угольная кислота, сернистая кислота, гидроксид аммония, гидроксиды серебра (I), меди (I):
2AgOH → Ag2O + H2O
2CuOH → Cu2O + H2O
При нагревании разлагаются на оксиды большинство нерастворимых гидроксидов — кремниевая кислота, гидроксиды тяжелых металлов — гидроксид железа (III) и др.:
4. Еще один способ получения оксидов — разложение сложных соединений — солей .
Например , нерастворимые карбонаты и карбонат лития при нагревании разлагаются на оксиды:
Соли, образованные сильными кислотами-окислителями (нитраты, сульфаты, перхлораты и др.), при нагревании, как правило, разлагаются с с изменением степени окисления:
Более подробно про разложение нитратов можно прочитать в статье Окислительно-восстановительные реакции.
Химические свойства оксидов
Значительная часть химических свойств оксидов описывается схемой взаимосвязи основных классов неорганических веществ.
Химические свойства основных оксидов
Подробно про химические свойства оксидов можно прочитать в соответствующих статьях:
Основные способы получение оксидов
1) Непосредственное взаимодействие простых веществ с кислородом в различных условиях. Например:
2) Окисление сложных веществ кислородом. Например:
3) Термическое разложение кислородсодержащих соединений (гидроксидов, солей). Например:
4) Восстановление менее активных металлов более активными металлами. Например:
Следует отметить, что реакции этого типа используются для получения пассивных металлов из природных рудных образований.
Основные химические свойства оксидов
1) Основные оксиды, образованные щелочными и щелочноземельными металлами, непосредственно соединяются с водой, образуя растворимые в воде основания – щелочи. Например:
2) Основные оксиды взаимодействуют с кислотными оксидами и с кислотами. Например:
3) Кислотные оксиды, за исключением оксидов нерастворимых в воде, непосредственно соединяются с водой, образуя кислоты. Например:
4) Кислотные оксиды взаимодействуют с основными оксидами и с основаниями с образованием солей. Например:
5) Амфотерные оксиды взаимодействуют как с кислотами, так и со щелочами, образуя соли. Например, при нагревании твердых веществ:
В растворах щелочей образуются комплексные соли (гидроксокомплексы). Например:
С кислотами амфотерные оксиды образуют обычные соли. Например:
Кислотно – основные свойства оксидов одного и того же элемента зависят от степени окисления атома этого элемента. Так с повышением степени окисления атома элемента кислотные свойства его оксидов увеличиваются, а основные ослабевают.
Рассмотрим зависимость кислотно-основных свойств от степени окисления на примере соединений хрома (табл. 4)
Зависимость кислотно-основных свойств оксидов хрома от степени окисления атома хрома
| степень окисления | +2 | +3 | + 6 |
| формула оксида | CrO | Cr2O3 | CrO3 |
| характер оксида | основной | амфотерный | кислотный |
| формула гидроксида | Cr(OH)2 | Cr(OH)3 | H2CrO4 |
Таким образом, повышение степени окисления атома хрома кислотные свойства его оксидов увеличиваются, а основные ослабевают.
В периодах Периодической системы кислотные свойства оксидов увеличиваются слева направо, а в группе кислотные свойства оксидов уменьшаются сверху вниз.Например, изменение характера оксидов для элементов третьего периода в высшей степени окисления (табл. 5)
Дата добавления: 2019-04-03 ; просмотров: 1031 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Урок 2. Основные классы неорганических соединений
Оксиды
Оксиды — сложные вещества, молекулы которых состоят из атомов двух химических элементов, один из которых — кислород. Атом кислорода в оксидах всегда имеет степень окисления –2.
Определите, какое из следующих соединений — оксид:
Оксидом является последнее соединение — P2O5 (в состав РН3 не входит атом кислорода, а в состав H3PO4 входят атомы трёх химических элементов: H, Р, O).
Оксиды называют по схеме:
оксид чего? (название элемента).
Например: СаО — оксид кальция.
Если оксид образован химическим элементом с переменной валентностью, то после названия элемента, нужно указать его валентность.
Например: Fe2О3 — оксид железа III, FеО — оксид железа II.
Задание 2.1. Среди следующих соединений найдите оксиды и назовите их:
Задание 2.2. Составьте формулы следующих оксидов: оксид хрома III, оксид углерода IV, оксид магния, оксид серы VI, оксид азота V, оксид калия, оксид марганца VI.
Многие оксиды могут реагировать с кислотами или основаниями. Продуктами таких реакций являются соли. Поэтому такие оксиды называются солеобразующими.
Однако существует небольшая группа оксидов, которые к таким реакциям не способны. Такие оксиды называются несолеобразующими:
Задание 2.3. Назовите эти несолеобразующие оксиды.
Некоторые оксиды имеют особые (тривиальные) названия:
Солеобразующие оксиды делятся на три группы: основные, кислотные, амфотерные.
Точно установить характер оксида можно, только изучая его химические свойства. Например, кислотные оксиды реагируют с основаниями и не реагируют с кислотами. Основные оксиды реагируют с кислотами и не реагируют с основаниями. Амфотерные оксиды могут реагировать и с кислотами, и с основаниями, причём, реагируя с кислотами, они проявляют свойства основных оксидов, а реагируя с основаниями, — кислотных.
Отсюда вывод: в химических реакциях участвуют вещества с противоположными свойствами:
- основание и кислота;
- металл и неметалл;
- окислитель и восстановитель.
Впрочем, последние два случая мы рассмотрим позднее (см. уроки 2.4 и 7).
Поэтому, если определить по формуле оксида, какими свойствами он обладает, — можно предсказать, возможна ли эта реакция или нет! Но КАК это сделать? Вот некоторые правила:
- неметаллы образуют только кислотные оксиды*;
- металлы могут образовывать разные оксиды — основные, амфотерные, кислотные — в зависимости от валентности металла.
* Обратите внимание, что и безразличные оксиды образуются только неметаллами.
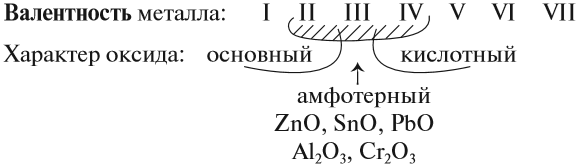
Предсказать свойства оксида металла может помочь эта схема.
Итак, основные оксиды металлов от кислотных оксидов металлов отличить легко: малая валентность металла — основный оксид; большая — кислотный. Но как быть с амфотерными оксидами? «Любимая» валентность металлов в этих оксидах — III. Но есть и исключения. Поэтому желательно запомнить формулы наиболее часто встречающихся амфотерных оксидов:
Задание 2.4. Назовите эти амфотерные оксиды.
Задание 2.5. Классифицируйте нижеприведённые оксиды:
Упражнение рекомендуется выполнить по схеме:
1. Определить, не является ли данный оксид несолеобразующим;
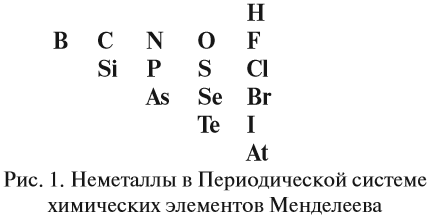
2. Определить, какой элемент входит в состав оксида: металл или неметалл, для чего выписать из таблицы Менделеева символы элементов – неметаллов: они расположены в главных подгруппах выше линии БОР — АСТАТ и на этой линии. Это:
3. Если в состав оксида входит атом неметалла — то оксид кислотный;
4. Для атома металла определить валентность, и по схеме определить характер оксида: основный, амфотерный или кислотный.
- Сr2О3 — амфотерный, так как хром — металл с низкой валентностью III;
- N2O3 — кислотный оксид, так как азот — неметалл;
- СrO3 — кислотный оксид, так как хром — металл с высокой валентностью VI.
Зная характер оксида, можно описать его свойства.
Свойства кислотных оксидов
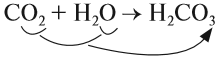
1. Кислотные оксиды, кроме SiО2, реагируют c водой, образуя кислоту:
Чтобы составить формулу кислоты, нужно «сложить» все атомы исходных веществ, записывая на первом месте символ водорода, на втором — символ элемента, образующего оксид, и на последнем — символ кислорода. Если индексы получились чётными, их можно сократить:
Эти же реакции можно записать в виде «арифметического примера»:
Задание 2.6. Составьте уравнения реакций с водой для кислотных оксидов из задания 2.5, зная, что реакции идут по схеме:
кислотный оксид + вода → кислота
2. Кислотные оксиды реагируют с основными оксидами, образуя соль соответствующей кислоты, т. е. кислоты, которая образуется при взаимодействии этого оксида с водой (см. выше):
Для того чтобы составить такое уравнение, нужно:
- составить формулу кислоты («прибавив» к молекуле оксида молекулу воды);
- определить валентность кислотного остатка (это часть молекулы кислоты без атомов водорода). В данном случае кислотный остаток имеет состав СО3, его валентность равна числу атомов водорода в кислоте, т. е. II;
- составить формулу соли, записав вместо атомов водорода атом металла из основного оксида с его валентностью (в данном случае — натрий);
- составить формулу соли по валентности металла и кислотного остатка.
Задание 2.7. Составьте уравнения реакций с оксидом кальция кислотных оксидов из задания 2.5, зная, что реакции идут по схеме:
кислотный оксид + основный оксид → соль
3. Кислотные оксиды реагируют с основаниями, образуя соль соответствующей кислоты и воду:
Принципы составления уравнения те же, что и для реакций с основными оксидами (см. пункт 2).
Задание 2.8. Составьте уравнения реакций с гидроксидом натрия NаОН кислотных оксидов из задания 2.5, зная, что реакции идут по схеме:
кислотный оксид + основание → соль + вода
ЗАПОМНИТЕ! Кислотные оксиды и с кислотами и кислотными оксидами НЕ РЕАГИРУЮТ!
Свойства основных оксидов
1. Основные оксиды реагируют с водой, образуя основание. Реакция происходит, если получающееся основание растворимо в воде.
Общая формула оснований Ме(ОН)х, где х — валентность металла, равная числу ОН групп.
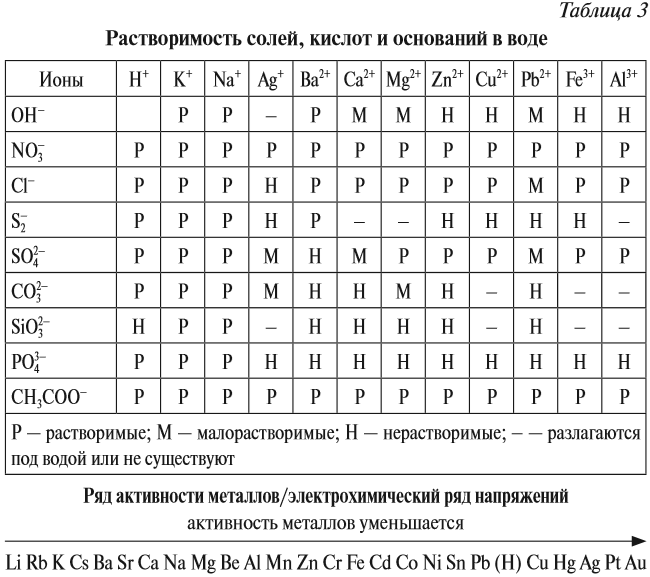
Последняя реакция не идет, так как основание Fe(ОН)3 нерастворимо в воде. Растворимость веществ в воде можно определить по таблице растворимости (рис. 2).
При определении возможности протекания данной реакции можно использовать и другое правило.
Основный оксид реагирует с водой, если он образован активным металлом. Такие металлы стоят в ряду напряжений до магния (см. табл. 3).
Задание 2.9. Составьте уравнения реакций с водой для основных оксидов из задания 2.5, зная, что реакции идут по схеме:
основный оксид + вода → основание
2. Основные оксиды реагируют с кислотами, образуя соль и воду:
Обратите внимание: при составлении формулы соли нужно вместо атомов водорода в формуле кислоты написать символ металла, а затем составить полученную формулу по валентности.
Задание 2.10. Составьте уравнения реакций с Н2SО4 для основных оксидов из задания 2.5, зная, что реакции идут по схеме:
основный оксид + кислота → соль + вода
3. Основные оксиды реагируют с кислотными оксидами, образуя соль (см. задание 2.7).
4. Некоторые основные оксиды реагируют при нагревании с водородом, при этом образуется металл и вода:
ЗАПОМНИТЕ! Основные оксиды с основаниями и основными оксидами НЕ РЕАГИРУЮТ!
ВЫВОД. В реакцию легче всего вступают вещества с противоположными свойствами, и не вступают в реакцию вещества со сходными свойствами.
Свойства амфотерных оксидов
Амфотерные оксиды (от греч. amphi — двойной) проявляют двойственные свойства: они могут реагировать и с кислотами, и с основаниями (точнее, со щелочами). При этом образуются соль и вода.
* Такая реакция не происходит, но эта схема позволяет определить состав «кислотного остатка» и его валентность, а затем составить химическую формулу соли.
Задание 2.11. Составьте уравнения реакций с КОН и с НNО3 для амфотерных оксидов из задания 2.5.
Задание 2.12. С какими веществами (Н2О, NаОН, НСl) могут реагировать оксиды: Cr2O3, CrO, SO3, V2O5?
Составьте уравнения необходимых реакций. При составлении уравнений реакций помните:
- реагируют вещества с противоположными свойствами;
- сначала определите, какой это оксид (см. задание 2.5);
- затем, исходя из свойств этого оксида, составьте уравнения, пользуясь схемами заданий 2.6–2.10 и вышеприведенными уравнениями реакций для амфотерных оксидов.
Способы получения оксидов
Оксиды могут быть получены при разложении некоторых кислот, оснований, солей:
Оксиды обычно получают при сгорании в кислороде простых и сложных веществ:
Обратите внимание! При сгорании сложных веществ образуются оксиды элементов, которые входят в его состав. Исключение составляют только азот и галогены (F, Cl, Br, I), которые выделяются в виде простых веществ. Например:
Выводы
Молекулы оксидов состоят из атомов двух элементов. Один из этих элементов — кислород. Оксиды, образующие соли, бывают кислотные, амфотерные и основные. Оксиды реагируют с веществами, которые проявляют противоположные свойства.
- Основные оксиды — с кислотными оксидами или кислотами.
- Кислотные оксиды — с основными оксидами или основаниями.
- Амфотерные — и с кислотами, и с основаниями (щелочами).
В каждой из таких реакций образуется соль и вода.
Кислоты
Кислоты — это сложные вещества, в состав молекул которых входит активный атом водорода и кислотный остаток. Этот активный атом водорода в химических реакциях способен замещаться на атом металла, в результате чего всегда получается соль.
В формулах неорганических кислот этот атом водорода записывается на первом месте*:
* В химических формулах органических кислот атом водорода стоит в конце, например, CH3–COOH уксусная кислота
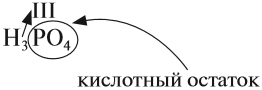
В состав любой кислоты кроме атомов водорода входит кислотный остаток. Кислотный остаток — это часть молекулы кислоты без атомов водорода (которые могут быть замещены на атом металла). Валентность кислотного остатка равна числу таких атомов водорода:
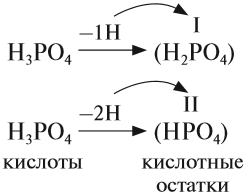
При определении валентности кислотного остатка учитываются те атомы водорода, которые участвовали в реакции или могут участвовать в ней. Так, фосфорной кислоте Н3РО4, в зависимости от условий, могут соответствовать кислотные остатки иного состава:
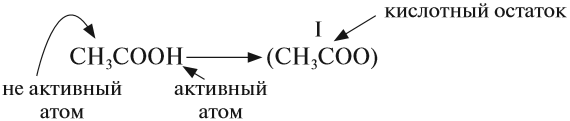
У органических кислот не все атомы водорода в молекуле способны замещаться на атом металла:
Задание 2.13. Определите состав и валентность кислотных остатков для кислот, учитывая, что все атомы водорода кислот участвуют в реакции:
По числу атомов водорода кислоты делят на одноосновные и многоосновные:
- НСl — одноосновная, так как один атом водорода;
- Н2СО3 — двухосновная, так как два атома водорода.
По составу кислоты делят на:
Бескислородные кислоты представляют собой растворы некоторых газов в воде, при этом и растворённому газу, и полученному раствору приписывают одинаковые свойства, хотя это не так. Например, из простых веществ водорода и хлора получается газ хлороводород:
Этот газ не проявляет кислотных свойств, если он сухой: его можно перевозить в металлических ёмкостях, и никакой реакции не происходит. Но при растворении хлороводорода в воде получается раствор, который проявляет свойства сильной кислоты, её перевозить в металлических ёмкостях нельзя! Этот раствор называется «соляная кислота».
Названия бескислородных кислот составляют по принципу:
«ЭЛЕМЕНТ» + «ВОДОРОД»ная кислота
- H2S — сероводородная кислота (это раствор газа сероводорода в воде);
- НСl — хлороводородная (соляная) кислота (это раствор газа хлороводорода в воде);
- НF — фтороводородная (плавиковая) кислота (это раствор газа фтороводорода в воде).
Кислородсодержащие кислоты могут быть получены при действии воды на кислотные оксиды (см. задание 2.6). Исходные кислотные оксиды называются «АНГИДРИДЫ кислот»:
Метафосфорная кислота неустойчива и, присоединяя воду, превращается в более устойчивую кислоту:
или в суммарном виде:
Таким образом, Р2O5 — ангидрид фосфорной кислоты, а также некоторых других, менее устойчивых кислот.
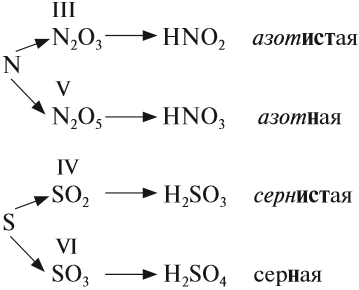
Обратите внимание! Название кислородосодержащей кислоты содержит в виде корня название элемента, входящего в состав ангидрида:
Если элементу соответствуют несколько кислот, то для кислоты с большей валентностью элемента, входящего в состав ангидрида, в названии употребляют суффикс «Н» или «В». Для кислот с меньшей валентностью элемента в названиях добавляют еще один суффикс «ИСТ».
Валентность элемента проще всего определять по формуле ангидрида:
Обратим внимание, что в названии сернистой кислоты основной суффикс -ИСТ-, а суффикс -Н- введён дополнительно для благозвучия.
Сведём всё известное о названиях кислот в таблицу 4.
Задание 2.14. Заполнить табл. 4, заменив знаки вопросов формулами и названиями соответствующих кислот.
Задание 2.15. Напишите НА ПАМЯТЬ формулы кислот: кремниевой, сернистой, серной, сероводородной, азотистой, азотной, соляной, фосфорной, угольной. Укажите ангидриды этих кислот (там, где они существуют).
Свойства кислот
Главным свойством всех кислот является их способность образовывать соли. Соли образуются в любой реакции, в которой участвует кислота, при этом замещаются активные атомы водорода (один, все или несколько).
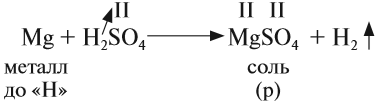
1. Кислоты реагируют с металлами, при этом атом водорода кислоты замещается на атом металла — в результате образуется растворимая соль* и водород:
* Если образуется нерастворимая соль, то эта соль закрывает поверхность металла и реакция останавливается.
Не все металлы способны вытеснять водород из растворов кислот: этот процесс возможен только для тех металлов, которые стоят в ряду напряжений ДО водорода (рис. 3 или таблица 3).
Задание 2.16. Составьте уравнения возможных реакций:
- серная кислота + алюминий →
- соляная кислота + серебро →
- бромоводородная кислота + цинк →
При составлении уравнений пользуйтесь рядом напряжений и схемой реакции:
кислота + металл (до водорода) → соль + водород
Не забывайте, составляя формулы солей, учитывать валентность металла и кислотного остатка.
Некоторые кислоты могут растворять металлы, которые стоят в ряду напряжения после водорода, но водород при этом не выделяется:
2. Кислоты реагируют с основаниями, образуя соль и воду*. Это реакция обмена, и поэтому валентность составных частей в результате реакции не меняется:
* Реакция между кислотой и основанием называется реакцией нейтрализации.
Задание 2.17. Составьте аналогичные уравнения реакций по схеме:
кислота + основание → соль + вода
- серной кислоты и Fe(ОН)3;
- соляной кислоты и Ва(ОН)2;
- сернистой кислоты и NаОН.
- составить формулу соли по валентности металла и кислотного остатка;
- расставить коэффициенты.
3. Кислоты могут реагировать с солями. При этом сильная кислота вытесняет более слабую из её соли.
- К сильным кислотам относятся: серная, азотная, соляная и др.
- К слабым кислотам относятся: угольная, кремниевая, сероводородная, азотистая.
Происходит реакция обмена: образуется новая соль и новая кислота.
Более подробно о подобных реакциях см. в уроке 6.
Задание 2.18. Составьте НА ПАМЯТЬ формулы: а) сильных, б) слабых кислот.
Задание 2.19. Составьте уравнения реакций по схеме:
(более сильная) кислота + соль → соль + кислота (более слабая):
4. И, наконец, выяснив свойства кислот, зададим себе вопрос: а можно ли обнаружить кислоту в растворе? Например, в одном стакане налита вода, а в другом — раствор кислоты. Как определить, где кислота? Хотя многие кислоты кислые на вкус, пробовать их НЕЛЬЗЯ — это опасно! Выручают особые вещества — ИНДИКАТОРЫ. Это соединения, которые изменяют цвет в присутствии кислот:
- синий ЛАКМУС становится красным;
- оранжевый МЕТИЛОРАНЖ тоже становится красным.
Выводы
- по числу атомов водорода на одноосновные, двухосновные и т. д.,
- по наличию атома кислорода в составе молекулы на бескислородные и кислородсодержащие,
- по силе на сильные и слабые,
- по устойчивости на устойчивые и неустойчивые.
- с активными металлами (до «Н»),
- с основаниями,
- с основными и амфотерными оксидами,
- с солями более слабых кислот.
Кислоты обнаруживаются индикаторами в кислой («красной») области.
Основания
Основания — это сложные соединения, в состав молекул которых входит атом металла и гидроксогруппа ОН:
Валентность ОН-группы равна I.
Основания называют по схеме:
гидроксид (чего?) металла (n),
где n — переменная валентность металла.
- Са(ОН)2 — гидроксид кальция,
- Fе(OH)3 — гидроксид железа (III),
- NH4OH — гидроксид аммония.
Обратите внимание. В состав последнего основания не входит атом металла. Это исключение. Валентность группы NН4 (аммоний) равна I.
Основания бывают растворимые в воде и нерастворимые в воде. Это легко определить по таблице растворимости.
Растворимые в воде основания называются ЩЕЛОЧАМИ. В состав щелочей входят атомы активных металлов (они находятся в начале ряда напряжений, до магния). Гидроксид аммония тоже относится к щелочам, так как существует только в растворах.
Задание 2.20. Составьте, пользуясь таблицей растворимости или рядом напряжений, химические формулы 2–3 щелочей.
Свойства и способы получения щелочей
Щёлочи можно получить действием активного металла (К, Nа, Cа, Ва) или его оксида на воду:
1. Растворы щелочей реагируют с кислотными и амфотерными оксидами (см. урок 2.1) и с кислотами (см. урок 2.2). Последняя реакция называется реакцией НЕЙТРАЛИЗАЦИИ:
Реакция нейтрализации характерна для всех кислот!
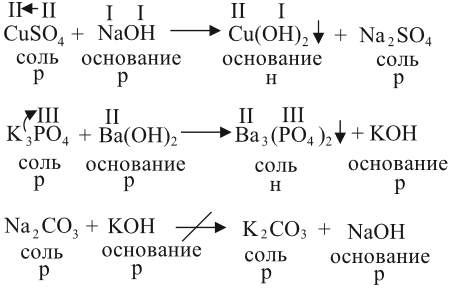
2. Растворы щелочей реагируют с растворами солей. Реакция происходит, если образуется хотя бы одно нерастворимое соединение. Эта реакция относится к реакциям обмена, т. е. в результате получается новая соль и новое основание:
- Последняя реакция не происходит, так как оба полученных вещества растворимы в воде.
- Валентности составных частей исходных молекул определяйте по кислотному остатку или по числу групп ОН.
- Полученные значения валентностей используйте при составлении формул полученных веществ.
- Растворимость получаемых веществ определяйте по таблице растворимости.
Задание 2.21. Расставьте коэффициенты в вышеприведённых уравнениях реакций.
Задание 2.22. Составьте уравнения реакций обмена:
Определите, какая из реакций не происходит и почему.
3. Растворы щелочей, как и растворы кислот, способны изменять окраску индикаторов:
- фиолетовый лакмус синеет,
- оранжевый метилоранж желтеет,
- бесцветный фенолфталеин краснеет.
Все изменения окрасок индикаторов можно свести в таблицу 5.
Обратите внимание: если к воде добавить кислоты, то в растворе будет кислая среда; если добавить щелочь — щелочная; в чистой воде среда нейтральная.
Вопрос 1. Можно ли при помощи фенолфталеина узнать, что налито в стакане: вода? НCl? КОН? А при помощи лакмуса?
Вопрос 2. Почему реакция между кислотой и щелочью названа реакцией нейтрализации?
Свойства и способы получения нерастворимых в воде оснований
Среди нерастворимых в воде оснований следует выделить особую группу веществ — амфотерные гидроксиды. Их свойства будут рассмотрены ниже. Способы получения их такие же, как и для нерастворимых оснований.
Нерастворимые основания получают, действуя на раствор соли, в состав которой входит нужный атом металла, раствором щёлочи:
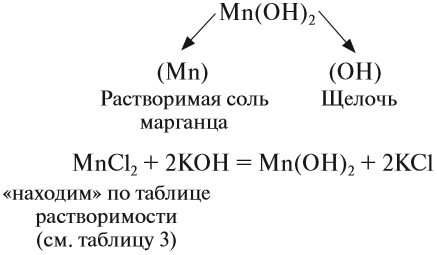
Попробуем определить, какие вещества нужно взять для того, чтобы получить гидроксид марганца (II):
Задание 2.23. Напишите уравнения реакций, при помощи которых можно получить: а) гидроксид железа (III), б) гидроксид железа (II).
Свойства нерастворимых в воде оснований во многом отличаются от свойств щелочей: нерастворимые в воде основания не могут реагировать с растворами солей, а также с амфотерными и некоторыми кислотными оксидами. Они не изменяют окраску индикатора.
1. Нерастворимые основания могут реагировать с кислотами, если при этом происходит растворение исходного нерастворимого вещества (осадка):
Таким образом, эта реакция возможна, если образуется растворимая соль (см. таблицу 3).
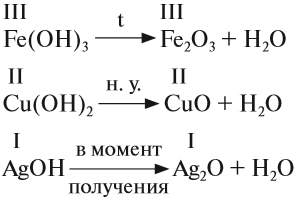
2. Нерастворимые основания разлагаются при нагревании. При этом, чем меньше активность металла (см. ряд напряжений), тем легче разлагается основание на оксид и воду:
Свойства амфотерных гидроксидов
Амфотерные гидроксиды соответствуют амфотерным оксидам. Это означает, что в состав амфотерного гидроксида входит тот же атом металла и с той же валентностью, что и в состав амфотерного оксида:
Как вы думаете, почему эти вещества называются амфотерными? (Если ответить не можете — загляните в урок 2.1.)
Ответ простой — амфотерные соединения проявляют двойственные свойства, т. е. реагируют) и с кислотами, и со щелочами (и растворяются при этом):
Если эта реакция происходит с растворами щелочей, то вместо вещества состава Na3AlO3 (или NaAlO2)* образуется сложное комплексное соединение:
* Ортоалюминиевая кислота H3AlO3 теряет молекулу H2O, и образуется метаалюминиевая кислота HAlO2, в которой кислотный остаток AlO2 имеет валентность I.
Задание 2.24. Составьте уравнения реакций с кислотой и со щёлочью для амфотерных гидроксидов: а) гидроксида цинка; б) гидроксида хрома (III).
Выводы
Молекулы неорганических оснований содержат гидроксогруппу ОН. Все неорганические основания, кроме NH4OH, содержат атом металла. Основания делят на растворимые в воде (щёлочи) и нерастворимые в воде.
Растворы щёлочей реагируют:
- с кислотами (реакция нейтрализации),
- с кислотными и амфотерными оксидами,
- с растворами солей.
Щёлочи обнаруживаются индикаторами в щелочной («синей») области. Нерастворимые в воде основания не изменяют окраску индикатора, могут реагировать с некоторыми кислотами и кислотными оксидами, а также термически неустойчивы.
Соли — это продукт реакции между кислотой и основанием, например реакции нейтрализации. Даже если такая реакция невозможна, ЛЮБОЙ соли можно поставить в соответствие основание и кислоту. Поэтому в состав любой соли входит остаток основания (обычно атом металла или группа NH4) и остаток кислоты (кислотный остаток).
Задание 2.25. Попробуйте определить для каждой из этих солей
где в её молекуле остаток кислоты, а где — остаток основания. Определите валентности составных частей.
Обратите внимание, что в состав некоторых солей входят атомы водорода или группы ОН. Такое различие подсказывает, что соли могут быть разных типов. Рассмотрим три вида солей.
Средние соли. Такие соли получаются, если кислота и основание полностью прореагировали:
Кислые соли. Такие соли получаются, если не все атомы водорода кислоты были замещены на атом металла:
Кислотные остатки таких солей содержат атом водорода. Кислые соли образуются в результате гидролиза некоторых солей, а также при взаимодействии средней соли с ангидридом «своей» кислоты:
Кислые соли могут проявлять некоторые свойства кислот, например они могут реагировать с щелочами:
Основные соли. Такие соли образуются, если не все группы ОН основания замещены на кислотный остаток:
Такие соли содержат гидроксогруппу ОН. Основные соли образуются в результате гидролиза некоторых солей. Основные соли могут проявлять некоторые свойства оснований. Например, они могут реагировать с кислотами:
Способы получения солей
Вспомните, во многих примерах, которые иллюстрировали свойства оксидов, кислот, оснований, — продуктом реакции была соль. Попробуем обобщить эти сведения и выяснить, в результате каких процессов можно получить СОЛЬ заданного состава. Прежде всего, отметим, что способы получения солей можно условно разбить на 2 группы:
- I — получение солей из веществ, которые не являются солями;
- II — получение солей из других солей.
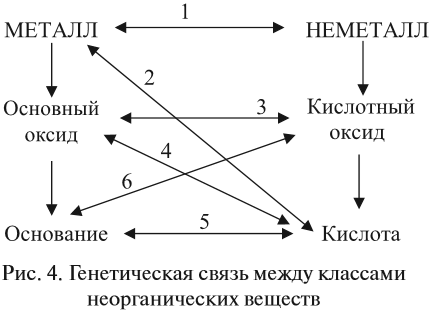
Реакции I группы основаны на том, что в реакцию вступают противоположные по свойствам вещества (рис. 4).
Приведём конкретные примеры:
1. Металл + неметалл (галоген или сера):
2. Металл + кислота:
3. Основный оксид + кислотный оксид:
4. Основный оксид + кислота:
5. Основание + кислота:
6. Основание + кислотный оксид:
Задание 2.26. Расставьте коэффициенты в этих уравнениях. Приведите свои примеры каждого типа.
Реакции II группы являются реакциями обмена или замещения. В каждой из таких реакций участвует соль, и поэтому способы получения солей по группе II фактически являются химическими свойствами солей:
7. Более активный металл вытесняет менее активный из растворов его солей:
обратный процесс не идёт:
Активность металлов можно определять по ряду напряжений:
В этом ряду любой металл активнее всех металлов, стоящих после него (правее него).
8. Сильная кислота вытесняет более слабую кислоту из её соли:
9. Щёлочь, реагируя с солью, образует новое основание и новую соль
Эта реакция происходит, если оба исходных вещества растворимы, а хотя бы одно из полученных веществ — нерастворимо.
10. Соль, вступая в реакцию обмена с другой солью, образует две новые соли
Эта реакция также происходит, если оба исходных вещества растворимы, а хотя бы одно из полученных веществ — нерастворимо.
Например, эта реакция:
невозможна, так как обе полученные соли растворимы. А этот процесс:
невозможен потому, что СаСО3 (мел) нерастворим в воде.
Названия солей
Названия солей происходят от латинского названия химического элемента, который входит в состав кислотного остатка (исключая кислород):
- S — сульфур;
- N — нитрогениум;
- С — карбонеум;
- Si — силициум.
Очевидно, что для солей разного состава должны быть разные названия. Это достигается введением суффиксов:
- для солей бескислородных кислот -ИД-;
- для солей кислородсодержащих кислот -ИТ- (меньшая валентность элемента), АТ- (бОльшая валентность элемента).
Задание 2.27. Составьте названия вышеприведённых солей серусодержащих кислот.
При правильной работе должно получиться:
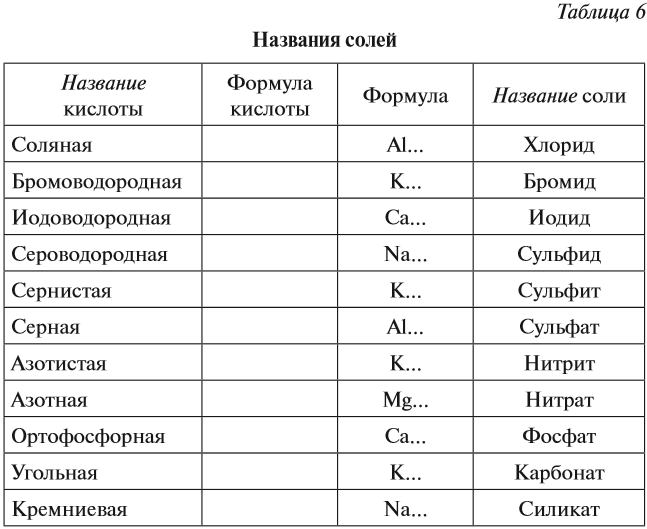
Аналогично составляют названия остальных солей (табл. 6).
Задание 2.28. Дополните таблицу 6, составив химические формулы солей тех металлов, которые указаны в таблице.
При составлении названий кислых солей используют частицу «гидро»:
При составлении названий основных солей используют частицу «гидроксо»:
Задание 2.29. Назовите все соли, которые встречаются в тексте и уравнениях реакций этого раздела.
Задание 2.30. Составьте по 3–4 уравнения реакций получения:
Выводы
Соли состоят из остатков веществ, которые проявляют противоположные свойства: кислоты и основания.