1. Элемент 13-й группы периодической таблицы химических элементов, третьего периода, с атомным номером 13:
а) алюминий +
б) цинк
в) медь
2. В атоме алюминия число свободных 3d-орбиталей равно:
а) 0
б) 5 +
в) 4
3. Верны ли утверждения о гидроксиде алюминия:
1. гидроксид алюминия проявляет только кислотные свойства
2. гидроксид алюминия проявляет только основные свойства
а) только 1
б) только 2
в) оба верны
г) оба не верны +
4. Реакции концентрированной серной кислоты с алюминием при (о.у.) соответствует уравнение:
а) не взаимодействуют +
б) 2Al + 6H2SO4 = Al2(SO4)3 + 3SO2 + 6H2O
в) 2Al + 3H2SO4 = Al2(SO4)3 + 3H2
5. При нагревании гидроксида алюминия образуется:
а) H2
б) Al
в) Al2O3 +
6. При нагревании гидроксида алюминия образуется:
а) H2
б) H2O +
в) Al
7. Веществами Х и Y в схеме химической реакции Al2S3 + H2O → X + Y являются:
а) Al(HS)3 и H2S
б) Al2O3 и Al(HS)3
в) Al(OH)3 и H2S +
8. Сумма протонов, нейтронов и электронов в атоме 27Al равна:
а) 40 +
б) 27
в) 72
9. В ряду Al → Si → P → S:
а) увеличивается число энергетических уровней в атомах
б) уменьшается высшая степень окисления элементов
в) уменьшается радиус атома +
10. Алюминий реагирует с:
а) концентрированная азотная кислот
б) соляная кислота +
в) кислород
11. Алюминий реагирует с:
а) гидроксид натрия +
б) нашатырь
в) хлорид натрия
12. Водород может выделиться при протекании реакции:
а) Fe + CuSO4 =
б) Al + NaOH + H2O = +
в) Ag + HCl =
13. Алюминий относится к такой группе металлов:
а) лёгких +
б) тяжелых
в) черных
14. Наиболее распространённый металл и по распространённости такой по счету химический элемент в земной коре:
а) второй
б) первый
в) третий +
15. Впервые алюминий был получен датским физиком:
а) Эрстедом +
б) Орстедом
в) Эрстедтом
16. До развития промышленного электролитического способа получения алюминия этот металл:
а) был дороже платины
б) был дороже золота +
в) не был востребован
17. Al2O3 • H2O, название:
а) нефелины
б) алуниты
в) бокситы +
18. В природных водах алюминий содержится в виде таких химических соединений:
а) токсичных
б) малотоксичных +
в) среднетоксичных
19. Алюминий образует прочную химическую связь с:
а) магнием
б) водородом
в) кислородом +
20. Плотность алюминия:
а) 3712 кг/м³
б) 2712 кг/м³ +
в) 1712 кг/м³
21. Температура плавления у технического алюминия:
а) 658 °C +
б) 858 °C
в) 568 °C
22. Температура плавления у алюминия высокой чистоты:
а) 860 °C
б) 660 °C +
в) 560 °C
23. При нормальных условиях алюминий покрыт тонкой и прочной … плёнкой:
а) кислотной
б) щелочной
в) оксидной +
24. До конца этого века алюминий в промышленных масштабах не производился:
а) 18
б) 19 +
в) 17
25. В этом году Сент-Клер Девиль получил алюминий электролизом расплава хлорида натрия-алюминия:
а) 1858
б) 1857
в) 1856 +
26. Электропроводность алюминия всего в 1,7 раза меньше, чем у:
а) железа
б) меди +
в) цинка
27. Благодаря комплексу свойств широко распространён в таком оборудовании:
а) тепловом +
б) охладительном
в) нет верного ответа
28. Сульфид алюминия используется для производства:
а) углеводорода
б) серы
в) сероводорода +
29. Алюминий – очень сильный:
а) раскислитель +
б) растворитель
в) восстановитель
30. В стекловарении используются:
а) гидроксид алюминия
б) оксид алюминия +
в) нитрат алюминия
Уравнения реакций алюминия с веществами. Алюминотермия
Решение задач на составление уравнений химических реакций
Задание 362
Составьте электронные и молекулярные уравнения реакций: а) алюминия с раствором щелочи; б) бора с концентрированной азотной кислотой.
Решение:
а) С растворами щелочей алюминий реагирует энергично, поскольку они растворяют оксидную плёнку:
б) Бор с концентрированной азотной кислотой реагирует с образованием ортоборной кислоты Н3ВО3 и NO2:
Задание 363
Какой процесс называют алюминотермией? Составьте электронные и молекулярные уравнения реакции, на которой основано применение термита (смесь А1 и Ее3О4).
Решение:
Алюминотермия – это процесс выделения металлов из их оксидов при действии на них алюминия. Этот процесс возможен благодаря большому значению (Al2O3) = -1583,3 кДж/моль. Этот весьма общий метод получения металлов был предложен Н. Н. Бекетовым в 1859 г. Алюминотермия используется для получения термита.
8Al 0 + 3Fe3O4 = 8Al 3+ + 9Fe 0 + 12O 2-
Задание 364
Составьте уравнения реакций, которые нужно провести для осуществления следующих превращений:
В → Н3ВО3 → Na2B4O7 → Н3ВО3.
Уравнение окислительно-восстановительной реакции составьте на основании электронных уравнений.
Решение:
а) Бор растворяется в концентрированной серной кислоте с образованием ортоборной кислоты и оксида серы (IV):
2B 0 + 3S 6+ = 2B 3+ + 3S 4+
б) При нейтрализации Н3ВО3 образуются не ортобораты, содержащие ион ВО3 3- , а получаются тетрабораты, содержащие ион B4O7 2- :
в) Тетрабораты гидролизуются с образованием ортоборной кислоты и метабората:
Тест на химию щелочных и щелочноземельных металлов, магния и алюминия.
Из предложенного списка элементов выберите те, которые имеют 1 неспаренный электрон на внешнем уровне в основном состоянии. Число верных ответов может быть любым.
Ответ: 245
Из предложенного списка элементов выберите те, которые не имеют неспаренных электронов на внешнем уровне в основном состоянии. Число верных ответов может быть любым.
Ответ: 14
Из предложенного списка элементов выберите те, которые имеют электроны на d-подуровнях. Число верных ответов может быть любым.
Ответ: 35
Из предложенного списка элементов выберите те, которые имеют валентные электроны на p-подуровне. Число верных ответов может быть любым.
Ответ: 34
Из предложенного списка металлов выберите те, которые реагируют с водой при любых условиях. Число верных ответов может быть любым.
Ответ: 145
Из предложенного списка металлов выберите те, которые реагируют с водой только при нагревании. Число верных ответов может быть любым.
Ответ: 3
Из предложенного списка металлов выберите те, которые не реагируют с водой при любых условиях. Число верных ответов может быть любым.
Ответ: 2
Из предложенного списка металлов выберите те, которые реагируют с водой при обычных условиях. Число верных ответов может быть любым.
Ответ: 125
Из предложенного списка металлов выберите те, которые не реагируют со щелочами. Число верных ответов может быть любым.
Ответ: 235
Из предложенного списка металлов выберите те, которые реагируют со щелочами. Число верных ответов может быть любым.
Ответ: 34
Из предложенного списка металлов выберите те, которые реагируют с кислородом с образованием оксидов. Число верных ответов может быть любым.
Ответ: 245
Из предложенного списка металлов выберите те, которые реагируют с кислородом с образованием продуктов, в которых степень окисления атомов неметалла отличается от -2. Число верных ответов может быть любым.
Ответ: 35
Из предложенного списка элементов выберите те, которые образуют соединения со степенью окисления +1. Число верных ответов может быть любым.
Ответ: 14
Из предложенного списка элементов выберите те, которые образуют соединения со степенью окисления +2. Число верных ответов может быть любым.
Ответ: 13
Из предложенного списка соединений выберите те, которые обладают выраженными окислительными свойствами. Число верных ответов может быть любым.
- 1. Li2O
- 2. Al2O3
- 3. Na2O2
- 4. MgO
- 5. CaO
Ответ: 3
Из предложенного списка соединений выберите те, которые относятся к оксидам. Число верных ответов может быть любым.
- 1. BaO2
- 2. CO2
- 3. K2O2
- 4. NO
- 5. BeO
Ответ: 245
Из предложенного списка соединений выберите те, которые относятся к пероксидам. Число верных ответов может быть любым.
- 1. CO
- 2. MgO
- 3. H2O2
- 4. BaO
- 5. Na2O2
Ответ: 35
Из предложенного списка соединений выберите те, которые не относятся к оксидам. Число верных ответов может быть любым.
- 1. SO2
- 2. BaO2
- 3. NO2
- 4. Al2O3
- 5. K2O2
Ответ: 25
Из предложенного списка оксидов выберите те, которые проявляют амфотерные свойства. Число верных ответов может быть любым.
4) оксид бериллия
5) оксид алюминия
Ответ: 45
Из предложенного списка веществ выберите те, которые не проявляют амфотерные свойства. Число верных ответов может быть любым.
1) гидроксид натрия
2) гидроксид бериллия
4) оксид стронция
5) оксид алюминия
Ответ: 14
Из приведенного списка веществ выберите те, которые реагируют с водой. Число верных ответов может быть любым.
2) оксид алюминия
3) пероксид натрия
4) оксид бериллия
Ответ: 135
Из приведенного списка веществ выберите те, которые не реагируют с водой. Число верных ответов может быть любым.
2) негашеная известь
3) оксид алюминия
4) оксид кремния
Ответ: 134
Из приведенного списка веществ выберите те, которые в водном растворе дают нейтральную среду. Число верных ответов может быть любым.
1) поваренная соль
3) бертолетова соль
5) гашеная известь
Ответ: 13
Из приведенного списка веществ выберите те, которые в водном растворе дают щелочную среду. Число верных ответов может быть любым.
1) кальцинированная сода
2) гашеная известь
3) питьевая сода
4) поваренная соль
5) перхлорат калия
Ответ: 123
Из приведенного списка веществ выберите те, которые в водном растворе дают кислую среду. Число верных ответов может быть любым.
1) сульфат кальция
2) нитрат натрия
3) сульфат алюминия
5) бромид бериллия
Ответ: 35
Из приведенного списка веществ выберите те, которые реагируют с углекислым газом. Число верных ответов может быть любым.
1) оксид алюминия
2) оксид кальция
3) гидроксид алюминия
4) гидроксид стронция
Ответ: 245
Из приведенного списка веществ выберите те, которые реагируют с оксидом кремния при нагревании. Число верных ответов может быть любым.
2) негашеная известь
3) сульфат натрия
4) поваренная соль
Ответ: 125
Из приведенного списка веществ выберите те, которые реагируют с азотом. Число верных ответов может быть любым.
4) пероксид натрия
Ответ: 235
Из приведенного списка веществ выберите те, которые реагируют с сернистым газом. Число верных ответов может быть любым.
1) негашеная известь
2) тетрагидроксоалюминат натрия
4) хлорид кальция
Ответ: 125
Из приведенного списка веществ выберите те, которые реагируют с поташом при сплавлении. Число верных ответов может быть любым.
2) оксид алюминия
4) оксид кремния
5) оксид бериллия
Ответ: 245
Из приведенных пар соединений выберите те, между которыми возможно химическое взаимодействие. В ответ запишите уравнение реакции.
1) магний + калий
2) магний + аргон
3) магний + железо
4) магний + песок
5) магний + негашеная известь
Ответ:
2Mg + SiO2 = 2MgO +Si
или
4Mg + SiO2 = Mg2Si + 2MgO
Из приведенных пар соединений выберите те, между которыми возможно химическое взаимодействие. В ответ запишите уравнение реакции.
1) алюминий + оксид бериллия
2) алюминий + гидроксид цинка
3) алюминий + поваренная соль
4) алюминий + сульфат натрия
5) алюминий + хлорид меди (II)
Ответ: 2Al + 3CuCl2 = 2AlCl3 + 3Cu
Из приведенных пар соединений выберите те, между которыми возможно химическое взаимодействие.
1) гидроксид бериллия + азот
2) гидроксид бериллия + сера
3) гидроксид бериллия + едкий натр
4) гидроксид бериллия + кремниевая кислота
5) гидроксид бериллия + кислород
Из приведенных пар соединений выберите те, между которыми возможно химическое взаимодействие.
1) пероксид натрия + кислород
2) пероксид натрия + азот
3) пероксид натрия + водород
4) пероксид натрия + натрий
5) пероксид натрия + серебро
Из приведенных пар соединений выберите те, между которыми возможно химическое взаимодействие.
1) хлорид лития + сульфат цинка
2) хлорид лития + нитрат аммония
3) хлорид лития + бромид серебра
4) хлорид лития + сульфид свинца
5) хлорид лития + фторид натрия
Ответ: LiCl + NaF = LiF + NaCl
В заданной схеме превращений
Na X
Y
Веществами X и Y являются соответственно
2) пероксид натрия
3) гидрид натрия
4) гидроксид натрия
Ответ: 24
В заданной схеме превращений
SiO2 X
MgCl2
Веществами X и Y являются соответственно
1) силикат магния
3) карбид магния
5) соляная кислота
Первым укажите X, вторым Y
Ответ: 25
В заданной схеме превращений
Na2CO3 Y
Na[Al(OH)4]
Веществами X и Y являются соответственно
1) оксид алюминия
2) хлорид алюминия
3) фторид алюминия
4) алюминат натрия
5) карбонат алюминия
Первым укажите X, вторым Y
Ответ: 14
В заданной схеме превращений
X Y
NaHCO3
Веществами X и Y являются соответственно
1) поваренная соль
2) тетрагидроксоалюминат натрия
3) бромид натрия
Первым укажите X, вторым Y
Ответ: 42
В заданной схеме превращений
X Na2CO3
Na2BeO2
Веществами X и Y являются соответственно
1) оксид бериллия
3) гидроксид натрия
4) хлорид бериллия
Первым укажите X, вторым Y
Ответ: 31
Запишите уравнение реакции горения лития в кислороде.
Ответ: 4Li + O2 = 2Li2O
Запишите уравнение реакции горения натрия в кислороде.
Запишите уравнение реакции горения магния в кислороде.
Ответ: 2Mg + O2 = 2MgO
Запишите уравнение реакции горения кальция в кислороде.
Ответ: 2Ca + O2 = 2CaO
Запишите уравнение реакции горения алюминия.
Запишите уравнение реакции, протекающей при взаимодействии калия с азотом при нагревании.
Ответ: 6K + N2 = 2K3N
Запишите уравнение реакции алюминия с серой.
Ответ: 2Al + 3S = Al2S3
Запишите уравнение реакции кальция с фосфором при нагревании.
Ответ: 3Ca + 2P = Ca3P2
Запишите уравнение реакции оксида лития с водой.
Ответ: Li2O + H2O = 2LiOH
Запишите уравнение реакции негашеной извести с водой.
Ответ: CaO + H2O = Ca(OH)2
Запишите уравнение реакции горячего раствора едкого натра с хлором.
Ответ: 6NaOH + 3Cl2 = NaClO3 + 5NaCl + 3H2O
Запишите уравнение реакции порошка серы с концентрированным раствором гидроксида калия.
Запишите уравнение реакции порошка кремния с раствором гидроксида цезия.
Запишите уравнение реакции восстановления песка порошком магния.
Ответ:
2Mg + SiO2 = 2MgO + Si
или
4Mg + SiO2 = Mg2Si + 2MgO
Запишите уравнение реакции раскаленного магния с углекислым газом.
Ответ: 2Mg + CO2 = 2MgO + C
Запишите уравнение реакции порошка алюминия с раствором гидроксида калия.
Ответ: 2Al + 2KOH + 6H2O = 2K[Al(OH)4] + 3H2
Запишите уравнение реакции оксида бериллия с раствором бромоводородной кислоты.
Ответ: BeO + 2HBr = BeBr2 + H2O
Запишите уравнение реакции алюминиевой стружки с разбавленной серной кислотой.
Запишите уравнение реакции, протекающей между магниевым порошком и концентрированной серной кислотой при нагревании.
Запишите уравнение реакции кальция с очень разбавленной азотной кислотой.
Магний растворили в очень разбавленной азотной кислоте. В процессе протекания реакции газ не выделялся. Запишите уравнение проведенной реакции.
Запишите уравнение реакции, протекающей при взаимодействии пероксида натрия с углекислым газом.
Запишите уравнение реакции пероксида натрия с холодным разбавленным раствором серной кислоты.
Запишите уравнение реакции пероксида калия с горячим раствором серной кислоты.
Запишите уравнение реакции, протекающей при сплавлении оксида хрома (III) с пероксидом натрия.
Запишите уравнение реакции пероксида натрия с концентрированной соляной кислотой.
Запишите уравнение реакции, протекающей при сплавлении поташа с оксидом алюминия.
Запишите уравнение реакции, протекающей при сплавлении мела с оксидом алюминия.
Запишите уравнение реакции алюмината калия с водой.
Запишите уравнение реакции, протекающей при взаимодействии раствора тетрагидроксоалюмината натрия с избытком углекислого газа.
Запишите уравнение реакции тетрагидроксоалюмината калия с избытком сернистого газа.
Запишите уравнение реакции тетрагидроксоалюмината цезия с избытком сероводорода.
Запишите уравнение реакции прокаливания тетрагидроксоалюмината натрия.
Запишите уравнение реакции железной окалины с порошком алюминия.
Запишите уравнение реакции алюминия со раствором, содержащим нитрат и гидроксид калия.
Ответ: 8Al + 3KNO3 + 5KOH + 18H2O = 8K[Al(OH)4] + 3NH3
Запишите уравнение реакции лития с водой.
Ответ: 2Li + 2H2O = 2LiOH + H2
Запишите уравнение реакции бария с водой.
Запишите уравнение реакции хлорида алюминия с раствором карбоната калия.
Запишите уравнение реакции оксида алюминия с раствором едкого кали.
Запишите уравнение реакции оксида алюминия с расплавом гидроксида калия.
Установите соответствие между веществом и набором реагентов, с каждым из которых оно может взаимодействовать.
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||||||||||||||||
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||||||||||||||
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||||||||||||
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||||||||||
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||||||||
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||||||
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||||
| ВЕЩЕСТВО | РЕАГЕНТЫ | ||
| ВЕЩЕСТВО | РЕАГЕНТЫ |
| ВЕЩЕСТВО | РЕАГЕНТЫ |


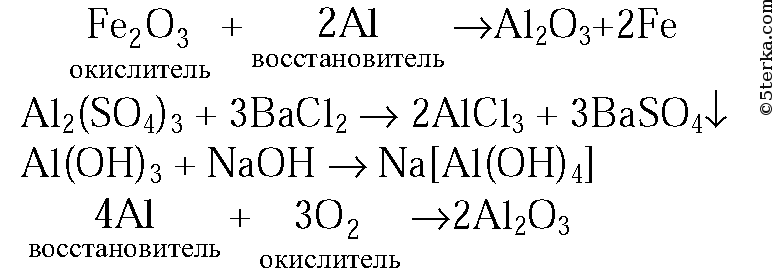
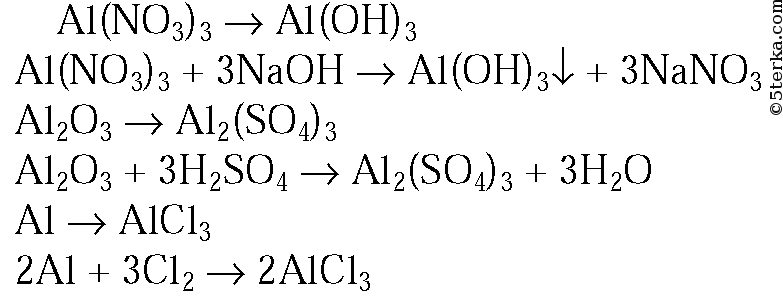
 Решебник по химии за 9 класс (А.М.Радецкий, 2011 год),
Решебник по химии за 9 класс (А.М.Радецкий, 2011 год),