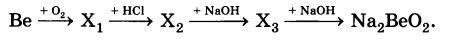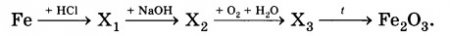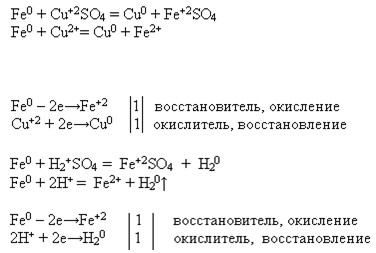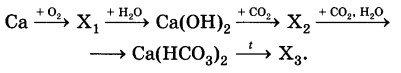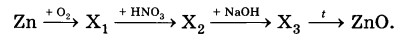- Основные разделы
- Контрольные работы
- Ответы на контрольную работу по теме «Металлы»(Габриелян)
- Составьте уравнения реакций по схеме назовите вещество х1 первую реакцию рассмотрите с точки овр
- Составьте молекулярные уравнения реакций, идущих по схеме NO → N02 → HN03 → NaN03. Уравнение 1 рассмотрите с точки зрения теории
- Ваш ответ
- решение вопроса
- Похожие вопросы
Основные разделы
Контрольные работы
Ответы на контрольную работу по теме «Металлы»(Габриелян)
- Post category:Контрольные работы по химии 9 класс
- Reading time: 12 минут чтения
ЗАДАНИЕ 1
Напишите уравнения возможных реакций взаимодействия натрия и цинка с веществами: хлором, водой, соляной кислотой.
Рассмотрите одну из записанных реакций в свете ОВР.
2Nа + 2Н2О = 2NаОН + Н2
2Nа + 2НСl = 2NаСl + Н2
2Nа + Cl2 = 2NаСl
Zn + Cl2 = ZnCl2
Zn0 -2e→Zn2+ окисляется, восстановитель
Cl20+2e→2Cl- восстанавливается, окислитель
Zn + H2O = ZnO + H2.
Zn + 2HCl = ZnCl2 + H2
ЗАДАНИЕ 2
Напишите уравнения реакций, с помощью которых можно осуществить превращения по схеме
Fe →FeCl2 →Fe(N03)2 →Fe(OH)2 →FeO.
Превращение 3 рассмотрите в свете ТЭД.
Fe + 2HCl = FeCl2 + H2
FeCl2 + 2AgNO3 = 2AgCl + Fe(NO3)2
Fe(NO3)2 + 2NaOH = Fe(OH)2 + 2NaNO3
Fе2++ 2NO3-+ 2Na++2OH- =2Na++2NO3-+ Fе(ОН)2
Fе2++ 2OH- = Fе(ОН)2
Fе(ОН)2= FеО+ Н2О
ЗАДАНИЕ 3
При взаимодействии 12 г магния с избытком соляной кислоты выделилось 10 л водорода (н. у.). Вычислите объемную долю выхода продукта реакции.
Mg + 2HCl = MgCl2 + H2
n (Mg) = 12/24 = 0,5 моль
V (H2) = 10/22,4 = 0,446 моль
n (Mg) = n (H2) по уравнению (теор.)
выход = 0,446 /0,5 = 0,89 = 89 %
ЗАДАНИЕ 1
Напишите уравнения возможных реакций лития и меди с веществами: хлором, водой, соляной кислотой.
Рассмотрите одну из записанных реакций в свете ОВР.
2Li + Cl2 = 2LiCl
2Li + 2H2O = 2LiOH + H2
2Li + 2HCl = 2LiCl + H2
Cu + Cl2 = CuCl2
Cu + H2O = не реагирует
Cu + HCl = не реагирует
2Li+CL2= 2LiCL
Li- e—> Li+ восстановитель
CL2+2e—-> 2CL- окислитель
ЗАДАНИЕ 2
Напишите уравнения реакций, с помощью которых можно осуществить превращения по схеме
Са →CaO →Са(ОН)2 →Ca(N03)2 → Са3(Р04)2.
Превращение 3 рассмотрите в свете ТЭД.
2Ca+O2=2CaO
CaO+2NaOH=Ca(OH)2+Na2O
2HNO3 + Ca(OH)2 =Ca(NO3)2 + 2H2O
2H+ +2NO3- + Ca(OH)2 =Ca2+ +2NO3- + 2H2O
2H+ + Ca(OH)2 =Ca2+ +2H2O
3Ca(NO3)2 + 2Н3PO4 = Ca3(PO4)2 + 6HNO3
ЗАДАНИЕ 3
При термическом разложении 10 г известняка было получено 1,68 л углекислого газа (н. у.). Вычислите объемную долю выхода продукта реакции.
CaCO3 = CaO+CO2
n (CaCO3) = 10/100 = 0,1 моль
V (CO2) = 1,68/22,4 = 0,075 моль
n (CaCO3) = n (CO2) по уравнению (теор.)
выход = 0,075/0,1 = 0,75 = 75 %
ЗАДАНИЕ 1
Напишите уравнения возможных реакций кальция и железа с веществами: хлором, водой, соляной кислотой.
Рассмотрите одну из записанных реакций в свете ОВР.
Са + Cl2 = CaCl2
Ca + 2HCl = CaCl2 + H2
Ca + 2H2O = Ca(OH)2 + H2
2Fe + 3Cl2 = 2FeCl3
Fe + 2HCl = FeCl2 + H2
ЗАДАНИЕ 2
Напишите уравнения реакций, с помощью которых можно осуществить превращения по схеме:
Аl →Аl203 →АlСl3 →Аl(ОН)3 →Al(N03)3.
Превращение 3 рассмотрите в свете ТЭД.
4Al + 3O2 = 2 Al2O3
Al2O3 + 6HCl = 2AlCl3 + 3H2O
AlCl3 + 3NH3 + 3H2O = Al(OH)3 + 3NH4Cl
Al3+ +3Cl- + 3NH3 + 3H2O = Al(OH)3 + 3NH4+ +Cl-
Al3+ + 3NH3 + 3H2O = Al(OH)3 + 3NH4+
Аl(ОН)3+3НNО3=Аl(NО3)3+3Н2О.
ЗАДАНИЕ 3
При взаимодействии 23 г натрия с водой было получено 8,96 л водорода (н. у.). Найдите объемную долю выхода продукта реакции (в %).
2Na + 2H2O = 2NaOH + H2 ↑
n (Na) = 23/23= 1 моль
V (H2) = 8,96/22,4 = 0,4 моль
n (Na) : n (H2) = 2:1
n (H2) = 1/ 2 = 0,5 моль по уравнению (теор.)
выход = 0,4/0,5 = 0,8 = 80 %
ЗАДАНИЕ 1
Напишите уравнения возможных реакций металлов калия и магния с хлором, водой, соляной кислотой.
Рассмотрите одну из этих реакций в свете ОВР.
2K + 2H2O = 2KOH + H2.
2К + CI2 = 2КCI
2К + 2HCI = 2КCI + H2
Mg + 2HCl = MgCl2 + H2
Mg + Cl2 = MgCl2
Mg 0 -2e→ Mg 2+ окисляется, восстановитель
Cl20+2e→2Cl- восстанавливается, окислитель
Mg+2H2O=Mg(OH)2+H2
ЗАДАНИЕ 2
Напишите уравнения реакций для данных переходов:
Li →Li20 →LiOH →Li2S04.
Превращение 3 рассмотрите в свете ТЭД.
4Li + O2 = 2Li2O
Li2O + H2O = 2LiOH
2LiOH + Н2SO4 = Li2SO4 + 2Н2О
2Li+ +2OH- + 2Н+ +SO42- = 2Li+ +SO42- + 2Н2О
2OH- + 2Н+ — = 2Н2О
ЗАДАНИЕ 3
При взаимодействии 60 г кальция с водой выделилось 30 л водорода (н. у.). Найдите объемную долю выхода продукта реакции.
Са + 2Н2О = Са(ОН)2 + Н2
n (Са) = 60/40= 1,5 моль
V (H2) = 30/22,4 = 1,34 моль
n (Са) = n (H2) = по уравнению (теор.)
выход = 1,34/1,5 = 0,89 = 89 %
ЗАДАНИЕ 1
Напишите уравнения возможных реакций магния и алюминия с веществами: кислородом, бромом, разбавленной серной кислотой.
Рассмотрите две из этих реакций в свете ОВР, а одну — в свете ТЭД.
2 Мg + O2 = 2 МgО
Мg 0 -2e→ Мg 2+ окисляется, восстановитель
О20+4e→2 О 2- восстанавливается, окислитель
Мg + Br 2 = Мg Br2
Мg 0 -2e→ Мg 2+ окисляется, восстановитель
Br 20+2e→2 Br — восстанавливается, окислитель
Мg + Н2SO4 = МgSО4 + Н2
Мg + 2Н+ = Мg2+ + Н2
4Al + 3O2 = 2Al2O3,
2Al + 3H2SO4 = Al2(SO4)3 + 3H2
2Al + 3Br2 = 2AlBr3
ЗАДАНИЕ 2
Определите формулы веществ Х1 и Х2 в цепочке превращений:
Са →Х1 →Са(ОН)2 →Х2 →Са(НС03)2.
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
2Ca+O2=2CaO
CaO+H2O=Ca(OH)2
Ca(OH)2 + CO2 = CaCO3 ↓ + H2O
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
ЗАДАНИЕ 3
При взаимодействии 12 г магния с избытком соляной кислоты выделилось 10 л водорода (н. у.). Вычислите объемную долю выхода продукта реакции (в %).
Mg + 2НСl = MgCl2 + Н2
n (Mg) = 12/24= 0,5 моль
n (H2) = n (Mg) по уравнению (теор.)
n (H2) = 10/22,4 = 0,44 моль (пр.)
ŋ = V (H2) (пр.)/ V (H2) (теор.) = n (H2) (пр.)/ n (H2) (теор.) = 0,44/0,5 = 0,89 = 89%
ЗАДАНИЕ 1
Напишите уравнения возможных реакций меди и магния с веществами: кислородом, иодом, разбавленной серной кислотой.
Рассмотрите две из этих реакций в свете ОВР, а одну — в свете ТЭД.
2Cu + O2 = 2CuO
2Cu + I2 = 2CuI
Cu + H2SO4 = не идет
2 Мg + O2 = 2 МgО
Мg 0 -2e→ Мg 2+ окисляется, восстановитель
О20+4e→2 О 2- восстанавливается, окислитель
Мg + Н2SO4 = МgSО4 + Н2
Мg + 2Н+ = Мg2+ + Н2
Мg + I 2 = Мg I 2
Мg 0 -2e→ Мg 2+ окисляется, восстановитель
I 20+2e→2 I — восстанавливается, окислитель
ЗАДАНИЕ 2
Определите формулы веществ X1 и Х2 в цепочке превращений:
Zn →Х1→ ZnS04 →Х2 →ZnO.
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
2Zn + O2 = 2ZnO
ZnO+H2SO4 —>ZnSO4 + H2O
ZnSO4 + 2NaOH (разб.) = Zn(OH)2↓ + Na2SO4
Zn(OH)2= ZnO + H2O
ЗАДАНИЕ 3
При термическом разложении 10 г карбоната кальция было получено 1,68 л углекислого газа (н. у.). Вычислите объемную долю выхода продукта реакции.
CaCO3 → CaO + CO2
n (CaCO3) = 10/100= 0,1 моль
n (CO2) = n (CaCO3) по уравнению (теор.)
n (CO2) = 1,68/22,4 = 0,075 моль (пр.)
ŋ = V (CO2) (пр.)/ V (CO2) (теор.) = n (CO2) (пр.)/ n (CO2) (теор.) = 0,075/0,1 = 0,75 = 75%
ЗАДАНИЕ 1
Напишите уравнения возможных реакций железа и цинка с веществами: кислородом, хлором, разбавленной серной кислотой.
Рассмотрите две из этих реакций в свете ОВР, а одну — в свете ТЭД.
3Fe + 2O2 = Fe2O3 • FeO
Fe + Н2SO4 = FeSO4 + Н2
2Fe + 3Cl2 = 2FeCl3
2Zn + O2 = 2ZnO
Zn 0 -2e→ Zn 2+ окисляется, восстановитель
О20+4e→2 О 2- восстанавливается, окислитель
Zn + Cl2 = ZnCl2
Zn0 -2e→Zn2+ окисляется, восстановитель
Cl20+2e→2Cl- восстанавливается, окислитель
Zn + H2SO4 = ZnSO4 + H2
Zn + 2Н+ = Zn 2+ + Н2
ЗАДАНИЕ 2
Определите формулы веществ Х1 и Х2 в цепочке превращений:
Fe →Х1 →Fe(OH)2 →Х2 →Fe.
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
Fe — 1 —> FeCl2 — 2 —> Fe (OH)2 — 3 —> FeO -4-> Fe
1. Fe + 2HCl —> FeCl2 + H2
2. FeCl2 + 2NaOH —> Fe(OH)2 + 2NaCl
Fe2+ + 2OH- —> Fe (OH)2
3. Fe (OH)2 — t —> FeO + H2O
4. FeO + C = Fe + CO
ЗАДАНИЕ 3
При взаимодействии 23 г натрия с водой было получено 8,96 л водорода (н. у.). Найдите объемную долю выхода продукта реакции.
2Na + 2H2O = 2NaOH + H2 ↑
n (Na) = 23/23= 1 моль
2n (H2) = n (Na) по уравнению (теор.)
n (H2) = 0,5 моль теор.
n (H2) = 8,96/22,4 = 0,4 моль (пр.)
ŋ = V (H2) (пр.)/ V (H2) (теор.) = n (H2) (пр.)/ n (H2) (теор.) = 0,4/0,5 = 0,8 = 80%
ЗАДАНИЕ 1
Напишите уравнения возможных химических реакций бериллия и железа с веществами: кислородом, бромом, разбавленной серной кислотой.
Рассмотрите две из этих реакций в свете ОВР, а одну — в свете ТЭД.
3Fe + 2O2 = Fe2O3 • FeO
Fe + Н2SO4 = FeSO4 + Н2
2Fe + 3Br 2 = 2Fe Br3
2 Ве + O2 = 2 ВеО
Ве0 -2e→ Ве 2+ окисляется, восстановитель
О20+4e→2 О 2- восстанавливается, окислитель
Ве + Br 2 = Ве Br2
Ве 0 -2e→ Ве 2+ окисляется, восстановитель
Br 20+2e→2 Br — восстанавливается, окислитель
Ве + Н2SO4 = Ве SО4 + Н2
Ве + 2Н+ = Ве 2+ + Н2
ЗАДАНИЕ 2
Определите формулы веществ Х1 и Х2 в цепочке превращений:
Fe → Х1 →Fe(OH)3 →Х2 →Fe.
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
Fe 1→FeCl3 2→Fe(OH)3 3→Fe2O3 4→ Fe
1. 2Fe + 3Cl2 t →2FeCl3
2. FeCl3+ 3NaOH → Fe(OH)3 ↓ + 3NaCl
3. 2Fe(OH)3 t → Fe2O3 + H2O
4. 2Fe2O3 + 3C t → 4 Fe + 3CO2
ЗАДАНИЕ 3
При взаимодействии 60 г кальция с водой выделилось 30 л водорода (н. у.). Найдите объемную долю выхода продукта реакции (в %).
Ca + 2H2О = Ca(OH)2 + Н2
n (Ca) = 60/40= 1,5 моль
n (H2) = n (Ca) по уравнению (теор.)
n (H2) = 30/22,4 = 1,34 моль (пр.)
ŋ = V (H2) (пр.)/ V (H2) (теор.) = n (H2) (пр.)/ n (H2) (теор.) = 1,34/1,5 = 0,89 = 89%
ЗАДАНИЕ 1
Напишите уравнения возможных реакций магния, алюминия и серебра с неметаллом, водой, кислотой, раствором соли.
Реакции металлов с растворами кислоты и соли рассмотрите с точки зрения ОВР и ТЭД.
1. Mg + 2HCl = MgCl2 + H2
Mg + 2H+ = Mg2+ + H2
Mg0 — 2e = Mg2+ восстановитель
2H+ + 2e= H2 окислитель
Mg + Cl2 = MgCl2
Mg+2H2O=Mg(OH)2+H2
Mg + CuCl2 = MgCl2 + Cu
Mg0 + Cu2+ = Mg2+ + Cu0
Mg0 — 2e = Mg2+ восстановитель
Cu2+ + 2e= Cu0 окислитель
2. 2Al + 6HCl = 2AlCl3 + 3H2
2Al + 6H+ = 2Al3+ + 3H02
Al 0 — 3e = Al3+ восстановитель
2H+ + 2e= H2 окислитель
2Al + 3Cl2 = 2AlCl3
2Al + 6H2O = 2Al(OH)3 + 3H2
3HgCI2 + 2Al = 2AICI3 + 3Hg
3Hg2+ + 2Al0 = 2AI3+ + 3Hg0
Hg2+ + 2е = Hg0 восстановитель
Al0 – 3е= AI3+ окислитель
3. Ag + 2HCl = не реагирует
2Ag + S = Ag2S
Ag+ H2O = не реагирует
Ag + FeCl3 = AgCl + FeCl2
Ag0 + Fe3+= Ag++ Fe2+
Ag0 — 1е= Ag+ восстановитель
Fe3++1е= Fe2+окислитель
ЗАДАНИЕ 2
Определите формулы веществ Х1, Х2 и Х3 в цепочке превращений:
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
2Ве + О2 = 2ВеО
ВеО +2HCl = BeCl2 + H2O
BeCl2 + 2NaOH = Be(OH)2 + 2NaCl
Be(OH)2 + 2NaOH= Na2BeO2 + 2H2O
ЗАДАНИЕ 3
При взаимодействии 12 г технического магния, содержащего 5% примесей, с избытком соляной кислоты, выделилось 10 л водорода (н. у.). Вычислите объемную долю выхода продукта реакции.
Mg + 2HCl = MgCl2 + H2
n(Mg) = 12-12*0,05/24 = 11,4 /24= 0,475 моль
n (H2) (теор.) = n(Mg) =0,475 моль
n (H2) = 10/22,4 = 0,44 моль (пр.)
ŋ = V (H2) (пр.)/ V (H2) (теор.) = n (H2) (пр.)/ n (H2) (теор.) = 0,44/0,475 = 0,92 = 92%
ЗАДАНИЕ 1
Напишите уравнения возможных реакций лития, меди, бария, алюминия с веществами: неметаллом, водой, кислотой, раствором соли.
Реакции металлов с растворами кислоты и соли рассмотрите с точки зрения ОВР и ТЭД.
1. 2Li + Сl2 = 2LiСl
2Li + 2H2O = 2LiOH + H2
2Li + 2НСl = 2LiСl + Н2
2Li0 + 2Н+ = 2Li+ + Н02
Li0 – 1e = Li+ восстановитель
2Н+ + 2e= Н02 окислитель
2Li + CuСl 2= 2LiС1 + Cu
2Li0 + Cu2+ = 2Li+ + Cu0
Li0 – 1e = Li+ восстановитель
Cu2+ + 2e= Cu0 окислитель
2. 2Al + 6HCl = 2AlCl3 + 3H2
2Al + 6H+ = 2Al3+ + 3H02
Al 0 — 3e = Al3+ восстановитель
2H+ + 2e= H2 окислитель
2Al + 3Cl2 = 2AlCl3
2Al + 6H2O = 2Al(OH)3 + 3H2
3HgCI2 + 2Al = 2AICI3 + 3Hg
3Hg2+ + 2Al0 = 2AI3+ + 3Hg0
Hg2+ + 2е = Hg0 восстановитель
Al0 – 3е= AI3+ окислитель
3. Ва + 2HCl = ВаCl2 + H2
Ва + 2H+ = Ва 2+ + H2
Ва 0 — 2e = Ва 2+ восстановитель
2H+ + 2e= H2 окислитель
Ва + Cl2 = ВаCl2
Ва +2H2O= Ва(OH)2+H2
Ва + CuCl2 = ВаCl2 + Cu
Ва + Cu2+ = Ва 2+ + Cu0
Ва 0 — 2e = Ва 2+ восстановитель
Cu2+ + 2e= Cu0 окислитель
4. Cu + Cl2 = CuCl2
Cu + H2O = не реагирует
Cu + HCl = не реагирует
Cu + 2FeCl3 = CuCl2 + 2FeCl2.
Cu 0 + Fe3+= Cu2 ++ Fe2+
Cu 0 — 2е= Cu + восстановитель
Fe3++1е= Fe2+окислитель
ЗАДАНИЕ 2
Определите формулы веществ Х1, Х2 и Х3 в цепочке превращений:
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
Fe + 2HСl → FeCl2 + H2↑
FeCl2+ 2NaOH → Fe(OH)2 + 2NaCl
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3↓
2Fe(OH)3 = Fe2O3 + 3H2O
ЗАДАНИЕ 3
При термическом разложении 20 г известняка, содержащего 10% некарбонатных примесей, было получено 3,23 л углекислого газа (н. у.).
Вычислите объемную долю выхода продукта реакции (в %).
CaCO3 = CaO+CO2
n (CaCO3) = 20-20*0,1/100= 18/100=0,18 моль
V (CO2) = 3,23/22,4 = 0,145 моль (практ.)
n (CaCO3) = n (CO2) по уравнению (теор.)= 0,18 моль
выход = 0,145/0,18 = 0,801 = 80,1 %
ЗАДАНИЕ 1
Напишите уравнения возможных реакций кальция, железа и цинка с неметаллом, водой, кислотой, раствором соли.
Реакции металлов с растворами кислоты и соли рассмотрите с точки зрения ОВР и ТЭД.
1. Са + 2HCl = СаCl2 + H2
Са0 + 2H+ = Са 2+ + H2
Са 0 — 2e = Са 2+ восстановитель
2H+ + 2e= H2 окислитель
Са + Cl2 = СаCl2
Са +2H2O= Са(OH)2+H2
Са + CuCl2 = СаCl2 + Cu
Са + Cu2+ = Са 2+ + Cu0
Са 0 — 2e = Са 2+ восстановитель
Cu2+ + 2e= Cu0 окислитель
2.
2Fe + 3Cl2 t →2FeCl3
3. 2Zn + O2 = 2ZnO
Zn + H2O = ZnO + H2
Zn + H2SO4 = ZnSO4 + H2
Zn + 2Н+ = Zn 2+ + Н2
Zn 0 + 2H+ = Zn 2+ + H02
Zn 0 — 2e = Zn 2+ восстановитель
2H+ + 2e= H2 окислитель
Zn + CuSO4 = Cu + ZnSO4
Zn 0 + Cu2+ = Zn 2+ + Cu0
Zn 0 — 2e = Zn 2+ восстановитель
Cu2+ + 2e= Cu0 окислитель
ЗАДАНИЕ 2
Определите формулы веществ Х1, Х2 и Х3 в цепочке превращений:
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
2Ca+O2=2CaO
CaО+H2O=Ca(OH)2
Ca(OH)2+H2CO3=CaCO3+2H2O
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
Ca(HCO3)2 t →CaCO3↓ + CO2 + H2O
ЗАДАНИЕ 3
Прй взаимодействии 24,15 г технического натрия, содержащего 5% примесей, было получено 8,96 л водорода (н. у.).
Вычислите объемную долю выхода продукта реакции (в %).
2Na + 2H2O = 2NaOH + H2
n(Na) = 24,15-24,15*0,05/23 =23 /23= 1 моль
n (H2) (теор.) = 0,5 n(Mg) =0,5 моль
n (H2) = 8,96/22,4 = 0,4 моль (пр.)
ŋ = V (H2) (пр.)/ V (H2) (теор.) = n (H2) (пр.)/ n (H2) (теор.) = 0,4/0,5 = 0,8 = 80%
ЗАДАНИЕ 1
Напишите уравнения возможных реакций бериллия, железа и меди с веществами: неметаллом, водой, кислотой, раствором соли.
Реакции металлов с растворами кислоты и соли рассмотрите с точки зрения ОВР и ТЭД.
1. 2 Ве + O2 = 2 ВеО
Ве + Н2SO4 = ВеSО4 + Н2
Ве + 2Н+ = Ве 2+ + Н2
2. Cu + Cl2 = CuCl2
Cu + H2O = не реагирует
Cu + HCl = не реагирует
Cu + 2FeCl3 = CuCl2 + 2FeCl2.
Cu 0 + Fe3+= Cu2 ++ Fe2+
Cu 0 — 2е= Cu + восстановитель
Fe3++1е= Fe2+окислитель
3. 2Fe + 3Cl2 t →2FeCl3
ЗАДАНИЕ 2
Определите формулы веществ Х1, Х2 и Х3 в цепочке превращений:
Напишите уравнения реакций, с помощью которых можно осуществить превращения по данной схеме.
2Zn + O2 = 2ZnO
ZnO + 2HNO3 = Zn(NO3)2 + H2O
Zn(NO3)2 + 2NaOH = 2NaNO3 + Zn(OH)2
Zn(OH)2= ZnO + H2O
ЗАДАНИЕ 3
При взаимодействии 60 г технического кальция, содержащего 2% примесей, с водой было получено 30 л водорода (н. у.). Вычислите объемную долю выхода продукта реакции.
Ca + 2H2О = Ca(OH)2 + Н2
n(Ca) = 60-60*0,02/40 =58,8 /40= 1,47 моль
n (H2) (теор.) = n(Ca) =1,47 моль
n (H2) = 30/22,4 = 1.34 моль (пр.)
ŋ = V (H2) (пр.)/ V (H2) (теор.) = n (H2) (пр.)/ n (H2) (теор.) = 1,34/1,47 = 0,91 = 91%
Составьте уравнения реакций по схеме назовите вещество х1 первую реакцию рассмотрите с точки овр
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
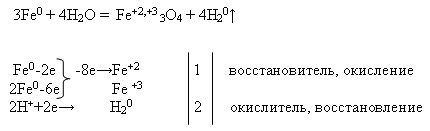
Задание 1 Какие из реакций, уравнения которых записаны ниже, относят к окислительно-восстановительным? Для окислительно-восстановительных реакций укажите окислитель и восстановитель, процессы окисления и восстановления, составьте электронные уравнения.
а) CaCO3 t ⟶ CaO + CO2;
Реакция не относится к окислительно-восстановительным, так как происходит без изменения степени окисления.
б) CO2 + 2Mg t ⟶ 2MgO + C;
Схема окислительно-восстановительной реакции (ОВР).
C +4 O2 + Mg 0 ⟶ Mg +2 O + C 0
Mg 0 -2ē ⟶ Mg +2 |2 |4|2 ― процесс окисления
C +4 +4ē ⟶ C 0 |4 | |1 ― процесс восстановления
Проводим вертикальную черту и пишем за ней число электронов, которые отдали и присоединили атомы магния и углерода. Находим наименьшее общее кратное для чисел 2 и 4. Это число 4, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 2 и 4, записываем результат за третьей чертой в строках, касающихся элементов магния и углерода. Множители 2 и 1 являются искомыми коэффициентами.
В приведённой реакции магний — восстановитель, а оксид углерода (IV) (за счёт атомов углерода в степени окисления +4) — окислитель.
в) Ba(NO3)2 + Na2SO4 ⟶ 2NaNO3 + BaSO4;
Реакция не относится к окислительно-восстановительным, так как происходит без изменения степени окисления.
г) 2Al + Cr2O3 t ⟶ Al2O3 + 2Cr
Схема окислительно-восстановительной реакции (ОВР) .
Al 0 + Cr2 + 3 O3 ⟶ Al2 +3 O3 + Cr 0
2Al 0 -6ē ⟶ 2Al +3 |6 |6|1 ― процесс окисления
Cr +3 +3ē ⟶ Cr 0 |3| |2 ― процесс восстановления
Проводим вертикальную черту и пишем за ней число электронов, которые отдали и присоединили атомы алюминия и хрома. Находим наименьшее общее кратное для чисел 6 и 3. Это число 6, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 6 и 3 , записываем результат за третьей чертой в строках, касающихся элементов алюминия и хрома. Множители 1 и 2 являются искомыми коэффициентами.
В приведённой реакции алюминий — восстановитель, а оксид хрома (III) (за счёт атомов хрома в степени окисления +3) — окислитель.
Задание 2 Дайте характеристику реакции синтеза аммиака по всем изученным вами признакам классификации химических реакций.
3H2 + N2 ⇄ 2NH3 + Q (кат.)
Реакция соединения, экзотермическая, окислительно-восстановительная, каталитическая, обратимая.
Задание 3 Из следующих утверждений выберите истинные:
а) к окислительно-восстановительным будут относиться все реакции ионного обмена;
б) все реакции ионного обмена не будут являться окислительно-восстановительными; Истина
в) все реакции замещения являются окислительно-восстановительными; Истина
г) только некоторые реакции замещения являются окислительно-восстановительными реакциями;
д) к окислительно-восстановительным реакциям относят те реакции соединения и разложения, в которых участвует хотя бы одно простое вещество; Истина
е) все реакции разложения и соединения не являются окислительно-восстановительными.
Обоснуйте свою точку зрения, докажите её примерами уравнений реакций.
б) Истина, т.к. все реакции ионного обмена протекают без изменения степеней окисления, поскольку среди реагентов и продуктов реакции нет простых веществ.
FeCl2 + 2KOH = Fe(OH)2 + 2KCl
Fe +2 Cl2 -1 + K +1 O -2 H +1 ⟶ Fe +2 (O -2 H +1 )2 + K +1 Cl -1
K2CO3 + 2HNO3 = 2KNO3 + H2O + CO2↑
K2 +1 C +4 O3 -2 + H +1 N +5 O3 -2 ⟶ K +1 N +5 O3 -2 + H2 +1 O -2 + C +4 O2 -2 ↑
CaCl3 + Na2CO3 = CaCO3↓ + 2NaCl
Ca +2 Cl3 -1 + Na2 +1 C +4 O3 -2 ⟶ Ca +2 C +4 O3 -2 ↓ + Na +1 Cl -1
в) Истина, т.к. по определению в реакциях замещения атомы простого вещества (степень окисления 0) замещают атомы одного из химических элементов в сложном веществе, т.е. изменяется степень окисления, поэтому все реакции замещения являются окислительно-восстановительными.
Fe + H2SO4 = FeSO4 + H2 ↑
Fe 0 + H2 +1 S +4 O4 -2 ⟶ Fe +2 S +4 O4 -2 + H2 0
Fe + CuSO4 = FeSO4 + Cu
Fe 0 + Cu +2 S +6 O4 -2 ⟶ Fe +2 S +6 O4 -2 + Cu 0
д) Истина. Если в реакции соединения и разложения участвует хотя бы одно простое вещество (степень окисления 0) , то степень окисления изменяется, следовательно, такие реакции относятся к окислительно-восстановительным.
SO2 + O2 = SO3
S +4 O2 -2 + O2 0 ⟶ S +6 O3 -2
2KClO3 = 2KCl + O2 (кат.MnO2)
K +1 Cl +5 O3 -2 ⟶ K +1 Cl -1 + O2 0
Задание 4 Согласны ли вы с утверждением, что HNO3 проявляет только окислительные свойства, а NH3 – только восстановительные? Согласны.
Ответ обоснуйте.
Азотная кислота HNO3 проявляет только окислительные свойства за счет атома азота в максимальной степени окисления (+5), которую может только понизить.
Аммиак NH3 проявляет только восстановительные свойства за счет атома азота в минимальной степени окисления (-3), которую может только повысить.
Задание 5 Какое из веществ ― сероводород H2S и серная кислота H2SO4 ― проявляет только окислительные или только восстановительные свойства?
Серная кислота H2SO4 за счет атома серы проявляет только окислительные свойства, а с ероводород H2S ― только восстановительные свойства.
Почему?
Сероводород H2S только восстановительные свойства проявляет за счет атома серы в минимальной степени окисления (-2), которую может только повысить.
Серная кислота H2SO4 только окислительные свойства проявляет за счет атомов серы в максимальной степени окисления (+6), которую может только понизить.
Задание 6 Обоснуйте тезис, что SO2 может быть и окислителем, и восстановителем.
В оксиде серы (IV) SO2 сера находится в промежуточной степени окисления +4, которую может понизить, реагируя с восстановителями, до -2, или повысить, реагируя с окислителями, до +6, поэтому SO2 может быть и окислителем, и восстановителем.
Задание 7 Расставьте коэффициенты методом электронного баланса в следующих схемах реакций:
а) NH3 + O2 ⟶ NO + H2O;
4NH3 + 5O2 ⟶ 4NO + 6H2O
Схема окислительно-восстановительной реакции.
N -3 H3 + O2 0 ⟶ N +2 O -2 + H2O -2
N -3 -5ē ⟶ N +2 |5|20|4 ― процесс окисления
O2 0 +4ē ⟶ 2O -2 |4| |5 ― процесс восстановления
Проводим вертикальную черту и пишем за ней число электронов, которые отдали и присоединили атомы азота и кислорода. Находим наименьшее общее кратное для чисел 5 и 4. Это число 20, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 5 и 4, записываем результат за третьей чертой в строках, касающихся элементов азота и кислорода. Множители 4 и 5 являются искомыми коэффициентами. Поскольку элемент азот изменил степень окисления полностью (в правой части схемы этот элемент ни в одном веществе не проявляет такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы этого элемента в формуле исходного вещества и продукта реакции, поэтому ставим коэффициент 4 перед формулой двух соединений азота (NH3, NO). Поскольку элемент кислород изменил степень окисления не полностью, поэтому ставим коэффициент 5 только перед формулой кислорода:
4NH3 + 5O2 ⟶ 4NO + H2O
Подбираем коэффициенты для остальных соединений. Получим уравнение:
4NH3 + 5O2 = 4NO + 6H2O
В приведённой реакции аммиак — восстановитель (за счёт атомов азота в степени окисления -3) , а кислород — окислитель.
б) Al + I2 ⟶ AlI3;
2Al + 3I2 = 2AlI3
Схема окислительно-восстановительной реакции.
Al 0 + I2 0 ⟶ Al +3 I3 -1
Al 0 -3ē ⟶ Al +3 |3|6|2 ― процесс окисления
I2 0 +2ē ⟶ 2I -1 |2| |3 ― процесс восстановления
Проводим вертикальную черту и пишем за ней число электронов, которые отдали и присоединили атомы алюминия и йода. Находим наименьшее общее кратное для чисел 3 и 2. Это число 6, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 3 и 2, записываем результат за третьей чертой в строках, касающихся элементов алюминия и йода. Множители 2 и 3 являются искомыми коэффициентами. Поскольку элементы изменили степень окисления полностью (в правой части схемы эти элементы ни в одном веществе не проявляют такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы элемента алюминия в формуле исходного вещества и продукта реакции, поэтому ставим коэффициент 2 перед формулой двух соединений алюминия ( Al , AlI3), а поскольку различным является индекс элемента йода ― ставим коэффициент 3, поскольку относится к двум атомам йода, перед формулой йода :
2Al + 3I2 = 2AlI3
В приведённой реакции алюминий — восстановитель, а йод— окислитель.
в) HNO3 + P + H2O ⟶ H3PO4 + NO;
5HNO3 + 3P + 2H2O = 3H3PO4 + 5NO
Схема окислительно-восстановительной реакции.
HN +5 O3 + P 0 + H2O ⟶ H3P +5 O4 + N +2 O
P 0 -5ē ⟶ P +5 |5|15|3 ― процесс окисления
N +5 +3ē ⟶ N +2 |3| |5 ― процесс восстановления
Проводим вертикальную черту и пишем за ней число электронов, которые отдали и присоединили атомы фосфора и азота. Находим наименьшее общее кратное для чисел 5 и 3. Это число 15, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 5 и 3, записываем результат за третьей чертой в строках, касающихся элементов фосфора и азота. Множители 5 и 3 являются искомыми коэффициентами. Поскольку элементы изменили степень окисления полностью (в правой части схемы эти элементы ни в одном веществе не проявляют такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы этих элементов в формуле исходного вещества и продукта реакции, поэтому коэффициент 2 ставим перед формулой двух соединений фосфора (P, H3PO4), а коэффициент 3 ― перед формулой двух соединений азота (HNO3, NO) :
5HNO3 + 3P + H2O = 3H3PO4 + 5NO
Подбираем коэффициенты для остальных соединений. Получим уравнение:
5HNO3 + 3P + 2H2O = 3H3PO4 + 5NO
В приведённой реакции фосфор — восстановитель, а азотная кислота (за счёт атомов азота в степени окисления +5) — окислитель.
г) HCl + KMnO4 ⟶ Cl2 + KCl + MnCl2 + H2O.
16HCl + 2KMnO4 = 5Cl2 + 2KCl + 2MnCl2 + 8H2O
Схема окислительно-восстановительной реакции.
HCl -1 + KMn +7 O4 ⟶ Cl2 0 + KCl -1 + Mn +2 Cl2 -1 + H2O
2Cl -1 -2ē ⟶ Cl2 0 |2|10|5 ― процесс окисления
Mn +7 + 5ē ⟶ Mn +2 |5| |2 ― процесс восстановления
Проводим вертикальную черту и пишем за ней число электронов, которые отдали и присоединили атомы хлора и марганца. Находим наименьшее общее кратное для чисел 2 и 5. Это число 10, которое записываем за второй вертикальной чертой посередине, и поделив его поочередно на 2 и 5, записываем результат за третьей чертой в строках, касающихся элементов хлора и марганца. Множители 5 и 2 являются искомыми коэффициентами. Поскольку элемент марганец изменил степень окисления полностью (в правой части схемы этот элемент ни в одном веществе не проявляет такую же степень окисления, как в исходном веществе) и одинаковыми являются индексы этого элемента в формуле исходного вещества и продукта реакции, поэтому коэффициент 2 ставим перед формулой двух соединений марганца ( KMnO4 , MnCl2). Поскольку элемент хлор изменил степень окисления не полностью, поэтому ставим коэффициент 5 только перед формулой хлора:
HCl + 2KMnO4 ⟶ 5Cl2 + KCl + 2MnCl2 + H2O
Подбираем коэффициенты для остальных соединений. Получим уравнение:
16HCl + 2KMnO4 = 5Cl2 + 2KCl + 2MnCl2 + 8H2O
В приведённой реакции хлороводородная кислота — восстановитель (за счёт атомов хлора в степени окисления -1) , а перманганат калия (за счёт атомов марганца в степени окисления +7) — окислитель.
Задание 8 Назовите окислитель в реакциях взаимодействия цинка с соляной и азотной кислотами. Для последней реакции используйте аналогию взаимодействия азотной кислоты с медью.
Zn + 2HCl = ZnCl2 + H2↑
Zn 0 + 2H +1 Cl ⟶ Zn +2 Cl2 + H2 0 ↑
В приведённой реакции хлорная кислота (за счёт атомов водорода в степени окисления +1) — окислитель, поскольку степень окисления водорода понижается от +1 до 0.
3Zn + 8HNO3 (конц.) = 3Zn(NO3)2 + 2NO↑ + 4H2O
Zn 0 + HN +5 O3 ⟶ Zn +2 (NO3)2 + 2N +2 O↑ + H2O
В приведённой реакции азотная кислота (за счёт атомов азота в степени окисления +5) — окислитель, поскольку степень окисления азота понижается от +5 до +2.
Составьте молекулярные уравнения реакций, идущих по схеме NO → N02 → HN03 → NaN03. Уравнение 1 рассмотрите с точки зрения теории
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,405
- гуманитарные 33,632
- юридические 17,905
- школьный раздел 607,990
- разное 16,855
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.