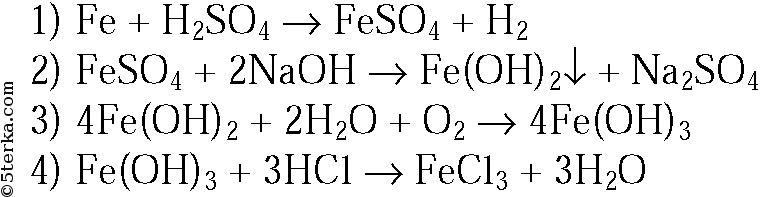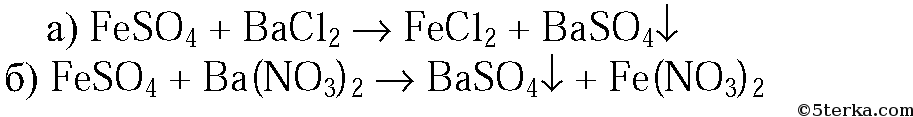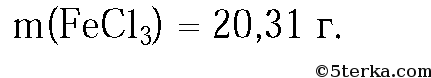Видео:Получение и превращения гидроксидов железа Fe(OH)2 и Fe(OH)3Скачать

Ваш ответ
Видео:8 класс. Составление уравнений химических реакций.Скачать

решение вопроса
Видео:Fe + H2SO4 → FeSO4 + H2 | Реакция взаимодействия железа и серной кислотыСкачать

Похожие вопросы
- Все категории
- экономические 43,415
- гуманитарные 33,633
- юридические 17,906
- школьный раздел 608,079
- разное 16,856
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Видео:Подлинность СТРЕПТОЦИДА. Реакция с MgSO4, Ca(NO3)2, FeSO4, Pb(NO3)2, Hg(NO3)2. Опыты по химии.Скачать

Схемы превращений веществ. Составление уравнений реакций превращений железа
Задание 237.
Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
Fe → FeSO4 → Fe(OH)2 → Fe(OH)3 → FeCl3
Решение:
Уравнения реакций, которые надо провести для осуществления следующих превращений:
Задание 429 (ш)
Составьте молекулярные и ионно-молекулярные уравнения реакций, которые надо провести для осуществления превращений:
Fe → FeCl2 → Fe(CN)2 → К4[Fe(CN)6] → К3[Fe(CN)6]
К окислительно-восстановительным реакциям составьте электронные уравнения.
Решение:
Молекулярные и ионно-молекулярные уравнения реакций, которые надо провести для осуществления превращений: Fe → FeCl2 → Fe(CN)2 → К4[Fe(CN)6] → К3[Fe(CN)6]
а) Fe + 2HCl = FeCl2 + H2↑ (молекулярная форма);
Fe + 2H + = Fe 2+ + H2 0 (ионно-молекулярная форма).
б) FeCl2 + 2KCN = Fe(CN)2↓ + 2KCl (молекулярная форма);
Fe 2+ + 2CN — = Fe(CN)2↓ (ионно-молекулярная форма).
в) В избытке цианида калия осадок Fe(CN)2 растворяется вследствие образования комплексного соединения К4[Fe(CN)6]:
Fe(CN)2 + 4KCN → К4[Fe(CN)6] (молекулярная форма);
Fe(CN)2 + 4CN — → [Fe(CN)6] 4- (ионно-молекулярная форма).
г) При действии хлора или брома на раствор жёлтой кровяной соли анион [Fe(CN)6] 4- превращается в анион [Fe(CN)6] 3- :
Данная реакция является окислительно-восстановительной, так как атом железа увеличивает свою степень окисления от +2 до +3, т. е. проявляет свойства восстановителя; атомы хлора уменьшают свою степень окисления от 0 до -1, т. е. проявляют свойства окислителя:
Видео:Решение цепочек превращений по химииСкачать

Вариант 4
Видео:Гидролиз солей. 9 класс.Скачать

Вопросы:
1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
2. Какую реакцию среды имеют водные растворы солей железа(III)? Почему?
3. Как, исходя из сульфата железа(→), получить: а) хлорид железа(II); б) нитрат железа(II)? Напишите уравнения соответствующих реакций.
4. Рассчитайте массу железа, которое должно вступить в реакцию с раствором серной кислоты, чтобы выделился такой же объем водорода (н. у.), который выделяется при взаимодействии с раствором серной кислоты 8,1 алюминия. (Ответ: 25,2 г.)
Видео:ОВР часть 2Скачать

Ответы и решения:
2. Водные растворы солей железа(III) имеют кислую среду, т.к. соли образованы слабым основанием и сильной кислотой и в воде гидролизуются.

задача №4
к главе «Тема VI. Железо. Металлургия. Работа 1. Железо и его соединения».
🎥 Видео
How to Balance FeCl2 + NaOH = Fe(OH)2 + NaClСкачать

How to Balance Fe + H2SO4 = FeSO4 + Fe2(SO4)3 + H2O + SO2 (Iron + Concentrated Sulfuric acid)Скачать

Расстановка коэффициентов в химических реакциях: как просто это сделатьСкачать

How to Balance Fe2(SO4)3 + LiOH = Fe(OH)3 + Li2SO4Скачать

Fe + 2HCl → FeCl2 + H2 | Реакция взаимодействия железа и хлороводородаСкачать

FeSO4+KMnO4+H2SO4=Fe2(SO4)3+MnSO4+K2SO4+H2O расстановка коэффициентов методом электронного балансаСкачать
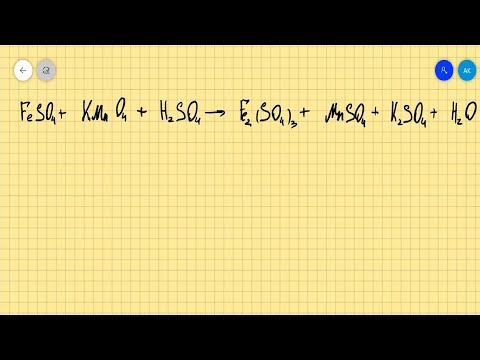
How to find the Oxidation Number for Fe in FeCl2Скачать

8 класс. ОВР. Окислительно-восстановительные реакции.Скачать

Задание 22.5Скачать

How to Write the Net Ionic Equation for FeCl2 + KOH = Fe(OH)2 + KClСкачать

Электролитическая диссоциация кислот, оснований и солей. 9 класс.Скачать

Соединения железаСкачать

Составление формул соединений. 8 класс.Скачать