Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,401
- гуманитарные 33,632
- юридические 17,905
- школьный раздел 607,977
- разное 16,854
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Гидролиз нитрата меди (II)
Cu(NO3)2 — соль образованная слабым основанием и сильной кислотой, поэтому реакция гидролиза протекает по катиону.
Первая стадия (ступень) гидролиза
Полное ионное уравнение
Cu 2+ + 2NO3 — + HOH ⇄ CuOH + + NO3 — + H + + NO3 —
Сокращенное (краткое) ионное уравнение
Cu 2+ + HOH ⇄ CuOH + + H +
Вторая стадия (ступень) гидролиза
Молекулярное уравнение
CuOHNO3 + HOH ⇄ Cu(OH)2 + HNO3
Полное ионное уравнение
CuOH + + NO3 — + HOH ⇄ Cu(OH)2 + H + + NO3 —
Сокращенное (краткое) ионное уравнение
CuOH + + HOH ⇄ Cu(OH)2 + H +
Среда и pH раствора нитрата меди (II)
В результате гидролиза образовались ионы водорода (H + ), поэтому раствор имеет кислую среду (pH
Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: нитрат меди (II), сульфид калия
Решение:
Нитрат меди (II) Cu(NO3)2– соль слабого двухкислотного основания и сильной кислоты. Катионы слабого основания Cu 2+ связывают гидроксид ионы из воды. Гидролиз такой соли идет по катиону:
Сокращенное ионно-молекулярное уравнение гидролиза:
Cu 2+ + H2O 
полное ионно-молекулярное уравнение:
Cu 2+ + 2NO3 — + H2O 
Cu(NO3)2+ H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH 2– связывают ионы водорода из воды, образуя анионы кислой соли HS – . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
S 2– + H2O 
полное ионно-молекулярное уравнение:
2К + + S 2– + H2O 
К2S + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7).
22. Какие из солей Al2(SO4)3, K2S, Pb(NO3)2, KCl подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
Решение:
Сульфат алюминия Al2(SO4)3– соль слабого трехкислотного основания и сильной кислоты. Гидролиз такой соли идет по катиону слабого основания с образованием катионов основной соли AlOH 2+ .
Сокращенное ионно-молекулярное уравнение гидролиза:
Al 3+ + H2O 
полное ионно-молекулярное уравнение:
2Al 3+ + 3SO4 2- + 2H2O 
Al2(SO4)3 + 2H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH 2– связывают ионы водорода из воды, образуя анионы кислой соли HS – . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
S 2– + H2O 
полное ионно-молекулярное уравнение:
2К + + S 2– + H2O 
К2S + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7).
Нитрат свинца (II) Pb(NO3)2– соль слабого двухкислотного основания и сильной кислоты. Катионы слабого основания Pb 2+ связывают гидроксид ионы из воды. Гидролиз такой соли идет по катиону:
Сокращенное ионно-молекулярное уравнение гидролиза:
Pb 2+ + H2O 
полное ионно-молекулярное уравнение:
Pb 2+ + 2NO3 — + H2O 
Pb(NO3)2+ H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH + и анионы Cl – . Катионы K + не могут связывать анионы OH – , так как KOH – сильный электролит. Анионы Cl – не могут связывать катионы Н + , так как НCl – сильный электролит. Таким образом, можно сделать вывод, что хлорид калия не гидролизуется. Равновесие между ионами и молекулами воды не нарушается, и раствор остается нейтральным, рН равен 7.
Как изменится цвет лакмуса в растворах солей: хлорида натрия, карбоната натрия, хлорида меди (II)? Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей.
Решение:
Хлорид натрия NaCl —соль сильной кислоты и сильного основания. При растворении в воде хлорид натрия диссоциирует на ионы Na + и анионы Cl – . Катионы Na + не могут связывать анионы OH – , так как NaOH – сильный электролит. Анионы Cl – не могут связывать катионы Н + , так как НCl – сильный электролит. Таким образом, можно сделать вывод, что хлорид натрия не гидролизуется. Равновесие между ионами и молекулами воды не нарушается, и раствор остается нейтральным, рН равен 7. Цвет лакмуса не изменяется.
Карбонат натрия Na2CO3 – соль двухосновной слабой кислоты и сильного основания. Анионы слабой кислоты CO3 2– связывают ионы водорода из воды, образуя анионы кислой соли HCO3 — . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
CO3 2– + H2O 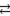
полное ионно-молекулярное уравнение:
2Na + + CO3 2– + H2O 
Na2CO3 + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7). Цвет лакмуса меняется с фиолетового на синий.
Хлорид меди (II) CuCl2– соль слабого двукислотного основания и сильной кислоты. Гидролиз такой соли идет по катиону слабого основания с образованием катионов основной соли CoOH + .
Сокращенное ионно-молекулярное уравнение гидролиза:
Cu 2+ + H2O 
полное ионно-молекулярное уравнение:
Cu 2+ + 2Cl — + H2O 
CuCl2+ 2H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH .