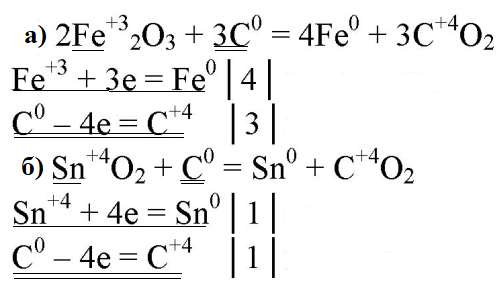- Реакция взаимодействия оксида олова (IV) и углерода
- Реакция взаимодействия карбоната свинца (II) и гидроксида натрия
- Реакция взаимодействия оксида углерода (II) и гидроксида натрия
- Реакция взаимодействия галлия и азотной кислоты
- Выбрать язык
- Разделы
- ТОП 5 записей
- Популярные записи
- Элементы, реакции, вещества
- Предупреждение.
- Вопросы к параграфу 32 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
- § 32. Химические свойства углерода. Адсорбция
- Вопросы и задания
- 1. При каких процессах образуется древесный уголь? Каково его строение, свойства и применение?
- 2. С помощью каких явлений, которые вы наблюдаете в жизни, можно доказать, что хлеб, молоко, мясо содержат углерод?
- 3. Переведите таблицу 24 в текст.
- 4. Составьте уравнения реакций, протекающих при нагревании угля: 1) с оксидом железа(III); 2) с оксидом олова(IV). Покажите переход электронов и подчеркните одной чертой окислитель, а двумя — восстановитель.
- 5. Основываясь на свойствах углерода и пользуясь рисунком 32, поясните, для каких целей применяют углерод.
- 6. Обсудите с соседом по парте, где в повседневной жизни вы можете встретиться с веществами, в состав которых входят атомы элементов IVA-группы.
- Восстановление металлов
- Восстановление углеродом или водородом
- Похожие страницы:
- Leave a Comment
Реакция взаимодействия оксида олова (IV) и углерода
Уравнение реакции взаимодействия оксида олова (IV) и углерода:
SnO2 + 2C → Sn + 2CO
Реакция взаимодействия оксида олова (IV) и углерода.
В результате реакции образуются олово и оксид углерода (II).
Реакция протекает при условии: при температуре 800-900 °C.
Формула поиска по сайту: SnO2 + 2C → Sn + 2CO.
Реакция взаимодействия карбоната свинца (II) и гидроксида натрия
Реакция взаимодействия оксида углерода (II) и гидроксида натрия
Реакция взаимодействия галлия и азотной кислоты
Выбрать язык
Разделы
ТОП 5 записей
Популярные записи
Элементы, реакции, вещества
Предупреждение.
Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций.
Химические реакции и информация на сайте
не предназначены для проведения химических и лабораторных опытов и работ.
Вопросы к параграфу 32 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
§ 32. Химические свойства углерода. Адсорбция
Вопросы и задания
1. При каких процессах образуется древесный уголь? Каково его строение, свойства и применение?
Древесный уголь — твёрдый пористый продукт, разновидность угля, образующийся при нагревании древесины без доступа воздуха. В образовавшемся древесном угле множество капилляров и пор, что делает его хорошим адсорбентом.
Применяют древесный уголь в производстве кристаллического кремния, черных и цветных металлов, сероуглерода, активированного угля, фильтрах для очистки воды, противогазах, как экологически чистое топливо.
2. С помощью каких явлений, которые вы наблюдаете в жизни, можно доказать, что хлеб, молоко, мясо содержат углерод?
Если эти продукты подгорают при жарке, то образуется уголь, значит они содержат углерод.
3. Переведите таблицу 24 в текст.
Кислород легко окисляет углерод до степени окисления +4 с образованием углекислого газа.
В реакциями с оксидами металлов углерод также проявляет свои восстановительные свойства, в результате реакции образуется углекислый газ и металл.
Реакция углерода с углекислым газом и водой приводит к образованию угарного газа.
Углерод может окислять сильные восстановители: металлы — до карбидов, водород — до метана.
4. Составьте уравнения реакций, протекающих при нагревании угля: 1) с оксидом железа(III); 2) с оксидом олова(IV). Покажите переход электронов и подчеркните одной чертой окислитель, а двумя — восстановитель.
5. Основываясь на свойствах углерода и пользуясь рисунком 32, поясните, для каких целей применяют углерод.
- При производстве органических веществ (метанол, бензин, красители);
- В медицине (активированный уголь);
- В ювелирном производстве (алмазы);
- В производстве полимеров (резина).
6. Обсудите с соседом по парте, где в повседневной жизни вы можете встретиться с веществами, в состав которых входят атомы элементов IVA-группы.
В повседневной жизни мы постоянно сталкиваемся с объектами, в составе которых присутствует углерод. Например:
— в изделия из резины и пластика – (игрушки, бытовая техника, одежда и т.д.) — в составе полимеров;
— NaHCO3 – пищевая сода; CaCO3 – мел, мрамор, известняк — в виде карбонатов;
— в еде, лекарственных средствах, красителях и т.д. — в виде органических веществ.
В форме SiO2 – песока — кремний наиболее распространён; его формы также входят в состав стекла и разнообразных минералов. Кремний применяется также в составе полупроводников в бытовой электронике.
Восстановление металлов
Восстановление углеродом или водородом
Водород для восстановления окислов применяют реже, он дороже и взрывоопасен, но необходим в тех случаях, когда уг лерод может образовать с металлами иногда нежелательные карбиды, например при восстановлении вольфрама и молибдена:
Похожие страницы:
Понравилась статья поделись ей
Leave a Comment
Для отправки комментария вам необходимо авторизоваться.