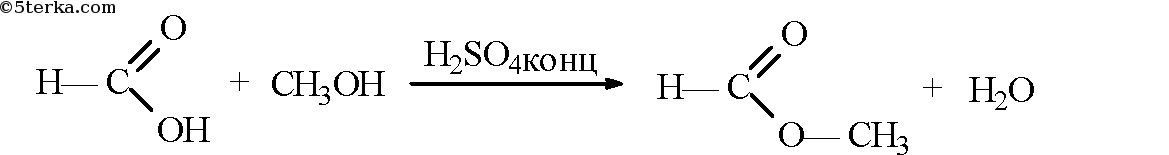- 13. Составьте уравнение реакции получения метилформиата — сложного эфира метанола и муравьиной кислоты. В каких условиях следует проводить эту реакцию?
- Acetyl
- Сложные эфиры: способы получения и свойства
- Классификация сложных эфиров
- По числу карбоксильных групп:
- Номенклатура сложных эфиров
- Химические свойства сложных эфиров
- 2. Переэтерификация
- 3.Восстановление сложных эфиров
- Получение сложных эфиров
- 1. Этерификация карбоновых кислот спиртами
- 2. Соли карбоновых кислот с галогеналканами
- Составьте уравнение реакции получения метилформиата сложного эфира метанола и муравьиной кислоты
13. Составьте уравнение реакции получения метилформиата — сложного эфира метанола и муравьиной кислоты. В каких условиях следует проводить эту реакцию?

задача №13
к главе «Глава 4. Кислородсодержащие соединения. § 20. Карбоновые кислоты».
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
Нажмите на значок глаза возле рекламного блока, и блоки станут менее заметны. Работает до перезагрузки страницы.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Сложные эфиры: способы получения и свойстваСложные эфиры: способы получения, химические и физические свойства, строение.
Общая формула предельных сложных эфиров: СnH2nO2 Классификация сложных эфировПо числу карбоксильных групп:
Например, общая формула сложных эфиров двухосновных карбоновых кислот CnH2n-2O4 Номенклатура сложных эфировВ названии сложного эфира сначала указывают алкильную группу, связанную с кислородом, затем кислоту, заменяя суффикс в названии кислоты (-овая кислота) на суффикс -оат.
Химические свойства сложных эфиров
В присутствии кислот гидролиз сложных эфиров протекает как реакция, обратная этерификации. при гидролизе сложных эфиров образуются спирты и карбоновые кислоты. R-COO-R’ + H2O = R-COOH + R’-OH Например , при гидролизе метилацетата образуются уксусная кислота и метанол. При щелочном гидролизе сложных эфиров образуются соли карбоновых кислот и спирты. Например , при щелочном гидролизе этилформиата образуются этанол и формиат натрия: При щелочном гидролизе этилацетата образуются ацетат и этанол: Щелочной гидролиз сложных эфиров — реакция, имеющая промышленное значение. Гидролиз жиров в присутствии оснований — древнейший способ получения мыла. Первые способы получения мыла связаны со смешиванием жира с золой. Один из основных компонентов животного жира — тристеарат глицерина. В щелочной среде тристеарат глицерина разлагается на глицерин и соль стеариновой кислоты: 2. ПереэтерификацияПереэтерификация — это реакция превращения одного сложного эфира в другой под действием соответствующих спиртов в присутствии катализатора (кислоты или основания) R-COO-CH3 + R’-OH = R-COOR’ + CH3-OH 3.Восстановление сложных эфировСложные эфиры восстанавливаются с разрывом связи С-О карбоксильной группы. При этом образуется смесь спиртов.
Получение сложных эфиров1. Этерификация карбоновых кислот спиртамиКарбоновые кислоты вступают в реакции с одноатомными и многоатомными спиртами с образованием сложных эфиров.
2. Соли карбоновых кислот с галогеналканамиПри взаимодействии солей карбоновых кислот с галогеналканами образуются сложные эфиры. Составьте уравнение реакции получения метилформиата сложного эфира метанола и муравьиной кислотыFOR-DLE.ru — Всё для твоего DLE 😉 На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх. |
Задание 1
Какие вещества называют карбоновыми кислотами?
Карбоновыми кислотами называют органические вещества, содержащие в молекуле карбоксильную группу, связанную с углеводородным радикалом.
Приведите формулы и названия пяти представителей гомологического ряда предельных одноосновных карбоновых кислот.
Метановая (муравьиная) кислота H―COOH,
этановая (уксусная) кислота CH3―COOH,
пропановая (пропионовая) кислота CH3―CH2―COOH,
бутановая (маслянная) кислота CH3―CH2―CH2―COOH,
пентановая (валериановая) кислота CH3―CH2―CH2―CH2―COOH
Задание 2
Напишите формулы следующих кислот:
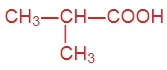 | 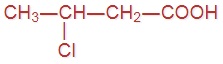 | 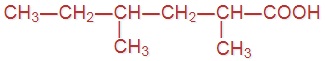 |
Задание 3
Молярная масса предельной одноосновной карбоновой кислоты равна 130 г/моль. Какова молекулярная формула этой кислоты. Дано:
Дано: M(CnH2n+1COOH)=130 г/моль
Найти: формула CnH2n+1COOH−?
Решение
По условию задачи M(CnH2n+1COOH)=130 г/моль, поэтому Mr(CnH2n+1COOH)=130
Mr(CnH2n+1COOH)=(n+1)•Ar(C)+(2n+2)•Ar(H)+2•Ar(O)=(n+1)•12+(2n+2)•1+2•16=12n+12+2n+2+32=14n+46
Составляем алгебраическое уравнение и решаем его:
14n+46=130
14n=130 — 46
14n=84
n=84 : 14
n=6, поэтому формула кислоты: C6H13COOH
Ответ: C6H13COOH
Задание 4
Какие признаки верно отражают свойства уксусной кислоты:
1) газообразное вещество;
2) без запаха;
3) с резким запахом;
4) плохо растворима в воде;
5) слабый электролит?
Задание 5
В пищевой промышленности уксусную кислоту используют как регулятор кислотности и консервант (код E260). Напишите структурные формулы предыдущего и последующего представителей данного гомологического ряда, имеющих коды E236 и E280 соответственно.
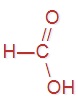 | 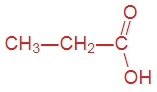 |
Напишите уравнение реакции получения каждой кислоты.
Во время кипячения спирта с окислителем спирт окисляется до карбоновой кислоты:
CH3OH + О2 t,кат. ⟶ HCOOH + H2O
C3H7OH + O2 t,кат. ⟶ C2H5COOH + H2O
Задание 6
В чём сходство и различие химических свойств неорганических и органических кислот? Ответ подтвердите уравнениями химических реакций.
Сходство.
1) Реагируют с активными металлами с образованием солей и выделением водорода:
Ca + 2HCl ⟶ CaCl2 + H2↑
Ca + 2CH3COOH ⟶ (CH3COO)2Ca + H2↑
2) Реагируют с оксидами металлов с образованием солей и воды:
MgO + 2HCl ⟶ MgCl2 + H2O
MgO + 2CH3COOH ⟶ (CH3COO)2Mg + H2O
3) Реагируют с основаниями с образованием солей и воды:
NaOH + HCl ⟶ NaCl + H2O
NaOH + CH3COOH ⟶ CH3COONa + H2O
4) Реагируют с солями, если в результате реакции выделяется газ, образуется осадок или слабый электролит:
CaCO3 + 2HCl ⟶ CaCl2 + H2O + CO2↑
CaCO3 + 2CH3COOH ⟶ (CH3COO)2Ca + H2O + CO2↑
Различие.
Карбоновые кислоты в присутствии концентрированной серной кислоты вступают во взаимодействие со спиртами, с образованием сложных эфиров (реакция этерификации):
CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O (при H2SO4(конц.))
Задание 7
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
этан ⟶ хлорэтан ⟶ этиловый спирт ⟶ уксусный альдегид ⟶ уксусная кислота ⟶ ацетат калия и этиловый эфир уксусной кислоты.
C2H6 + Cl2 ⟶ C2H5Cl + HCl
C2H5Cl + NaOH ⟶ C2H5OH + NaCl
2C2H5OH + O2 t,кат. ⟶ 2CH3CHO + 2H2O
2CH3CHO + O2 кат. ⟶ 2CH3COOH
CH3COOH + KOH ⟶ CH3COOK + H2O
CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O (при ⇄H2SO4(конц.))
Задание 8
Достаточно ли 100 г 66%-ного раствора уксусной кислоты для растворения 30 г карбоната кальция? Какая масса ацетата кальция при этом получится?
Дано: m(раствора)=100 г, ω(CH3COOH)=66%, m(CaCO3)=30 г
Найти: m ((CH3COO)2Ca)—?
Решение
1. Рассчитываем массу уксусной кислоты в растворе:
m( CH3COOH )=ω( CH3COOH )•m(раствора):100%=66%•100 г:100%=66 г
2. Количество вещества рассчитываем по формуле: n=m/M, где M ― молярная масса.
M( CH3COOH )=60 г/моль, M(CaCO3)=100 г/моль
n( CH3COOH )=m( CH3COOH )/M( CH3COOH )=66 г : 60г/моль=1,1 моль
n( CaCO3 )=m( CaCO3 )/M( CaCO3 )=30 г : 100 г/моль=0,3 моль
3. Составим химическое уравнение:
CaCO3 + 2CH3COOH ⟶ (CH3COO)2Ca + H2O + CO2↑
По уравнению реакции 1 моль карбоната кальция реагирует с 2 моль уксусной кислоты, поэтому с 0,3 моль карбоната кальция прореагирует в 2 раза больше количества вещества уксусной кислоты, то есть 0,6 моль. По условию задачи имеем 1,1 моль уксусной кислоты, следовательно кислота взята в избытке (её хватит), она реагирует не полностью, поэтому расчеты будем проводить по данным карбоната кальция.
По уравнению реакции количество вещества карбоната кальция и ацетата кальция одинаковое, поэтому:
n( (CH3COO)2Ca )=n( CH3COOH )=0,3 моль
4. Рассчитываем массу карбоната кальция количеством вещества 0,3 моль по формуле: m = n • M, где M ― молярная масса.
M ( (CH3COO)2Ca )=158 г/моль
m( (CH3COO)2Ca )=n ( (CH3COO)2Ca ) • M( (CH3COO)2Ca )=0,3 моль • 158 г/моль=47,4 г
Ответ: уксусной кислоты достаточно; получится 47,4 г ацетата кальция.
Задание 9
Почему жжение от ужаления муравья утихает, если потереть пострадавшее место нашатырным спиртом (водным раствором аммиака)?
Происходит нейтрализация муравьиной кислоты, которая вызывает жжение и содержится в составе жалящей жидкости, с аммиаком, содержашемся в составе нашатырного спирта:
HCOOH + NH3 ⟶ HCOONH4
Нашатырный спирт представляет собой водный раствор аммиака с массовой долей растворенного вещества 10%.
Задание 10
Докажите с помощью уравнений реакций, что муравьиная кислота может проявлять как свойства альдегидов, так и свойства кислот. Муравьиная кислота, в отличие от других карбоновых кислот, содержит альдегидную группу CНO, поэтому как и альдегиды, способна реагировать с аммиачным раствором оксида серебра (при этом происходит восстановление серебра) и со свежеполученным осадком гидроксида меди (II) при нагревании (при этом медь восстанавливается до одновалентной меди) :
HCOOH + Ag2O аммиачный р-р t → H2O + CO2 + 2Ag↓
HCOOH + 2Cu(OH)2 ⟶ Cu2O + CO2 + 3H2O
Задание 12
Есть ли у вас на кухне уксусная кислота? Какие правила техники безопасности необходимо соблюдать при её использовании? Почему?
С уксусной кислотой необходимо обращаться очень осторожно, т.к. её пары могут вызвать ожоги дыхательных путей и слизистых оболочек глаз.