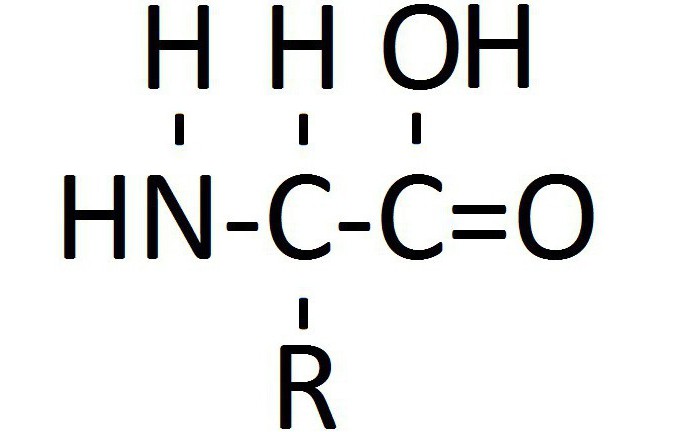Химические вещества, содержащие структурные компоненты молекулы карбоновой кислоты и амина, называются аминокислотами. Это общее название группы органических соединений, в составе которых присутствует углеводородная цепь, карбоксильная группа (-СООН) и аминогруппа (-NH2). Их предшественниками являются карбоновые кислоты, а молекулы, у которых водород у первого углеродного атома замещен аминогруппой, называются альфа-аминокислотами.
Всего 20 аминокислот имеют ценность для ферментативных реакций биосинтеза, протекающих в организме всех живых существ. Эти вещества называются стандартными аминокислотами. Существуют также нестандартные аминокислоты, которые включены в состав некоторых специальных белковых молекул. Они не встречаются повсеместно, хотя выполняют важную функцию в живой природе. Вероятно, радикалы этих кислот модифицируются уже после биосинтеза.
- Общая информация и список веществ
- Глицин, аланин, валин
- Тирозин, гистидин, триптофан
- Фенилаланин, лейцин и изолейцин
- Пролин, серин, цистеин
- Аргинин, метионин, треонин
- Аспарагин, лизин, глутамин
- Аспарагиновая и глутаминовая кислота
- Химическая структура
- Физические свойства
- Определение структуры участка ДНК, кодирующего указанный полипептид
- 1. Транскрипция и трансляция данного фрагмента гена до мутации
- 2. Транскрипция и трансляция данного фрагмента гена после мутации
- Какие существуют заменимые и незаменимые аминокислоты
- Аминокислоты
- Что такое аминокислоты?
- Заменимые, условно незаменимые и незаменимые
- Что мы узнали?
- Продукты богатые аминокислотами
- СТАТЬИ ПО ТЕМЕ:
- Заменимые аминокислоты
- Аланин
- Аргинин
- Аспарагин
- Аспарагиновая кислота, также известная как L-аспартат
- Цистеин
- Глютаминовая кислота, также известная как глутамат
- Глютамин
- Глицин
- Пролин
- Серин
- Тирозин
- Суточная норма потребления аминокислот
- Незаменимые аминокислоты
- Гистидин
- Изолейцин
- Лейцин
- Лизин
- Метионин
- Фенилаланин
- Треонин
- Триптофан
- Валин
- Нехватка и переизбыток аминокислот
- Функции аминокислот в организме
- Популярные классификации
- Другие наиболее популярные классификации
- Аминокислоты для бодибилдеров
- Для здоровья и красоты
- Особенности строения природных аминокислот
- Какие бывают аминокислоты?
- Вред, побочные эффекты, противопоказания
- Нехватка и переизбыток
Общая информация и список веществ
Известны две большие группы аминокислот, которые были выделены по причине закономерностей их нахождения в природе. В частности, существуют 20 аминокислот стандартного типа и 26 нестандартных аминокислот. Первые находят в составе белков любого живого организма, тогда как вторые являются специфическими для отдельных живых организмов.
20 аминокислот стандартных делятся на 2 типа в зависимости от способности синтезироваться в человеческом организме. Это заменимые, которые в клетках человека способны образовываться из предшественников, и незаменимые, для синтеза которых не существует ферментных систем или субстрата. Заменимые аминокислоты могут не присутствовать в пище, так как их организм может синтезировать, восполняя их количество при необходимости. Незаменимые аминокислоты не могут быть получены организмом самостоятельно, а поэтому должны поступать с пищей.
Биохимиками определены названия аминокислот из группы незаменимых. Всего их известно 8:
- метионин;
- треонин;
- изолейцин;
- лейцин;
- фенилаланин;
- триптофан;
- валин;
- лизин;
- также часто сюда относят гистидин.
Это вещества с различным строением углеводородного радикала, но обязательно с наличием карбоксильной группы и аминогруппы у альфа-С-атома.
В группе заменимых аминокислот присутствует 11 веществ:
- аланин;
- глицин;
- аргинин;
- аспарагин;
- кислота аспарагиновая;
- цистеин;
- кислота глютаминовая;
- глютамин;
- пролин;
- серин;
- тирозин.
В основном их химическое строение проще, нежели у незаменимых, поэтому их синтез дается организму легче. Большинство незаменимых аминокислот невозможно получить только из-за отсутствия субстрата, то есть молекулы-предшественника путем реакции переаминирования.
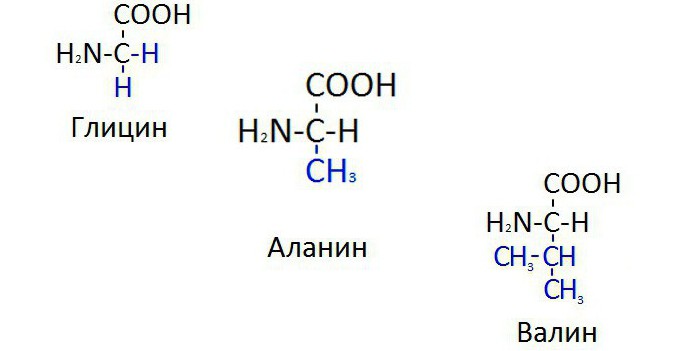
Глицин, аланин, валин
В биосинтезе белковых молекул наиболее часто используется глицин, валин и аланин, (формула каждого вещества указана ниже на рисунке). Эти аминокислоты самые простые по химической структуре. Вещество глицин и вовсе является простейшим в классе аминокислот, то есть помимо альфа-углеродного атома соединение не имеет радикалов. Однако даже простейшая по структуре молекула играет важную роль в обеспечении жизнедеятельности. В частности, из глицина синтезируется порфириновое кольцо гемоглобина, пуриновые основания. Порфировое кольцо — это белковый участок гемоглобина, призванный удерживать атомы железа в составе целостного вещества.
Глицин участвует в обеспечении жизнедеятельности головного мозга, выступая тормозным медиатором ЦНС. Это означает, что он в большей степени участвует в работе коры головного мозга — его наиболее сложно организованной ткани. Что важнее, глицин является субстратом для синтеза пуриновых оснований, нужных для образования нуклеотидов, которые кодируют наследственную информацию. Вдобавок глицин служит источником для синтеза других 20 аминокислот, тогда как сам может быть образован из серина.
У аминокислоты аланин формула немногим сложнее, чем у глицина, так как она имеет метильный радикал, замененный на один атом водорода у альфа-углеродного атома вещества. При этом аланин также остается одной из самых часто вовлекаемых в процессы биосинтеза белков молекулой. Она входит в состав любого белка в живой природе.
Неспособный синтезироваться в организме человека валин — аминокислота с разветвленной углеводородной цепочкой, состоящей из трех углеродных атомов. Изопропиловый радикал придает молекуле больший вес, однако из-за этого невозможно найти субстрат для биосинтеза в клетках человеческих органов. Поэтому валин должен обязательно поступать с пищей. Он присутствует преимущественно в структурных белках мышц.
Результаты исследований подтверждают, что валин необходим для функционирования центральной нервной системы. В частности, за счет его способности восстанавливать миелиновую оболочку нервных волокон он может использоваться в качестве вспомогательного средства при лечении рассеянного склероза, наркоманий, депрессий. В большом количестве содержится в мясных продуктах, рисе, сушеном горохе.
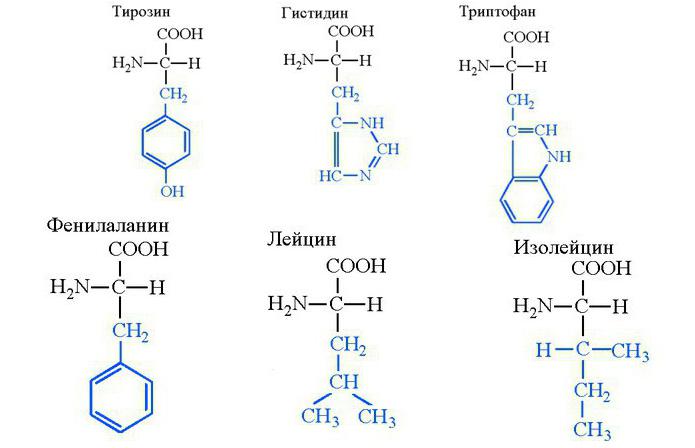
Тирозин, гистидин, триптофан
В организме тирозин способен синтезироваться из фенилаланина, хотя в большом количестве поступает с молочной пищей, преимущественно с творогом и сырами. Входит в состав казеина — животного белка, в избытке содержащемся в творожных и сырных продуктах. Ключевое значение тирозина в том, что его молекула становится субстратом синтеза катехоламинов. Это адреналин, норадреналин, дофамин — медиаторы гуморальной системы регуляции функций организма. Тирозин способен быстро проникать и через гематоэнцефалический барьер, где быстро превращается в дофамин. Молекула тирозина участвует в меланиновом синтезе, обеспечивая пигментацию кожи, волос и радужки глаза.
Аминокислота гистидин входит в состав структурных и ферментных белков организма, является субстратом синтеза гистамина. Последний регулирует желудочную секрецию, участвует в иммунных реакциях, регулирует заживление повреждений. Гистидин является незаменимой аминокислотой, и организм восполняет ее запасы только из пищи.
Триптофан так же неспособен синтезироваться организмом из-за сложности своей углеводородной цепочки. Он входит в состав белков и является субстратом синтеза серотонина. Последний является медиатором нервной системы, призванным регулировать циклы бодрствования и сна. Триптофан и тирозин — эти названия аминокислот следует помнить нейрофизиологам, так как из них синтезируются главные медиаторы лимбической системы (серотонин и дофамин), обеспечивающие наличие эмоций. При этом не существует молекулярной формы, обеспечивающей накопление незаменимых аминокислот в тканях, из-за чего они должны присутствовать в пище ежедневно. Белковая еда в количестве 70 граммов в сутки полностью обеспечивает эти потребности организма.
Фенилаланин, лейцин и изолейцин
Фенилаланин примечателен тем, что из него синтезируется аминокислота тирозин при ее недостатке. Сам фенилаланин является структурным компонентом всех белков в живой природе. Это метаболический предшественник нейромедиатора фенилэтиламина, обеспечивающий ментальную концентрацию, подъем настроения и психостимуляцию. В РФ в концентрации свыше 15% оборот данного вещества запрещен. Эффект фенилэтиламина схожий с таковым у амфетамина, однако первый не отличается пагубным воздействием на организм и отличается лишь развитием психической зависимости.
Одно из главных веществ группы аминокислот — лейцин, из которого синтезируются пептидные цепи любого белка человека, включая ферменты. Соединение, применяемое в чистом виде, способно регулировать функции печени, ускорять регенерацию ее клеток, обеспечивать омоложение организма. Поэтому лейцин — аминокислота, которая выпускается в виде лекарственного препарата. Она отличается высокой эффективностью в ходе вспомогательного лечения цирроза печени, анемии, лейкоза. Лейцин — аминокислота, существенно облегчающая реабилитацию пациентов после химиотерапии.
Изолейцин, как и лейцин, не способен синтезироваться организмом самостоятельно и относится к группе незаменимых. Однако это вещество не является лекарственным средством, так как организм испытывает в нем небольшую потребность. В основном в биосинтезе участвует только один его стереоизомер (2S,3S)-2-амино-3-метилпентановая кислота.
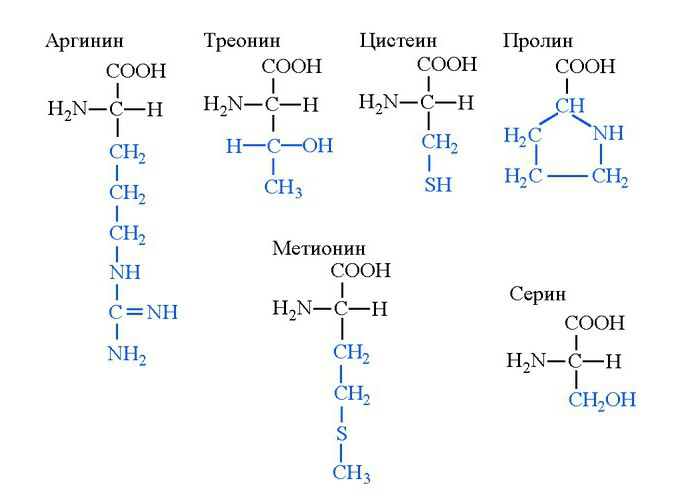
Пролин, серин, цистеин
Вещество пролин — аминокислота с циклическим углеводородным радикалом. Ее основная ценность в наличии кетонной группы цепочки, из-за чего вещество активно используется в синтезе структурных белков. Восстановление кетона гетероцикла до гидроксильной группы с образованием гидроксипролина формирует множественные водородные связи между цепочками коллагена. В результате нити этого белка сплетаются между собой и обеспечивают прочную межмолекулярную структуру.
Пролин — аминокислота, обеспечивающая механическую прочность тканей человека и его скелета. Наиболее часто она находится в коллагене, входящем в состав костей, хряща и соединительной ткани. Как и пролин, цистеин является аминокислотой, из которой синтезируется структурный белок. Однако это не коллаген, а группа веществ альфа-кератинов. Они образуют роговой слой кожи, ногти, имеются в составе чешуек волос.
Вещество серин — аминокислота, существующая в виде оптических L и D-изомеров. Это заменимое вещество, синтезируемое из фосфоглицерата. Серин способен образовываться в ходе ферментативной реакции из глицина. Данное взаимодействие обратимое, а поэтому глицин может образовываться из серина. Основная ценность последнего в том, что из серина синтезируются ферментативные белки, точнее их активные центры. Широко серин присутствует в составе структурных белков.
Аргинин, метионин, треонин
Биохимиками определено, что избыточное потребление аргинина провоцирует развитие заболевания Альцгеймера. Однако помимо негативного значения у вещества присутствуют и жизненно-важные для размножения функции. В частности, за счет наличия гуанидиновой группы, пребывающей в клетке в катионной форме, соединение способно образовывать огромное количество водородных межмолекулярных связей. Благодаря этому аргинин в виде цвиттер-иона обретает способность связаться с фосфатными участками молекул ДНК. Результатом взаимодействия является образование множества нуклеопротеидов — упаковочной формы ДНК. Аргинин в ходе изменения рН ядерного матрикса клетки может отсоединяться от нуклеопротеида, обеспечивая раскручивание цепи ДНК и начало трансляции для биосинтеза белка.
Аминокислота метионин в своей структуре содержит атом серы, из-за чего чистое вещество в кристаллическом виде имеет неприятный тухлый запах из-за выделяемого сероводорода. В организме человека метионин выполняет регенераторную функцию, способствуя заживлению мембран печеночных клеток. Поэтому выпускается в виде аминокислотного препарата. Из метионина синтезируется и второй препарат, предназначенный для диагностики опухолей. Синтезируется он путем замещения одного углеродного атома на его изотоп С11. В таком виде он активно накапливается в опухолевых клетках, давая возможность определять размеры новообразований головного мозга.
В отличие от указанных выше аминокислот, треонин имеет меньшее значение: аминокислоты из него не синтезируются, а его содержание в тканях невелико. Основная ценность треонина — включение в состав белков. Специфических функций эта аминокислота не имеет.
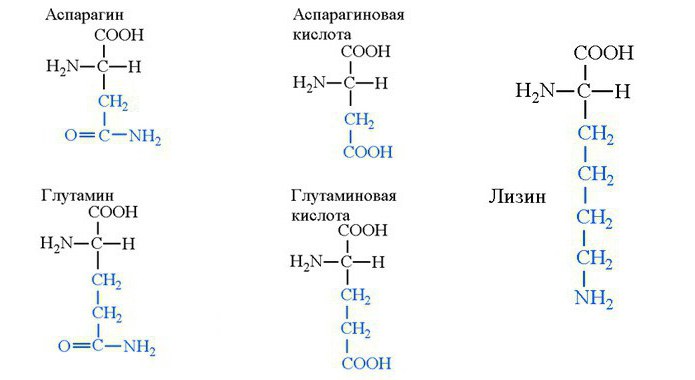
Аспарагин, лизин, глутамин
Аспарагин — распространенная заменимая аминокислота, присутствующая в виде сладкого на вкус L-изомера и горького D-изомера. Из аспарагина образуются белки организма, а путем глюконеогенеза синтезируется оксалоацетат. Это вещество способно окисляться в цикле трикарбоновых кислот и давать энергию. Это означает, что помимо структурной функции аспарагин выполняет и энергетическую.
Неспособный синтезироваться в организме человека лизин — аминокислота с щелочными свойствами. Из нее в основном синтезируются иммунные белки, ферменты и гормоны. При этом лизин — аминокислота, самостоятельно проявляющая антивирусные средства против вируса герпеса. Однако вещество в качестве препарата не используется.
Аминокислота глутамин присутствует в крови в концентрациях, намного превышающих содержание прочих аминокислот. Она играет главную роль в биохимических механизмах азотистого обмена и выведения метаболитов, участвует в синтезе нуклеиновых кислот, ферментов, гормонов, способна укреплять иммунитет, хотя в качестве лекарственного препарата не используется. Но глутамин широко применяется среди спортсменов, так как помогает восстанавливаться после тренировок, удаляет метаболиты азота и бутирата из крови и мышц. Этот механизм ускорения восстановления спортсмена не считается искусственным и справедливо не признается допинговым. Более того, лабораторные способы уличения спортсменов в таком допинге отсутствуют. Глутамин также в значительном количестве присутствует в пище.
Аспарагиновая и глутаминовая кислота
Аспарагиновая и глутаминовая аминокислоты чрезвычайно ценные для организма человека из-за своих свойств, активирующих нейромедиаторов. Они ускоряют передачу информации между нейронами, обеспечивая поддержание работоспособности структур мозга, лежащих ниже коры. В таких структурах важна надежность и постоянство, ведь эти центры регулируют дыхание и кровообращение. Поэтому в крови присутствует огромное количество аспарагинивой и глутаминовой аминокислоты. Пространственная структурная формула аминокислот указана на рисунке ниже.
Аспарагиновая кислота участвует в синтезе мочевины, устраняя аммиак из головного мозга. Она является значимым веществом для поддержания высокой скорости размножения и обновления клеток крови. Разумеется, при лейкозе этот механизм вреден, а поэтому для достижения ремиссии используются препараты ферментов, разрушающих аспарагиновую аминокислоту.
Одну четвертую часть от числа всех аминокислот в организме составляет глутаминовая кислота. Это нейромедиатор постсинаптических рецепторов, необходимый для синаптической передачи импульса между отростками нейронов. Однако для глутаминовой кислоты характерен и экстрасинаптический путь передачи информации — объемная нейротансмиссия. Такой способ лежит в основе памяти и представляет собой нейрофизиологическую загадку, ведь пока не выяснено, какие рецепторы определяют количество глутамата вне клетки и вне синапсов. Однако предполагается, что именно количество вещества вне синапса имеет важность для объемной нейротрансмиссии.
Химическая структура
Все нестандартные и 20 стандартных аминокислот имеют общий план строения. Она включает циклическую или алифатическую углеводородную цепочку с наличием радикалов или без них, аминогруппу у альфа-углеродного атома и карбоксильную группу. Углеводородная цепочка может быть любой, чтобы вещество имело реакционную способность аминокислот, важно расположение основных радикалов.
Аминогруппа и карбоксильная группа должны быть присоединены к первому углеродному атому цепочки. Согласно принятой в биохимии номенклатуре, он называется альфа-атомом. Это важно для образования пептидной группы — важнейшей химической связи, благодаря которой существуют белок. С точки зрения биологической химии, жизнью называется способ существования белковых молекул. Главное значение аминокислот — это образование пептидной связи. Общая структурная формула аминокислот представлена в статье.
Физические свойства
Несмотря на схожую структуру углеводородной цепи, аминокислоты по физическим свойствам значительно отличаются от карбоновых кислот. При комнатной температуре они являются гидрофильными кристаллическими веществами, хорошо растворяются в воде. В органическом растворителе из-за диссоциации по карбоксильной группе и отщепления протона аминокислоты растворяются плохо, образуя смеси веществ, но не истинные растворы. Многие аминокислоты имеют сладкий вкус, тогда как карбоновые кислоты — кислые.
Указанные физические свойства обусловлены наличием двух функциональных химических групп, из-за которых вещество в воде ведет себя как растворенная соль. Под действием молекул воды от карбоксильной группы отщепляется протон, акцептором которого является аминогруппа. За счет смещения электронной плотности молекулы и отсутствия свободно двигающихся протонов рН (показатель кислотности) раствор остается достаточно стабильным при добавлении кислот или щелочей с высокими константами диссоциации. Это означает, что аминокислоты способны образовывать слабые буферные системы, поддерживая гомеостаз организма.
Важно, что модуль заряда диссоциированной молекулы аминокислоты равен нулю, так как протон, отщепленный от гидроксильной группы, принимается атомом азота. Однако на азоте в растворе формируется положительный заряд, а на карбоксильной группе — отрицательный. Способность диссоциировать напрямую зависит от кислотности, а поэтому для растворов аминокислот существует изоэлектрическая точка. Это рН (показатель кислотности), при котором наибольшее количество молекул имеют нулевой заряд. В таком состоянии они неподвижны в электрическом поле и не проводят ток.
Определение структуры участка ДНК, кодирующего указанный полипептид
Задача 91.
Полипептид состоит из следующих аминокислот: валин – аланин – глицин – лизин – триптофан – валин – серин – глутаминовая кислота — тирозин. Определите структуру участка ДНК, кодирующего указанный полипептид.
Решение:
В условиях задачи последовательность аминокислот в полипетиде дана. По этим сведениям нетрудно установить строение иРНК, которая управляла синтезом данного полипептида. По таблице генетического кода находим структуру триплета валина (ГУУ), затем для аланина (ГЦУ), глицина (ЦАА), лизина (ААА), триптофана (УГГ), валина (ГУУ), серина (УЦУ), глутаминовой кислоиы (ГАА) и тирозина (УАУ). Подобрав кодирующие триплеты, составляем иРНК для данного полипептида: ГУУГЦУГГУАААГУУУЦУГААУАУ. По цепочке иРНК можно восстановить участок нити ДНК, с которой она снималась. Урацил вставал против аденина ДНК, гуанин – против цитозина и т.д. Следовательно, участок интересующей нас цепи ДНК будет иметь следующее строение:
участок иРНК: ГУУ ГЦУ ЦАА ААА УГГ ГУУ УЦУ ГАА УАУ
участок ДНК: ЦАА ЦГА ГТТ ТТТ АЦЦ ЦАА АГА ЦТТ АТА
Но ДНК состоит из двух цепочек. Зная строение одной цепи, по принципу комплементарности достраиваем вторую. Целиком участок двухцепочечной ДНК, кодирующий данный полипептид, будет иметь следующее строение:
1-я цепь ДНК: ЦАА ЦГА ГТТ ТТТ АЦЦ ЦАА АГА ЦТТ АТА
2-я цепь ДНК: ГТТ ГЦТ ЦАА ААА ТГГ ГТТ ТЦТ ГАА ТАТ.
Задача 92.
Фрагмент гена представлен 21 основанием экзона и пятью последующими основаниями интрона: АТАТАТГЦАТГЦГЦГЦАТАТГ ТАЦ. В девятом положении данной последовательности оснований произошла замена А на Ц. Смодулируйте транскрипцию и трансляцию данного фрагмента гена до мутации и после.
Решение:
Экзоны – это кодирующие последовательности ДНК генов эукариот, представленные в зрелой молекуле РНК. Интроны – это некодирующие участки генов эукариот, которые транскрибируются, но затем вырезаются из первичного транскрипта во время сплайсинга и не входят в состав зрелых РНК, т.е. не транслируются.
Транскрипция представляет собой синтез молекулы иРНК на молекуле ДНК. То есть ДНК служит матрицей для синтеза иРНК.
Трансляция (от лат. translatio — перенос, перемещение) — процесс синтеза белка из аминокислот на матрице информационной (матричной) РНК (иРНК, мРНК), осуществляемый рибосомой.
Информационная РНК по принципу комплементарности снимает информацию с ДНК. Этот процесс называется транскрипцией. При этом к цитозину присоединяется гуанин, к гуанину – цитозин, к тимину – аденин, однако к аденину ДНК присоединяется не тимин, а урацил. Таким образом, для решения задачи достаточно произвести замену нуклеотидов по схеме:
Ц → Г, Г → Ц, А →У, Т → А.
1. Транскрипция и трансляция данного фрагмента гена до мутации
а) транскрипция данного фрагмета гена до мутации, получим:
цепочка ДНК – А Т А Т А Т Г Ц А Т Г Ц Г Ц Г Ц А Т А Т Г Т А Ц,
молекула иРНК – У А У А У А Ц Г У А Ц Г Ц Г Ц Г У А У А Ц А У Г.
б) Трансляция данного фрагмета гена до мутации, получим:
молекула иРНК – УАУ АУА ЦГУ АЦГ ЦГЦ ГУА УАЦ А У Г
По таблице генетического кода (иРНК) находим порядок аминокислот в белковой молекуле, получим: триплету (УАУ) соответствует аминокислота тирозин, триплету (АУА) — изолейцин, триплету (ЦГУ) — аргинин, триплету (АЦГ) — треонин, триплету (ЦГЦ) — аргинин, триплету (ГУА) — валин, триплету (УАЦ) — тирозин.
Таким образом, порядок аминокислот в участке молекулы белка будет иметь вид:
тирозин — изолейцин — аргинин — треонин — аргинин — валин — тирозин
2. Транскрипция и трансляция данного фрагмента гена после мутации
а) транскрипция данного фрагмета гена после мутации, получим:
цепочка ДНК – А Т А Т А Т Г Ц Ц Т Г Ц Г Ц Г Ц А Т А Т Г Т А Ц,
молекула иРНК – У А У А У А Ц Г Г А Ц Г Ц Г Ц Г У А У А Ц А У Г.
б) Трансляция данного фрагмета гена после мутации, получим:
молекула иРНК – УАУ АУА ЦГГ АЦГ ЦГЦ ГУА УАЦ А У Г
По таблице генетического кода (иРНК) находим порядок аминокислот в белковой молекуле, получим: триплету (УАУ) соответствует аминокислота тирозин, триплету (АУА) — изолейцин, триплету (ЦГГ) — аргинин, триплету (АЦГ) — треонин, триплету (ЦГЦ) — аргинин, триплету (ГУА) — валин, триплету (УАЦ) — тирозин.
Таким образом, порядок аминокислот в участке молекулы белка после мутации будет иметь вид:
тирозин — изолейцин — аргинин — треонин — аргинин — валин — тирозин
Вывод:
Данная мутация, приведшая к замене в девятом положении данной последовательности А на Ц, не приводит к нарушению первичной структуры полипептида. Структура полипептида как до мутации так и после мутации имеет вид:
тирозин — изолейцин — аргинин — треонин — аргинин — валин — тирозин.
Задача 93.
Последовательность нуклеотидов на иРНК ЦГГГГЦУУЦУАГААЦГАУГАГ. Укажите соответствующий этой последовательности участок гена антисмысловой нити ДНК, а также фрагмент белка, соответствующий данному участку ДНК.
Решение:
В соответствии с принципом комплементарности азотистым основаниям кодонов иРНК соответствуют определеные коды ДНК. При этом напротив цитозина иРНК становится гуанин ДНК, напротив гуанина — цитозин, напротив тимина — аденин, напротив урацила — аденин. Таким образом, для решения задачи достаточно произвести замену нуклеотидов по схеме:
Ц → Г, Г → Ц, А→ У, Т → А.
Последовательности участок гена антисмысловой нити ДНК будет иметь вид:
молекула иРНК — ЦГГ ГГЦ УУЦ УАГ ААЦ ГАУ ГАГ;
цепочка ДНК – ГЦЦ ЦЦГ ААГ АТЦ ТТГ ЦТА ЦТЦ.
Определим фрагмент белка, соответствующий данному участку ДНК
По таблице генетического кода (ДНК) находим порядок аминокислот в белковой молекуле, получим: триплету (ГЦЦ) соответствует аминокислота аргинин, триплету (ЦЦГ) — глицин, триплету (ААГ) — фенилаланин, триплету (АТЦ) — тирозин, триплету (ТТГ) — лизин, триплету (ЦТА) — аспарагиновая кислота, триплету (ЦТЦ) — глутаминовая кислота.
Таким образом, порядок аминокислот в участке молекулы белка будет иметь вид:
аргинин — глицин — фенилаланин — тирозин — лизин — аспарагиновая кислота — глутаминовая кислота.
Какие существуют заменимые и незаменимые аминокислоты
07 февраля, 2020 года 2016-02-07 11:53:45 Ольга Стешкина Питание
Здравствуйте, уважаемые читатели моего блога! Если вы серьезно относитесь к собственному здоровью, предлагаю вместе окунуться в мир органических соединений. Сегодня я расскажу про аминокислоты в продуктах питания, таблица которых будет прилагаться для удобства в статье. Так же поговорим о необходимой суточной норме для человека.
Аминокислоты
Многие из нас знают об этих органических соединениях, но не все смогут объяснить, что это и зачем они нужны. Поэтому, начнем с азов.
Аминокислоты – это структурные химические единицы, которые образуют белки
Последние участвуют абсолютно во всех физиологических процессах организма. Они формируют мышцы, сухожилия, связки, органы, ногти, волосы и являются частью костей. Замечу, что гормоны и ферменты, регулирующие рабочие процессы в организме, тоже представляют собой белки. Они уникальны по своей структуре и цели у каждого из них свои. Белки синтезируются из аминокислот, которые человек получает из пищи. Отсюда напрашивается интересный вывод – не белки самый ценный элемент, а аминокислоты.
Что такое аминокислоты?
Аминокислоты – это органические кислоты, содержащие одну или несколько аминогрупп. Эти структурные элементы высвобождаются при гидролизе молекул белков. Они занимают центральное положение в азотистом обмене, так как являются его конечным продуктом.
В природе их встречается около 300. В человеческом теле содержится 69 аминокислот и их производных.
Они представляют собой структуры кристаллического свойства, имеющие вкусовые качества: сладкие, как глицин, горькие, как лейцин. Под воздействием высоких температур кислоты расплавляются, многие из них водорастворимые. Из кишечника они поступают в кровь, разносятся по тканям, внутренним органам, где синтезируют белки и участвуют в различных химических реакциях.
Определение и наличие аминокислот в составе крови важно для клинической практики, так как по этому признаку можно судить о функционировании почек и печени. При токсикозах в период беременности, нарушенном обмене веществ, деструктивных функциях почек, а также при заболеваниях раком, лихорадочных состояниях количество аминокислот в крови возрастает.
Содержание свободных аминокислот в мышечных тканях, мозговых, печени, значительно выше, чем в крови. Связано это с тем, что тканевые клетки активнее концентрируют аминокислоты из среды. Многие аминокислоты применяются в медицине. Это белковые гидролизаты, смеси аминокислот, применяемые в парентеральном питании. Избыток некоторых кислот вызывает токсические явления.
Заменимые, условно незаменимые и незаменимые
Удивительно, но растения и микроорганизмы способны самостоятельно синтезировать все аминокислоты. А вот человек и животные на такое не подписаны.
Заменимые аминокислоты. Производятся нашим организмом самостоятельно. К ним относятся:
- глютаминовая кислота;
- аспарагиновая кислота;
- аспарагин;
- глютамин;
- орнитин;
- пролин;
- аланин;
- глицин.
Условно незаменимые аминокислоты. Наш организм их создает, но не в достаточных количествах. К ним относятся гистидин и аргинин.
Незаменимые аминокислоты. Получить их можно только из добавок или пищевых продуктов. Более подробно о них написано в статье про незаменимые аминокислоты для человека.
Что мы узнали?
Аминокислоты – мономеры, состоящие из водорода, углерода, кислорода и азота. Некоторые соединения могут включать другие элементы, например, серу или фосфор. Для функционирования организма человеку необходимы 22 аминокислоты. При этом не все аминокислоты синтезируются в клетках. В связи с этим выделяют три группы аминокислот: заменимые (десять соединений), незаменимые (восемь) и частично незаменимые (четыре).
ХимияЗаменимые аминокислоты и частично заменимые – список
ХимияНезаменимые аминокислоты списком (химия, 11 класс)
Продукты богатые аминокислотами
Для полноценной работы нашего организма каждому человеку следует знать в каких продуктах содержатся органические соединения:
- Яйца – они подарят нам BCAA, метионин и фенилаланин. Усваиваются на ура гарантируя белковую подкормку для организма.
- Молочные продукты – обеспечивают человека аргинином, валином, лизином, фенилаланином и триптофаном.
- Белое мясо – содержит BCAA, гистидин, лизин, фенилаланин и триптофан.
- Рыба – отличный источник белка, который легко усваивается организмом. Богата метионином, фенилаланином и BCAA.
Многие уверены, что получить белок можно лишь из продуктов животного происхождения. Это неверно. Растительная пища тоже богата им и является источником органических соединений:
СТАТЬИ ПО ТЕМЕ:
- Сколько всего аминокислот, входящих в состав молекулы белка
- Незаменимые аминокислоты для человека: список и в каких продуктах они содержатся
- Для чего нужны аминокислоты при тренировках для женщин
- Бобовые – богаты фенилаланином, лейцином, валином, метионином, триптофан и треонином.
- Крупы – подарят организму лейцин, валин, гистидин и изолейцин.
- Орехи и семена – обеспечивают аргинином, треонином, изолейцином, гистидином и лизином.
Отдельно хочется выделить киноа. Этот злак не так популярен, как привычные нам гречка и пшено, а зря.
Потому что на 100 грамм продукта приходится порядка 14 грамм белка. Поэтому киноа незаменима для вегетарианцев и прекрасно подойдет мясоедам. Не будем также забывать о православных постах, которые несколько раз в год запрещают есть мясо, рыбу и молочную продукцию.
Для удобства я предлагаю ознакомиться со списком продуктов в виде таблицы. Ее можно

.
Заменимые аминокислоты
Аланин
Используется в качестве источника энергии, ускоряя превращение глюкозы в ходе энергетического обмена, а также способствует выведению токсинов из печени. Предотвращает распад мышечной ткани за счет так называемого цикла аланина, который упрощенно можно представить следующим образом: глюкоза – пируват – аланин – пируват – глюкоза. Цикл аланина увеличивает внутриклеточные запасы энергии и тем самым продлевает жизнь клеток. В ходе этого цикла избыток азота удаляется из организма (мочеотделение). Аланин может купировать симптомы, вызванные увеличением предстательной железы.
Источники аланина: мясо, птица, яйца, молочные продукты, рыба и некоторые растительные продукты, например, авокадо.
Аргинин
Одна из важнейших аминокислот в человеческом организме, которая необходима для поддержания здоровья суставов, печени, кожи и мышц. Благодаря восстановительным свойствам может использоваться людьми, страдающими от артрита и других заболеваний суставов. Укрепляет иммунную систему за счет увеличения образования Т-лимфоцитов. Участвует в синтезе креатина и в азотистом обмене, что имеет колоссальное значение для каждого бодибилдера. Также способствует снижению доли жировой ткани в организме и ускоряет заживление поврежденных тканей. Хотя аргинин и образуется в организме, возможность приема аминокислоты с пищевыми добавками следует рассмотреть лицам, страдающим от инфекции или ожогов, а также людям, желающим снизить массу тела, укрепить иммунную систему или набрать мышечную массу.
Естественные источники аргинина: мясо, молочные продукты, пшеница, шоколад, кокос, желатин, овес, арахис, соя и грецкий орех.
Применение: способствует увеличению мышечной массы и уменьшению накопления жира. Источники: цельная пшеница, орехи, семена, рис, шоколад, изюм, и соя.
Аспарагин
Тесно связан с аспарагиновой кислотой, необходим для работы нервной системы, кроме того, наш организм использует эту аминокислоту для синтеза аммиака.
Аспарагин можно найти в продуктах животного и растительного происхождения: говядина, мясо птицы, сыворотка, яйца, рыба, молочные продукты, спаржа, картофель, орехи, семена, цельное зерно.
Аспарагиновая кислота, также известная как L-аспартат
Способствует улучшению обменных процессов и принимает участие в синтезе других аминокислот, в частности, аргинина, лизина и изолейцина. Аспарагиновая кислота имеет большое значение для синтеза клеточной энергии, поскольку принимает участие в образовании аденозинтрифосфата (АТФ) – универсального топлива, которое обеспечивает энергией все внутриклеточные процессы. Поддерживает нервную систему благодаря повышению концентрации никотинамидадениндинуклеотида (NADH), вещества, которое стимулирует продукцию нейромедиаторов и других соединений, необходимых для нормальной работы головного мозга.
Аспарагиновая кислота может синтезироваться в организме, а среди ее источников следует назвать мясо птицы, молочные продукты, говядину и сахарный тростник.
Цистеин
Содержится в бета-кератине – главном структурном белке кожи, ногтей и волос. Лучше всего цистеин усваивается в виде N-ацетил цистеина (NAC). Цистеин может быть эффективен при лечении рака, бронхита, кашля курильщика, кардиологической патологии и септического шока.
Эта аминокислота образуется в организме, однако ее можно также получить из мяса, яиц, брокколи, лука, чеснока и красного перца.
Применение: способствует более быстрому восстановлению и поддержанию хорошей физической формы. Источники: мясо птицы, пшеница, брокколи, яйца, чеснок, лук и перец.
Глютаминовая кислота, также известная как глутамат
Важнейший возбуждающий нейромедиатор головного и спинного мозга. Играет ключевую роль в метаболизме жиров и углеводов, участвует в транспорте калия в спинномозговую жидкость и через гематоэнцефалический барьер. Головной мозг может использовать глютаминовую кислоту в качестве топлива. Может превращаться в глютамин или ГАМК (гамма-аминомасляная кислота).
Глютамин
Помогает создавать и поддерживать мышцы и удалять токсины из печени. Может проникать через гематоэнцефалический барьер и, после превращения в глютаминовую кислоту, выступать в качестве топлива для головного мозга. Также может повышать уровень ГАМК. Глютамин является важнейшим источником энергии для нервной системы. Препараты L-глютамина используются, главным образом, в бодибилдинге, однако на фоне приема глютамина люди также отмечают общий прилив сил и улучшение эмоционального фона. Глютамин образуется путем аминирования (присоединения аминогруппы) глютаминовой кислоты, благодаря чему помогает выводить из печени токсичный аммиак – азот не превращается в аммиак.
Также глютамин помогает транспортировать азот в другие органы и ткани, в особенности в мышцы, где он способствует повышению запасов гликогена. Это имеет большое значение для предупреждения распада мышечной ткани. До 60% аминокислот, содержащихся в мышцах, приходится на глютамин. Также глютамин важен для иммунной системы и может помочь при лечении ревматоидного артрита, хронической усталости и склеродермии.
Глютамин содержится во многих продуктах, однако он быстро разрушается в процессе приготовления. Петрушка и шпинат в сыром виде – отличные источники этой аминокислоты.
Применение: Дополнительный источник энергии во время диеты. Источники: большое количество во всех белковых продуктах.
Глицин
Эта аминокислота помогает строить мышечную ткань, участвует в превращении глюкозы в энергию и повышает уровень креатина, чем способствует набору мышечной массы. Коллаген примерно на 30% состоит из глицина. Фактически, без этой аминокислоты организм не сможет залечивать раны и другие повреждения тканей.
Отличными источниками глицина являются высокобелковые продукты, например, рыба, мясо, молоко, бобы или сыр.
Пролин
Пролин нужен для образования коллагена и хрящевой ткани. Он стимулирует синтез коллагена, что в свою очередь способствует ремоделированию хряща, а потому может оказаться полезным для людей, страдающих от травм и заболеваний суставов. Эта аминокислота ускоряет процессы заживления и успешно применяется в период восстановления после травм, например, после ожогов.
Хорошими источниками пролина являются мясо, молочные продукты и яйца. Вегетарианцам следует рассмотреть возможность приема этой аминокислоты с пищевыми добавками.
Серин
Основная функция серина – поддержание нормального функционирования головного мозга и центральной нервной системы. Белки нервной ткани и ее защитные клетки содержат эту аминокислоту. Также она принимает участие в синтезе серотонина, химического соединения, оказывающего значительное влияние на настроение. Кроме того, серин участвует в метаболизме жиров и жирных кислот и способствует абсорбции креатина.
Мясо, молочные продукты, пшеница (глютен), соя и арахис – примеры хороших источников этой аминокислоты.
Тирозин
Эта аминокислота способствует нормальной работе всего организма. Тирозин помогает контролировать аппетит, а его дефицит чреват снижением артериального давления, замедлением обменных процессов и повышенной утомляемостью. Кроме того, тирозин содействует образованию нейромедиаторов, что имеет большое влияние на взаимодействие человеческого организма с окружающей средой.
Суточная норма потребления аминокислот
Мы каждый день нуждаемся в органических соединениях, но бывают такие периоды в жизни, когда их надобность увеличивается:
- во время занятий спортом;
- в период болезни и выздоровления;
- в период умственных и физических нагрузок.
И, наоборот, бывает, что потребность в них понижается в случае врожденных нарушений, которые связаны с усвояемостью аминокислот.
Следовательно, для комфорта и бесперебойной работы организма следует знать суточную норму потребления органических соединений. Согласно диетологическим таблицам она варьируется от 0,5 грамм до 2 грамм в сутки.
Усвояемость аминокислот зависит от типа тех продуктов, в которых они содержатся. Очень хорошо усваиваются органические соединения из белка яиц.
Тоже самое можно сказать про творог, рыбу и нежирное белое мясо. Также здесь огромную роль играет сочетание продуктов. Например, молоко и гречневая каша. В таком случае человек получает полноценный белок и комфортный для организма процесс его усвоения.
Незаменимые аминокислоты
Незаменимые — это кислоты, которые не могут быть синтезированы в организме. Но они лежат в основе многих жизненно важных процессов, от которых зависит работа организма.
Недостаток их приводит к развитию многих заболеваний, включая нервную, иммунную и пищеварительную системы. Группа незаменимых кислот поступает в организм вместе с пищей. Они содержатся в продуктах растительного и животного происхождения.
Гистидин
Кислота частично заменимая, используется для производства гистамина, который необходим для иммунного ответа, пищеварения, сексуальной функции, ритмичности циклов сна и бодрствования.
Необходим для роста и восстановления тканей, поддерживает производство нервных клеток, которые образуют защитную оболочку вокруг нервов. Является медиатором воспаления, стимулирует секрецию соляной кислоты. Кислоту в виде препарата назначают при язвах и других заболеваниях желудочно-кишечного тракта.
Изолейцин
Кислота, имеющая разветвлённую цепь, участвует в мышечном метаболизме, концентрируется преимущественно в мышечной ткани. Помогает вырабатывать гемоглобин, регулирует энергию, повышает выносливость организма.
Лейцин
Вторая аминокислота с разветвлённой цепью, которая участвует в синтезе белка, восстановлении мышц. Помогает регулировать уровень сахара, стимулирует заживление органов, участвует в выработке гормона роста.
Лизин
Синтезирует белок, участвует в выработке гормонов, ферментов, транспортирует жирные кислоты в клетки. Является составной частью коллагена. Используется в организме для усвоения кальция, поддерживает баланс азота. Положительно влияет на половые функции женщин и мужчин – улучшает эрекцию, повышает либидо.
Метионин
Способствует обмену веществ, детоксикации, необходим для роста тканей. Помогает в усвоении цинка и селена, является составной частью фосфолипидов. Кислота способствует переработке жиров, помогает при токсикозе во время беременности, предупреждает жировые отложения на поверхности печени, почек.
Кислота в виде лекарственного препарата используется при заболеваниях печени, различных формах жирового перерождения печени, отравлениях.
Фенилаланин
Является предшественником дофамина, адреналина, норадреналина. Играет важную роль в структуре и функции белков и ферментов, а также в производстве других аминокислот. В результате химических реакций трансформируется в тирозин, способствует улучшению памяти, снижению аппетита.
Треонин
Является основной частью структурных белков, таких как коллаген и эластин. Они нужны для регенерации кожи, соединительной ткани, обеспечивая её эластичность и упругость. Играет большую роль в жировом обмене и иммунных функциях.
Триптофан
Витамин, является составной частью пуриновых нуклеотидов. Необходим для поддержания правильного азотного баланса, является предшественником серотонина, который регулирует аппетит, сон, настроение. Как биологический предшественник никотиновой кислоты, оказывает терапевтическое действие при пеллагре (разновидность авитаминоза). Нейтрализует вредное воздействие никотина.
Валин
Третья аминокислота с разветвлённой цепью. Помогает стимулировать рост и регенерацию мышц, участвует в производстве энергии.
Нехватка и переизбыток аминокислот
Какие признаки могут означать нехватку органических соединений в организме:
- слабая сопротивляемость инфекциям;
- ухудшение состояния кожи;
- задержка роста и развития;
- выпадение волос;
- сонливость;
- анемия.
Помимо нехватки аминокислот в организме может возникнуть их переизбыток. Его признаки следующие: нарушения в работе щитовидной железы, заболевания суставов, гипертония.
Следует знать, что подобные проблемы могут возникнуть если в организме нехватка витаминов. В случае нормы, избыток органических соединений будет нейтрализован.
В случае нехватки и переизбытка аминокислот очень важно помнить, что определяющим фактором здесь является питание.
Грамотно составляя рацион, вы прокладываете себе путь к здоровью. Отметим, что такие болезни как сахарный диабет, нехватка ферментов или поражение печени. Они ведут к абсолютно неконтролируемому содержанию в организме органических соединений.
Функции аминокислот в организме
Аминокислоты незаменимые и заменимые необходимы не только для строительства белковых молекул, они выполняют и другие функции:
- Участвуют в формировании других аминокислот.
- Принимают участие в образовании гормонов, медиаторов и нейротрансмиттеров.
- Входят в состав природных соединений: желчных кислот, коферментов, антибиотиков.
- Являются источниками метаболитов, участвующих в обмене веществ.
- Поддерживают умственную активность человека.
- Восстанавливают ткани после повреждений.
- Регулируют работу центральной нервной системы.
- Отвечают за гормональный фон.
Аминокислоты участвуют почти во всех процессах, происходящих в организме.
Популярные классификации
В научном мире для систематизации аминокислот используют разные параметры. Существует несколько классификаций, применяемых для этих веществ. Как уже отмечалось, различают заменимые и незаменимые аминокислоты. Меж тем, эта классификация не отражает объективной степени важности каждого из названных веществ, так как все аминокислоты – значимы для человеческого организма.
Другие наиболее популярные классификации

Учитывая радикалы, аминокислоты делятся на:
- неполярные (аланин, валин, изолейцин, лейцин, метионин, пролин, триптофан, фенилаланин);
- полярные незаряженные (аспарагин, глутамин, серин, тирозин, треонин, цистеин);
- полярные с отрицательным зарядом (аспартат, глутамат);
- полярные с положительным зарядом (аргинин, лизин, гистидин).
Учитывая функциональность группы:
- ароматические (гистидин, тирозин, триптофан, фенилаланин);
- гетероциклические (гистидин, пролин, триптофан);
- алифатические (в свою очередь создают еще несколько подгрупп);
- иминокислота (пролин).
Учитывая биосинтетические семейства аминокислот:
- семейство пентоз;
- семейство пирувата;
- семейство аспартата;
- семейство серина;
- семейство глутамата;
- семейство шикимата.
Согласно иной классификации различают 5 видов аминокислот:
- серосодержащие (цистеин, метионин);
- нейтральные (аспарагин, серин, треонин, глутамин);
- кислые (глутаминовая кислота, аспарагиновая кислота) и основные (аргинин, лизин);
- алифатические (лейцин, изолейцин, глицин, валин, аланин);
- ароматические (фенилаланин, триптофан, тирозин).
Помимо того, есть вещества, биологические свойства которых очень напоминают аминокислоты, хотя на самом деле они таковыми не являются. Яркий пример – таурин, названный аминокислотой не совсем верно.
Аминокислоты для бодибилдеров

Своя классификация аминокислот существует и у бодибилдеров. В спортивном питании применяют 2 вида питательных веществ: свободные аминокислоты и гидролизаты. К первым принадлежат глицин, глутамин, аргинин, которые характеризуются максимальной скоростью транспортировки. Вторая группа – это протеины, расщепленные к уровню аминокислот. Такие вещества усваиваются организмом значительно быстрее, чем обычные белки, а значит, и мышцы получают свою «порцию» протеинов быстрее.
Также для бодибилдеров особое значение имеют незаменимые аминокислоты. Они важны для поддержания формы мышечной ткани. А поскольку организм не в состоянии синтезировать их самостоятельно, для культуристов важно включать в рацион большое количество мясо-молочной продукции, сою и яйца. Кроме того, желающие нарастить мускулатуру прибегают к биодобавкам, содержащим аминокислоты.
Для здоровья и красоты
Помимо того, что аминокислоты играют важную роль в синтезе ферментов и белков, они важны для здоровья нервной и мышечной систем, для выработки гормонов, а также поддержания структуры всех клеток в организме.
А для бодибилдеров аминокислоты являются одним из самых значимых веществ, так как способствуют восстановлению организма. Будучи основой для протеинов, аминокислоты являются незаменимыми веществами для красивых мускул. Эти полезные элементы помогают сделать тренировки более эффективными, а после занятий избавляют от болезненных ощущений. В качестве биодобавок предотвращают разрушение мышечных тканей и являются идеальным дополнением к белковой диете. Также в функции аминокислот входит сжигание жира и подавление чрезмерного аппетита.
Особенности строения природных аминокислот
Строение аминокислот тесно связано с их функциями. Сходные по химической структуре вещества делают сходную работу. Попробуем разобраться, чтобы потом не путаться в аннотациях к препаратам.
Все аминокислоты слеплены по одному лекалу.
Голова – аминный остаток, содержащий азот N.
Углеродный скелет, состоящий из цепочки атомов углерода (в простейшем случае – один углерод, к которому «спереди» прицеплен аминный остаток, а сзади – карбоновый хвост)
Хвост – остаток карбоновой кислоты – СООН
Сбоку к углеродному скелету может быть присоединена еще какая-нибудь химическая группировка, которая придает данному веществу особые свойства.
Углеродная цепочка вместе с кислотным хвостом, присоединенная к аминной голове, называется мудреным словом «алифатический радикал».
Какие бывают аминокислоты?
Соединений, из которых образуются белки, всего в природе двадцать одно. Некоторые из них человеческий организм способен синтезировать в ходе метаболизма (обмена веществ), а другие — нет. Вообще, в природе существуют такие аминокислоты: гистидин, валин, лизин, изолейцин, лейцин, треонин, метионин, фенилаланин, триптофан, цистеин, тирозин, аргинин, аланин, глутамин, аспарагин, глицин, пролин, карнитин, орнитин, таурин, серин. Первые девять из перечисленных выше аминокислот являются незаменимыми. Также существуют условнонезаменимые — те, которые организм может использовать вместо незаменимых в крайних случаях. Это, к примеру, тирозин и цистеин. Первая может быть использована вместо фенилаланина, а вторая — если нет метионина. Незаменимые аминокислоты в продуктах — обязательное условие здорового питания.
Вред, побочные эффекты, противопоказания
Нужно знать не только, сколько аминокислот должно поступать с пищей, но и чем они опасны. В допустимых дозировках эти вещества не могут навредить человеку.
Нехватка и переизбыток
Признаками избытка кислот в организме являются:
- психические нарушения (тревога, возбудимость);
- низкая устойчивость к стрессу;
- повышение уровня общего холестерина в крови;
- нарушение стула по типу диареи;
- желчная колика (в результате образования камней в желчном пузыре);
- артериальная гипертензия;
- дисфункция щитовидной железы;
- тошнота;
- мигрень;
- учащенное мочеиспускание (поллакиурия);
- галлюцинации;
- головокружение;
- рвота;
- боль в правом подреберье (в результате воспаления печени);
- дисфункция поджелудочной железы (для аминокислоты аргинин).
вещество имеет противопоказание к приему и при злоупотреблении возможно появление побочных эффектов
В случае употребления таблетированных препаратов, порошков или капсул иногда наблюдаются следующие нежелательные реакции:
- частый жидкий стул;
- вздутие живота;
- дезориентация;
- учащенное сердцебиение;
- падение артериального давления;
- аллергия (сыпь на коже, зуд, покраснение);
- тошнота;
- рвота.
Противопоказаниями к приему в качестве добавки кислот могут быть:
- Заболевания печени (вирусный и другие формы гепатита, цирроз, гепатоз, печеночная недостаточность).
- Печеночная энцефалопатия.
- Индивидуальная непереносимость компонентов препарата.
- Возраст. Таблетки с метионином нельзя принимать детям младше 6 лет.
- Наличие сахарного диабета (для фенилаланина).
- Беременность.
- Заболевания почек.
рацион питания, обогащённый белками, обладает биологической ценностью для человека