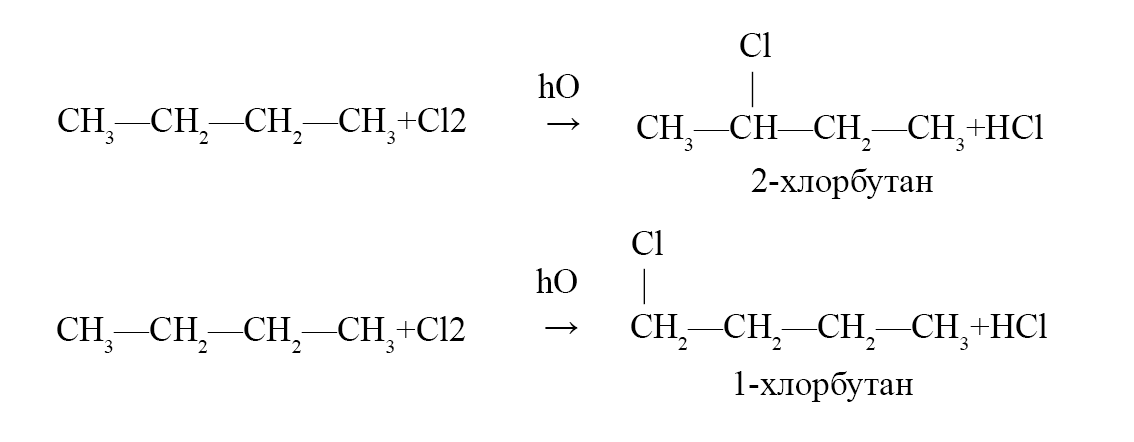- 1. Напишите уравнение реакции монобромирования этана.
- 2. Напишите уравнения реакций, которые протекают при взаимодействии н-бутана с хлором. Считайте, что только один атом водорода в молекуле н-бутана замещается на хлор. Подпишите названия образующихся органических веществ.
- 3. Сколько хлорпроизводных можно получить в результате хлорирования этана? Напишите уравнения реакций получения всех возможных хлорпроизводных этана, назовите хлорпроизводные. Можно ли при записи уравнений реакций в данном случае использовать молекулярные формулы?
- Please wait.
- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Бутан: способы получения и химические свойства
- Гомологический ряд бутана
- Строение бутана
- Изомерия бутана
- Структурная изомерия
- Химические свойства бутана
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование бутана
- 2. Дегидрирование бутана
- 3. Окисление бутана
- 3.1. Полное окисление – горение
- 3.2. Каталитическое окисление
- 4. Изомеризация бутана
- Получение бутана
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 3. Гидрирование алкенов и алкинов
- 4. Синтез Фишера-Тропша
- 5. Получение бутана в промышленности
1. Напишите уравнение реакции монобромирования этана.
C H 3 − C H 3 + B r 2 → h v C H 3 − C H 2 B r + H B r mathrm<CH_3CH_3Br_2<xrightarrow>CH_3CH_2BrHBr> C H 3 − C H 3 + B r 2 h v
C H 3 − C H 2 B r + H B r
2. Напишите уравнения реакций, которые протекают при взаимодействии н-бутана с хлором. Считайте, что только один атом водорода в молекуле н-бутана замещается на хлор. Подпишите названия образующихся органических веществ.
3. Сколько хлорпроизводных можно получить в результате хлорирования этана? Напишите уравнения реакций получения всех возможных хлорпроизводных этана, назовите хлорпроизводные. Можно ли при записи уравнений реакций в данном случае использовать молекулярные формулы?
Можно получить 9 хлорпроизводных:
1) C H 3 − C H 3 + C l 2 → h v C H 3 − C H 2 C l + H C l mathrm<CH_3CH_3Cl_2<xrightarrow>CH_3CH_2ClHCl> C H 3 − C H 3 + C l 2 h v
C H 3 − C H 2 C l + H C l (хлорэтан)
2) C H 3 − C H 3 + 2 C l 2 → h v C H 3 − C H C l 2 + 2 H C l mathrm<CH_3CH_32Cl_2<xrightarrow>CH_3CHCl_22HCl> C H 3 − C H 3 + 2 C l 2 h v
C H 3 − C H C l 2 + 2 H C l (1,1-дихлорэтан)
3) C H 3 − C H 3 + 2 C l 2 → h v C H 2 C l − C H 2 C l + 2 H C l mathrm<CH_3CH_32Cl_2<xrightarrow>CH_2ClCH_2Cl2HCl> C H 3 − C H 3 + 2 C l 2 h v
C H 2 C l − C H 2 C l + 2 H C l (1,2-дихлорэтан)
4) C H 3 − C H 3 + 3 C l 2 → h v C H 3 − C C l 3 + 3 H C l mathrm<CH_3CH_33Cl_2<xrightarrow>CH_3CCl_33HCl> C H 3 − C H 3 + 3 C l 2 h v
C H 3 − C C l 3 + 3 H C l (1,1,1-трихлорэтан)
5) C H 3 − C H 3 + 3 C l 2 → h v C H C l 2 − C H 2 C l + 3 H C l mathrm<CH_3CH_33Cl_2<xrightarrow>CHCl_2<C_2>Cl3HCl> C H 3 − C H 3 + 3 C l 2 h v
C H C l 2 − C H 2 C l + 3 H C l (1,1,2-трихлорэтан)
6) C H 3 − C H 3 + 4 C l 2 → h v C H 2 C l − C C l 3 + 4 H C l mathrm<CH_3CH_34Cl_2<xrightarrow><C_2>ClCCl_34HCl> C H 3 − C H 3 + 4 C l 2 h v
C H 2 C l − C C l 3 + 4 H C l (1,1,1,2-тетрахлорэтан)
7) C H 3 − C H 3 + 4 C l 2 → h v C H C l 2 − C H C l 2 + 4 H C l mathrm<CH_3CH_34Cl_2<xrightarrow>CHCl_2CHCl_24HCl> C H 3 − C H 3 + 4 C l 2 h v
C H C l 2 − C H C l 2 + 4 H C l (1,1,2,2=тетрахлорэтан)
8) C H 3 − C H 3 + 5 C l 2 → h v C H C l 2 − C C l 3 + 5 H C l mathrm<CH_3CH_35Cl_2<xrightarrow>CHCl_2CCl_35HCl> C H 3 − C H 3 + 5 C l 2 h v
C H C l 2 − C C l 3 + 5 H C l (пентахлорэтан)
9) C H 3 − C H 3 + 6 C l 2 → h v C C l 3 − C C l 3 + 6 H C l mathrm<CH_3CH_36Cl_2<xrightarrow>CCl_3CCl_36HCl> C H 3 − C H 3 + 6 C l 2 h v
C C l 3 − C C l 3 + 6 H C l (гексахлорэтан)
При записи уравнений реакций 2-7 нельзя использовать молекулярные формулы.
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 703405bfab711e71 • Your IP : 87.119.247.227 • Performance & security by Cloudflare
Бутан: способы получения и химические свойства
Бутан C4H10 – это предельный углеводород, содержащий четыре атома углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, нерастворим в воде и не смешивается с ней.
Гомологический ряд бутана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение бутана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :
При образовании связи С–С происходит перекрывание sp 3 -гибридных орбиталей атомов углерода:
При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:
Это соответствует тетраэдрическому строению.
| Например, в молекуле бутана C4H10 атомы водорода располагаются в пространстве в вершинах тетраэдров, центрами которых являются атомы углерода. При этом углеродный скелет имеет зигзагообразное строение. |
Изомерия бутана
Структурная изомерия
Для бутана характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
| Например. Для н-бутана (алкана с линейной цепью) существует изомер с разветвленным углеродным скелетом – изобутан |
| Бутан | Изобутан |
 |  |
Для бутана не характерна пространственная изомерия.
Химические свойства бутана
Бутан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для бутана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для бутана характерны радикальные реакции.
Бутан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Бутан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании бутана образуется смесь хлорпроизводных.
| Например, при хлорировании бутана образуются 1-хлорбутан и 2-хлорбутан: Бромирование протекает более медленно и избирательно.
|