Карбонат кальция CaCO3 — соль кальция и угольной кислоты. Белый, при прокаливании разлагается, плавится без разложения под избыточным давлением CO2. Практически не растворяется в воде.
Относительная молекулярная масса Mr = 100,09; относительная плотность для тв. и ж. состояния d= 2,93; tпл = 1242º C при избыточном давлении.
Видео:Решение задач на термохимические уравнения. 8 класс.Скачать

Способ получения
1. Карбонат кальция можно получить путем взаимодействия хлорида кальция и карбоната кальция , образуется карбонат кальция и хлорид натрия:
2. В результате взаимодействия при комнатной температуре оксида кальция и углекислого газа происходит образование карбоната кальция:
3. Гидроксид кальция вступает в взаимодействие с углекислым газом и образует карбонат кальция и воду:
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Качественная реакция
Качественная реакция на карбонат кальция — взаимодействие его с раствором сильных кислот. В результате реакции происходит бурное выделение углекислого газа, образование которого можно проверить, если пропустить его через известковую воду, которая мутнеет из-за образования осадка:
1. При взаимодействии с хлороводородной кислотой, карбонат кальция образует хлорид кальция, углекислый газ и воду:
Видео:РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

Химические свойства
1. Карбонат кальция разлагается при температуре выше 900 — 1200º С, с образованием оксида кальция и углекислого газа:
2. Карбонат кальция вступает в реакцию со многими сложными веществами :
2.1. Карбонат кальция реагирует с оксидами :
2.1.1. Карбонат лития вступает в взаимодействие с оксидом кремния при 800º С и образует на выходе силикат кальция и углекислый газ:
2.2. Карбонат кальция реагирует с кислотами :
2.2.1. При взаимодействии с разбавленной хлороводородной кислотой карбонат кальция образует хлорид кальция, углекислый газ и воду:
2.2.2. Карбонат кальция реагирует с разбавленной плавиковой кислотой . Взаимодействие карбоната кальция с плавиковой кислотой приводит к образованию фторида кальция, воды и углекислого газа:
2.2.3. Карбонат кальция взаимодействует с сероводородной кислотой при 900º С и образует сульфид кальция, воду и углекислый газ:
3. Карбонат кальция реагирует с простыми веществами:
3.1. Карбонат кальция при 800 — 850º С вступает в реакцию с углеродом (коксом) образуя оксид кальция и угарный газ:
CaCO3 + C = CaO + 2CO
Видео:Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Подготовка к ЕГЭ по ХимииСкачать

Составьте молекулярное уравнение реакции получения карбоната кальция укажите происходит ли в ходе
1) Составьте молекулярное уравнение реакции карбоната кальция с соляной кислотой, о которой говорилось в тексте;
2) Укажите признак, который наблюдается при протекании этой реакции.
Прочитайте следующий текст и выполните задания 5—7.
Карбонат кальция в природе встречается в виде минералов — кальцита, арагонита и витерита, является главной составной частью известняка, мрамора, мела, входит в состав скорлупы яиц. Получить карбонат кальция можно при пропускании углекислого газа
через избыток раствора гидроксида кальция
. Эту реакцию используют для обнаружения углекислого газа и определении его количественного содержания в воздухе. Нерастворимый в воде карбонат кальция может растворяться в кислотах, например в соляной кислоте
. Карбонат кальция используется как белый пищевой краситель Е170. Являясь основой мела, он используется для письма на школьных досках, используется в быту для побелки потолков, покраски стволов деревьев, для подщелачивания почвы в садоводстве. Кроме того, карбонат кальция является важнейшим компонентом продукции бытовой химии — средств для чистки сантехники, кремов для обуви.
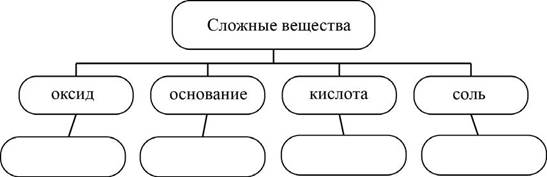
Сложные неорганические вещества можно классифицировать по четырём группам, как показано на схеме. В эту схему для каждой из четырёх групп впишите по одной химической формуле веществ из числа тех, о которых говорится в приведённом тексте.
| оксид | основание | кислота | соль |
Химические формулы запишите в таблицу в следующем формате: Al2(SO4)3.
1. — бинарное соединение, в котором один из атомов является кислородом, что говорит о его принадлежности к классу оксидов.
2. — является основанием, так как это основный гидроксид.
3. Кислота должна иметь ион водорода, примером может служить соляная кислота .
4. Соль состоит из иона металла и иона кислотного остатка, известным примером является карбонат кальция
Ответ: Оксид — , основание —
, кислота —
, соль —
.
Видео:ТИПОВЫЕ ЗАДАЧИ ПО ХИМИИ: Химическое Количество Вещества, Моль, Молярная Масса и Молярный ОбъемСкачать

Для выполнения заданий 5–7 необходимо использовать информацию, которая содержится в приведённом ниже тексте.
Карбонат кальция (CaCO3) в природе встречается в виде минералов – кальцита, арагонита и витерита, является главной составной частью известняка, мрамора, мела, входит в состав скорлупы яиц.
Получить карбонат кальция можно при пропускании углекислого газа (CO2) через избыток раствора гидроксида кальция (Ca(OH)2). Эту реакцию используют для обнаружения углекислого газа и определения его количественного содержания в воздухе.
Нерастворимый в воде карбонат кальция может растворяться в кислотах, например в соляной кислоте (HCl).
Карбонат кальция используется как белый пищевой краситель Е170. Являясь основой мела, он используется для письма на школьных досках, используется в быту для побелки потолков, покраски стволов деревьев, для подщелачивания почвы в садоводстве. Кроме того, карбонат кальция является важнейшим компонентом продукции бытовой химии – средств для чистки сантехники, кремов для обуви.
Сложные неорганические вещества можно классифицировать по четырём группам, как показано на схеме. В эту схему для каждой из четырёх групп впишите по одной химической формуле веществ из числа тех, о которых говорится в приведённом выше тексте.
1. Составьте молекулярное уравнение реакции получения карбоната кальция. Ответ:
2. Укажите, происходит ли в ходе этой реакции изменение степеней окисления атомов. Ответ:

© 2018 Федеральная служба по надзору в сфере образования и науки Российской Федерации 4
| ВПР. Химия. 11 класс. Вариант 10 | Код |
7 1. Составьте молекулярное уравнение реакции карбоната кальция с соляной кислотой,
о которой говорилось в тексте. Ответ:
2. Укажите признак, который наблюдается при протекании этой реакции.

8При исследовании минерализации бутилированной воды в ней были обнаружены следующие анионы: Cl – , F – , NO3 – . Наличие одного из перечисленных ионов было доказано в результате добавления к воде раствора AgNO3.
1. Какое изменение наблюдается при проведении описанного опыта? (Концентрация веществ достаточна для проведения анализа.)
2. Запишите сокращённое ионное уравнение протекающей химической реакции. Ответ:
9Дана схема окислительно-восстановительной реакции:
KI + Cl2 + H2O → KIO3 + HCl
1. Составьте электронный баланс этой реакции. Ответ:
2. Укажите окислитель и восстановитель. Ответ:
3. Расставьте коэффициенты и запишите получившееся уравнение реакции. Ответ:


10Дана схема превращений:
Al → Al2(SO4)3 → Al(OH)3 → AlCl3
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения.
© 2018 Федеральная служба по надзору в сфере образования и науки Российской Федерации 5
| ВПР. Химия. 11 класс. Вариант 10 | Код | |||||||
| Для выполнения заданий 11–13 используйте вещества, структурные формулы которых | ||||||||
| приведены ниже: | ||||||||
| 1) CH3 | CH2 | OH | 2) CH2 | CH2 | 3) CH | CH | ||
| 4) CH2 | CH | CH | CH2 | 5) CH | CH | CH | C | O |
| OH | ||||||||
| 11Из приведённого | перечня выберите | вещества, | которые | соответствуют указанным |






в таблице классам/группам органических соединений. Запишите номера этих веществ
в соответствующую графу таблицы.
| Алкадиен | Карбоновая кислота |




12В предложенные схемы химических реакций впишите структурные формулы пропущенных веществ, выбрав их из приведённого выше перечня, и расставьте коэффициенты.
| 1) . | + H2 | Pt | CH3 | CH2 | CH2 | CH3 |
| 2) . | + Na | CH3 | CH | ONa + H2 | ||
| 13Уксусный | альдегид – летучая | жидкость | с фруктовым запахом. Его используют |




в производстве уксусной кислоты, некоторых полимеров. В лабораторных условиях уксусный альдегид можно получить в соответствии с приведённой схемой превращений:
| СaC | H2O | X | CH | C O |
| H |



Выберите из предложенного перечня вещество Х и запишите уравнения двух реакций,
с помощью которых можно осуществить эти превращения. При написании уравнений реакций используйте структурные формулы органических веществ.
Запишите название вещества X.
© 2018 Федеральная служба по надзору в сфере образования и науки Российской Федерации 6
| ВПР. Химия. 11 класс. Вариант 10 | Код |
14Одним из важных понятий в экологии и химии является «предельно допустимая концентрация» (ПДК). ПДК – это такая концентрация вредного вещества в окружающей
среде, присутствуя в которой постоянно, данное вещество не оказывает в течение всей жизни прямого или косвенного неблагоприятного влияния на настоящее или будущее поколение , не снижает работоспособности человека, не ухудшает его самочувствия и условий жизни.
ПДК хлора в воздухе составляет 0,03 мг/м 3 .
В помещении столовой площадью 32 м 2 и высотой потолка 3 м при влажной уборке
с использованием хлорсодержащих дезинфицирующих средств в воздух выделилось 2,4 мг хлора. Определите и подтвердите расчётами, превышает ли концентрация хлора в воздухе данного помещения значение ПДК. Предложите способ, позволяющий снизить концентрацию хлора в помещении.


15Для борьбы с заболеваниями садово-огородных культур используют 3%-ный раствор перманганата калия. Рассчитайте массу перманганата калия и массу воды, которые необходимы для приготовления 5 кг такого раствора. Запишите подробное решение задачи.

© 2018 Федеральная служба по надзору в сфере образования и науки Российской Федерации 7
📽️ Видео
Получение ОКСИДА КАЛЬЦИЯ. Разложение КАРБОНАТА КАЛЬЦИЯ ( МЕЛА). Реакция с водой. Опыты по химииСкачать

Молярная масса. 8 класс.Скачать

Взаимодействие карбоната кальция с соляной кислотой I ЕГЭ по химииСкачать

ХИМИЯ С НУЛЯ — Как решать задачи по Химии на Массовую ДолюСкачать

Практическая работа №5. Получение углекислого газа, качественная реакция на карбонат ионыСкачать

Опыты по химии. Разложение карбоната кальция при нагреванииСкачать

8 класс. Массовая доля растворенного вещества. Решение задач.Скачать

Получение Карбоната Кальция - чистого мела. CaCO3.Скачать

Расстановка Коэффициентов в Химических Реакциях // Подготовка к ЕГЭ по ХимииСкачать

Как расставлять коэффициенты в уравнении реакции? Химия с нуля 7-8 класс | TutorOnlineСкачать

Как за 4 МИНУТЫ выучить Химию? Химическое Количество, Моль и Закон АвогадроСкачать

Химические уравнения - Как составлять уравнения реакций // Составление Уравнений Химических РеакцийСкачать

Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Химия ПростоСкачать

Химия ЕГЭ 2022 / Задание 28Скачать

Химия. 7 класс. Реакции разбавленных кислот с карбонатами /02.02.2021/Скачать