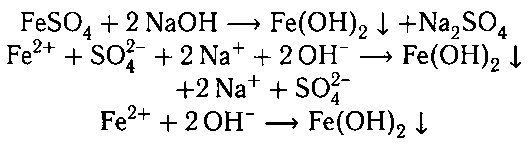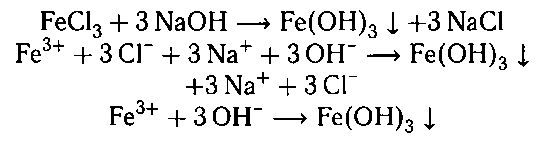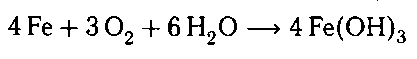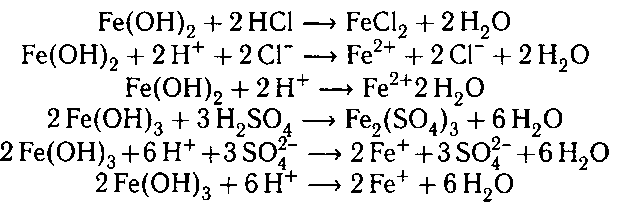1) Составьте молекулярное уравнение реакции гидроксида железа (II) с соляной кислотой, о которой говорилось в тексте;
2) Укажите признак, который наблюдается при протекании этой реакции.
Прочитайте следующий текст и выполните задания 5—7.
Железо это блестящий, серебристо-белый, мягкий металл, с давних пор широко применяемый человеком. Известно большое количество руд и минералов, содержащих железо. Наибольшее практическое значение имеют красный железняк магнитный железняк
сидерит
мелантерит
вивианит
Свойства соединений железа в значительной степени зависят от степени окисления железа. Так, в степени окисления +2 железо образует оксид
который проявляет основные свойства, ему соответствует гидроксид
Эти соединения способны реагировать с растворами сильных кислот, например с соляной кислотой (
) с образование хлорида железа (II)
Железо один из самых используемых металлов, на него приходится до 95% мирового металлургического производства. Железо является основным компонентом сталей и чугунов важнейших конструкционных материалов.
Сложные неорганические вещества можно классифицировать по четырём группам, как показано на схеме. В эту схему для каждой из четырёх групп впишите по одной химической формуле веществ из числа тех, о которых говорится в приведённом тексте.
| оксид | основание | кислота | соль |
Химические формулы запишите в таблицу в следующем формате: Al2(SO4)3.
1. Оксид бинарное соединение, в котором один из атомов является кислородом в степени окисления −2. Из предложенных соединений оксидами являются и
2. — является основанием, так как это основный гидроксид.
3. Кислота должна иметь ион водорода, примером может служить соляная кислота
4. Соль состоит из иона металла и иона кислотного остатка, примерами являются и
Ответ: Оксид или
или
основание
кислота
соль
или
или
или
Гидроксид железа (II)
Гидроксид железа (II)
Способы получения
1. Гидроксид железа (II) можно получить действием раствора аммиака на соли железа (II).
Например , хлорид железа (II) реагирует с водным раствором аммиака с образованием гидроксида железа (II) и хлорида аммония:
2. Гидроксид железа (II) можно получить действием щелочи на соли железа (II).
Например , хлорид железа (II) реагирует с гидроксидом калия с образованием гидроксида железа (II) и хлорида калия:
FeCl2 + 2KOH → Fe(OH)2↓ + 2KCl
Химические свойства
1. Гидроксид железа (II) проявляется основные свойства , а именно реагирует с кислотами . При этом образуются соответствующие соли.
Например , гидроксид железа (II) взаимодействует с соляной кислотой с образованием хлорида железа (II):
2. Гидроксид железа (II) взаимодействует с кислотными оксидами сильных кислот .
Например , гидроксид железа (II) взаимодействует с оксидом серы (VI) с образованием сульфата железа (II):
3. Гидроксид железа (II) проявляет сильные восстановительные свойства , и реагирует с окислителями. При этом образуются соединения железа (III) .
Например , гидроксид железа (II) взаимодействует с кислородом в присутствии воды:
Гидроксид железа (II) взаимодействует с пероксидом водорода:
При растворении Fe(OH)2 в азотной или концентрированной серной кислотах образуются соли железа (III):
4. Г идроксид железа (II) разлагается при нагревании :
Лабораторные опыты 18 и 19 Химия 9 класс Рудзитис, Фельдман
Кто сделал лабы?
Получение гидроксида железа(II) и взаимодействие его с кислотами.
1. Налейте в пробирку 2—3 мл свежеприготовленного раствора сульфата железа(II) и добавьте немного раствора гидроксида натрия. 2. К полученному осадку добавьте немного соляной кислоты.
Получение гидроксида железа(III) и взаимодействие его с кислотами.
1. Налейте в пробирку 2—3 мл раствора хлорида железа(III) и добавьте немного раствора гидроксида натрия. 2. К полученному осадку добавьте немного серной кислоты.
Задания.
1. Как получают гидроксид железа(II) и гидроксид железа(III)?
2. Какого цвета полученные осадки? 3. Какие вещества образуются при взаимодействии полученных осадков с кислотами? 4. Напишите уравнения соответствующих реакций в молекулярном, ионном и сокращенном ионном виде. 5. Как можно определить ионы железа Fе2+ и Fе3+?
Получение гидроксида железа(II) и взаимодействие его с кислотами.
Получение гидроксида железа(III) и взаимодействие его с кислотами.
1. Гидроксид железа (II) получают действием
щелочей на водные растворы солей железа (II):
Гидроксид железа (III) получают взаимодействи-
ем солей железа (III) со щелочами:
Также можно получить взаимодействием чисто-
го железа при нагревании с водой в присутствии
кислорода воздуха:
3. Гидроксид железа (II) зеленого цвета, гид-
роксид железа (III) бурого цвета.
4. При взаимодействии полученных осадков с
кислотами получаются соли железа:
5. Ионы Fe 2+ от Fe 3 + можно отличить по цвету их
гидроксидов: зеленого Fe(OH)2, бурого — Fe(OH)3.