Оксид углерода (II)
Строение молекулы и физические свойства
Оксид углерода (II) («угарный газ») – это газ без цвета и запаха. Сильный яд. Небольшая концентрация угарного газа в воздухе может вызвать сонливость и головокружение. Большие концентрации угарного газа вызывают удушье.
Строение молекулы оксида углерода (II) – линейное. Между атомами углерода и кислорода образуется тройная связь, за счет дополнительной донорно-акцепторной связи:
Способы получения
В лаборатории угарный газ можно получить действием концентрированной серной кислоты на муравьиную или щавелевую кислоты:
НСООН → CO + H2O
В промышленности угарный газ получают в газогенераторах при пропускании воздуха через раскаленный уголь:
CO2 + C → 2CO
Еще один важный промышленный способ получения угарного газа — паровая конверсия метана. При взаимодействии перегретого водяного пара с метаном образуется угарный газ и водород:
Также возможна паровая конверсия угля:
C 0 + H2 + O → C +2 O + H2 0
Угарный газ в промышленности также можно получать неполным окислением метана:
Химические свойства
Оксид углерода (II) – несолеобразующий оксид . За счет углерода со степенью окисления +2 проявляет восстановительные свойства.
1. Угарный газ горит в атмосфере кислорода . Пламя окрашено в синий цвет:
2. Оксид углерода (II) окисляется хлором в присутствии катализатора или под действием света с образованием фосгена. Фосген – ядовитый газ.
3. Угарный газ взаимодействует с водородом при повышенном давлении . Смесь угарного газа и водорода называется синтез-газ. В зависимости от условий из синтез-газа можно получить метанол, метан, или другие углеводороды.
Например , под давлением больше 20 атмосфер, при температуре 350°C и под действием катализатора угарный газ реагирует с водородом с образованием метанола:
4. Под давлением оксид углерода (II) реагирует с щелочами. При этом образуется формиат – соль муравьиной кислоты.
Например , угарный газ реагирует с гидроксидом натрия с образованием формиата натрия:
CO + NaOH → HCOONa
5. Оксид углерода (II) восстанавливает металлы из оксидов .
Например , оксид углерода (II) реагирует с оксидом железа (III) с образованием железа и углекислого газа:
Оксиды меди (II) и никеля (II) также восстанавливаются угарным газом:
СО + CuO → Cu + CO2
СО + NiO → Ni + CO2
6. Угарный газ окисляется и другими сильными окислителями до углекислого газа или карбонатов.
Например , пероксидом натрия:
Составьте молекулярное уравнение реакции гематита с оксидом углерода 2
1) Составьте молекулярное уравнение реакции магнетита с оксидом углерода (II);
2) Укажите, является ли эта реакция окислительно-восстановительной или она протекает без изменения степеней окисления.
Прочитайте следующий текст и выполните задания 5—7.
Металл железо известен человеку ещё с глубокой древности. Использовать изделия из него начали ещё в начале 1-го тысячелетия до н. э. В Древнем Египте железо называли «небесный металл», его древнегреческое название означает «звёздный», а древнеримское переводится как «капнувший с неба». Такое название металла объяснялось очень просто: в древности люди не умели добывать соединения железа и получать из них металл, а использовали только метеоритное железо, то есть буквально железо, упавшее с неба. Широкое использование железа не прекращается и в настоящее время. Известно, что в самородном виде в природе железо практически не встречается, однако его соединения, такие как гематит , магнетит
и пирит, широко распространены. Из этих соединений металл и получают в настоящее время. Один из способов получения железа заключается в восстановлении его оксида под действием оксида углерода (II)
при высокой температуре. В чистом виде железо представляет собой серебристо-серый тугоплавкий металл, обладающий превосходными механическими свойствами: большой прочностью и способностью прокатываться, протягиваться и штамповаться. В основном этот металл используют в виде сплавов — чугуна, стали и др. Взаимодействие железа и оксидов железа с кислотами (например,
) приводит к образованию солей, которые также широко применяются. Так, например хлорид железа (III)
используется при окрашивании тканей, при производстве красящих пигментов, в качестве коагулянта при очистке воды. Сульфат железа (II)
используется при окрашивании ткани и шерсти, в сельском хозяйстве и в медицине. При взаимодействии сульфата железа (II) с гидроксидом натрия
образуется гидроксид железа (II)
. Это соединение используется при изготовлении железо-никелевых аккумуляторов.
Сложные неорганические вещества можно классифицировать по четырём группам, как показано на схеме. В эту схему для каждой из четырёх групп впишите по одной химической формуле веществ из числа тех, о которых говорится в приведённом тексте.
| оксид | основание | кислота | соль |
Химические формулы запишите в таблицу в следующем формате: Al2(SO4)3.
1. — бинарное соединение, в котором один из атомов является кислородом, что говорит о его принадлежности к классу оксидов.
2. — является основанием, так как это основный гидроксид.
3. Кислота должна иметь ион водорода, примером может служить соляная кислота .
4. Соль состоит из иона металла и иона кислотного остатка, известным примером является хлорид железа (III) .
Ответ: Оксид — , основание —
, кислота —
, соль —
.
Возможны также другие варианты ответа для граф «оксид» , «основание»
«кислота»
и «соль»
ВПР по химии 11 класс
Всероссийская проверочная работа по химии.
Просмотр содержимого документа
«ВПР по химии 11 класс»
Из курса химии Вам известны следующие способы разделения смесей: отстаивание, фильтрование, дистилляция (перегонка), действие магнитом, выпаривание, кристаллизация. На рисунках 1–3 представлены примеры использования некоторых из перечисленных способов.
Какие из названных способов разделения смесей можно применить для очищения:
1) смеси железного и алюминиевого порошка;
Запишите в таблицу номер рисунка и название соответствующего способа разделения смеси.
Способ разделения смеси
Смеси железного и алюминиевого порошка
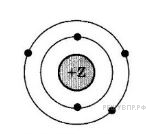
На рисунке изображена модель электронного строения атома некоторого химического элемента.
На основании анализа предложенной модели выполните следующие задания:
1) определите химический элемент, атом которого имеет такое электронное строение;
2) укажите номер периода и номер группы в Периодической системе химических элементов Д. И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот химический элемент.
Ответы запишите в таблицу.
Периодическая система химических элементов Д. И. Менделеева — богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений, о закономерностях изменения этих свойств, о способах получения веществ, а также о нахождении их в природе. Например, известно, что с увеличением порядкового номера химического элемента в периодах электроотрицательность атомов увеличивается, а в группах — уменьшается.
Учитывая эти закономерности, расположите в порядке уменьшения электроотрицательности следующие элементы: 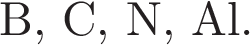
В ответе укажите обозначения элементов разделяя &. Например, 11&22.
В приведённой ниже таблице перечислены характерные свойства веществ, которые имеют молекулярное и ионное строение.
Характерные свойства веществ
— при обычных условиях имеют жидкое, газообразное и твёрдое агрегатное состояние;
— имеют низкие значения температур кипения и плавления;
— имеют низкую теплопроводность
— твёрдые при обычных условиях;
— в расплавах и растворах проводят
Используя данную информацию, определите, какое строение имеют вещества йодоводород 
кальция
Запишите ответ в отведённом месте:
1) йодоводород 
2) карбонат кальция 
Сложные неорганические вещества можно классифицировать по четырём группам, как показано на схеме. В эту схему для каждой из четырёх групп впишите по одной химической формуле веществ из числа тех, о которых говорится в приведённом тексте.
Химические формулы запишите в таблицу в следующем формате: Al2(SO4)3.
Прочитайте следующий текст и выполните задания 5—7.
Металл железо известен человеку ещё с глубокой древности. Использовать изделия из него начали ещё в начале 1-го тысячелетия до н. э. В Древнем Египте железо называли «небесный металл», его древнегреческое название означает «звёздный», а древнеримское переводится как «капнувший с неба». Такое название металла объяснялось очень просто: в древности люди не умели добывать соединения железа и получать из них металл, а использовали только метеоритное железо, то есть буквально железо, упавшее с неба. Широкое использование железа не прекращается и в настоящее время. Известно, что в самородном виде в природе железо практически не встречается, однако его соединения, такие как гематит 







1) Составьте молекулярное уравнение реакции железа с кислородом с образованием гематита.
2) Укажите, является ли эта реакция окислительно-восстановительной или она протекает без изменения степеней окисления.
1) Составьте молекулярное уравнение упомянутой в тексте реакции между сульфатом железа (II) и гидроксидом калия.
2) Укажите признак реакции, протекающей между сульфатом железа (II) и гидроксидом калия.
При исследовании минерализации бутилированной воды в ней были обнаружены следующие анионы: , , . Для проведения качественного анализа к этой воде добавили раствор .
1. Какое изменение наблюдается при проведении описанного опыта? (Концентрация веществ достаточна для проведения анализа).
2. Запишите сокращённое ионное уравнение протекающей химической реакции.
Дана схема окислительно-восстановительной реакции:
1. Составьте электронный баланс этой реакции.
2. Укажите окислитель и восстановитель.
3. Расставьте коэффициенты в уравнении реакции.
Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения.
Из приведённого перечня выберите вещества, которые соответствуют указанным в таблице классам/группам органический соединений. Запишите номера этих веществ в соответствующие графы таблицы.
В предложенные схемы химических реакций впишите структурные формулы пропущенных веществ, выбрав их из приведённого выше перечня, и расставьте коэффициенты.
Изопропиловый спирт благодаря низкой токсичности используется в качестве растворителя в косметике, парфюмерии, бытовой химии, в средствах для очистки стёкол, оргтехники и т. п. Изопропиловый спирт можно получить в соответствии с приведённой схемой превращений:
Выберите из предложенного перечня вещество Х и запишите уравнения двух реакций, с помощью которых можно осуществить эти превращения. При написании уравнений реакций используйте структурные формулы органических веществ. Запишите название вещества Х.
Одним из важных понятий в экологии и химии является «предельно допустимая концентрация» (ПДК). ПДК — это такая концентрация вредного вещества в окружающей среде, присутствуя в которой постоянно, данное вещество не оказывает в течение всей жизни прямого или косвенного неблагоприятного влияния на настоящее или будущее поколение, не снижает работоспособности человека, не ухудшает его самочувствия и условий жизни.
ПДК акролеина в воздухе рабочей зоны составляет 0,2 мг/м 3 .
В рабочем помещении одного из ресторанов быстрого питания площадью 32 м 2 и высотой потолка 3,2 м в процессе длительной тепловой обработки жира в воздух выделилось 25,6 мг акролеина. Определите и подтвердите расчётами, превышает ли концентрация акролеина в воздухе данного помещения значение ПДК. Предложите способ, позволяющий снизить концентрацию акролеина в помещении.
Раствор формальдегида зачастую используют в медицине как антисептик. Чему равен объём (н. у.) формальдегида, который потребуется для получения 1 л формалина ( = 1,11 г/мл) с массовой долей формальдегида 10%? (Ответ дайте с точностью до десятых).