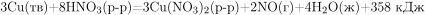Материалы в помощь студентам и научным работникам
Задание с ответами: химия. ЕГЭ — 2018
Согласно термохимическому уравнению реакции
при получении 15,68 л (н.у.) оксида азота (II) количество выделившейся теплоты будет равно
Сведения для решения
Количество моль азота = 15,68/22,4 = 0,7 моль. Количество теплоты, указанное в данной реакции относится к выделению 2 моль оксида азота (II). Составим пропорцию:
2 моль — 358 кДж
Откуда х = 0,7*358/2 = 125,3 кДж
Правильный ответ: 3
Согласно термохимическому уравнению реакции 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O + 385 кДж, при получении 15,68 л NO (н.у.),
В 13:29 поступил вопрос в раздел Разное, который вызвал затруднения у обучающегося.
Вопрос вызвавший трудности
Ответ подготовленный экспертами Учись.Ru
Для того чтобы дать полноценный ответ, был привлечен специалист, который хорошо разбирается требуемой тематике «Разное». Ваш вопрос звучал следующим образом: Согласно термохимическому уравнению реакции 3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O + 385 кДж, при получении 15,68 л NO (н.у.),
После проведенного совещания с другими специалистами нашего сервиса, мы склонны полагать, что правильный ответ на заданный вами вопрос будет звучать следующим образом:
1. Определим количество вещества NO:
n = V / Vm
n(NO) = 15,68/ 22,4л/моль = 0,7 моль
2. Составляем пропорцию с учетом коэффициентов в уравнении реакции
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O + 385 кДж
По уравнению 2 моль NO — 385 кДж
По условию 0,7 моль NO — Q
Решаем пропорцию
Q = 0,7*385/2 = 134,75 кДж
НЕСКОЛЬКО СЛОВ ОБ АВТОРЕ ЭТОГО ОТВЕТА:
Работы, которые я готовлю для студентов, преподаватели всегда оценивают на отлично. Я занимаюсь написанием студенческих работ уже более 4-х лет. За это время, мне еще ни разу не возвращали выполненную работу на доработку! Если вы желаете заказать у меня помощь оставьте заявку на этом сайте. Ознакомиться с отзывами моих клиентов можно на этой странице.
Панфилова Аэлита Иосифовна — автор студенческих работ, заработанная сумма за прошлый месяц 56 019 рублей. Её работа началась с того, что она просто откликнулась на эту вакансию
ПОМОГАЕМ УЧИТЬСЯ НА ОТЛИЧНО!
Выполняем ученические работы любой сложности на заказ. Гарантируем низкие цены и высокое качество.
Деятельность компании в цифрах:
Зачтено оказывает услуги помощи студентам с 1999 года. За все время деятельности мы выполнили более 400 тысяч работ. Написанные нами работы все были успешно защищены и сданы. К настоящему моменту наши офисы работают в 40 городах.
Ответы на вопросы — в этот раздел попадают вопросы, которые задают нам посетители нашего сайта. Рубрику ведут эксперты различных научных отраслей.
Полезные статьи — раздел наполняется студенческой информацией, которая может помочь в сдаче экзаменов и сессий, а так же при написании различных учебных работ.
Красивые высказывания — цитаты, афоризмы, статусы для социальных сетей. Мы собрали полный сборник высказываний всех народов мира и отсортировали его по соответствующим рубрикам. Вы можете свободно поделиться любой цитатой с нашего сайта в социальных сетях без предварительного уведомления администрации.
Площадка Учись.Ru разработана специально для студентов и школьников. Здесь можно найти ответы на вопросы по гуманитарным, техническим, естественным, общественным, прикладным и прочим наукам. Если же ответ не удается найти, то можно задать свой вопрос экспертам. С нами сотрудничают преподаватели школ, колледжей, университетов, которые с радостью помогут вам. Помощь студентам и школьникам оказывается круглосуточно. С Учись.Ru обучение станет в несколько раз проще, так как здесь можно не только получить ответ на свой вопрос, но расширить свои знания изучая ответы экспертов по различным направлениям науки.
Тренажер задания 27 ЕГЭ по химии
Тренировочные упражнения по теме «Расчёты теплового эффекта (по термохимическим уравнениям)» в формате ЕГЭ по химии (тренажер задания 27 ЕГЭ по химии).
Теория по теме «Термохимические задачи» (теория для решения задания 27 ЕГЭ по химии):
Расчёты теплового эффекта (по термохимическим уравнениям).
Тренажер по теме «Термохимические задачи» — 10 вопросов, при каждом прохождении новые.
Тренировочный тест по теме «Термохимические задачи» — полный тест из всех вопросов.
Задание 1. Определите количество теплоты, которая выделится при взаимодействии 40 л азота (при н.у.) и 40 л водорода (при н.у.) по реакции, протекающей в соответствии c термохимическим уравнением:
Ответ выразите в кДж и запишите с точностью до десятых.
Задание 2. Рассчитайте количество теплоты (в кДж), которую нужно затратить для получения 56 л (н.у.) углекислого газа по реакции, протекающей в соответствии c термохимическим уравнением:
(Запишите число с точностью до десятых.)
Задание 3. Какой объём (в л.) кислорода потребуется для окисления 250 л оксида азота(II) до оксида азота(IV)? Объёмы газов измерены при одинаковых условиях. (Запишите число с точностью до целых.)
Задание 4. При образовании аммиака согласно уравнению реакции
выделилось 230 кДж теплоты. Определите объём (н.у.) вступившего в реакцию водорода. Ответ выразите в л и запишите с точностью до целых.
Задание 5. Определите количество теплоты, которая выделится при сгорании 44,8 л этена (н.у.) в 200 л (н.у.) кислорода в соответствии с термохимическим уравнением:
Выразите ответ в кДж и запишите с точностью до целых.
Задание 6. Определите количество теплоты, которое поглощается при разложении 2525 г технического нитрата калия, в котором массовая доля инертных примесей составляет 20%, в соответствии с термохимическим уравнением реакции.
Ответ выразите в кДж и запишите с точностью до целых.
Задание 7. Определите количество теплоты, которое поглощается при получении 100,8 л (н.у.) углекислого газа в соответствии с термохимическим уравнением реакции
Ответ выразите в кДж и запишите с точностью до десятых.
Задание 8. При образовании 340 г аммиака согласно уравнению реакции
выделилось 920 кДж теплоты. Определите объём (н.у.) водорода, который потребуется израсходовать, чтобы выделилось 230 кДж теплоты. Ответ выразите в л и запишите с точностью до целых.
Задание 9. В реакцию, термохимическое уравнение которой
вступило 8,51 г технического оксида магния, в котором массовая доля примесей составляет 6%. Определите количество выделившейся при этом теплоты. Ответ выразите в кДж и запишите с точностью до десятых.
Задание 10. При образовании 170 г аммиака согласно уравнению реакции
выделилось 460 кДж теплоты. Определите, какое количество теплоты выделится, если в реакцию вступит 20 л (при н.у.) водорода. Ответ выразите в кДж и запишите с точностью до десятых.
Задание 11. Согласно уравнению реакции
при сжигании 44,8 л оксида углерода(II) выделилось 566 кДж теплоты. Вычислите массу израсходованного кислорода, если в реакции выделилось 141,5 кДж теплоты. Ответ выразите в г и запишите с точностью до целых.
Задание 12. Какой объём углекислого газа образуется при сжигании 5 л угарного газа? (Выход продукта считать равным 100 %.) Объёмы газов измерены в одинаковых условиях. (Выразите ответ в литрах и запишите число с точностью до целых.)
Задание 13. В соответствии с термохимическим уравнением реакции
определите количество теплоты, необходимое для разложения 3,4 г нитрата серебра (Ответ выразите в кДж и запишите число с точностью до сотых.)
Задание 14. Какой объём кислорода потребуется для каталитического окисления 100 л аммиака до оксида азота(II)? Объёмы газов измерены при одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)
Задание 15. В соответствии с термохимическим уравнением
определите какое количество теплоты нужно затратить для получения 10,8 г серебра. (Ответ выразите в кДж и запишите число с точностью до сотых.)
Задание 16. Какой объём водорода потребуется для полного гидрирования 5,6 л пропена? Объёмы газов измерены при одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до десятых.)
Задание 17. В ходе реакции
выделилось 395 кДж тепла. Чему равна масса оксида серы(VI), полученного при этом? (Ответ выразите в граммах и запишите число с точностью до целых.)
Задание 18. Найдите объём азота, который образуется при горении 15 л аммиака. Объёмы газов измерены при одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до десятых.)
Задание 19. Какой объём кислорода потребуется для полного сгорания 10 л ацетилена? Объёмы газов измерены в одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)
Задание 20. Согласно термохимическому уравнению реакции
определите количество выделившейся теплоты при получении 31,36 л (н.у.) оксида азота(II). (Ответ выразите в кДж и запишите число с точностью до десятых.)
Задание 21. Какой объём кислорода необходим для окисления 40 л оксида азота(II)? Объёмы газов измерены в одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)
Задание 22. Согласно термохимическому уравнению реакции
Определите количество выделившейся теплоты при получении 15,68 л (н. у.) оксида азота(II) (Ответ выразите в кДж и запишите число с точностью до десятых.)
Задание 23. Определите объём газообразного продукта, который получится при взаимодействии 1,5 л водорода с избытком хлора. Объёмы газов измерены при одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)
Задание 24. Cогласно уравнению
определите сколько выделится теплоты при получении 25 г железа. (Ответ выразите в кДж и запишите число с точностью до целых.)
Задание 25. В результате реакции, термохимическое уравнение которой
выделилось 123 кДж теплоты. Определите объём (н.у.) получившегося при этом кислорода. (Ответ выразите в литрах и запишите число с точностью до десятых.)
Задание 26. Какой объём кислорода потребуется для полного сжигания 26 л угарного газа? Объёмы газов измерены при одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)
Задание 27. Найдите объём оксида углерода(VI), который образуется при сжигании 20 л угарного газа в избытке кислорода. Объёмы газов измерены при одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)
Задание 28. Согласно уравнению
определите сколько выделится теплоты при окислении 4,8 г угля до оксида углерода(II). (Ответ выразите в кДж и запишите число с точностью до целых.)
Задание 29. Найдите объём оксида серы(IV), который образуется при сжигании 32 л сероводорода в избытке кислорода. Объёмы газов измерены при одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)
Задание 30. В соответствии с термохимическим уравнением
определите массу угля которая при горении выделяет 98,5 кДж теплоты. (Ответ выразите в граммах и запишите число с точностью до целых.)
Задание 31. Какой объём кислорода потребуется для полного сгорания 6 л ацетилена? Объёмы газов измерены в одинаковых условиях. (Ответ выразите в литрах и запишите число с точностью до целых.)