- Кремний
- Положение в периодической системе химических элементов
- Электронное строение кремния
- Физические свойства, способы получения и нахождение в природе кремния
- Качественные реакции
- Соединения кремния
- Способы получения кремния
- Химические свойства
- Бинарные соединения кремния
- Силициды металлов
- Силан
- Карбид кремния
- Галогениды кремния
- Оксид кремния (IV)
- Физические свойства и нахождение в природе
- Химические свойства
- Кремниевая кислота
- Строение молекулы и физические свойства
- Способы получения
- Химические свойства
- Силикаты
- Кремний
- Получение
- Физические свойства
- Химические свойства и применение
- Оксид кремния (IV). Кремниевая кислота и ее соли. Стекло. Цемент
- Скачать:
- Химические свойства кислот
- Диссоциация
- Разложение
- Взаимодействие кислот с металлами
- Таблица: химические свойства кислот-окислителей
- Взаимодействие кислот с основаниями
- Взаимодействие кислот с солями
- Взаимодействие кислот с основными и амфотерными оксидами
- Восстановительные свойства бескислородных кислот
- Способность окрашивать индикаторы
- Вопросы для самоконтроля
Кремний
Положение в периодической системе химических элементов
Кремний расположен в главной подгруппе IV группы (или в 14 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение кремния
Электронная конфигурация кремния в основном состоянии :
+14Si 1s 2 2s 2 2p 6 3s 2 3p 2
Электронная конфигурация кремния в возбужденном состоянии :
+14Si * 1s 2 2s 2 2p 6 3s 1 3p 3
Атом кремния содержит на внешнем энергетическом уровне 2 неспаренных электрона и 1 неподеленную электронную пару в основном энергетическом состоянии и 4 неспаренных электрона в возбужденном энергетическом состоянии.
Степени окисления атома кремния — от -4 до +4. Характерные степени окисления -4, 0, +2, +4.
Физические свойства, способы получения и нахождение в природе кремния
Кремний — второй по распространенности элемент на Земле после кислорода. Встречается только в виде соединений. Оксид кремния SiO2 образует большое количество природных веществ – горный хрусталь, кварц, кремнезем.
Простое вещество кремний – атомный кристалл темно-серого цвета с металлическим блеском, довольно хрупок. Температура плавления 1415 °C, плотность 2,33 г/см 3 . Полупроводник.
Качественные реакции
Качественная реакция на силикат-ионы SiO3 2- — взаимодействие солей-силикатов с сильными кислотами . Кремниевая кислота – слабая. Она легко выделяется из растворов солей кремниевой кислоты при действии на них более сильными кислотами.
Например , если к раствору силиката натрия прилить сильно разбавленный раствор соляной кислоты, то кремниевая кислота выделится не в виде осадка, а в виде геля. Раствор помутнеет и «застынет».
Na2SiO3 + 2HCl = H2SiO3 + 2 NaCl
Видеоопыт взаимодействия силиката натрия с соляной кислоты (получение кремниевой кислоты) можно посмотреть здесь.
Соединения кремния
Основные степени окисления кремния +4, 0 и -4.
Наиболее типичные соединения кремния:
| Степень окисления | Типичные соединения |
| +4 | оксид кремния (IV) SiO2 бинарные соединения с неметаллами (карбид кремния SiC) |
| -4 | силан SiH4 силициды металлов (силицид натрия Na4Si) |
Способы получения кремния
В свободном состоянии кремний был получен Берцелиусом в 1822 г. Его латинское название «силиций» произошло от латинского слова « sile х», что означает «кремень». Аморфный кремний в лаборатории можно получить при прокаливании смеси металлического магния с диоксидом кремния. Для опыта диоксид кремния следует тщательно измельчить. При нагревании смеси начинается бурная реакция. Одним из продуктов этой реакции является аморфный кремний.
SiO2 + 2Mg → Si + 2MgO
Видеоопыт взаимодействия оксида кремния (IV) с магнием можно посмотреть здесь.
Еще один способ получения кремния в лаборатории — восстановление из оксида алюминием:
В промышленности использовать дорогие алюминий и магний неэффективно, поэтому используют другие, более дешевые способы:
1. Восстановление из оксида коксом в электрических печах:
SiO2 + 2C → Si + 2CO
Однако в таком процессе образующийся кремний загрязнен примесями карбидов кремния, и для производства, например, микросхем уже не подходит.
2. Наиболее чистый кремний получают восстановлением тетрахлорида кремния водородом при 1200 °С:
SiCl4 +2H2 → Si + 4HCl
или цинком :
SiCl4 + 2Zn → Si + 2ZnCl2
3. Также чистый кремний получается при разложении силана :
Химические свойства
При нормальных условиях кремний существует в виде атомного кристалла, поэтому химическая активность кремния крайне невысокая.
1. Кремний проявляет свойства окислителя (при взаимодействии с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (при взаимодействии с элементами, расположенными выше и правее). Поэтому кремний реагирует и с металлами , и с неметаллами .
1.1. При обычных условиях кремний реагирует с фтором с образованием фторида кремния (IV):
При нагревании кремний реагирует с хлором, бромом, йодом :
1.2. При сильном нагревании (около 2000 о С) кремний реагирует с углеродом с образованием бинарного соединения карбида кремния (карборунда):
C + Si → SiC
При температуре выше 600°С взаимодействует с серой:
Si + 2S → SiS2
1.3. Кремний не взаимодействует с водородом .
1.4. С азотом кремний реагирует в очень жестких условиях:
1.5. В реакциях с активными металлами кремний проявляет свойства окислителя. При этом образуются силициды:
2Ca + Si → Ca2Si
Si + 2Mg → Mg2Si
1.6. При нагревании выше 400°С кремний взаимодействует с кислородом :
2. Кремний взаимодействует со сложными веществами:
2.1. В водных растворах щелочей кремний растворяется с образованием солей кремниевой кислоты. При этом щелочь окисляет кремний.
2.2. Кремний не взаимодействует с водными растворами кислот , но аморфный кремний растворяется в плавиковой кислоте с образованием гексафторкремниевой кислоты :
При обработке кремния безводным фтороводородом комплекс не образуется:
С хлороводородом кремний реагирует при 300 °С, с бромоводородом – при 500 °С.
2.3. Кремний растворяется в смеси концентрированных азотной и плавиковой кислот :
3Si + 4HNO3 + 12HF → 3SiF4 + 4NO + 8H2O
Бинарные соединения кремния
Силициды металлов
Силициды – это бинарные соединения кремния с металлами, в которых кремний имеет степень окисления -4. Химическая связь в силицидах металлов — ионная.
Силициды, как правило, легко гидролизуются в воде или в кислой среде.
Например , силицид магния разлагается водой на гидроксид магния и силан:
Соляная кислота легко разлагает силицид магния:
Получают силициды сплавлением простых веществ или восстановлением смеси оксидов коксом в электропечах:
2Mg + Si → Mg 2 Si
2MgO + SiO2 + 4C → Mg2Si + 4CO
Силан
Силан – это бинарное соединение кремния с водородом SiH4, ядовитый бесцветный газ.
Если поместить порошок силицида магния в очень слабый раствор соляной кислоты, то на поверхности раствора образуются пузырьки газа. Они лопаются и загораются на воздухе. Это горит силан. Он образуется при взаимодействии кислоты с силицидом магния:
Видеоопыт получения силана из силицида магния можно посмотреть здесь.
На воздухе силан горит с образованием SiO2 и H2O:
Видеоопыт сгорания силана можно посмотреть здесь.
Силан разлагается водой разлагается с выделением водорода:
Силан разлагается (окисляется) щелочами :
Силан при нагревании разлагается :
Карбид кремния
В соединениях кремния с неметаллами — ковалентная связь.
Рассмотрим карбид кремния – карборунд Si +4 C -4 . Это вещество с атомной кристаллической решеткой. Он имеет структуру, подобную структуре алмаза и характеризуется высокой твердостью и температурой плавления, а также высокой химической устойчивостью.
Карборунд окисляется кислородом при высокой температуре:
Карборунд окисляется кислородом в расплаве щелочи :
Галогениды кремния
Хлорид и фторид кремния – галогенангидриды кремниевой кислоты.
SiCl4.
Получают галогениды кремния действием хлора на сплав оксида кремния с углем :
Галогениды кремния разлагаются водой до кремниевой кислоты и хлороводорода:
Хлорид кремния (IV) восстанавливается водородом :
SiCl4 + 2H2 → Si + 4HCl
Оксид кремния (IV)
Физические свойства и нахождение в природе
Оксид кремния (IV) – это твердое вещество с атомной кристаллической решеткой. В природе встречается в виде кварца, речного песка, кремнезема и прочих модификаций:
Химические свойства
Оксид кремния (IV) – типичный кислотный оксид . За счет кремния со степенью окисления +4 проявляет слабые окислительные свойства.
1. Как кислотный оксид, диоксид кремния (IV) взаимодействует с растворами и расплавами щелочей и в расплаве с основными оксидами . При этом образуются силикаты.
Например , диоксид кремния взаимодействует с гидроксидом калия:
Еще пример : диоксид кремния взаимодействует с оксидом кальция.
SiO2 + CaO → CaSiO3
2. Оксид кремния (IV) не взаимодействует с водой , т.к. кремниевая кислота нерастворима .
3. Оксид кремния (IV) реагирует при сплавлении с карбонатами щелочных металлов . При этом работает правило: менее летучий оксид вытесняет более летучий оксид из солей при сплавлении.
Например , оксид кремния (IV) взаимодействует с карбонатом калия. При этом образуется силикат калия и углекислый газ:
4. Из кислот диоксид кремния реагирует только с плавиковой или с газообразным фтороводородом :
5. При температуре выше 1000 °С оксид кремния реагирует с активными металлами, при этом образуется кремний.
Например , оксид кремния взаимодействует с магнием с образованием кремния и оксида магния:
SiO2 + 2Mg → Si + 2MgO
Видеоопыт взаимодействия оксида кремния (IV) с магнием можно посмотреть здесь.
При избытке восстановителя образуются силициды:
SiO2 + 4Mg → Mg2Si + 2MgO
6. Оксид кремния (IV) взаимодействует с неметаллами.
Например , оксид кремния (IV) реагирует с водородом в жестких условиях. При этом оксид кремния проявляет окислительные свойства:
Еще пример : оксид кремния взаимодействует с углеродом. При этом образуется карборунд и угарный газ:
SiO2 + 3С → SiС + 2СО
При сплавлении оксид кремния взаимодействует с фосфатом кальция и углем:
Кремниевая кислота
Строение молекулы и физические свойства
Кремниевые кислоты — очень слабые, малорастворимые в воде соединения общей формулы nSiO2•mH2O. Образует коллоидный раствор в воде.
Метакремниевая H2SiO3 существует в растворе в виде полимера:
Способы получения
Кремниевая кислота образуется при действии сильных кисло т на растворимые силикаты (силикаты щелочных металлов).
Например , при действии соляной кислоты на силикат натрия:
Видеоопыт получения кремниевой кислоты из силиката натрия можно посмотреть здесь.
Даже слабая угольная кислота вытесняет кремниевую кислоту из солей:
Химические свойства
1. Кремниевая кислота — нерастворимая. Кислотные свойства выражены очень слабо, поэтому кислота реагирует только с сильными основаниями и их оксидами :
Например , кремниевая кислота реагирует с концентрированным гидроксидом калия:
2. При нагревании кремниевая кислота разлагается на оксид и воду :
Силикаты
Силикаты — это соли кремниевой кислоты. Большинство силикатов нерастворимо в воде, кроме силикатов натрия и калия, их называют «жидким стеклом».
Способы получения силикатов:
1 . Растворение кремния, кремниевой кислоты или оксида в щелочи:
2. Сплавление с основными оксидами:
СаО + SiO2 → CaSiO3
3. Взаимодействие растворимых силикатов с солями:
Оконное стекло (натриевое стекло) — силикат натрия и кальция: Na2O·CaO·6SiO2.
Стекло получают при сплавлении в специальных печах смеси соды Na2CO3, известняка CaCO3 и белого песка SiO2:
Для получения специального стекла вводят различные добавки, так стекло содержащее ионы Pb 2+ – хрусталь; Cr 3+ – имеет зеленую окраску, Fe 3+ – коричневое бутылочное стекло, Co 2+ – дает синий цвет, Mn 2+ – красновато-лиловый.
Кремний
Кварц, горный хрусталь, аметист, халцедон, топаз, оникс… Трудно поверить, но все эти и многие другие «чудеса подземного мира» состоят из одного и того же вещества – кремнезема, или оксида кремния (IV) SiO2.
Предположения о том, что в кремнеземе содержится новый, еще неизвестный элемент, высказывались учеными уже в XVIII столетии. Однако в виде простого вещества кремний был выделен лишь в XIX в. Й. Я. Берцелиусом. Вначале он нагревал смесь кремнезёма с порошком железа и углём до 1500 0 С, но чистый кремний получить не удавалось: в присутствии железа образуется ферросилиций – сплав, содержащий оба эти элемента. Поняв, в чем ошибка, Берцелиус изменил способ синтеза. В 1823 г., когда он пропустил над калием пары фторида кремния (IV), удача, наконец, улыбнулась ему. По реакции SiF4 + 4K = Si + 4KF был получен порошок аморфного кремния. Берцелиус доказал также, что, сгорая на воздухе, кремний переходит в кремнезём.

По содержания в земной коре (28%) Si уступает только кислороду. В природе кремний встречается исключительно в форме соединений. Обычный речной песок представляет собой кремнезём, загрязненный примесью глины и соединений железа. Наряду с глиной (Al2O3∙2SiO2∙2H2O) он образуется при выветривании полевого шпата под действием углекислого газа и влаги воздуха:

Получение
В промышленности для получения кремния используют чистый песок SiO2. В электрических печах при высокой температуре происходит восстановление кремния из его оксида коксом (углем):
SiO2 + 2C = Si + 2CO↑
В лаборатории в качестве восстановителей используют магний или алюминий:
SiO2 + 2Mg = Si + 2MgO
Наиболее чистый кремний получают восстановлением тетрахлорида кремния водородом или цинком:
Физические свойства
Полученный указанными выше способами аморфный кремний представляет собой бурый порошок с температурой плавления 1420 0 С. Существует и другая аллотропная модификация кремния – кристаллический кремний. Это твердое вещество темно-серого цвета со слабым металлическим блеском, обладает тепло-и электропроводностью. Кристаллический кремний получают перекристаллизацией аморфного кремния. Аморфный кремний является более реакционноспособным, чем химически довольно инертный кристаллический кремний. Кристаллический кремний – полупроводник, его электропроводность возрастает при освещении и нагревании. Это обусловлено строением кристаллов. Структура кристаллического кремния аналогична структуре алмаза. В его кристалле каждый атом окружен тетраэдрически четырьмя другими и связан с ними ковалентной связью, хотя эта связь значительно слабее, чем между атомами углерода в алмазе. В кристалле кремния даже при обычных условиях ковалентные связи частично разрушаются, поэтому в нем имеются свободные электроны, которые обусловливают небольшую электропроводность. При освещении, нагревании, а также при наличии некоторых примесей увеличивается число разрушаемых связей, а значит, увеличивается число свободных электронов и возрастает электропроводность.
Химические свойства и применение
По химическим свойствам кремний во многом схож с углеродом, что объясняется одинаковой структурой внешнего электронного слоя. При обычных условиях кремний довольно инертен, что обусловлено прочностью его кристаллической решетки. Непосредственно при комнатной температуре он взаимодействует только с фтором. При температуре 400 – 600 0 С кремний реагирует с хлором и бромом, а в кислороде измельченный кремний сгорает. С азотом и углеродом кремний реагирует при очень высоких температурах. Во всех указанных реакциях кремний играет роль восстановителя.
Кремний как восстановитель взаимодействует и с некоторыми сложными веществами, например с фтороводородом:
С другими галогеноводородами он в реакцию не вступает.
Кремний не растворяется даже в азотной кислоте, так как на его поверхности образуется плотная оксидная пленка (SiO2), которая препятствует реакции. Однако со смесью HNO3 и HF кремний реагирует потому, что фтороводородная кислота растворяет SiF4:
Водные растворы щелочей растворяют кремний с образованием растворимых солей кремниевой кислоты – силикатов, при этом происходит выделение водорода:
Восстановительные свойства кремния используют для получения некоторых металлов из их оксидов. Например:
2MgO + Si = 2Mg + SiO2
При взаимодействии с металлами кремний играет роль окислителя. Соединения кремния с металлами называются силицидами:
При обработке силицида магния соляной кислотой или водой образуется простейшее водородное соединение кремния – силан SiH4:
Силан – ядовитый газ с неприятным запахом, легко самовоспламеняется на воздухе:
Кремний широко применяется в технике для получения различных полупроводниковых материалов и сплавов. Сплав кремния с железом – ферросилиций (сталь, содержащая 15% кремния) обладает большой кислотоустойчивостью. Из такой стали изготавливают химическую аппаратуру.
Оксид кремния (IV). Кремниевая кислота и ее соли. Стекло. Цемент
Оксид кремния (IV) SiO2 (кремнезем, ангидрид кремниевой кислоты) – твердое тугоплавкое вещество (температура плавления 1713 0 С), нерастворимое в воде, из всех кислот только фтороводородная кислота постепенно разлагает его:
Как кислотный оксид SiO2 при нагревании или сплавлении реагирует с основными оксидами, щелочами и некоторыми солями с образованием солей кремниевой кислоты – силикатов. Например:
Полученные искусственным путем силикаты натрия и калия – растворимое стекло – сильно гидролизованы. Их концентрированный раствор, называемый жидким стеклом, имеет сильнощелочную реакцию. Жидкое стекло применяется для изготовления несгораемых тканей, пропитки деревянных изделий, в качестве клея и т.д.
Кремниевая кислота H2SiO3 относится к очень слабым кислотам. В воде она практически нерастворима, но легко образует коллоидные растворы. Ее можно получить из растворов силикатов действием на них более сильных кислот. H2SiO3 выпадает из раствора в виде студенистого осадка (геля):
Постепенно при обычных условиях или быстрее при нагревании кремниевая кислота разлагается на воду и ангидрид кремниевой кислоты SiO2:
Стекло. Сырьем для производства стекла являются сода Na2CO3, известняк CaCO3 и песок SiO2. Из этих компонентов получают обычное оконное стекло:
В стекла особого назначения – огнеупорные, обладающие большой механической прочностью – при варке добавляют оксиды бария, свинца, бора. Окрашенные стекла получают добавлением оксидов кобальта (синее стекло), оксида хрома (зеленое стекло), добавлением оксида свинца получают хрустальное стекло.
Цемент представляет собой смесь силикатов, главными компонентами которых являются: оксид кальция, оксид кремния (IV), оксиды алюминия и железа (III).
В промышленности цемент получают спеканием глины и известняка СаСО3. Если образующийся при этом порошок смешать с водой, то получается масса, постепенно твердеющая на воздухе. При добавлении к цементу песка или щебня в качестве наполнителя получают бетон, который широко используют в строительстве. Прочность бетона возрастает, если в него вводится каркас из железных стержней. Железобетонные панели, блоки перекрытий – основа современного строительства.
Скачать:
Скачать бесплатно реферат на тему: «Кремний» КРЕМНИЙ.docx (224 Загрузки)
Скачать бесплатно реферат на тему: «Керамика» Керамика.docx (217 Загрузок)
Скачать бесплатно реферат на тему: «Бетон» Бетон.docx (Одна Загрузка)
Скачать рефераты по другим темам можно здесь
*на изображении записи фотография аметиста
Химические свойства кислот
О чем эта статья:
8 класс, 9 класс, ЕГЭ/ОГЭ
Кислоты — это сложные химические вещества, состоящие из одного или нескольких атомов водорода, способных замещаться атомами металла, и кислотных остатков.
Рассмотрим подробнее общие свойства кислот.
Диссоциация
Кислоты — это электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Диссоциация кислот происходит ступенчато. По способности к диссоциации кислоты разделяют на две группы:
Хорошо диссоциирующие (сильные): H2SO4, HCl, HBr, HNO3, HClO4, HI.
Разложение
В результате реакций разложения кислородсодержащих кислот образуются кислотный оксид и вода. Бескислородные кислоты образуют простые вещества. Для разложения некоторых кислот необходимо нагревание или излучение (HCl, HNO3, H3PO4) другие же разлагаются самопроизвольно в момент образования (H2CO3, H2SO3, HNO2).
Взаимодействие кислот с металлами
Металл может вытеснять водород из кислоты только в том случае, если металл стоит левее водорода в ряду активности металлов. Продукты реакции — соль и водород.
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
Высокая окислительная способность серной и азотной кислот позволяет им вступать в реакции с металлами. Продукты реакции будут зависеть от активности металла и от концентрации кислот.
Таблица: химические свойства кислот-окислителей
На холоду — пассивация
На холоду — пассивация
Реакция не проходит
На холоду — пассивация
На холоду — пассивация
Взаимодействие кислот с основаниями
Кислоты реагируют с основаниями и амфотерными гидроксидами, в результате образуются соль и вода. Взаимодействие кислот с основаниями называют реакцией нейтрализации.
NaOH + HCl = NaCl + H2O
Взаимодействие кислот с солями
Сильные кислоты вытесняют слабые из растворов их солей, при этом образуются новая соль и новая кислота. Условие протекания реакции кислот с солями — одним из продуктов реакции должны быть нерастворимая соль или слабая кислота, вода, газ.
Взаимодействие кислот с основными и амфотерными оксидами
Кислоты вступают в реакцию с основными и амфотерными оксидами (последние ведут себя как основные оксиды). В результате реакции образуется соль и вода.
Восстановительные свойства бескислородных кислот
Бескислородные кислоты (кроме HF) проявляют восстановительные свойства за счет химического элемента, который входит в состав аниона, при действии на них различных окислителей.
Например, в качестве окислителей для всех галогеноводородных кислот выступают диоксид марганца MnO2, перманганат калия KMnO4, дихромат калия K2Cr2O7.
Результат этих реакций — образование свободных галогенов.
Из галогеноводородных кислот наибольшая восстановительная активность — у йодоводородной. Ее могут окислять оксид железа (III) и соль трехвалентного железа.
Высокая восстановительная активность характерна для сероводородной кислоты, она может быть окислена диоксидом серы.
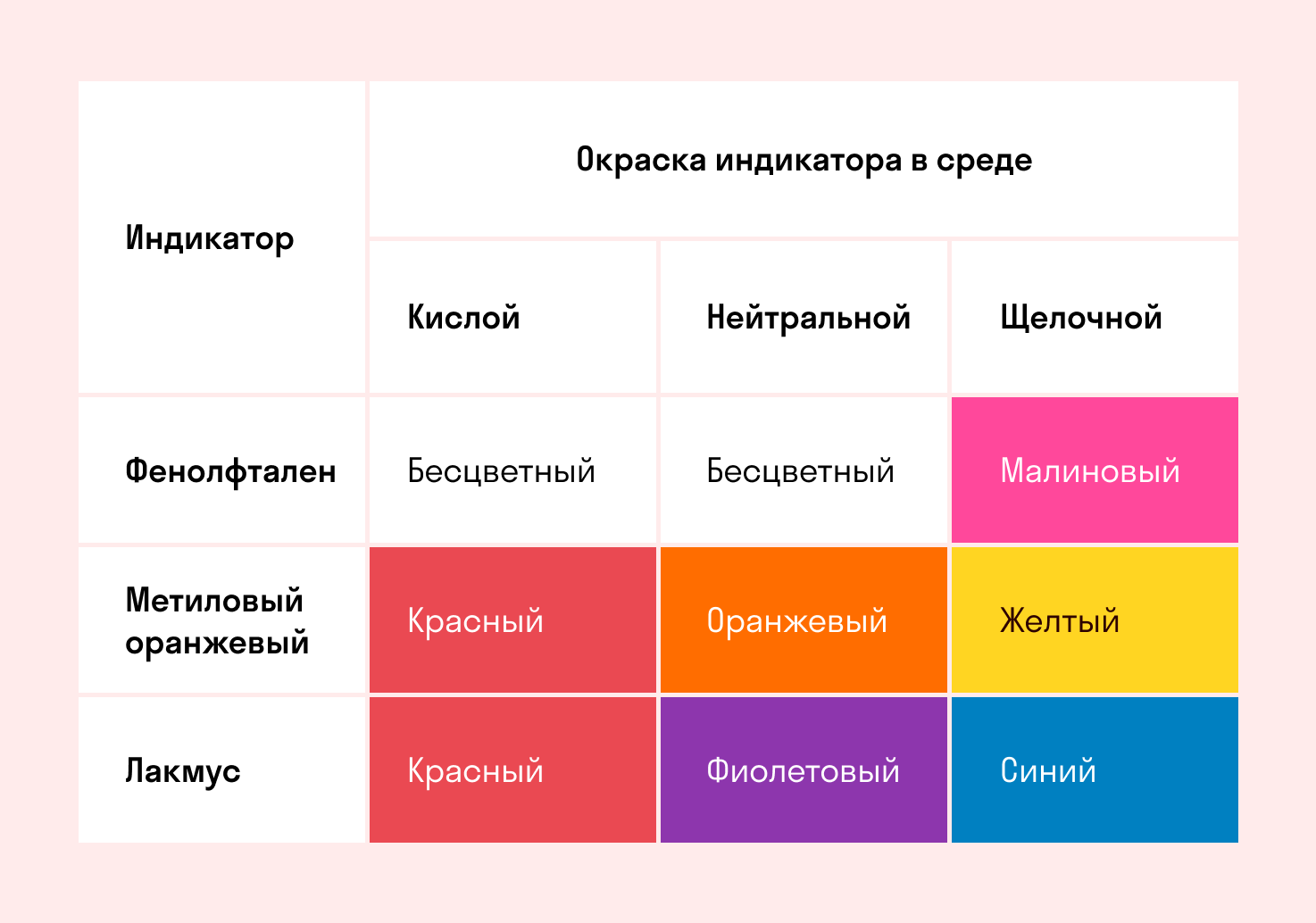
Способность окрашивать индикаторы
Индикаторы кислот — это специальные вещества, при помощи которых определяют наличие кислот в растворе.
Вопросы для самоконтроля
С чем реагируют кислоты?
При каких условиях кислоты взаимодействуют с солями? Приведите пример.
Составьте уравнения реакций и назовите продукты реакций:
Разбавленный раствор серной кислоты реагирует с: медью, хлоридом меди, сульфатом меди, цинком?
Соляная кислота вступает в реакцию с каждым из двух веществ: