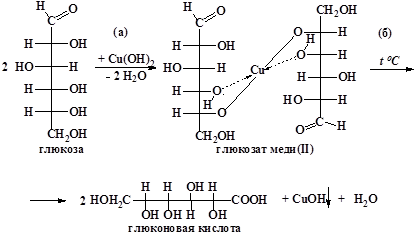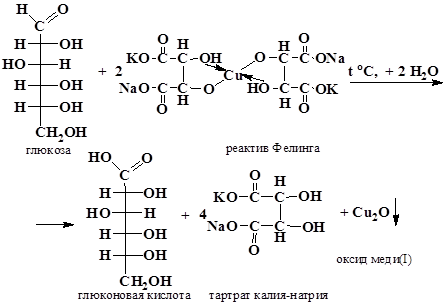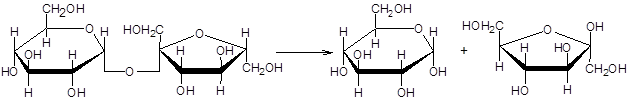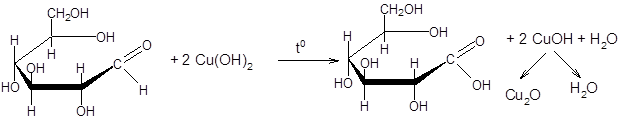Тема: Углеводы. Моносахариды.
Опыт №1. Реакция Троммера.
Ход исследования: В пробирку вносят 5-6 капель 1% раствора глюкозы добавляют 2-3 капли 10% едкого натра NaOH и по каплям добавляют 5% раствор сульфата меди до образования легкой неисчезающей мути. Пробирку осторожно нагревают, сначала появляется желтое окрашивание жидкости, а затем образуется желтый или кирпично-красный осадок. В реакции Троммера окислителем является гидрат окиси меди Cu(OH)2, который при восстановлении постепенно переходит в гидрат закиси меди, а затем в закись меди. Химизм реакции:
Укажите, какие свойства проявляет в этой реакции глюкоза.
Сделать вывод о проделанной работе.
Опыт №2. Реакция Фелинга.
Реакция Фелинга является видоизменением реакции Троммера и отличается от нее тем, что для окисления глюкозы применяют реактив Фелинга, в состав которого входят сульфат меди (II) CuSO4, сегнетова соль и NaOH. В этом реактиве медь находится в виде соединения с сегнетовой солью, благодаря чему гидрат окиси меди не выпадает в осадок.
Ход исследования: В пробирку вносят 5-6 капель 1% раствора глюкозы, добавляют 3-5 капель реактива Фелинга и нагревают. Появляется желтое окрашивание, затем образуется желтый или кирпично-красный осадок.
Реакция протекает аналогично реакции Троммера. Запишите уравнения реакции. Укажите, какие свойства проявляет глюкоза в этой реакции. Сделайте вывод о проделанной работе.
Опыт №3. Реакция Селиванова на фруктозу.
Ход исследования: В пробирку вносят 5-6 капель фруктозы и добавляют 2-3 капли реактива Селиванова (0,5 г резорцина в 100 мл 20% соляной кислоты). Содержимое пробирки кипятят 2-3 минуты или нагревают в кипящей водяной бане в течение 5-7 минут. Постепенно образуется вишнево-красное окрашивание.
Кетогексозы при нагревании с соляной кислотой или серной теряют три молекулы воды с образованием продукты конденсации вишнево-красного цвета.
Сделать вывод о проделанной работе.
Опыт №4. Реакции на пентозы
Ход исследования: В пробирку вносят щепотку древесных опилок или соломы, в которых содержатся полисахариды – пентозаны. Опилки или солому смачивают концентрированной соляной кислотой после чего добавляют несколько кристалликов флороглюцина. Появляется малиново-красное окрашивание. Пентозаны, содержащиеся в опилках и соломе, под влиянием соляной кислоты расщепляются до пентоз. Пентозы под действием соляной кислоты теряют воду и образуют фурфурал.
Пентозаны → пентоза → фурфурол + флороглюцин → малиновое окрашивание
Фурфурол с флороглюцином дает продукт конденсации малинового цвета.
Опыт №1. Изучение восстанавливающих свойств дисахаридов.
Ход исследования: В три пробирки раздельно вносят по 5-6 капель 1% раствора сахарозы, мальтозы и лактозы. Затем со всеми тремя растворами проделывают реакцию Фелинга и отмечают в таблице 1, какие дисахариды восстанавливают гидроксид меди.
Реакция Фелинга является видоизменением реакции Троммера и отличается от нее тем, что для окисления глюкозы применяют реактив Фелинга, в состав которого входят сульфат меди (II) CuSO4, сегнетова соль и NaOH. В этом реактиве медь находится в виде соединения с сегнетовой солью, благодаря чему гидрат окиси меди не выпадает в осадок.
В пробирку вносят 5-6 капель 1% раствора глюкозы, добавляют 3-5 капель реактива Фелинга и нагревают. Появляется желтое окрашивание, затем образуется желтый или кирпично-красный осадок.
| Дисахариды | Реакция Фелинга | Реакция Селиванова | Восстанавливающий или невосстанавливающий дисахарид |
| Мальтоза | |||
| Лактоза | |||
| Сахароза |
Объяснить причину разного отношения дисахаридов к реактиву Фелинга. Записать формулы оксо-формы восстанавливающих дисахаридов
Сделать вывод о проделанной работе.
Опыт №2. Реакция Селиванова с дисахаридами.
Ход исследования: В три пробирки раздельно вносят по 5-6 капель 1% растворов сахарозы, мальтозы, лактозы и проделывают с этими растворами реакцию Селиванова. В пробирку вносят 5-6 капель фруктозы и добавляют 2-3 капли реактива Селиванова (0,5 г резорцина в 100 мл 20% соляной кислоты). Содержимое пробирки кипятят 2-3 минуты или нагревают в кипящей водяной бане в течение 5-7 минут. Постепенно образуется вишнево-красное окрашивание.
Кетогексозы при нагревании с соляной кислотой или серной теряют три молекулы воды с образованием продукты конденсации вишнево-красного цвета.
Сравнивают полученные результаты и делают вывод, в каких дисахаридах содержится фруктоза. Результаты исследований, произведенных с дисахаридами, заносят в таблицу 1 и делают заключение о свойствах дисахаридов. Положительный результат реакции обозначают знаком (+), а отрицательный знаком (-)
Записать формулу дисахарида, содержащего фруктозу. Сделать вывод о проделанной работе
Опыт №3. Кислотный гидролиз (декстринизация) крахмала.
Ход исследования: В пробирку наливают около 3 мм 1% раствора крахмала, добавляют около 1 мм 10% раствора серной кислоты и оставляют в кипящей водяной бане. Через 2-3 мин. после начала нагревания на водяной бане стеклянной палочкой берут одну каплю жидкости из пробирки и смешивают ее с каплей взятой другой палочкой реактива Люголя на стекле с подложенным под него листом белой бумаги. Последующие пробы проделывают через каждую минуту. Отмечают, какое при этом образуется окрашивание, и сразу записывают полученный результат в таблицу 2. Взятие проб продолжают до тех пор, пока последние капли гидролизата не перестанут изменять цвет реактива Люголя. Затем оставшуюся в пробирке жидкость охлаждают, нейтрализуют по лакмусу 10% раствором щелочи и проделывают реакцию Фелинга (занятие №13) Наблюдают образование кирпично–красного осадка закиси меди. По полученным данным составляют таблицу цветного ряда декстринов.
| № пробы |
| Цвет жидкости |
| Название декстринов |
При гидролизе крахмал распадается на ряд промежуточных продуктов. В целом гидролиз крахмала можно выразить следующей схемой:
Цветной ряд декстринов, образующихся при гидролизе крахмала:
Крахмал с йодом дает синее окрашивание
Амилодекстрины – с йодом дают окрашивание от сине-фиолетового до темно-фиолетового
Флаводекстрины — с йодом дают желто-оранжевое окрашивание
Эритродекстрины — с йодом дают окрашивание от красно-бурого до красно- оранжевого
Видео:Качественные реакции на глюкозуСкачать

Опыт 4. Обнаружение моносахаридов реактивом Толленса
МОНОСАХАРИДЫ
Цель работы. Сопоставить свойства альдоз и кетоз, познакомиться с их качественными реакциями.
Опыт 1. Проба Троммера на глюкозу
Здесь последовательно осуществляются две качественные реакции на глюкозу: (а) доказательство наличия в молекуле глюкозы нескольких ОН-групп по образованию синего раствора гликоната меди (II) и (б) доказательство наличия в молекуле глюкозы альдогруппы, — реакция «медного зеркала».
(а) Качественная реакция на a-гликольный фрагмент
В большой пробирке смешивают 1 мл 1 %-го раствора глюкозы и 0,5 мл 10 %-го раствора гидроксида натрия. Затем по каплям добавляют 5 %-й раствор CuSO4. Образующийся вначале голубой осадок гидроксида меди(II) при встряхивании растворяется и получается синий прозрачный раствор сахарата меди:
2 СuOH ® Cu2O¯ + H2O
(б) Окисление моносахаридов гидроксидом меди(II) – качественная реакция на альдогруппу (проба Троммера)
3/4 высоты пробирки), перемешайте. Пробирку сильно наклоните и грейте только в верхней части раствора (см. рис. 7). Нагрейте до кипения, но не кипятите (при кипячении начнет разлагаться нерастворившийся осадок Cu(OH)2 с образованием черного CuO, что «затемнит» внешний эффект). Через несколько секунд нагретая часть раствора изменит цвет на оранжево-желтый – образуется осадок CuOH. При избытке щелочи или более длительном нагреве может образоваться желто-красный осадок Cu2O.
Cu 2+ из состава сахарата восстанавливается до Cu 1+ (в составе CuOH или Cu2O), а глюкоза окисляется до глюконовой кислоты:
Опыт 2. Эпимеризация кетозы в альдозу
Фруктоза, не имеющая альдогруппы, тем не менее, тоже дает положительную пробу Троммера. Это обусловлено явлением эпимеризации – стереоизомеризацией кетозы в альдозу при нагреве в щелочной среде. Этот процесс проходит через стадию “енолизации” (образования ендиола):
Восстановительная способность фруктозы (кетозы) связана с предварительным ее превращением (эпимеризацией) в альдозу, которая, собственно, и дает положительную реакцию Троммера.
Опыт с фруктозой проводится аналогично опыту 1, только требует более длительного нагревания. Напишите реакцию образования фруктоната меди (II) (взаимодействия Cu(OH)2 с фруктозой).
Опыт 3. Обнаружение моносахаридов реактивом
Фелинга
Реактивом Фелинга легко окисляются как альдозы, так и кетозы.
В две пробирки наливают по 1 мл 1 %-го раствора глюкозы и фруктозы. В каждую из них добавляют по 1 мл реактива Фелинга. Содержимое пробирок тщательно перемешивают и нагревают верхнюю часть раствора до начинающегося кипения (или на водяной бане в течение 5 мин). В обоих пробирках в верхней части жидкости появляется желтый осадок гидроксида меди(I) CuOH, переходящий в красно-оранжевый осадок оксида меди(I) Cu2O. Цвет нижней части пробирок не изменяется.
Опыт 4. Обнаружение моносахаридов реактивом Толленса
(реакция “серебряного зеркала ”)
В две чистые и сухие пробирки наливают по 2-3 мл реактива Толленса (получение – см. стр.13). В одну из них добавляют 1-2 мл 1 %-го раствора глюкозы, а во вторую – столько же 1 %-го раствора фруктозы. Пробирки нагревают на водяной бане (70-80 °С) 10 минут. (Во время нагревания пробирки нельзя встряхивать, иначе серебро выпадет в виде черного осадка.)
Металлическое серебро выделяется на стенках обеих пробирок в виде зеркального налета.
Объясните, почему кетоны не дают реакцию серебряного и медного зеркала, а кетозы дают такую реакцию?
Видео:Качественная реакция глюкозы с гидроксидом меди (II)Скачать

Специфичность действия ферментов
Читайте также:
|