Натрий — это щелочной металл, серебристо-белого цвета. Легкий, очень мягкий, низкая температура плавления.
Относительная молекулярная масса Mr = 22,990; относительная плотность по твердому состоянию d = 0,968; относительная плотность по жидкому состоянию d = 0, 27; tпл = 97,83º C; tкип = 886º C.
Видео:Опыты по химии. Окраска пламени солями щелочных и щелочноземельных металловСкачать

Способ получения
1. Натрий получают в промышленности электролизом расплава гидроксида натрия, в результате образуется натрий, кислород и вода:
4NaOH → 4Na + O2↑ + 2H2O
Видео:Окрашивание пламени солями натрияСкачать

Качественная реакция
Качественная реакция на натрий — окрашивание пламени солями натрия в желтый цвет .
Видео:Окрашивание пламени солями натрияСкачать

Химические свойства
Натрий — активный металл; на воздухе реагирует с кислородом и покрывается оксидной пленкой. Воспламеняется при умеренном нагревании; окрашивает пламя газовой горелки в темно-красный цвет.
1. Натрий — сильный восстановитель . Поэтому он реагирует почти со всеми неметаллами :
1.1. Натрий легко реагирует с галогенами с образованием галогенидов:
2Na + I2 = 2NaI
1.2. Натрий реагирует с серой с образованием сульфида натрия:
2Na + S = Na2S
1.3. Натрий активно реагирует с фосфором и водородом . При этом образуются бинарные соединения — фосфид натрия и гидрид натрия:
3Na + P = Na3P
2Na + H2 = 2NaH
1.4. С азотом натрий реагирует при температуре 100º С и электрическом разряде с образованием нитрида:
1.5. Натрий реагирует с углеродом с образованием карбида:
1.6. При взаимодействии с кислородом при температуре 250–400º C натрий образует пероксид натрия:
2. Натрий активно взаимодействует со сложными веществами:
2.1. Натрий реагирует с водой . Взаимодействие натрия с водой приводит к образованию щелочи и водорода:
2Na 0 + 2 H2 O = 2 Na + OH + H2 0
2.2. Натрий взаимодействует с кислотами . При этом образуются соль и водород.
Например , натрий реагирует с разбавленной соляной кислотой :
2Na + 2HCl = 2NaCl + H2 ↑
2.3. Натрий может реагировать с аммиаком , при этом образуются амид натрия и водород:
2.4. Н атрий может взаимодействовать с гидроксидами:
Например , натрий взаимодействует с гидроксидом натрия при температуре 600º С:
2Na + 2NaOH = 2Na2O + H2
Видео:Окрашивание пламени соединениями натрияСкачать

Общая характеристика катионов I аналитической группы
Первая группа катионов
К первой аналитической группе относят катионы Na + , K + и NH4 + .
Соответствующие первым двум катионам элементы Na и К находятся в главной подгруппе первой группы периодической системы Д. И. Менделеева и являются s 1 — элементами. Все s 1 элементы — сильные восстановители, легко от- дают электрон, образуя катионы с зарядом + 1 и оболочкой инертного газа.
Катион NH4 + сложный ион, свойства его сходны со свойствами катиона К + , что объясняется зарядом ионов и близким значением их ионных радиусов. Сходные свойства приводят к одинаковому действию некоторых реактивов на эти ионы.
Соединения катионов Na + , K + , NH4 + , как правило, характеризуются хорошей растворимостью в воде и других полярных растворителях. Именно поэтому группа не имеет группового реактива. Только с крупными анионами катионы I группы дают труднорастворимые соединения, например, КНС4Н4О6, Na3[Со(NO2)6], K[Sb(OH)6]. Поэтому реактивы, содержащие подобные анионы, служат для обнаружения катионов I группы.
Гидроксиды калия и натрия — сильные щелочи, раствор аммиака в воде (гидроксид аммония NH4OH) — слабое основание.
Ионы Na + и К + гидролизу не подвергаются, поэтому соли этих катионов и сильных кислот имеют нейтральную реакцию раствора, а соли слабых кислот — щелочную. Катион NH4 + гидролизуется:
Следовательно, его соли, образованные сильными кислотами, имеют кислую реакцию раствора, а соли слабых кислот — нейтральную, слабокислую или слабощелочную, в зависимости от константы диссоциации слабой кислоты.
Катионы К + , Na + , NH4 + в растворе бесцветны и большинство их соединений также бесцветны, окрашенными являются соли, например, К2СrO4 (анион СrO 2- имеет желтую окраску), КМпО4 (анион МпО4 — имеет фиолетовую окраску).
Катионы I группы не проявляют способности к комплексообразованию, но могут входить во внешнюю сферу комплексных соединений.
Ионы Na + и К + имеют постоянную, устойчивую степень окисления и не участвуют в окислительно-восстановительных реакциях. Катион NH4 + может быть окислен только
очень сильными окислителями (хлорная вода, царская водка и другие) до свободного азота. Характерными реакциями этих ионов являются реакции обмена.
Соединения катионов I группы склонны к образованию пересыщенных растворов, поэтому при выполнении аналитических реакций, сопровождающихся образованием осадков, требуется тщательное перемешивание реакционной смеси. Как правило, осадки медленно кристаллизуются и имеют характерную форму кристаллов, что позволяет открывать эти ионы микрокристаллоскопическими реакциями. Для обнаружения катионов Na + и К + широко используют метод окрашивания пламени.
Реакции катиона калия К +
1. Гидротартрат натрия NaHC4H4O6(кислая соль винной кислоты) об- разует с растворами солей калия белый кристаллический осадок:
Осадок растворим в минеральных кислотах и щелочах (образование средних солей). Составьте и запишите соответствующие уравнения реакций.
Опыт.В пробирку налить 4 — 5 капель раствора соли калия (КСl, KNO3, K2SO4), прибавить равный объем гидротартрата натрия. Перемешать реакционную смесь стеклянной палочкой (если осадок не выпадает, слегка потереть ею о стенки пробирки) и охладить раствор под струей водопроводной воды. Чтобы убедиться в том, что осадок кристаллический, следует, закрыв про- бирку, сильно наклонить ее и рассмотреть прилипшие к стенкам и ко дну кристаллы КНС4Н4О6 (при подобном испытании аморфные и мелкокристаллические осадки легко отстают от стенок пробирки).
Испытать действие кислот и щелочей на осадок. Для этого, взмутив раствор, разделить его на три пробы. К первой добавить 1 — 2 капли сильной кислоты, ко второй — щелочи. К содержимому третьей пробы прибавить 2 капли дистиллированной воды и нагреть на водяной бане, осадок растворится. Он также растворяется при добавлении холодной воды. Реакция эта сравнительно малочувствительна (предельное разбавление 1:1000). На основании вышеизложенного можно сделать заключение об условиях проведения реакции. Реакцию необходимо проводить в нейтральной среде, при охлаждении и при достаточно большой концентрации ионов калия (разбавленные растворы можно предварительно упарить). Открытию катиона К + мешают ионы NH4 + , образующие с реактивом аналогичный осадок.
2. Гексанитрокобальтат(III) натрияNa3[Co(NO2)6] образует с катионом К + кристаллический желтый осадок комплексной соли гексанитро(III)кобальтата натрия-калия:
Осадок растворим в сильных кислотах (образование нестойкой кислоты Н3[Со(NO)2)6]). Присутствие щелочей мешает реакции, так как щелочь разлагая реактив, образует темно-бурый осадок Со(ОН)3.
Опыт.В пробирку налить 1 — 2 капли раствора КС1, прибавить 1 — 2 капли раствора реактива. Если осадок не выпадает, потереть стеклянной палочкой о стенки пробирки. Убедиться в том, что осадок кристаллический. Разделить осадок на две части. К первой добавить сильную кислоту до растворения осадка, ко второй — 4-5 капель уксусной кислоты СН3СООН (осадок не растворяется). Следовательно, реакцию необходимо проводить в нейтральной или слабокислой среде. Кроме того, следует учесть, что реактив должен быть свежеприготовленным, т. к. он сравнительно быстро разлагается и его бурая окраска переходит в розовую. Катион NH4 + мешает обнаружению иона К + . Реакция более чувствительная, чем первая (предельное разбавление составляет 1 : 13000).
3. Гексанитрокупрат (II) натрия-свинца Na2Pb[Cu(NO2)6]образует с катионами К + черные или коричневые кристаллы кубической формы:
Опыт А)В пробирку налить 2-3 капли раствора КС1, прибавить равный объем реактива, дать постоять и рассмотреть образовавшийся осадок.
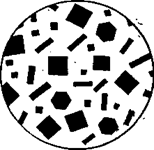
Б)Реакцию можно выполнять микрокристаллоскопическим методом. На чистое, сухое предметное стекло нанести каплю раствора соли калия, выпарить досуха, охладить и обработать каплей реактива. Через минуту рассмотреть образовавшиеся кристаллы под микроскопом (рис. 1).
Условия проведения реакции — в слабокислой или нейтральной среде (рН = 6 ÷ 7). Реакция достаточно чувствительная, обнаруживаемый минимум 7,5 мкг.
 |
2. Окрашивание пламени.Ионы К + окрашивают пламя в бледно- фиолетовый цвет.
Опыт.Платиновую или нихромовую проволочку тщательно очистить, для чего смочить ее в растворе НС1 и прокалить в пламени горелки до полного исчезновения окраски пламени. Ушком раскаленной проволочки при- коснуться к кристаллам соли калия и внести его в пламя горелки. Фиолетовое окрашивание пламени лучше наблюдать через синее стекло или флакон с раствором индиго.
Реакции катиона натрия Na +
1. Гексагидроксостибат (V) калияK[Sb(OH)6] образует с катионом Na + белый кристаллический осадок Na[Sb(OH)6]:
Осадок растворим в щелочи:
Кислоты разлагают реактив с образованием аморфного осадка метасурьмяной кислоты HSbO3:
Опыт.В пробирку налить 2 — 3 капли раствора соли NaCl, прибавить равный объем реактива, перемешать стеклянной палочкой и, если осадок не выпадает, потереть ею о стенки пробирки и охладить. Убедиться в том, что осадок кристаллический. Реакция малочувствительная, обнаруживаемый минимум — 0,3 мг. Реакция проводится в строго нейтральной среде при достаточно большой концентрации ионов Na + в растворе, при охлаждении и в отсутствии катионов NH4 + .
2. Окрашивание пламени.Соли натрия окрашивают пламя в желтый цвет. Окраска устойчивая, не исчезает в течение нескольких секунд. Реакция очень чувствительная; предел обнаружения этой реакции составляет 3 ∙ 10 -4 мкг, поэтому с ее помощью можно открывать ион Na + как примесь в реактивах. Вывод о присутствии натрия надо делать с большой осторожностью, только при очень яркой окраске пламени.
Опыт.Реакция проводится так же, как и на ион К + .
Реакции катиона аммония NH4 +
1. Щелочи NaOH и КОНпри нагревании разлагают соли аммония с вы- делением газообразного аммиака:
Опыт.В пробирку поместить 2 — 3 капли соли аммония, прибавить 1 — 2 капли раствора щелочи (не касаясь края пробирки) и нагреть. Выделение аммиака можно обнаружить по характерному запаху (специфическая реакция) или по изменению окраски влажной индикаторной бумаги, поднесенной к отверстию пробирки. Красная лакмусовая бумага синеет.
Реакция чувствительная, обнаруживаемый минимум — 0,01 мкг.
2. Реактив Несслера— раствор тетраиодомерурат (II) калия K2[HgJ4] и КОН образует с солями аммония красно-бурый аморфный осадок иодида оксодимеркурат (II) аммония [NH2Hg2O]J:
Опыт.К капле разбавленного раствора соли аммония на предметном стекле (или в пробирке) добавить 1-2 капли реактива Несслера. Наблюдать выпадение осадка.
Реакция очень чувствительная (обнаруживаемый минимум — 0,25 мкг).
Условия проведения опыта: при выполнении опыта необходимо брать избыток реактива Несслера, так как осадок растворим в солях аммония; открытию катиона NH4 + мешают катионы Fe 3+ , Cr 3+ , Co 2+ , Ni 2+ и другие, образующие окрашенные осадки с КОН.
В табл.1 представлены результаты действия некоторых реагентов на катионы I группы.
Видео:Окрашивание пламени солями натрияСкачать

Работа 1. Реакции катионов первой аналитической группы
Цель: изучить характерные качественные реакции наиболее распространенных катионов I группы, схему анализа катионов I группы.
Задачи: провести реакции обнаружения катионов калия, натрия, лития и катиона аммония, отметить их особенности, оформить лабораторную работу, ответить на теоретические вопросы, сделать выводы.
Оборудование: штатив с пробирками, водяная баня, пипетки на 1 мл, спиртовка, держатели для пробирок, спички, кобальтовое стекло, предметные стекла, микроскоп, платиновая, нихромовая или алюминиевая проволока, стеклянная палочка, индикаторная бумага или фильтровальная бумага, тигель (фарфоровая чашка).
Реактивы:
| 1. | соли калия, натрия, аммония и лития | 2. | гексанитрокобальтат (III) натрия — Na3[Co(NO2)6] |
| 3. | гидротартрат натрия – NaHC4H4O6 | 4. | нитрат ртути (II) или фенолфталеин (при необходимости) |
| 5. | гидроксид натрия – NaOH | 6. | соляная кислота – HCl |
| 7. | гексагидроксиантимонат калия (V) – K[Sb(OH)6] | 8. | гексанитрокупрат натрия и свинца – Na2Pb[Cu(NO2)6] |
| 9. | сульфат аммония – (NH4)SO4 | 10. | хлорид аммония – NH4Cl |
| 11. | гидроксид аммония – NH4ОН | 12. | гидроксид калия – KOH |
| 13. | уранилацетат – UO2(CH3COO)2, уранилацетат магния | 14. | реактив Несслера – K2[HgJ4] – щелочной р-р комплексной соли ртути |
| 15. | фторид аммония – NH4F | 16. | уксусная кислота – CH3COOH |
1.1. Реакции катиона калия К +
Опыт 1.1.1 Действие гексанитрокобальтата (III) натрия Na3[Co(NO2)6]
Данный реактив осаждает из нейтрального или слабощелочного раствора желтый кристаллический осадок гексанитрокобальтата (III) калия – натрия:
Этой реакции мешает:
а) сильнокислая среда, в которой образуется нестойкая кислота H3[Co(NO2)6], разлагающаяся с выделением оксида азота, однако, в уксусной кислоте ни сам реактив, ни осадок не разрушаются;
б) присутствие щелочей, которые разлагают реактив:
в) присутствие иона аммония, который образует с этим реактивом аналогичный осадок.
Таким образом, реакцию следует проводить в слабокислой среде при рН 3…5, в отсутствие ионов аммония, сильных окислителей и восстановителей.
Для выполнения реакции необходим свежеприготовленный раствор гексанитрокобальтата (III) натрия. Так как при хранении реактив разлагается с выделением ионов Со 2+ , имеющих розовую окраску. Порозовевший раствор реактива не пригоден к использованию.
Эта реакция очень чувствительна. Реакцию используют для осаждения иона K + из сыворотки при перманганатометрическом определении калия в крови.
Реакция является фармакопейной.
Выполнение опыта:
К небольшому количеству 1-2 мл раствора соли калия прилить немного раствора гексанитрокобальтата (III) натрия Na3[Co(NO2)6], встряхнуть и оставить на некоторое время. Наблюдать образование осадка. Рассмотреть каплю осадка в микроскоп, зарисовать форму кристаллов в тетрадь.
Изучить отношение осадка к кислотам, щелочам (Внимание! Концентрированные растворы кислот и щелочей находятся под тягой в вытяжном шкафу). Для этого разделить содержимое пробирки с осадком на две части. В первую пробирку прилить избыток раствора соляной кислоты, перемешать и наблюдать растворение значительной части раствора. Во вторую – добавить 2-3 капли раствора гидроксида натрия, наблюдать образование аморфного осадка гидроксида кобальта (III) желто-зеленоватого цвета.
Записать в тетрадь приведенное выше уравнение реакции и составить полное и сокращенное молекулярно-ионные уравнения.
Опыт 1.1.2. Действие гидротартрата натрия NaHC4H4O6
Гидротартрат натрия NaHC4H4O6, или винная кислота, в присутствии ацетата натрия при достаточной концентрации ионов калия К + в растворе дает белый кристаллический осадок гидротартрата калия:
Осадок растворяется в сильных кислотах и щелочах, поэтому реакцию проводят в нейтральной или слабокислой средах:
Реакцию следует проводить при охлаждении под струей водопроводной воды, так как растворимость осадка гидротартрата калия КНС4Н4О6 повышается при увеличении температуры. Для ускорения выпадения осадка стенки пробирки потирают стеклянной палочкой для образования центров кристаллизации.
Реакция протекает при больших концентрациях ионов калия К + и является малочувствительной. Реакцию проводят при рН 5…7 и, как уже упоминалось выше, в холодном растворе. Ионы аммония NH + 4 мешают определению ионов калия К + из-за того, что также дают белый кристаллический осадок с этими реагентами и поэтому соли аммония предварительно разлагают при нагревании.
Реакция является фармакопейной.
Выполнение опыта:
К небольшому количеству раствора соли калия прилить такое же количество раствора гидротартрата натрия NaHC4H4O6 , затем потереть стеклянной палочкой о стенки пробирки, охладив пробирку, при необходимости, под струей холодной воды из под крана. Наблюдать образование объёмистого мелкокристаллического осадка белого цвета. Каплю осадка перенести на предметное стекло и рассмотреть под микроскопом.
Изучить отношение осадка к сильным кислотам и щелочам, температуре. Для этого необходимо разделить содержимое пробирки на три части. В первую пробирку добавить несколько капель соляной кислоты, во вторую – гидроксид натрия. Наблюдать растворение осадков. Третью пробирку поместить в стакан с горячей водой, перемешать содержимое пробирки стеклянной палочкой. После охладить при комнатной температуре. Наблюдать исчезновение и появление осадка вновь.
Записать в тетрадь уравнения реакций, составить полное и сокращенное молекулярно-ионные уравнения.
Опыт 1.1.3. Микрокристаллоскопическая реакция с гексанитрокупратом натрия и свинца Na2Pb[Cu(NO2)6]
При взаимодействии солей калия с гексанитрокупратом натрия и свинца Na2Pb[Cu(NO2)6] образуется микрокристаллический осадок комплексной соли гексанитрокупрата калия и свинца:
Выполнение опыта:
Выпарить до суха на предметном стекле каплю раствора соли калия (на водяной бане), смочить сухой остаток каплей реактива Na2Pb[Cu(NO2)6] (тройным нитритом натрия, свинца и меди).
Наблюдать под микроскопом образующиеся характерные чёрные кубические кристаллы K2Pb[Cu(NO2)6].
Зарисовать в тетрадь кристаллы, записать уравнение реакции в молекулярном и молекулярно-ионном виде.
Опыт 1.1.4. Реакция окрашивания пламени солями калия (фармакопейный тест)
Соли калия или их растворы, внесенные на платиновой, нихромовой или алюминевой проволоке в бесцветное пламя горелки, окрашивают его в фиолетовый цвет. Присутствие даже ничтожных следов натрия, окрашивающего пламя в желтый цвет, что мешает увидеть окраску. Поэтому пламя рассматривают через синее кобальтовое стекло.
Выполнение опыта:
Взять проволоку, убедиться, что она чистая, для чего внести ее в пламя спиртовки. Если пламя не окрашивается, можно проводить реакцию на обнаружение иона калия. Если окрашивается, то проволоку следует очистить, обработав концентрированной соляной кислотой и прокалив в пламени спиртовки до исчезновения окрашивания пламени.
Обмакнуть очищенную проволоку в пробирку с раствором соли калия и внести ее в пламя спиртовки. Пламя окрасится в характерный бледно-фиолетовый цвет. Рассмотреть пламя через синее кобальтовое стекло, поглощающее желтое окрашивание солей натрия.
Записать наблюдения в тетрадь.
1.2. Реакции катиона натрия Na +
Опыт 1.2.1. Реакция с гексагидроксиантимонатом (V) калия K[Sb(OH)6]
Соли натрия образуют с гексагидроксиантимонатом (V) калия K[Sb(OH)6] кристаллический осадок натриевой соли. Его следует отличать от аморфного осадка метасурьмяной кислоты HSbO3 , которая может выпасть в осадок при pH 2+ и Mg 2+ ), то она идет быстро с образованием желтых осадков тройных солей NaZn(UO2)3(CH3COO)9x9H2O или NaMg(UO2)3(CH3COO)9x9H2O. При наблюдении в микроскоп видны тетраэдры и октаэдры правильной формы. Полученные осадки обладают сильной люминесценцией в ультрафиолетовом свете.
Выполнение опыта:
Добавить 1 мл раствора реактива уранилацетата к исследуемому раствору соли натрия. Через некоторое время наблюдать образование желтого осадка.
Реакцию можно провести и другим способом: в чистой центрифужной пробирке к 1 капле прозрачного р-ра прибавляют 3 капли уранилацетата магния. Хорошо взболтать и оставить на 10 минут. Провести наблюдение. Записать уравнение реакции.
Опыт 1.2.3. Реакция окрашивания пламени солями натрия (фармакопейный тест)
Летучие соли натрия окрашивают пламя в ярко-желтый цвет. Реакция очень чувствительна и характерна для натрия.
Выполнение опыта:
Взять проволоку, убедиться, что она чистая, для чего внести ее в пламя спиртовки. Если пламя не окрашивается, можно проводить реакцию на обнаружение иона натрия. Если окрашивается, то проволоку следует очистить, обработав концентрированной соляной кислотой и прокалив в пламени спиртовки до исчезновения окрашивания пламени.
Обмакнуть очищенную проволоку в пробирку с раствором соли натрия и внести ее в пламя спиртовки. Пламя окрасится в характерный желтый цвет. Записать наблюдения в тетрадь.
1.3. Рекция катиона аммония NH 4 +
Опыт 1.3.1. Действие щелочей
При взаимодействии хлорида аммония и гидрооксида натрия выделяется аммиак. Аммиак, растворяясь в воде, образует основание гидроксид аммония NH4OH:
Выполнение опыта:
К небольшому количеству раствора соли аммония, например NH4Cl, прилить немного щелочи (NaОН или КОН) и нагреть. Реакция специфична.
Выделение аммиака NH3 можно обнаружить по запаху. Но лучше воспользоваться индикаторной бумагой. Для этого необходимо подержать в парах над нагреваемой пробиркой влажную лакмусовую или фенолфталеиновую бумажку, не касаясь внутренней поверхности ее стенок, — бумажка посинеет, а в случае с фенолфталеином станет малиновой. Вместо индикаторной бумаги можно применить фильтровальную бумагу, смоченную раствором нитрата ртути (II) Hg(NO3)2. Под действием аммиака бумага почернеет из-за выделившейся на ее поверхности металлической ртути.
Составить молекулярное и сокращенное молекулярно-ионное уравнения реакции получения NH4OH и уравнение реакции его разложения при нагревании.
Опыт 1.3.2. Действие реактива Несслера (К2 [HgJ4]+KOH)
При действии реактива Несслера на соль аммония образуется красно-бурый осадок комплексной соли иодида оксодимеркураммония. Реакция очень чувствительна и показывает присутствие даже случайных примесей NH4 + . Кроме того, это специфическая реакция:
Выполнение опыта:
К 1-2 мл раствора соли аммония прилить 2-3мл реактива Несслера и наблюдать образование красно-бурого осадка.
Записать уравнение в тетрадь, составить молекулярно-ионные уравнения реакции.
1.4. Реакции катиона лития Li +
Опыт 1.4.1. Реакция окрашивания пламени солями лития
Летучие соединения лития окрашивают бесцветное пламя горелки (спиртовки) в карминово-красный цвет. Реакция весьма чувствительна. Определению мешают ионы натрия. Желтую окраску ионов Na + маскируют, используя индиговую призму или кобальтовое стекло, не пропускающее желтых лучей.
Выполнение опыта:
Взять проволоку, убедиться, что она чистая, для чего внести ее в пламя спиртовки. Если пламя не окрашивается, можно проводить реакцию на обнаружение иона лития. Если окрашивается, то проволоку следует очистить, обработав концентрированной соляной кислотой и прокалив в пламени спиртовки до исчезновения окрашивания пламени.
Обмакнуть очищенную проволоку в пробирку с раствором соли лития и внести ее в пламя спиртовки. Пламя окрасится в характерный карминово-красный цвет. Рассмотреть пламя через синее кобальтовое стекло, поглощающее желтое окрашивание солей натрия.
Записать наблюдения в тетрадь.
Опыт 1.4.2. Реакция с фторидом аммония или калия
При нагревании смеси солей лития с фторидом калия или аммония выделяется белый аморфный осадок фторида лития, растворимый в уксусной кислоте:
Определению мешают ионы Mg 2+ , которые можно замаскировать, проводя реакцию в присутствии аммиака при рН 9-10.
Выполнение опыта:
В пробирку внести 3-4 капли раствора соли лития, 1- 2 капли концентрированного аммиака и 4-5 капель раствора фторида аммония NH4F. Смесь нагреть. Наблюдать медленно выпадающий аморфный осадок фторида лития.
Изучить растворимость осадка в уксусной кислоте. Для этого добавить в пробирку с осадком раствор уксусной кислоты.
Записать наблюдения и уравнения реакций в тетрадь.
Контрольные вопросы
1. По каким признакам классифицируют методы качественного анализа?
2. Назовите требования, предъявляемые к аналитическим реакциям?
3. Перечислите виды аналитических реакций?
4. С помощью каких методов проводят анализ смеси ионов?
5. На чем основана кислотно-основная классификация катионов?
6. На какие группы делит катионы кислотно-основная классификация?
7. На чем основана сульфидная классификация катионов?
8. На какие группы делит катионы сульфидная классификация?
9. Дайте характеристику первой группы катионов.
10. Есть ли групповой реагент у катионов данной группы?
11. Используя какой реактив(ы) можно обнаружить катион калия К + ?
12. В какой цвет окрашивают пламя соли натрия?
13. С помощью каких реакций обнаруживают ион аммония NH4 + ?
14. В какой цвет окрашивают пламя соли лития?
15. С помощью каких реакций обнаруживают ион аммония Li + ?
16. Что означает выражение «реакция является фармакопейной»?
Глава 2
Последнее изменение этой страницы: 2019-10-04; Просмотров: 1628; Нарушение авторского права страницы
🎦 Видео
Пирохимические реакции (окрашивание пламени горелки). Качественный анализ.Скачать

Окрашивание пламени солями калияСкачать

Окрашивание пламени солями натрияСкачать

Окрашивание пламени солями медиСкачать

10. Окрашивание пламени солями натрияСкачать

Качественные реакции на катионы. 9 класс.Скачать

Химия. 9 класс. Качественные реакции на катионы /07.10.2020/Скачать

Как Сделать ОГНЕННУЮ РАДУГУ? Самая большая в Мире!Скачать

Спектральный анализ. Окрашивание пламени ионами металловСкачать

Разбор задания 32. Желтая окраска пламениСкачать

Поджигаем спичку марганцовкой и перекисью водорода #shortsСкачать

Окрашивание пламени ионами натрияСкачать

Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

Реакция лития, натрия и калия с водойСкачать

Решение задач на термохимические уравнения. 8 класс.Скачать




