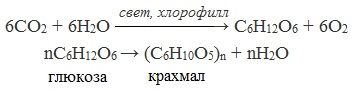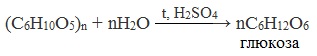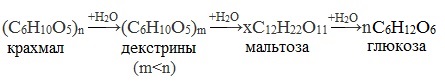Крахмал – ценный питательный продукт. Он входит в состав хлеба, картофеля, круп и наряду с сахарозой является важнейшим источником углеводов в человеческом организме.
Химическая формула крахмала (С6(Н2О)5) n .
- Строение крахмала
- Амилоза
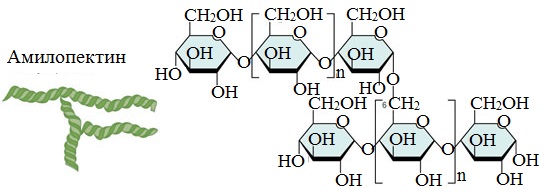
- Амилопектин
- Биологическая роль крахмала. Гликоген
- Превращение крахмала в организме человека и животных
- Нахождение в природе
- Физические свойства
- Химические свойства крахмала
- Получение крахмала
- Применение крахмала
- Как приготовить крахмальный клейстер
- Что такое крахмальный клейстер
- Как выглядит
- Вязкость и плотность
- Химическая формула
- Свойства крахмального клейстера
- Применение
- Крахмальный клейстер в фармацевтическом производстве
- Раствор Люголя
- Посев моркови в крахмальном клейстере
- Склейка гофрокартона
- Рецепт приготовления
- Водоотталкивающие добавки
- Качественная реакция на крахмал
- Крахмальный клейстер и йод: уравнение реакции
- Опыт с клейстером и глицерином
- Поведение крахмала в холодной воде
- Плюсы и минусы
- Опыт 7. Влияние температуры на химическое равновесие
Строение крахмала
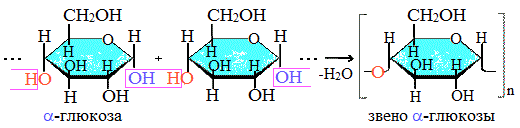
Крахмал состоит из 2 полисахаридов, построенных из остатков циклической a-глюкозы.
Как видно, соединение молекул глюкозы происходит с участием наиболее реакционноспособных гидроксильных групп, а исчезновение последних исключает возможность образования альдегидных групп, и они в молекуле крахмала отсутствуют. Поэтому крахмал не дает реакцию «серебряного зеркала».
Крахмал состоит не только из линейных молекул, но и из молекул разветвленной структуры. Этим объясняется зернистое строение крахмала.
В состав крахмала входят:
- амилоза (внутренняя часть крахмального зерна) — 10-20%;
- амилопектин (оболочка крахмального зерна) — 80-90%.
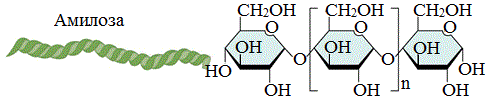
Амилоза
Амилоза растворима в воде и представляет собой линейный полимер, в котором остатки α–глюкозы связаны друг с другом через первый и четвертый атомы углерода (α-1,4-гликозидными связями).
Цепь амилозы включает 200 — 1000 остатков a-глюкозы (средняя мол. масса 160 000) .
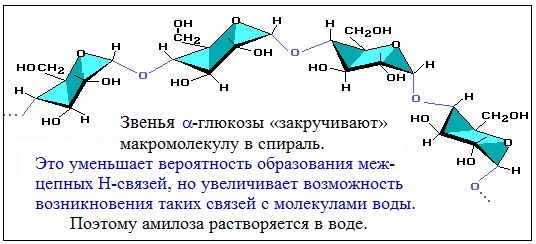
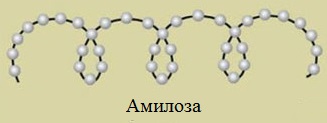
Макромолекула амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев a-глюкозы.
Амилопектин
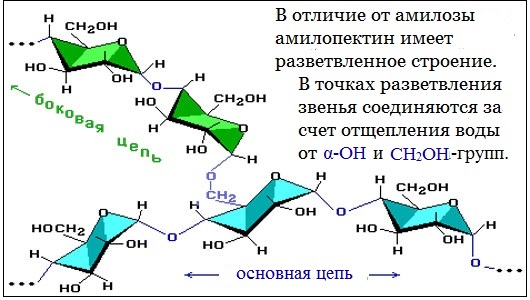
В отличие от амилозы, амилопектин не растворим в воде, и имеет разветвленное строение.
Подавляющее большинство глюкозных остатков в амилопектине связаны, как и в амилозе α-1,4-гликозидными связями. Однако в точках разветвлений цепи имеются α-1,6-гликозидные связи.
Молекулярная масса амилопектина достигает 1-6 млн.
Молекулы амилопектина также довольно компактны, так как имеют сферическую форму.
Биологическая роль крахмала. Гликоген
Крахмал – главное запасное питательное вещество растений, основной источник резервной энергии в растительных клетках.
Остатки глюкозы в молекулах крахмала соединены достаточно прочно и в то же время под действием ферментов легко могут отщепляться, как только возникает потребность в источнике энергии.
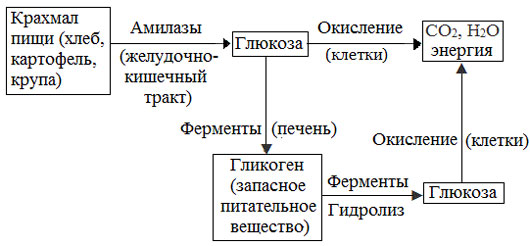
Амилоза и амилопектин гидролизуются под действием кислот или ферментов до глюкозы, которая служит непосредственным источником энергии для клеточных реакций, входит в состав крови и тканей, участвует в обменных процессах.
Гликоген (животный крахмал) – полисахарид, молекулы которого построены из большого числа остатков α–глюкозы. Он имеет сходное строение с амилопектином, но отличается от него большей разветвленностью цепей, а также большей молекулярной массой.
Содержится гликоген главным образом в печени и в мышцах.
Гликоген – белый аморфный порошок, хорошо растворяется даже в холодной воде, легко гидролизуется под действием кислот и ферментов, образуя в качестве промежуточных веществ декстрины, мальтозу и при полном гидролизе – глюкозу.
Превращение крахмала в организме человека и животных
Нахождение в природе
Крахмал широко распространен в природе. Он образуется в растениях в процессе фотосинтезе и накапливается в клубнях, корнях, семенах, а также в листьях и стеблях.
Крахмал содержится в растениях в виде крахмальных зерен. Наиболее богато крахмалом зерно злаков: риса (до 80%), пшеницы (до 70%), кукурузы (до 72%), а также клубни картофеля (до 25%). В клубнях картофеля крахмальные зерна плавают в клеточном соке, в злаках они плотно склеены белковым веществом клейковиной.
Физические свойства
Крахмал – белое аморфное вещество, без вкуса и запаха, нерастворимое в холодной воде, в горячей воде набухает и частично растворяется, образуя вязкий коллоидный раствор (крахмальный клейстер).
Крахмал существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
Химические свойства крахмала
Химические свойства крахмала объясняются его строением.
Крахмал не дает реакцию «серебряного зеркала», однако ее дают продукты его гидролиза.
1. Гидролиз крахмала
При нагревании в кислой среде крахмал гидролизуется с разрывом связей между остатками α-глюкозы. При этом образуется ряд промежуточных продуктов, в частности мальтоза. Конечным продуктом гидролиза является глюкоза:
Процесс гидролиза протекает ступенчато, схематически его можно изобразить так:
Видеоопыт «Кислотный гидролиз крахмала»
Реакцию превращения крахмала в глюкозу при каталитическом действии серной кислоты открыл в 1811 г. русский ученый К.Кирхгоф (реакция Кирхгофа).
2. Качественная реакция на крахмал
Так как молекула амилозы представляет собой спираль, то при взаимодействии амилозы с йодом в водном растворе молекулы йода входят во внутренний канал спирали, образуя так называемое соединение включения.
Раствор иода окрашивает крахмал в синий цвет. При нагревании окрашивание исчезает (комплекс разрушается), при охлаждении появляется вновь.
Крахмал + J2 – синее окрашивание
Видеоопыт «Реакция крахмала с йодом»
Данная реакция используется в аналитических целях для обнаружения, как крахмала, так и йода (йодкрахмальная проба)
3. Большинство глюкозных остатков в молекулах крахмала имеют по 3 свободных гидроксила (у 2,3,6-го атомов углерода), в точках разветвления – у 2-го и 3-го атомов углерода.
Следовательно, для крахмала возможны реакции, характерные для многоатомных спиртов, в частности образование простых и сложных эфиров. Однако эфиры крахмала большого практического значения не имеют.
Качественную реакцию на многоатомные спирты крахмал не дает, так как плохо растворяется в воде.
Получение крахмала
Из растений извлекают крахмал, разрушая клетки и отмывая его водой. В промышленном масштабе его получают главным образом из клубней картофеля (в виде картофельной муки), а также кукурузы, в меньшей степени – из риса, пшеницы и других растений.
Получение крахмала из картофеля
Картофель моют, измельчают и промывают водой и перекачивают в большие сосуды, где происходит отстаивание. Вода извлекает из измельченного сырья крахмальные зерна, образуя так называемое «крахмальное молоко».
Полученный крахмал ещё раз промывают водой, отстаивают и сушат в струе теплого воздуха.
Получение крахмала из кукурузы
Зерна кукурузы замачивают в теплой воде разбавленной сернистой кислоты с целью размягчения зерна и удаления из него основной части растворимых веществ.
Набухшее зерно дробят для удаления ростков.
Ростки, после всплывания на поверхность воды, отделяют и используют в дальнейшем для получения кукурузного масла.
Кукурузную массу повторно измельчают, обрабатывают водой для вымывания крахмала, затем отделяют отстаиванием или с помощью центрифуги.
Применение крахмала
Крахмал широко применяется в различных отраслях промышленности (пищевой, фармацевтической, текстильной, бумажной и т.п.).
Он является основным углеводом пищи человека – хлеба, круп, картофеля.
В значительных количествах перерабатывается на декстрины, патоку и глюкозу, используемые в кондитерском производстве.
Из крахмала, содержащегося в картофеле и зерне злаков, получают этиловый, н-бутиловый спирты, ацетон, лимонную кислоту, глицерин.
Крахмал используется как клеящее средство, применяется для отделки тканей, крахмаления белья.
В медицине на основе крахмала готовятся мази, присыпки и т.д.
Как приготовить крахмальный клейстер
Крахмальный клейстер применяется для соединения легких материалов: дерева, бумаги, картона. Используется для изготовления поделок из папье-маше, поклейки обоев, закрепления бумажных листов на поверхностях.
Что такое крахмальный клейстер
Это разновидность клея, приготовленная из картофельного либо кукурузного крахмала. Используется в быту, творчестве и производстве.
Обработка клейстера щелочью позволяет получить пищевую добавку Е1404, которая добавляется в консервы и хлебобулочные изделия. Также с веществом проводят химические опыты – реакции на крахмал и выявление содержания хлора в воздухе.
Как выглядит
Консистенция напоминает мутный кисель. На ощупь склизкий, слегка склеивает пальцы. Запах нейтральный.
Вязкость и плотность
Эти показатели определяют качественные свойства вещества:
- В процессе клейстеризации крахмал, разведенный водой, приобретает вязкость. Крахмал из картофеля дает более вязкое вещество, чем кукурузный. Вязкость зависит от многих условий: температуры, состава, технологии приготовления. У качественного продукта этот показатель высок.
- Плотность вещества – отношение массы к объему. Клейстер из картофельного крахмала более плотный, чем из кукурузы. Чем меньше воды добавлено в исходный порошок, тем плотнее получается продукт.
Хороший клейстер обладает высокой вязкостью.
Химическая формула
Крахмал является полисахаридом. Он состоит из амилозы и амилопектина. Химическая формула крахмального клейстера выглядит следующим образом:
Также формула зависит от добавок, применяемых для получения улучшенного вещества. Конечная субстанция является коллоидной взвесью крахмала в жидкости.
Свойства крахмального клейстера
Клейстеризация – процесс, происходящий с крахмальным порошком при нагревании в воде. Попавшие во влагу молекулы увеличиваются в диаметре благодаря содержанию амилопектина. Готовый раствор приобретает вязкость, которая имеет ключевое практическое значение.
Клейстер обладает способностью к склеиванию материалов, чем и обуславливается его ценность.
Применение
Простота приготовления и безопасность позволяют использовать продукт в различных областях быта и промышленности.
- Ремонт жилья. Используется как грунтовка и как замена обойному клею. Не оставляет следов и разводов, без проблем удаляется при необходимости. Наносится обыкновенной кисточкой.
- Творчество. Применяется для папье-маше как самостоятельный клей или в смеси с ПВА, в детских садах и начальных классах – для поделок и аппликаций.
- Производство. Используется для склеивания гофрокартона и в изготовлении таблеток в фармацевтике.
- Охрана здоровья. Для определения избыточных концентраций хлора смешивают крахмальный клейстер и йод: реакция, при которой йод выступает на поверхность, означает наличие опасного хлора в воздухе.
- Садовые работы. В клейстере высаживают семена моркови.
- Медицина. Используется при отравлении как вещество, которое облегчает рвоту и выводит токсины из организма.
Распространенность и простота в приготовлении позволяют употреблять продукт для самых разных нужд.
Крахмальный клейстер в фармацевтическом производстве
Добавляется как связывающее вещество в процессе овлажнения. Овлажнение – это технология, которая применяется для формирования нужных размера и массы таблетки. 5% раствор крахмала и воды смешивается с сиропом, желатином, спиртом для связывания таблетируемого вещества.
Раствор Люголя
Раствор Люголя получают смешиванием йода, йодида калия, глицерина и воды. Применяется при заболеваниях верхних дыхательных путей для уничтожения бактерий. В домашних условиях позволяет определить наличие крахмала в веществе.
Если капнуть раствор в крахмалосодержащую субстанцию, она посинеет. Таким образом можно определить качество сметаны или муки. Если в этих продуктах есть крахмал (чего быть не должно), они поменяют цвет.
Посев моркови в крахмальном клейстере
Технология улучшает всхожесть и упрощает процесс посадки, ведь морковные семечки очень мелкие, равномерно посеять их сложно.
Для посадки моркови в крахмальном клейстере потребуется:
- Отсортировать семена, высыпав их в подсоленную воду. Если они опали на дно, то дадут хорошие всходы. Всплывшее семечко не годится для посадки.
- Замочить семена на несколько суток. Каждые 12 часов необходимо менять воду.
- Сделать в почве бороздки глубиной в 2-3 см, утрамбовать дно, увлажнить.
- Вылить в бороздки клейстер, смешанный с семенами.
- Присыпать грунтом слоем 1-2 см.
Данный способ посадки гарантирует отличную всхожесть моркови.
Склейка гофрокартона
Клейстер из тапиоки, картофеля или кукурузы ценится как безвредное средство для производства гофрокартона. В состав добавляют буру, каустическую соду и медный купорос для предотвращения развития плесени.
Рецепт приготовления
Приготовить клейстер из крахмала можно дома. Помимо порошка, понадобится только вода.
Чтобы сделать крахмальный клейстер для детского творчества, достаточно одного пакетика крахмала, для ремонта потребуется больше.
- В стакане воды размешать 5 больших ложек крахмала до однородной консистенции.
- В тару вылить 200 г воды, довести до кипения.
- В кипящую воду вылить полученный раствор.
- Варить при непрерывном помешивании 3-4 минуты.
Перед использованием клейстер необходимо остудить. Можно перелить в бутылку или банку.
Сварить крахмальный клейстер можно другим способом:
- Смешать крахмал и воду в соотношении 1 к 10.
- Варить до кипения, помешивая.
- Остудить горячую смесь.
- Добавить присадки при необходимости.
В качестве присадки при приготовлении крахмального клейстера используется клей ПВА (соотношение с клейстером 1:2). Поливинилакрилат улучшает вязкость и скрепляющие свойства.
Водоотталкивающие добавки
Для придания гидрофобных свойств используются термореактивные добавки. Необходимы при изготовлении гофрокартона и изделий из него. Улучшают прочность шва и качество продукта.
Наибольшее распространение получили добавки серии CP-88. Они уменьшают расход клея. Использование CP-88 позволяет изделиям из гофрокартона держать шов в атмосфере с повышенной влажностью.
В быту такие присадки используют при поклейке обоев в сырых помещениях. При добавлении вещества следует держать окна открытыми. Качество полученного раствора не уступает дорогим обойным клеям.
Качественная реакция на крахмал
Лабораторный опыт требуется для определения углеводов в веществе. Входит в школьную программу уроков химии.
Для проведения реакции приготавливается небольшое количество клейстера, который разливается в две пробирки. В первую нужно добавить несколько капель йода, а вторую оставить для сравнения.
Пробирку с йодом нужно нагреть и понаблюдать за реакцией. Мальтодекстрины, образующиеся в процессе нагревания, не взаимодействуют с йодом. Окраска исчезнет.
Далее пробирка охлаждается. При охлаждении крахмал вновь вступает в реакцию с йодом и приобретает синий оттенок.
Крахмальный клейстер и йод: уравнение реакции
Чтобы провести опыт, потребуется сам клейстер и немного йода. Условия опыта:
- Небольшая пробирка частью заполняется клейстером.
- Добавляется йод в количестве 2-3 капель.
- Окрашивание в синий цвет свидетельствует о наличии крахмала в веществе.
- Цвет при окрашивании может разниться – от темно-синего до фиолетового.
- Если содержимое пробирки не окрасилось – в ней не клейстер, а другое вещество.
Опыт с клейстером и глицерином
В одну пробирку наливается глицерин, в другую – крахмал. В обе пробирки капается йод. Глицерин не дает реакции: раствор останется неокрашенным. Пробирка с крахмалом окрасится в характерный синий цвет.
Поведение крахмала в холодной воде
Основные вещества, входящие в состав крахмала – полисахариды амилоза и амилопектин. Оба вещества растворимы в горячей воде. Приготовить клейстер в холодной воде невозможно.
Плюсы и минусы
Широкое распространение и длительный опыт использования позволяет выделить следующие плюсы клейстера:
- Безопасность. Главное преимущество в детском творчестве. Крахмал относится к пищевым добавкам и нетоксичен при проглатывании, не склеивает пальцы, не раздражает слизистые оболочки.
- Простота получения. Приготовить клей можно при наличии всего двух компонентов: крахмала и воды. Процесс не требует специальных знаний и оборудования, занимает всего несколько минут.
- Универсальность. Незаменим в быту для поклейки обоев, в производстве, в творчестве и химических опытах. Облегчает работу в огороде, ремонт в доме.
- Доступность. Крахмал дешев, его можно купить практически в любом хозяйственном или продуктовом магазине.
Из минусов можно выделить:
- Слабую водостойкость. Без специальных присадок клей не годится для широкого производства. Клеевой шов может разойтись в помещении с очень высокой влажностью, клейстер бесполезен для поклейки обоев в туалете и ванной комнате.
- Небольшой срок годности. Без холодильника раствор «живет» от нескольких часов до суток. Максимальный срок хранения – не более 3 дней.
За свои преимущества клейстер до сих пор остается одним из самых популярных органических клеев.
Опыт 7. Влияние температуры на химическое равновесие
Налить в две пробирки 2-3 мл раствора крахмала и добавить в каждую из них по 2 капли иодной воды. Наблюдать появление синей окраски. Наг-реть одну из пробирок. Что наблюдаете? Определить на основе наблюдений, является ли эта реакция эндо- или экзотермической. Объяснить изменение окраски при нагревании смещением химического равновесия.
чяПри взаимодействии йода с крахмалом образуется вещество сложного состава , окрашенное в синий цвет. Эта реакция экзотермическая. Равновесие системы можно условно изобразить следующим уравнением:
крахмал + йод Û соединение синего цвета + Q
Йодокрахмал относится к особому классу соединений, называемых соединениями включения. Соединение образуется путем внедрения молекул йода в полости молекул крахмала.
Дата добавления: 2015-09-29 ; просмотров: 6292 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ