Задание 176. Дайте определения терминам «полимер», «реакция полимериза ции». Полимер — соединение, молекулы которого состоят из большого количества групп атомов одинакового строения. Реакцию соединения многих одинаковых молекул вследствие разрушения кратных связей называют реакцией полимеризации
Задание 177. Укажите правильное окончание предложения «На концах молекул полиэтилена находятся группы атомов …»:
Задание 178. Одна из молекул в образце полиэтилена тяжелеэ молекулы в оды в 700 раз. Определите значение n для формулы этой мо лекулы.
M ( ( -СH 2 — CH 2 — ) n ) =28n г/моль.
28n/18=700, 28n=700 • 18, n=700 • 18:28, n=450
Задание 179. Какой объем этилена образуется (в пересчете на нормаль ные условия) в результате термического разложения 3,5 г поли этилена?
Дано: формула полиэтилена ( -СH 2 — CH 2 — )k, m( ( -СH 2 — CH 2 — )k )=3,5 г.
Пишем уравнение термического разложения полиэтилена:
Вычисляем количество вещества полиэтилена по формуле n=m/M, где M=M r г/моль.
За уравнением реакции соотношение количества веществ полиэтилена и этилена n (( -СH 2 — CH 2 — )k ): n( СH 2 = CH 2)=1:k, то есть в результате термического розложения любого количества вещества полиэтилена образуется этилен в k раз большего количества, поэтому
n( СH 2 = CH 2)=n( -СH 2 — CH 2 — )n) • k=(1,125/k) • k=1,125 моль
С формулы n=V/VM, где VM=22,4 л/моль при н.у., находим объем этилена V=n•VM.
V( СH 2 = CH 2)=n( СH 2 = CH 2)•VM=0,125 моль•22,4 л/моль=2,8 л.
Ответ: V( СH 2 = CH 2)=2,8 л.
Задание 180. Какой объем воздуха (н.у.) необходим для сжигания 140 г полиэти лена? Считайте, что объемная доля кислорода в воздухе равна 20%.
Дано: формула полиэтилена ( -СH 2 — CH 2 — )k, m( ( -СH 2 — CH 2 — )k )=140 г,
φ(O2 )=20% либо 0,2. Найти: V(воздуха)-?
I cпособ
Вычисляем количество вещества полиэтилена по формуле n=m/M, где M=Mrг/моль.
Пишем уравнение горения полиэтилена:
Соотношение количества реагентов (в молях) равно соотношению соответствующих коэффициентов в уравнении реакции. За соотношением n (( -СH 2 — CH 2 — )k):n(О2 )=1:3k, видим, что количество вещества кислорода в 3k раза больше, поэтому
v(О2 )=3k • v(( -СH 2 — CH 2 — )m) = 3k • 5/k моль=15 моль.
С формулы n=V/VM, где VM=22,4 л/моль при н.у., находим объем V=n•VM.
С формулы вычисления объенной доли вещества φ(вещества)=V(вещества)/V(смеси) находим V(смеси)=V(вещества)/φ(вещества).
ІІ способ
Пишем уравнение горения полиэтилена :
Над формулами веществ ( -СH 2 — CH 2 — ) k и O 2 пишем cогласно условию задачи массу полиэтилена (140 г) и неизвестный объем кислорода (х л), а под формулами веществ — массу и объем соответствующего количества вещества согласно коэффициентам в химическом уравнении. Для этого вычисляем молярную массу (M=Mr г/моль) полиэтилена и, соответственно, массу 1 моль, так как прореагировало 1 моль полиэтилена с 3k моль кислорода O2 (1 моль газа при н.у. занимает объем 22,4 л, поэтому k моль кислорода займут в k раз больше объем, то есть 22,4k л, а 3k моль газа — 67,2k л).
M(( -СH 2 — CH 2 — )k)=28k г/моль, поэтому масса 1 моль=28k г.
Составляем пропорцию и решаем её:
по уравнению реакции: 28k г полимера реагирует с 67,2k л O2,
по условию задачи: 140 г полимера — с х л O2.
28k г / 140 г = 67,2k л / х л
х л • 28k г = 140 г • 67,2k л
х = 140 г • 67,2k л / 28k г
В воздухе кислорода около 20% по объему (или 1/5 часть), поэтому воздуха надо взять в 5 раз большего объема, то есть 5 • 336 л= 1680 л.
Ответ: V(воздуха)=1680 л.
Задание 181. Подготовьте сообщение об утилизации использованных изделий из полиэтилена.
1. Многократная переработка изделий из полиэтилена и других полимерных материалов.
2. Энергетическая утилизация: сжигание с применением соответствующих технологий для получения тепла.
Лабораторный опыт 13. Свойства полиэтилена ГДЗ Химия 10-11 класс Цветков.
Какие тут ответы и выыоды?
1. Образец полиэтилена нагрейте несильно (держите щипцами) над пламенем спиртовки или газовой горелки. Наблюдайте постепенное размягчение полимера и затем его плавление. Стеклянной или деревянной палочкой измените форму размягченного полиэтилена и дайте ему остыть. Попытайтесь изменить форму образца при обычной температуре. Какое свойство полиэтилена лежит в основе наблюдаемых явлений? Какое практическое значение оно имеет?
2. Подожгите образец полиэтилена. Обратите внимание, горит ли он вне пламени. Какого цвета пламя? Образуется ли при этом копоть? Обладают ли продукты горения запахом?
3. В пробирки с бромной водой и раствором перманганата калия поместите гранулы или мелкие кусочки полиэтилена. Наблюдайте, происходит ли изменение окраски растворов. Действуют ли эти вещества на полимер?
4. В пробирку с растворами серной кислоты и щелочи поместите измельченные кусочки полиэтилена.
Какой вывод о химических свойствах полимера можно сделать на основании проведенных опытов?
Горение полимеров и полимерные материалы пониженной горючести
Чт, 12 Ноябрь 2009 | Тема: Технологии
Существенным фактором, сдерживающим внедрение разнообразных полимерных материалов, является их пожарная опасность, обусловленная горючестью и сопутствующими процессами. Пожарная опасность материалов и изделий из них определяется в технике следующими характеристиками: 1) горючестью, то есть способностью материала загораться, поддерживать и распространять процесс горения; 2) дымовыделением при горении и воздействии пламени; 3) токсичностью продуктов горения и пиролиза — разложения вещества под действием высоких температур; 4) огнестойкостью конструкции, то есть способностью сохранять физико-механические (прочность, жесткость) и функциональные свойства изделия при воздействии пламени. В свою очередь, горючесть — это комплексная характеристика материала или конструкции. Она включает следующие величины: 1) температуру воспламенения или самовоспламенения; 2) скорости выгорания и распространения пламени по поверхности; 3) предельные параметры, характеризующие условия, при которых возможен самоподдерживающийся процесс горения, например состав атмосферы (кислородный индекс) или температура (температурный индекс).
Следует отметить, что перечисленные выше характеристики пожарной опасности и горючести часто являются противоречивыми и улучшение одного из свойств может сопровождаться ухудшением других. Кроме того, введение добавок, снижающих пожарную опасность полимерных материалов, обычно приводит к некоторому ухудшению физико-механических, диэлектрических и других эксплуатационных и технологических свойств, а также повышению стоимости материала. Поэтому снижение пожарной опасности полимерных материалов является задачей по оптимизации комплекса характеристик создаваемого материала.
Горение органических полимеров
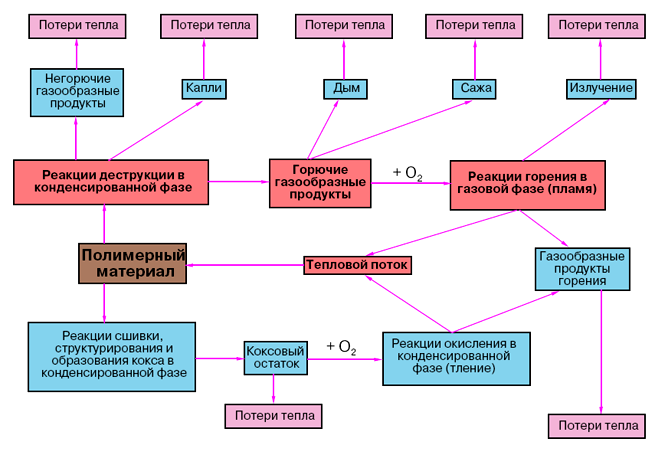
Горение полимеров представляет собой очень сложный физико-химический процесс (схема 1), включающий как химические реакции деструкции, сшивания и карбонизации полимера в конденсированной фазе (а также химические реакции превращения и окисления газовых продуктов), так и физические процессы интенсивных тепло- и массопередачи. Реакции в конденсированной фазе фактически приводят к двум основным типам продуктов: 1) газообразным веществам (горючим и негорючим) и 2) твердым продуктам (углеродсодержащим и минеральным). При протекании реакции в газовой фазе в предпламенной области образуются топливо для пламени, сажа и пр.
Схема 1.Схема горения полимерных материалов
Специфической особенностью химии пламени является наличие сложного пространственного распределения температуры и концентраций исходных и промежуточных веществ и продуктов, а также для большинства полимеров (а тем более полимерных материалов) — наличие огромного числа разнообразных продуктов деструкции как в конденсированной, так и в газовой, предпламенной области. Все это чрезвычайно затрудняет экспериментальные исследования и создание строгих количественных теорий процессов горения полимеров, которые бы учитывали все химические и другие особенности конкретных систем. Тем не менее, для горения большинства полимерных материалов характерны некоторые общие качественные закономерности, на чем мы кратко остановимся.
Процессы горения полимеров делятся на обычное газовое и гетерогенное горение, или тление. В первом случае большая часть тепла, ответственного за поддержание самостоятельного химического превращения, выделяется в газовой фазе при окислении газообразных продуктов деструкции полимера. При этом область максимальной скорости выделения тепла (газовое пламя) обычно отстоит от поверхности на расстояние порядка миллиметров и более в зависимости от конкретных условий горения. Поверхность полимера в таком случае оказывается значительно холоднее области газового пламени. Температуры поверхности составляют 400 — 650 0 С, а максимальные температуры в газовой фазе достигают 1100 — 1200 0 С и более. При тлении же все тепло выделяется, главным образом, в поверхностном слое конденсированной фазы, где и наблюдаются максимальные температуры (800 — 900 0 С).
При горении органических полимерных материалов окислителем является кислород воздуха, а горючим — водород и углеродсодержащие газообразные продукты деструкции полимера, которые в результате окисления превращаются в воду и углекислый газ или — при неполном окислении — в угарный газ (СО). Потоки горючего и окислителя в этом случае пространственно разделены, и химическая реакция их взаимодействия обычно лимитируется подачей реагентов к пламени диффузией или конвекцией. Газовое пламя носит тепловой характер, то есть его существование определяется наличием достаточно большого теплового эффекта при сгорании продуктов деструкции полимера и сильной температурной зависимостью скорости реакции окисления (большого значения эффективной энергии активации). При горении полимеров наблюдаются критические явления, характерные вообще для процессов горения. Снижение температуры пламени по тем или иным причинам приводит к скачкообразному переходу от одного режима окисления — горения — к другому — очень медленному окислению. Эти режимы различаются между собой по скоростям на многие порядки. Поэтому можно говорить о существовании критических условий, определяющих границы возможного горения данного материала. Следует отметить, что эти условия зависят от геометрии образцов и пламени, температуры полимера и газовой среды и не являются абсолютными характеристиками данного материала.
Одним из наиболее характерных примеров практического использования критических явлений при горении полимеров является экспериментальный метод оценки их горючести, впервые предложенный английским ученым Мартином. Образец в форме длинных брусков или цилиндров диаметром около 10 мм помещают в вертикальную трубу, в которую снизу подают кислород и азот в различном соотношении. Образец поджигают сверху специальной газовой горелкой, после чего горелку убирают, и образец либо продолжает самостоятельно гореть, сгорая практически до конца, либо быстро затухает. Такие опыты проводят при различном составе газовой атмосферы, то есть различном соотношении кислорода и азота. Критическая концентрация кислорода в смеси (в об. %), выше которой самостоятельное горение возможно, а ниже нет, называется кислородным индексом (КИ) и характеризует горючесть данного материала. Физическая суть метода заключается в том, что при уменьшении концентрации кислорода растет расход тепла на нагрев инертного газа — азота, уменьшается температура пламени и достигаются критические условия горения. В настоящее время этот метод широко используется экспериментаторами во всем мире.
Анализ процесса горения, приведенный на схеме 1, позволяет понять и возможные пути снижения горючести полимерного материала. Следует отметить, что в большинстве случаев невозможно добиться того, чтобы органический полимер стал абсолютно негорючим материалом и не сгорал в интенсивном огне (пожаре). Однако большинство пожаров возникает от малокалорийных источников тепла и огня — сигарет, спичек, свечей, короткого замыкания. Поэтому очень важно понизить горючесть полимера, чтобы он медленнее загорался, медленнее распространялось пламя, а для загорания требовались бы более жесткие условия (более высокие значения температур, потока энергии и т.д.).
Снижение горючести полимерных материалов
Что же нужно для снижения горючести? Все методы снижения горючести основаны на следующих принципах: 1) изменение теплового баланса пламени за счет увеличения различного рода теплопотерь; 2) снижение потока тепла от пламени на полимер за счет создания защитных слоев, например из образующегося кокса; 3) уменьшение скорости газификации полимера и 4) изменение соотношения горючих и негорючих продуктов разложения материала в пользу негорючих.
Наиболее простой способ изменения теплового баланса, увеличения потерь тепла — приклеивание полимера к поверхности теплопроводящего, например металлического, изделия. Если само изделие достаточно массивно, а толщина полимера не слишком велика, то горючесть конструкции может быть значительно ниже, чем самого полимера. Чем тоньше слой полимера, тем больше потери тепла через полимер в подложку и тем в более жестких условиях может происходить самостоятельное горение. Введение в полимер инертных наполнителей — еще один из способов снижения горючести полимерного материала. Под инертными наполнителями понимают такие, которые не оказывают существенного влияния на состав и количество продуктов пиролиза полимеров в газовой фазе и величину коксового остатка в условиях горения. Их можно разделить на две группы: 1) минеральные наполнители, устойчивые до температуры 1000 0 С — оксиды металлов, фториды кальция и лития, силикаты, технический углерод, неорганическое стекло, порошкообразные металлы и т.п.; 2) вещества, разлагающиеся при температурах ниже 400 — 500 0 С с поглощением тепла и обычно с выделением углекислого газа и/или паров воды, аммиака — гидроксиды, карбонаты, гидрокарбонаты металлов, аммонийфосфаты и т.д. Некоторые примеры таких соединений и реакции их разложения приведены на схеме 2.
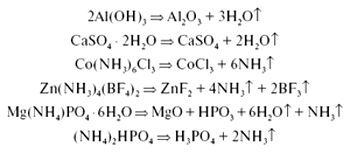
Дополнительное тепло при введении наполнителей первой группы тратится только на нагрев наполнителя от начальной температуры до температуры поверхности полимера. Однако, как оказывается, в балансе тепла вклад такого нагрева невелик и изменение кислородного индекса при введении разумного количества наполнителя мало. На рис. 1 приведены данные по изменению кислородного индекса при введении в полиэтилен и полиоксиметилен (полиформальдегид, полиацеталь) окиси алюминия (кривые 3 и 4 соответственно); штриховой линией (5 ) обозначен кислородный индекс материала, который может применяться в различных областях, например в строительстве, удовлетворяя международным стандартам по горючести (КИ = 27). Как видно, такая величина кислородного индекса достигается при степени наполнения 85 — 90 мас. %. Однако при больших степенях наполнения материал становится слишком хрупким, его физико-механические свойства обычно не удовлетворяют необходимым требованиям. Исключения могут составить некоторые материалы строительного назначения, получаемые прессованием и спеканием. Для переработки экструзией или литьем под давлением такие материалы обычно непригодны из-за высокой вязкости расплава. Поэтому для композиционных материалов, содержащих негорючие инертные наполнители первой группы, в том числе стеклянные волокна (стеклопластики), обычным методом снижения горючести является дополнительная модификация полимерной матрицы различными методами, о которых будет сказано ниже.
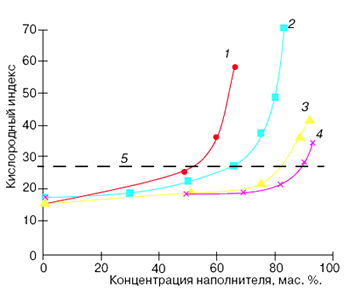
Больший эффект может быть получен введением наполнителя, разлагающегося с поглощением тепла. Классическим примером такого наполнителя является гидроксид алюминия Al(OH) 3 , от которого отщепляется вода. В этом случае тепло расходуется как на нагрев наполнителя, так и на разложение наполнителя и нагрев образующейся воды до температуры пламени, а заметное повышение кислородного индекса наблюдается при содержании Al(OH) 3 около 55 — 65мас. %. В этом случае снижение горючести существенно зависит от соотношения теплопотерь на разложение наполнителя и всех других потерь тепла от пламени, которые всегда тем выше, чем больше общая теплота горения полимера. Поэтому введение 60% Al(OH) 3 в полиэтилен не приводит к существенному повышению кислородного индекса (КИ увеличивается с 17,5 до 25 — 26), в то время как КИ полиформальдегида, обладающего значительно меньшей теплотой сгорания, при этом увеличивается от 15,3 до
Другой способ увеличения потерь тепла и снижения температуры пламени — увеличение инфракрасного излучения. Если в наиболее горячей области пламени не содержится твердых частиц, то вблизи предела горения (Т пл = 1000 — 1100 0 С) потери на излучение ничтожны. Однако при введении некоторых соединений в полимер, например бромсодержащих и фосфорсодержащих соединений, трехокиси сурьмы вместе с галоидуглеводородами, светимость пламени значительно возрастает за счет образования сажи и появления других твердых частиц. Интересно, что при этом возрастает поток излучения от пламени и на полимер. Поэтому, хотя пределы горения смещаются в сторону повышения кислородного индекса, скорости горения выше предела увеличиваются при введении таких соединений. Другими словами, эти соединения, с одной стороны, ингибируют горение (сдвигают пределы горения), а с другой, — могут промотировать его, увеличивая скорость выгорания, или распространения пламени по поверхности полимера. Скорость химической реакции окисления в газовой фазе может быть уменьшена и путем химического ингибирования. Такой способ особенно эффективен при достаточно большой доле цепного процесса в реакциях газового пламени. К сожалению, для большинства процессов горения полимеров, по-видимому, вклад цепного процесса (или длина кинетической цепи) невелик, хотя экспериментальных данных явно недостаточно.
Важным обстоятельством, влияющим на все стадии горения полимеров, является образование кокса при воздействии пламени на полимер. Первое важное следствие образования кокса — это снижение выхода горючих продуктов в газовую фазу, уменьшение потока горючих газов к пламени. Действительно, углерод, остающийся в твердой фазе, мог бы попасть в пламя и окислиться до CO 2 с большим тепловым эффектом. Конечно, в большом пожаре этим все дело и кончится, и никакой пользы от образования кокса мы не получим. Но еще раз заметим, что в данном случае нас интересуют слабые источники зажигания, поэтому эффект от образования кокса так важен. Вспомните, что топить печь углем очень хорошо, но разжигать огонь в печи надо с помощью лучины.
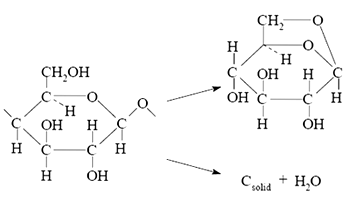
Схема 3. Два основных пути разложения целлюлозы
Таким образом, еще один из способов снижения горючести полимерных материалов — воздействие на направление деструкции полимера в сторону увеличения количества кокса. Наиболее ярким и исследованным примером сказанного могут служить полимеры на основе целлюлозы. Можно выделить два пути деструкции целлюлозы: с образованием воды и углеродного остатка и/или левоглюкозана (схема 3). При деструкции по второму направлению углерод остается в конденсированной фазе, а в газовую выделяется негорючая вода. В первом случае в газовой фазе оказывается углерод, окисляющийся в конце концов до СО 2 . Введение в целлюлозу соединений, способствующих ее дегидратации, то есть смещающих реакцию деструкции во втором направлении, — способ снижения горючести материалов на основе целлюлозы. К такого типа веществам относятся, например, фосфорсодержащие соединения, которые в процессе пиролиза превращаются в фосфорные кислоты. Последние являются активными дегидратирующими агентами.
Второй пример определяющей роли образования кокса получен при изучении горения хлорпарафинов. Если хлорпарафин при нагревании испаряется до разложения и остальные превращения претерпевает в газовой фазе, то действие хлора невелико и сводится лишь к слабому разбавлению горючих газов небольшим количеством хлористого водорода. КИ остается на уровне 17 — 19. Если же разложение хлорпарафина происходит в конденсированной фазе, то КИ становится весьма высоким (40 — 45). При этом существенно меняется состав газов, попадающих в пламя. Для низкомолекулярных хлорпарафинов состав газов по количеству углерода и водорода совпадает с химическим составом исходного вещества. При разложении же высокомолекулярного хлорпарафина в конденсированной фазе образуется значительное количество кокса, который не попадает в газовое пламя. Последнее обедняется углеродом и, соответственно, в нем существенно меняется соотношение между горючими газами (углеводородами) и инертным хлористым водородом. В этом случае тот же эффект теплового разбавления, но уже малого количества горючих газов большим количеством НСl, становится весьма значительным. Количественные оценки подтверждают справедливость такого объяснения изменения горючести этих соединений. Таким образом, на самом деле принципиальным оказывается изменение направления деструкции, благодаря чему изменяется соотношение горючих и негорючих веществ в газовой фазе.
Не нужно думать, что весь эффект при образовании кокса сводится лишь к снижению выхода топлива. Образование коксовой шапки на поверхности полимера между пламенем и пиролизующимся материалом экранирует последний от теплового потока, изменяет тепловой баланс в сторону увеличения теплопотерь, например, теплопотерь излучением от поверхности кокса, которая оказывается нагретой до значительно больших температур, чем поверхность полимера, или конвективных теплопотерь и т.д.
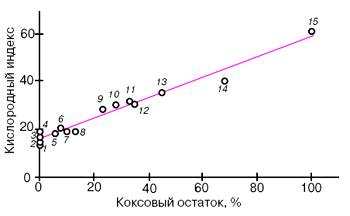
Следовательно, образование кокса в конденсированной фазе — важный процесс, существенно влияющий на механизм горения. Для многих углеводородных полимеров известна тенденция: чем больше кокса остается при их пиролизе, тем они менее горючи. На рис. 2 приведена корреляционная прямая, связывающая эти два параметра. С другой стороны, химическая структура полимера сама по себе во многом определяет направление его деструкции: чем больше в исходном полимере содержится конденсированных ароматических или гетероароматических группировок, тем выше выход кокса. Выход кокса при пиролизе полимера можно оценить, зная его химический состав. В первом приближении вклад различных групп, входящих в состав полимера, аддитивен. Такой подход позволяет до определенной степени прогнозировать горючесть новых полимеров и направленно их синтезировать.
Одним из наиболее эффективных ингибиторов процессов горения и тления различных полимеров является фосфор и его соединения. Действие фосфорсодержащих антипиренов (замедлителей горения) обычно объясняют следующим образом. При пиролизе полимеров, содержащих соединения фосфора, происходит образование фосфорной кислоты и ее ангидридов, которые катализируют дегидратацию и дегидрирование и способствуют процессу карбонизации. В последнее время стали применять не только низкомолекулярные, но и полимерные фосфорсодержащие антипирены. Эти полимерные добавки имеют лучшую совместимость с основным полимером, меньше мигрируют из полимерного материала, отличаются более высокой стойкостью к различным внешним воздействиям и при относительно низком содержании фосфора являются эффективными антипиренами.
Представляет интерес возможность придания огнестойкости полимерным композициям, содержащим обычные эпоксидные, полиэфирные и другие смолы путем армирования их «огнезащищенными» фосфорсодержащими химическими волокнами (то есть волокнами, модифицированными фосфорсодержащими химическими соединениями). В этом случае одновременно улучшаются физико-механические свойства за счет армирования прочными волокнами и снижается горючесть из-за усиления коксообразования на поверхности горящего полимера. В качестве эффективных антипиренов в последние годы широко применяются оксиды и гидроксиды различных металлов, соли органических и неорганических кислот, хелатные комплексы. Существенным преимуществом этих антипиренов является то, что их можно использовать в концентрациях, намного меньших, чем концентрации фосфора и галогенсодержащих соединений.
Идея защиты материала от огня путем образования на его поверхности коксовой «шапки» была доведена до логического конца, когда стали разрабатываться и применяться так называемые вспучивающиеся покрытия. Эти покрытия при воздействии огня образуют пористый пенококс, увеличивая свою толщину в десятки раз. Образующийся кокс имеет низкую теплопроводность и какое-то время защищает основной материал или конструкцию от теплового потока. Вспучивающиеся покрытия представляют собой сложные композиции, состоящие из полимерного связующего и целого ряда добавок для обеспечения вспенивания, необходимой вязкости и быстрой карбонизации при нагреве.
В последние годы интенсивное развитие получило введение антипиреновых добавок в полимерные композиции в виде микрокапсул. Оболочка капсулы изготовлена из полимера, например из желатина, поливинилового спирта, размеры ее составляют десятки или сотни микрон. Антипирены, используемые для этих целей, можно разделить на две группы: высококипящие, температура кипения которых выше температуры вскрытия микрокапсул, и низкокипящие, температура кипения которых значительно ниже температуры вскрытия микрокапсул. К первой группе относятся, например, трихлорэтилфосфат и трисдибромпропилфосфат. Механизм их действия и эффективность в микрокапсулированном виде аналогичны тому случаю, когда они введены в виде обычных добавок к полимеру. Это интенсификация процесса коксообразования, увеличение количества кокса и его пористости, а также снижение проницаемости кокса для горючих жидких и газообразных продуктов деструкции полимера. Основной эффект микрокапсулирования в этом случае состоит в улучшении совместимости антипирена с полимером, затруднении его «выпотевания» — выделения из полимера при длительной эксплуатации и повышении физико-механических свойств материала.
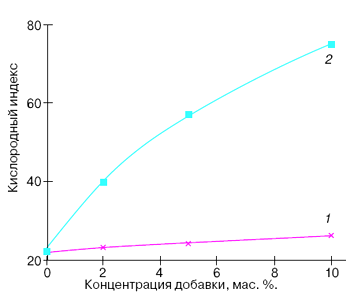
Совершенно новый и весьма эффективный механизм действия обнаружен для соединений второй группы. Это, например, четыреххлористый углерод, тетрафтордибромэтан и другие фреоны — галоидуглеводороды. Эти соединения в микрокапсулированном виде намного эффективнее снижают горючесть полимерной композиции, нежели введенные в чистом виде. Даже такое инертное при обычном способе введения соединение, как четыреххлористый углерод, при микрокапсулировании становится очень эффективным антипиреном (рис. 3). Характерна и экстремальная зависимость КИ композиции от размера микрокапсул. Значение оптимального размера зависит от природы антипирена и изменяется от 40 до 160 мкм.
Оказалось, что жидкость, находящаяся внутри микрокапсул, к моменту их вскрытия подвергается сильному перегреву (на 100 — 200 0 С выше температуры кипения). Устойчивое (метастабильное) перегретое состояние жидкости внутри них обусловлено отсутствием зародышей парообразования. При достижении температуры начала разложения оболочки микрокапсулы на ее поверхности образуются дефекты, которые и становятся зародышами образования газовой фазы. Если к этому моменту жидкость перегрета, происходит резкое увеличение давления и микрокапсула взрывается. Чем сильнее перегрета жидкость, тем сильнее взрыв. Наличие микровзрывов приводит к диспергированию полимерной матрицы: частички полимера отрываются от основной массы и уносятся из зоны пламени. Таким образом, органический полимер, который в обычных условиях под действием пламени пиролизуется, образуя горючие газовые продукты, в результате диспергирования уносится в виде твердых частиц, окруженных газовым облаком антипирена. Эффект диспергирования зависит также от состояния полимерной матрицы в момент вскрытия микрокапсул. Так, наибольший эффект от микрокапсулированных легко летучих фреонов наблюдался для эпоксидных полимеров, которые находятся в сшитом нетекучем состоянии при температуре диспергирования. Для термопластичных полимеров, которые при нагревании расплавляются и становятся сравнительно низковязкими, эффективность этих микрокапсулированных жидкостей значительно ниже — вместо диспергирования матрицы происходит как бы ее кипение. Полимерный материал, содержащий микрокапсулированный эффективный антипирен, такой например, как тетрафтордибромэтан, может быть не только негорючим, но и огнегасящим.
До сих пор пожары приносят огромный материальный ущерб, исчисляемый десятками миллиардов долларов в год, в них гибнут десятки тысяч людей. Роль современных полимерных материалов в этом особенно существенна. Поэтому поиски путей, ограничивающих горючесть полимеров и уменьшающих выделение дыма и токсичных продуктов при горении, продолжаются во всем мире и на это тратятся значительные финансовые и интеллектуальные средства. Отметим один важный момент. Многие способы ингибирования процессов горения основаны на введении в материал добавок (антипиренов), содержащих атомы хлора или брома, или на химической модификации полимеров также путем введения в них хлора или брома. В то же время сейчас уже однозначно установлено, что эти элементы, попадая в атмосферу, способствуют разрушению озонного слоя Земли. Поэтому одной из главных задач современного полимерного материаловедения является разработка безгалоидных способов снижения горючести.
А. А. Берлин
Источник: Соровский образовательный журнал
 Технологии [154] Технологии [154] |  Изделия [78] Изделия [78] |
 Оборудование [43] Оборудование [43] |  Сырье [113] Сырье [113] |
 Обзоры рынков [183] Обзоры рынков [183] |  Интервью [98] Интервью [98] |
 Репортаж [26] Репортаж [26] |  Все статьи Все статьи |
Статьи публикуются с разрешения автора и обязательным указанием ссылки на источник
Редакция оплачивает на договорной основе
технические статьи, маркетинговые отчеты, рецептуры, обзоры рынка
и другую отраслевую информацию и права не ее размещение
Приглашаем специалистов к сотрудничеству в качестве внештатных авторов и консультантов!
По вопросам публикации и оплаты статей обращайтесь в редакцию:
Тел: +7 (499) 490-77-79
Прислать сообщение