Бром – это химически активный неметалл, относящийся к группе галогенов, которые являются энергичными окислителями. Он активно применяется в различных сферах, включая медицину, промышленность, производство оружия. Химические свойства брома многочисленны, и сейчас о них стоит вкратце рассказать.
- Общая характеристика
- Основные химические свойства
- Бромная вода
- Другие реакции брома
- Двойные и тройные связи
- Токсичность
- Работа с бромом
- Применение
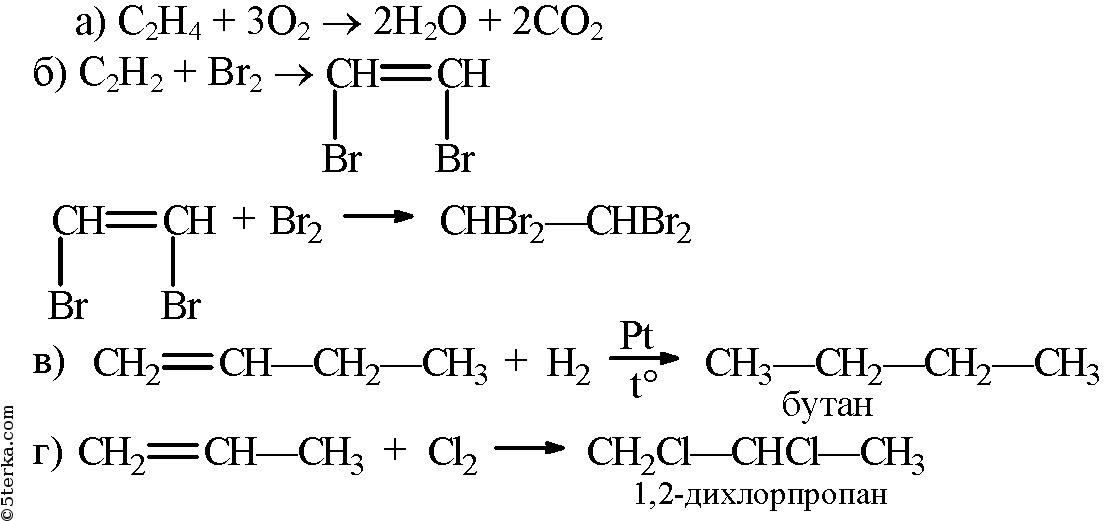
- 2. Напишите уравнения реакций: а) горения этилена в кислороде; б) взаимодействия ацетилена с бромом (две стадии); в) гидрирования бутена-1; г) взаимодействия пропилена с хлором. Назовите продукты реакций в и г.
- 2. Напишите уравнения реакций: а) горения этилена в кислороде; б) взаимодействия ацетилена с бромом (две стадии); в) гидрирования бутена-1; г) взаимодействия пропилена с хлором. Назовите продукты реакций в и г.
- Химические свойства брома
Общая характеристика
Данное вещество при нормальных условиях представляет собой красно-бурую жидкость. Она едкая, тяжелая, имеет неприятный запах, который немного напоминает йодный. Жидкость ядовитая, но про токсичные свойства химического элемента брома будет рассказано чуть позже. Общие характеристики можно выделить в следующий перечень:
- Атомная масса составляет 79,901 … 79,907 г/моль.
- Электроотрицательность равна 2.96 по шкале Полинга.
- Электродный потенциал нулевой.
- Всего шесть степеней окислений – 0, -1, +1, +3, +5 и +7.
- Энергия ионизации составляет 1142,0 (11,84) кДж/моль.
- Плотность равна 3,102 (25 °C) г/см³ при нормальных условиях.
- Температура кипения и плавления составляет 58,6 °C и −7,25 °C соответственно.
- Удельная теплота испарения и плавления равна 29,56 и 10,57 кДж/моль.
- Показатели молярной теплоемкости и объема равны 75,69 Дж/(K•моль) и 23,5 см³/моль соответственно.
Интересно, что название этого элемента с древнегреческого переводится как «зловоние». И кто знает, как пахнут бромовые растворы, понимает, о чем речь. Запах у него действительно не из приятных.
Основные химические свойства
Данное вещество существует в виде 2-атомных молекул Br2. Если увеличить температуру до 800 °C, то станет заметна их диссоциация на атомы. Чем выше будут градусы, тем интенсивнее будет осуществляться данный процесс.
К основным химическим свойствам брома стоит отнести его способность растворяться в воде. Это, конечно, характерно для всех галогенов, но он лучше остальных взаимодействует с Н2О. Растворимость составляет 3,58 грамм на 100 миллилитров воды при температуре в 20 °C.
Получающийся в итоге этой реакции раствор именуют бромной водой. У нее есть целый ряд специфических особенностей.
Бромная вода
На свету она постепенно выделяет кислород. Это возникает из-за того, что бромноватистая кислота, входящая в состав данного раствора, начинает разлагаться. Жидкость, кстати, имеет характерный желто-оранжевый цвет.
Бромную воду используют для проведения реакции, которая в виде формулы выглядит так: Br2 + Н2О → HBr + HBrO. Как можно видеть, в результате образуются такие вещества, как бромоводородная и неустойчивая бромноватистая кислоты.
Раствор является очень мощным окислителем. Бромная вода способна воздействовать на такие металлы, как никель, кобальт, железо, марганец и хром. Еще ее применяют в химическом синтезе определенных препаратов органического происхождения и при анализах. Также бромная вода задействуется при идентификации алкенов. Когда она вступает с ними в реакцию, то обесцвечивается. Кстати, особенность бромной воды в том, что она не замерзает даже при -20 °С.
А готовят ее обычно так: в 250 миллилитров дистиллированной воды добавляют бром в количестве 1 мл, интенсивно при этом перемешивая компоненты. Процесс осуществляется в вытяжном шкафу. Хранят раствор в емкости, выполненной из стекла темного цвета.
Другие реакции брома
Важно оговориться, что этот активный неметалл во всех отношениях смешивается с большинством органических растворителей. Чаще всего вследствие данного процесса их молекулы бромируются.
По своей химической активности данный элемент находится между хлором и иодом. С этими веществами он тоже взаимодействует. Вот, например, реакция с раствором иодида, вследствие которой образуется свободный иод: Br2 + 2Kl → I2 + 2KBr. А при воздействии на бромиды хлора появляется свободный бром: Cl2 + 2KBr → Br2 + 2KCl.
Со многими другими веществами рассматриваемый элемент тоже взаимодействует за счет своих химических свойств. Реакция брома с серой дает S2Br2. При взаимодействии с фосфором появляются PBr3 и PBr5. Это все бинарные неорганические соединения. Кроме перечисленных элементов, неметалл также взаимодействует с селеном и теллуром.
Но вот с чем бром не реагирует непосредственно, так это с азотом и кислородом. Зато с галогенами взаимодействует. А его реакции с металлами дают бромиды — MgBr2, CuBr2, AlBr3 и т.д.
И, конечно, рассказывая про физические и химические свойства брома, нельзя не упомянуть, что существуют также вещества, являющиеся устойчивыми к его действию. Это платина и тантал, а еще в какой-то мере свинец, титан и серебро.
Двойные и тройные связи
С веществами, которым они свойственны, также способен взаимодействовать обсуждаемый элемент. И, рассказывая про химические свойства брома, уравнения реакций данного типа тоже стоит рассмотреть. Вот одно из таковых: С2Н4 + Br2 → C2H4BR2. Это взаимодействие с этиленом. Ему как раз и свойственна двойная связь.
Интересно, что когда бром смешивается с растворами щелочей, карбоната калия или натрия, то результатом становится образование соответствующих броматов и бромидов (солей). Вот уравнение, демонстрирующее это: 3Br2 + 3Na2CO3 → 5NaBr + NaBrO3 + 3СО2.
И да, перечисляя важнейшие химические свойства брома, нельзя не упомянуть, что в жидком состоянии он легко взаимодействует с золотом. Результатом становится образование трибромида (AuBr3). А реакция выглядит следующим образом: 2Au + 3Br2 → 2AuBr3.
Токсичность
Химические свойства брома обусловливают его опасность для человеческого организма. Даже если его концентрация в воздухе превышает отметку в 0,001 % по объему, то возникают головокружение, раздражение слизистых оболочек, кровотечение из носа, а иногда даже удушье и спазмы дыхательных путей.
Смертельная доза для человека составляет всего 14 мг/кг перорально. Если возникло отравление бромом, то нужно:
- Вызвать «Скорую».
- Вывести потерпевшего на свежий воздух.
- Расстегнуть сдавливающую одежду.
- Постараться успокоить его.
- Промыть кожу водой, если вещество попало на покровы. Протереть после этого спиртом.
- Дать пострадавшему молоко с добавлением небольшого количества соды. Она нейтрализует действие брома.
- Промыть желудок, если вещество попало в организм через рот. Давать пить воду, но маленькими порциями, рекомендуется предложить сорбенты для уменьшения степени всасываемости.
Бром действительно опасное вещество. Его даже используют в производстве боевых отравляющих припасов.
Работа с бромом
Поскольку химические свойства брома обусловливают его токсичность, то люди, которые вынуждены с ним контактировать, используют специальные перчатки, противогазы и спецодежду.
Хранят вещество в толстостенной таре из стекла. Ее, в свою очередь, хранят в емкостях с песком. Он помогает защитить тару от разрушения, которое может возникнуть из-за встряхивания.
Кстати, из-за очень высокой плотности вещества бутылки с ним нельзя брать за горло. Оно легко может оторваться. А последствия от разлитого токсичного брома, да еще в таком количестве, катастрофичны.
Применение
Напоследок пару слов о том, как и где используют бром. Можно выделить следующие сферы и области применения:
- Химия. Бром задействован в органическом синтезе, а его раствором определяют качество непредельных соединений.
- Промышленность. С добавлением брома делают антипирены, которые придают пожароустойчивость таким материалам, как текстиль, древесина и пластик. А еще из него раньше активно изготавливали 1.2-дибромэтан, который был главной составляющей этиловой жидкости.
- Фотография. Бромид серебра используется как светочувствительное вещество.
- Ракетное топливо. Пентафторид брома – его мощный окислитель.
- Нефтедобыча. В этой сфере используются бромидные растворы.
- Медицина. Бромиды калия и натрия используют в качестве успокаивающих средств.
Так что каким бы токсичным ни было это вещество для человеческого организма, в некоторых сферах оно незаменимо.
2. Напишите уравнения реакций: а) горения этилена в кислороде; б) взаимодействия ацетилена с бромом (две стадии); в) гидрирования бутена-1; г) взаимодействия пропилена с хлором. Назовите продукты реакций в и г.
2. Напишите уравнения реакций: а) горения этилена в кислороде; б) взаимодействия ацетилена с бромом (две стадии); в) гидрирования бутена-1; г) взаимодействия пропилена с хлором. Назовите продукты реакций в и г.

задача №2
к главе «Тема III. Непредельные углеводороды (алкены, алкадиены и алкины). Работа 6 Итоговая работа по теме III. Вариант 4».
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
Нажмите на значок глаза возле рекламного блока, и блоки станут менее заметны. Работает до перезагрузки страницы.
Химические свойства брома
С другой стороны, у брома по сравнению с хлором и фтором больше размеры атомов и общее число электронов в молекуле, а поэтому сильнее межмолекулярное взаимодействие. Следствием этого является то, что температура кипения брома выше, чем фтора и хлора.
При стандартных условиях бром – жидкость. Молярная концентрация вещества в жидкой фазе больше, чем в газе, и реакции с жидким бромом протекают зачастую более энергично, чем с газообразным хлором. Например, компактные алюминий и железо, не реагирующие с хлором при комнатной температуре, возгораются в жидком броме при непродолжительном нагревании, хотя энтальпии образования бромидов менее экзотермичны, чем соответствующих хлоридов:
Следовательно, различия в течении реакций определяются исключительно кинетическими причинами.
Химическая активность брома ниже, чем хлора, но еще достаточно высока. Со многими металлами и неметаллами он химически взаимодействует при обычных условиях. Так, например, железо, цинк, алюминий горят в жидком броме, реакция между кристаллическим фосфором и бромом идет при обычных условиях. Бром по активности мало уступает хлору.
Взаимодействие брома с водородом происходит лишь при повышенной температуре и, по-видимому, включает цепные процессы.
BaS + 4Br2 + 4H2O = BaSO4 + 8HBr – эту реакцию проводят для получения раствора HBr.
Непосредственно бром не реагирует с кислородом, азотом, углеродом и благородными газами. Бром окисляется более легкими галогенами:
Реакции с кислородом не идут из-за очень низкой устойчивости оксидов всех галогенов.
В отличие от хлора, основные электроны атома брома включают не только s- и p-, но d-электроны. У атома брома имеет место 18-ти электронный предвнешний слой. Следствием этого является то, что вакантные d-АО атома брома меньше экранированы от положительного заряда ядра и менее эффективно участвуют в образовании связей. Соединения с положительными степенями окисления для брома менее характерны, чем для хлора. Это явление, известное как “вторичная периодичность”, которая особенно обнаруживается в кислородных соединениях брома. При этом 10 электронов 3d атомных орбиталей являются кайносимметричными, поэтому сильнее притянуты к атомному ядру.
Это главная причина, почему только сравнительно недавно (1968 г.) были получены производные брома в степени окисления +7, в частности бромная кислота HBrO4, при этом в качестве окислителя использовался XeF2.
Бром также как и хлор диспропорционирует в водном растворе, но склонность к диспропорционированию у него выражена менее ярко:
Br2 + H2O – HBr + HBrO (1), Кг = 4·10 -9 , Кр = 7,2·10 -9 , рК = 8,2
3BrO – ↔ BrO3 – + 2Br – (2)
4BrO – ↔ BrO4 – + 3Br –
Образующаяся в реакции (1) бромноватистая кислота не выделена в индивидуальном состоянии и может существовать лишь в разбавленных растворах.
Диспропорционирование аниона BrO – протекает довольно быстро уже при комнатной температуре, поэтому растворы, содержащие этот анион можно готовить или хранить лишь при температуре около 0 °C. Даже при слабом нагревании таких растворов по реакции (2) быстро образуется анион BrO3 – . Впрочем, для практического получения последнего удобнее окислять горячий щелочной раствор бромида хлором.
Чтобы получить производные BrO4 – нужны чрезвычайно сильные окислители.