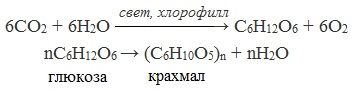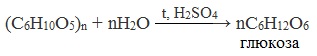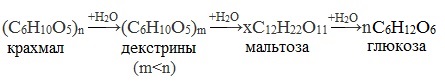Крахмал – ценный питательный продукт. Он входит в состав хлеба, картофеля, круп и наряду с сахарозой является важнейшим источником углеводов в человеческом организме.
Химическая формула крахмала (С6(Н2О)5) n .
Строение крахмала
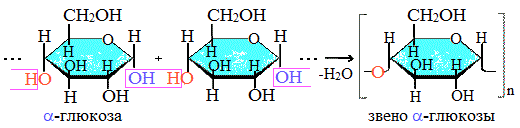
Крахмал состоит из 2 полисахаридов, построенных из остатков циклической a-глюкозы.
Как видно, соединение молекул глюкозы происходит с участием наиболее реакционноспособных гидроксильных групп, а исчезновение последних исключает возможность образования альдегидных групп, и они в молекуле крахмала отсутствуют. Поэтому крахмал не дает реакцию «серебряного зеркала».
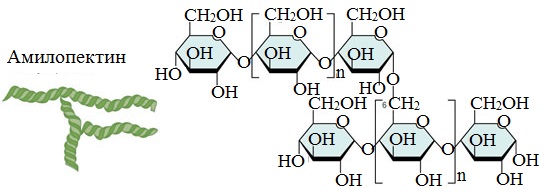
Крахмал состоит не только из линейных молекул, но и из молекул разветвленной структуры. Этим объясняется зернистое строение крахмала.
В состав крахмала входят:
- амилоза (внутренняя часть крахмального зерна) — 10-20%;
- амилопектин (оболочка крахмального зерна) — 80-90%.
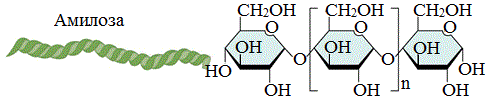
Амилоза
Амилоза растворима в воде и представляет собой линейный полимер, в котором остатки α–глюкозы связаны друг с другом через первый и четвертый атомы углерода (α-1,4-гликозидными связями).
Цепь амилозы включает 200 — 1000 остатков a-глюкозы (средняя мол. масса 160 000) .
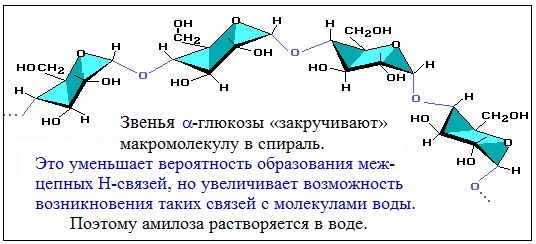
Макромолекула амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев a-глюкозы.
Амилопектин
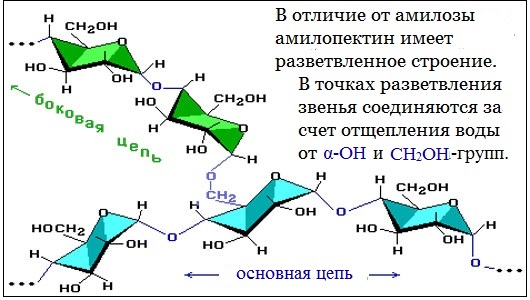
В отличие от амилозы, амилопектин не растворим в воде, и имеет разветвленное строение.
Подавляющее большинство глюкозных остатков в амилопектине связаны, как и в амилозе α-1,4-гликозидными связями. Однако в точках разветвлений цепи имеются α-1,6-гликозидные связи.
Молекулярная масса амилопектина достигает 1-6 млн.
Молекулы амилопектина также довольно компактны, так как имеют сферическую форму.
Биологическая роль крахмала. Гликоген
Крахмал – главное запасное питательное вещество растений, основной источник резервной энергии в растительных клетках.
Остатки глюкозы в молекулах крахмала соединены достаточно прочно и в то же время под действием ферментов легко могут отщепляться, как только возникает потребность в источнике энергии.
Амилоза и амилопектин гидролизуются под действием кислот или ферментов до глюкозы, которая служит непосредственным источником энергии для клеточных реакций, входит в состав крови и тканей, участвует в обменных процессах.
Гликоген (животный крахмал) – полисахарид, молекулы которого построены из большого числа остатков α–глюкозы. Он имеет сходное строение с амилопектином, но отличается от него большей разветвленностью цепей, а также большей молекулярной массой.
Содержится гликоген главным образом в печени и в мышцах.
Гликоген – белый аморфный порошок, хорошо растворяется даже в холодной воде, легко гидролизуется под действием кислот и ферментов, образуя в качестве промежуточных веществ декстрины, мальтозу и при полном гидролизе – глюкозу.
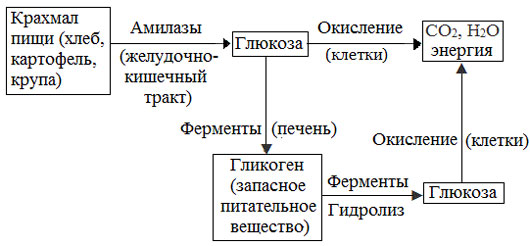
Превращение крахмала в организме человека и животных
Нахождение в природе
Крахмал широко распространен в природе. Он образуется в растениях в процессе фотосинтезе и накапливается в клубнях, корнях, семенах, а также в листьях и стеблях.
Крахмал содержится в растениях в виде крахмальных зерен. Наиболее богато крахмалом зерно злаков: риса (до 80%), пшеницы (до 70%), кукурузы (до 72%), а также клубни картофеля (до 25%). В клубнях картофеля крахмальные зерна плавают в клеточном соке, в злаках они плотно склеены белковым веществом клейковиной.
Физические свойства
Крахмал – белое аморфное вещество, без вкуса и запаха, нерастворимое в холодной воде, в горячей воде набухает и частично растворяется, образуя вязкий коллоидный раствор (крахмальный клейстер).
Крахмал существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
Химические свойства крахмала
Химические свойства крахмала объясняются его строением.
Крахмал не дает реакцию «серебряного зеркала», однако ее дают продукты его гидролиза.
1. Гидролиз крахмала
При нагревании в кислой среде крахмал гидролизуется с разрывом связей между остатками α-глюкозы. При этом образуется ряд промежуточных продуктов, в частности мальтоза. Конечным продуктом гидролиза является глюкоза:
Процесс гидролиза протекает ступенчато, схематически его можно изобразить так:
Видеоопыт «Кислотный гидролиз крахмала»
Реакцию превращения крахмала в глюкозу при каталитическом действии серной кислоты открыл в 1811 г. русский ученый К.Кирхгоф (реакция Кирхгофа).
2. Качественная реакция на крахмал
Так как молекула амилозы представляет собой спираль, то при взаимодействии амилозы с йодом в водном растворе молекулы йода входят во внутренний канал спирали, образуя так называемое соединение включения.
Раствор иода окрашивает крахмал в синий цвет. При нагревании окрашивание исчезает (комплекс разрушается), при охлаждении появляется вновь.
Крахмал + J2 – синее окрашивание
Видеоопыт «Реакция крахмала с йодом»
Данная реакция используется в аналитических целях для обнаружения, как крахмала, так и йода (йодкрахмальная проба)
3. Большинство глюкозных остатков в молекулах крахмала имеют по 3 свободных гидроксила (у 2,3,6-го атомов углерода), в точках разветвления – у 2-го и 3-го атомов углерода.
Следовательно, для крахмала возможны реакции, характерные для многоатомных спиртов, в частности образование простых и сложных эфиров. Однако эфиры крахмала большого практического значения не имеют.
Качественную реакцию на многоатомные спирты крахмал не дает, так как плохо растворяется в воде.
Получение крахмала
Из растений извлекают крахмал, разрушая клетки и отмывая его водой. В промышленном масштабе его получают главным образом из клубней картофеля (в виде картофельной муки), а также кукурузы, в меньшей степени – из риса, пшеницы и других растений.
Получение крахмала из картофеля
Картофель моют, измельчают и промывают водой и перекачивают в большие сосуды, где происходит отстаивание. Вода извлекает из измельченного сырья крахмальные зерна, образуя так называемое «крахмальное молоко».
Полученный крахмал ещё раз промывают водой, отстаивают и сушат в струе теплого воздуха.
Получение крахмала из кукурузы
Зерна кукурузы замачивают в теплой воде разбавленной сернистой кислоты с целью размягчения зерна и удаления из него основной части растворимых веществ.
Набухшее зерно дробят для удаления ростков.
Ростки, после всплывания на поверхность воды, отделяют и используют в дальнейшем для получения кукурузного масла.
Кукурузную массу повторно измельчают, обрабатывают водой для вымывания крахмала, затем отделяют отстаиванием или с помощью центрифуги.
Применение крахмала
Крахмал широко применяется в различных отраслях промышленности (пищевой, фармацевтической, текстильной, бумажной и т.п.).
Он является основным углеводом пищи человека – хлеба, круп, картофеля.
В значительных количествах перерабатывается на декстрины, патоку и глюкозу, используемые в кондитерском производстве.
Из крахмала, содержащегося в картофеле и зерне злаков, получают этиловый, н-бутиловый спирты, ацетон, лимонную кислоту, глицерин.
Крахмал используется как клеящее средство, применяется для отделки тканей, крахмаления белья.
В медицине на основе крахмала готовятся мази, присыпки и т.д.
Гидролиз крахмала
Крахмал (С6Н10О5)n – полисахарид, который состоит из двух фракций: 25% линейной амилозы и 75% разветвленного амилопектина. Он образуется на свету в растениях в процессе фотосинтеза.
Это вещество представляет собой белый порошок, который не растворяется в холодной воде, образуя взвесь. После отстаивания взвеси на дне ёмкости откладывается белый осадок, а воду легко можно слить. После высыхания крахмал восстанавливает все свои свойства.
В горячей же воде это вещество образует коллоидный раствор – это такая клейкая жидкость, которую ещё называют крахмальным клейстером и часто используют в быту в качестве склеивающего вещества. А ещё на этом его свойстве основано приготовление киселей и некоторых десертов.
Крахмал — это химически инертное вещество. Для того чтобы оно вступило в реакцию, необходимо участие в этом процессе катализаторов.
На его физических и химических свойствах основано применение этого вещества. Так, крахмал и его производные часто применяются в пищевой, текстильной и бумажной промышленностях. И для живых организмов он играет немаловажную роль.
Для использования этого органического вещества в промышленных целях его подвергают химическому воздейстивию. Гидролиз крахмала – это процесс обмена между ионами вещества и водой, который может быть ферментативным или кислотным.
Химический гидролиз крахмала — реакция каталитическая, так как происходит при нагревании в присутствии неорганических кислот. В ходе данной химической реакции образуется глюкоза, которую можно выразить уравнением:
(С6Н10О5)n + nH2O +(кат. H2SO4+t°) = nC6H12O6.
Но в последнее время большую популярность приобретает ферментативный гидролиз крахмала. Используя специальные технологии, из него получают этиловый спирт, патоку и глюкозу так же, как и при химическом гидролизе.
Преимущество этого процесса в том, что для него в качестве исходного материала берут крахмалосодержащие растения, например, рожь, картофель, кукурузу, рис и некоторые другие. Эти эти исходники, к тому же, содержат в своём составе амилолитические ферменты, которые и используют в процессе гидролиза.
Например, такими ферментами является изоамилазы и пуллуланазы, глюколиназы. Ферменты – природные катализаторы, которые ускоряют ход химических реакций. Схематически процесс расщепления крахмала под действием ферментов выглядит так: крахмал → растворимый крахмал (амилоза) → олигосахариды (декстрины) → дисахарид (мальтоза = солод) → α-глюкоза. Его можно выразить также уравнением:
(C6H10O5)n + nH2O +(кат.- фермент) = nC6H12O6
Наглядно можно увидеть, что произошел химический гидролиз, проведя эксперимент. Кипятим смесь крахмального клейстера с серной кислотой. Проверяем, произошел ли гидролиз — капаем йод. Если реакция отрицательная, то есть нет синего или фиолетового окрашивания, значит, гидролиз произошел.
Теперь доказываем, что продукт гидролиза – глюкоза. Добавляем к полученному раствору щелочь и сульфат меди (II)(CuSO4). Осадок гидроксида меди не выпадает, раствор приобретает ярко-синюю окраску. Нагреваем и видим образование осадка терракотового (кирпичного) цвета – это значит, что в растворе есть глюкоза, которая образовалась в ходе гидролиза.
В организме человека также происходит ферментативный гидролиз крахмала. Этот процесс очень важен, так как при этом образуются углеводы, в частности, глюкоза. Она окисляется в каждой клетке организма, образуя воду и углекислый газ, при этом выделяя энергию, которая необходима для нормального функционирования организма.
Гидролиз крахмала с помощью ферментов начинается в ротовой полости при пережевывании пищи. Слюна человека содержит фермент – амилазу, под действием которой крахмал расщепляется на более простые составляющие – декстрины. Этот процесс человек может даже ощутить. Ведь если долго жевать хлеб, то во рту появляется сладковатый вкус, который и свидетельствует о том, что начался процесс гидролиза крахмала. Избыток глюкозы, которая образуется в ходе гидролиза, откладывается в печени в виде запасного питательного вещества – гликогена.
Гидролиз крахмала
1) В пробирку налейте 2 мл крахмального клейстера, добавьте 6 мл воды и осторожно прилейте 0,5-1 мл раствора серной кислоты.
2) Кипятите смесь в течение 5 мин, затем нейтрализуйте её раствором гидроксида натрия и добавьте немного свежеприготовленного осадка гидроксида меди (II). Содержимое пробирки вновь нагрейте.
Что происходит с крахмалом при его нагревании в присутствии серной кислоты?
О чём свидетельствует появление осадка жёлтого и красного цвета? Напишите уравнения соответствующих реакций.
1) Крахмал при нагревании в присутствии серной кислоты легко подвергается гидролизу:
(C6H10O5)n + nH2O t, H₂SO₄ ⟶ nC6H12O6
2) В результате гидролиза крахмала обязуется глюкоза, которая вступает в реакцию при нагревании со свежеприготовленным гидроксидом меди (II), в начале появляется жёлтый осадок гидроксида меди (I), который при дальнейшем нагревании превращается в красный оксид меди (I):