- ПОДЕЛИТЬСЯ
- скачать вариант №11
- скачать вариант №12
- Скачать ответы для варианта №11
- Скачать ответы для варианта №12
- Решать тренировочный вариант №11 в формате ЕГЭ 2022 по химии 11 класс:
- Ответы для варианта:
- Решать тренировочный вариант №12 в формате ЕГЭ 2022 по химии 11 класс:
- Ответы для варианта:
- Сложные задания с 1 варианта:
- Сложные задания с 2 варианта:
- Пробный вариант 5. ЕГЭ 2021 по химии
- Тренировочный вариант №11.
- Ответы к первой части варианта №11
- Ответы ко второй части варианта №11
- Задание 29
- Задание 30
- Задание 31
- Задание 32
- Задание 33
- Задание 34
ПОДЕЛИТЬСЯ
2 новых пробных тренировочных варианта №11 и №12 по химии 11 класс в формате ЕГЭ 2022 по новой демоверсии из открытого источника ФИПИ со всем изменениями 2022 года.
скачать вариант №11
скачать вариант №12
Скачать ответы для варианта №11
Скачать ответы для варианта №12
Каждый вариант состоит из двух частей, включающих в себя 34 задания. Часть 1 содержит 28 заданий с кратким ответом, часть 2 содержит 6 заданий с развёрнутым ответом.
Ответом к заданиям 1–25 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки.
Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами.
Решать тренировочный вариант №11 в формате ЕГЭ 2022 по химии 11 класс:
Ответы для варианта:
Решать тренировочный вариант №12 в формате ЕГЭ 2022 по химии 11 класс:
Ответы для варианта:
Сложные задания с 1 варианта:
1)Из указанных в ряду химических элементов выберите два элемента, атомы которых на 3d-подуровне содержат десять электронов. 1) Cu 2) Mn 3) Ni 4) Co 5) Se
Ответ: 15
2)Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде. Расположите выбранные элементы в порядке ослабления кислотных свойств образованных ими водородных соединений. 1) O 2) Mg 3) N 4) Se 5) C
Ответ: 135
3)Из предложенного перечня химических элементов выберите два таких, которые не проявляют постоянную степень окисления в сложных веществах. 1) H 2) F 3) O 4) Ca 5) Cs
Ответ: 13
4)Из предложенного перечня соединений выберите два таких, в которых присутствует водородная связь. 1) C2H6 2) NH4Cl 3) NH3 4) HCl 5) H2O
Ответ: 35
5)Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) соли; Б) гидроксида; В) оксида.
Ответ: 149
6)Гидроксид X подвергли нагреванию, в результате чего он разложился с образованием оксида Y. Из предложенного перечня выберите вещества X и Y, удовлетворяющие условию задания. 1) SiO2 2) NaOH 3) H2SiO3 4) Na2O2 5) Na2O
Ответ: 31
7)Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 4321
8)Установите соответствие между исходными веществами и хромсодержащим продуктом, образующимся при их взаимодействии: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 1453
11)Из предложенного перечня соединений выберите два таких, молекулы которых содержат в своем составе карбоксильную группу. 1) этиловый эфир аминоуксусной кислоты 2) глицилаланин 3) анилин 4) фенол 5) трифторуксусная кислота
Ответ: 25
12)Из предложенного перечня превращений выберите все такие, которые могут быть осуществлены в одну стадию. 1) C6H5Cl → C6H5OH 2) C2H5Cl → C2H5OH 3) CH3COOH → CH3COOC6H5 4) CH3COOH → CH3CH2OH 5) C2H5OH → CH2=CH–CH=CH2
Ответ: 25
13)Из предложенного перечня выберите два вещества, которые взаимодействуют и с глюкозой, и с целлюлозой. 1) водород 2) сульфат меди(II) 3) гидроксид железа(III) 4) азотная кислота 5) кислород
Ответ: 45
17)Из предложенного перечня реакций выберите все такие, которые являются каталитическими. 1) 2SO2 + O2 = 2SO3 2) 4NH3 + 5O2 = 4NO + 6H2O 3) CaCO3 + 2HBr = CaBr2 + H2O + CO2 4) S + O2 = SO2 5) 4NH3 + 3O2 = 2N2 + 6H2O 6) 4KClO3 =KCl + 3KClO4
Ответ: 12
18)Из предложенного перечня внешних воздействий выберите все воздействия, которые приводят к увеличению скорости реакции. Zn(тв.) + 2OH- + 2H2O → [Zn(OH)4 ] 2- + H2(г)↑ 1) измельчение цинка 2) уменьшение температуры 3) добавление твердой щелочи 4) увеличение концентрации ионов [Zn(OH)4 ] 2- 5) испарение части воды из раствора Запишите в поле ответа номера выбранных воздействий.
Ответ:135
20)Установите соответствие между веществом и процессом, происходящим на аноде при электролизе его водного раствора с инертными электродами: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 233
21)Для веществ, приведённых в перечне, определите характер среды их водных растворов. 1) сульфат калия (0,1 моль/л) 2) уксусная кислота (0,001 моль/л) 3) гидроксид бария (0,1 моль/л) 4) гидроксид калия (0,11 моль/л)
Ответ: 3412
22)Установите соответствие между способом воздействия на равновесную систему и направлением смещения химического равновесия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой. FeO(тв.) + CO(г) ⇄ Fe(тв.) + CO2(г) – Q
Ответ: 2333
23)В замкнутый реактор поместили смесь оксидов азота(II) и (IV) с кислородом, затем нагрели. В результате протекания обратимой реакции 2NO(г) + O2(г) ⇆ 2NO2(г) в системе установилось равновесие. Используя данные, приведенные в таблице, определите исходную концентрацию кислорода (X) и равновесную концентрацию оксида азота(IV) (Y).
Ответ: 42
24)Установите соответствие между реагирующими веществами и свойством образующегося газообразного продукта: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 5471
25)Установите соответствие между углеводородом и способом его промышленного получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 321
26)Рассчитайте массу 12%-ного раствора серной кислоты (в граммах), полученного при разбавлении 30%-ного раствора массой 155 г. (Запишите число с точностью до десятых.)
Ответ: 387,5
27)Разложение гидроксида меди(II) происходит в соответствии с термохимическим уравнением Cu(OH)2(тв.) → CuO(тв.) + H2O(г) – 46 кДж Рассчитайте количество энергии (в кДж), которое нужно затратить на разложение 9,8 г исходного вещества. (Ответ округлите до десятых.)
Ответ: 4,6
28)Рассчитайте массовую долю инертных примесей в образце графита массой 15 г, если при его полном сгорании было получено 26,88 л (н.у.) углекислого газа. (Запишите число с точностью до целых.)
Ответ: 4
29)Из предложенного перечня веществ выберите вещества, между которыми окислительно-восстановительная реакция сопровождается выделением газа с запахом тухлых яиц. В ответе запишите уравнение только одной из возможных окислительновосстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня веществ выберите два сильных электролита, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
31)Нитрат серебра прокалили. Образовавшееся твердое вещество обработали концентрированной серной кислотой. Выделившийся газ поглотили большим избытком концентрированного водного раствора гидроксида калия. К полученному сильнощелочному раствору добавили раствор перманганата калия. Напишите уравнения четырех описанных реакций.
33)Электролиз 312 г 10%-ного раствора хлорида бария проводили до тех пор, пока суммарный объем газообразных продуктов не составил 4,48 л (н.у.). Из полученного раствора была отобрана порция массой 30,47 г. Рассчитайте массу 5%-ного раствора карбоната натрия, необходимого для полного осаждения катионов бария в отобранной порции раствора. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин.)
34)Некоторое органическое соединение содержит по массе 10,69% азота, 24,43% кислорода и 54,96% углерода. Известно, что данное соединение используется в производстве волокон. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекул; 3) напишите уравнение реакции искомого вещества с раствором соляной кислоты (используйте структурные формулы органических веществ).
Сложные задания с 2 варианта:
1)Определите, атомы каких элементов в основном состоянии содержат одинаковое количество неспаренных электронов. 1) S 2) Br 3) P 4) B 5) Zn
Ответ: 24
2)Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде. Расположите выбранные элементы в порядке убывания числа электронов на внешнем энергетическом уровне. 1) Se 2) Kr 3) K 4) Na 5) Cd
Ответ: 213
3)Из числа указанных в ряду элементов выберите два элемента, степень окисления которых в оксидах может принимать значение +4. 1) P 2) N 3) Fe 4) Mn 5) Ca
Ответ: 24
4)Из предложенного перечня видов химической связи выберите две, характерные для хлорида аммония. 1) водородная 2) ионная 3) ковалентная полярная 4) ковалентная неполярная 5) металлическая
Ответ: 23
5)Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) средней соли; Б) основного гидроксида; В) амфотерного гидроксида.
Ответ: 713
6)Вещество X является продуктом взаимодействия щелочи с раствором сильного электролита, а вещество Y – продукт взаимодействия другой щелочи с раствором слабого электролита. Из предложенного перечня выберите образовавшиеся вещества X и Y. 1) NaBr 2) MgBr2 3) K2S 4) CuS 5) NH4Br
Ответ: 13
7)Установите соответствие между названием вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 2534
8)Установите соответствие между исходным(и) веществом(-ами), вступающим(- и) в реакцию, и продуктами, которые образуются в ходе этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 6424
10)Установите соответствие между формулой вещества и классом/группой органических соединений, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 324
11)Из предложенного перечня соединений выберите два таких, которые являются изомерами бутилформиата. 1) этилацетат 2) пропилэтаноат 3) изобутилацетат 4) 2-метилбутановая кислота 5) 2,3-диметилбутановая кислота
Ответ: 24
12)Из предложенного перечня выберите все вещества, при взаимодействии каждого из которых с натрием протекает реакция замещения. 1) толуол 2) ацетилен 3) 3-метилбутин-1 4) 2-метилпропан 5) фенол
Ответ: 235
13)Из предложенного перечня выберите два вещества, с которыми взаимодействует аминоуксусная кислота. 1) аланин 2) водород 3) метиловый спирт 4) толуол 5) диэтиловый эфир
Ответ: 13
17)Из предложенного перечня типов реакций выберите все типы реакций, к которым можно отнести взаимодействие раствора карбоната натрия с серной кислотой. 1) окислительно-восстановительная 2) гомогенная 3) каталитическая 4) ионного обмена 5) необратимая
Ответ: 245
18)Из предложенного перечня химических реакций выберите все такие, скорость которых увеличится при повышении давления. 1) Na2CO3 + 2HCl(р-р) = CO2 + H2O + 2NaCl 2) 2SO2 + Ca(OH)2 = Ca(HSO3 ) 2 3) Fe + S = FeS 4) NH3(р-р) + HCl(р-р) = NH4Cl(р-р) 5) NH3(г) + HCl(г) = NH4Cl(тв)
Ответ: 25
19)Установите соответствие между схемой реакции и свойством фосфора в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 212
21)Для веществ, приведённых в перечне, определите характер среды их водных растворов. 1) метанол (0,1 моль/л) 2) диметиламин (0,2 моль/л) 3) хлорид метиламмония (0,01 моль/л) 4) муравьиная кислота (0,05 моль/л)
Ответ: 4312
22)Установите соответствие между уравнением обратимой химической реакции и направлением смещения химического равновесия при понижении давления: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 2213
23)В замкнутый реактор, содержащий катализатор, поместили пары метанола, смесь угарного газа и водорода, затем нагрели. В результате протекания обратимой реакции CO(г) + 2H2(г) ⇆ CH3OH(г) в системе установилось равновесие. Используя данные, приведенные в таблице, определите исходные концентрации угарного газа (X) и метанола (Y).
Ответ: 41
24)Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Ответ: 4343
26)Рассчитайте массовую долю серной кислоты в растворе (в %), полученном смешением 200 мл 10%-ного раствора серной кислоты (плотность раствора 1,07 г/мл) и 100 мл 35%-ного раствора серной кислоты (плотность раствора 1,26 г/мл). (Запишите число с точностью до десятых.)
Ответ: 19,3
27)Разложение карбоната кальция происходит в соответствии с термохимическим уравнением CaCO3(тв) → CaO(тв) + CO2(г) – 178 кДж Рассчитайте количество энергии (в кДж), которое нужно затратить для получения 28 г оксида кальция по данной реакции. (Ответ округлите до целых.)
Ответ: 89
28)Рассчитайте объем газовой смеси (в литрах), который можно получить при разложении 15 л аммиака (н.у.). Выход реакции разложения равен 95%. (Запишите число с точностью до десятых.)
Ответ: 29,3
29)Из предложенного перечня веществ выберите вещества, между которыми окислительно-восстановительная реакция протекает с изменением цвета раствора с фиолетового на зеленый. Выделение осадка или газа в этой реакции не наблюдается. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
30)Из предложенного перечня веществ выберите кислую соль и вещество, которое вступает с этой кислой солью в реакцию ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
31)Раствор сульфата алюминия был по каплям добавлен к избытку водного раствора тетрагидроксоалюмината натрия, при этом наблюдалось выделение осадка белого цвета. Полученный осадок отделили, высушили и прокалили. Образовавшийся в результате этого твердый остаток растворили в достаточном количестве концентрированной азотной кислоты. Образовавшийся раствор выпарили досуха, полученное вещество прокалили. Напишите уравнения четырех описанных реакций.
32)Раствор сульфата меди(II) массой 243,4 г подвергли электролизу с платиновыми электродами до выделения на электродах двух продуктов с общей массой 6,4 г, при этом соль в растворе израсходовалась не полностью. Порцию полученного раствора массой 59,25 г обработали избытком раствора хлорида бария, в результате чего выпало 11,65 г осадка. Определите массовую долю соли в исходном растворе. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин.)
34)Некоторое органическое вещество содержит 9,43% водорода, а также углерод и кислород, массовые доли которых равны. Это вещество реагирует с натрием и со свежеосажденным гидроксидом меди(II), молекула его содержит третичный атом углерода. На основании данных условия задания: 1) проведите необходимые вычисления (указывайте единицы измерения физических величин) и установите молекулярную формулу исходного органического вещества; 2) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле; 3) напишите уравнение реакции этого вещества с избытком натрия (используйте структурные формулы органических веществ).
Пробный вариант 5. ЕГЭ 2021 по химии
Часть 1
Ответом к заданиям 1–26 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Цифры в ответах на задания 5, 8, 9, 11, 16, 17, 21–26 могут повторяться.
Для выполнения заданий 1–3 используйте следующий ряд химических элементов. Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду
1) F 2) Cr 3) Mn 4) O 5) P
- Определите , атомы каких из указанных в ряду элементов в основном состоянии содержат валентные электроны на разных энергетических уровнях.
Запишите в поле ответа номера выбранных элементов.
- Из указанных в ряду химических элементов выберите три элемента-неметалла. Расположите выбранные элементы в порядке увеличения численного значения отношения количества нейтронов к количеству протонов в их атомах. Запишите в поле ответа номера выбранных элементов.
- Из числа указанных в ряду элементов выберите два элемента, которые не могут проявлять валентность и степень окисления равную номеру группы, в которой они расположены.
Запишите в поле ответа номера выбранных элементов.
- Из предложенного перечня выберите два вещества немолекулярного строения, которые очень тугоплавки, обладают высокой прочностью и твёрдостью.
2) формиат кальция
5) фосфорная кислота
Запишите в поле ответа номера выбранных веществ.
- Усоответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) ляпис | 1) оксид |
| Б) цианид калия | 2) основание |
| В) угарный газ | 3) соль средняя |
| 4) соль основная |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня соединений выберите два соединения, которые в водном растворе вступают в реакцию с хлором.
Запишите в поле ответа номера выбранных веществ.
- Имеется две пробирки с раствором гидроксида бария. К одной из пробирок добавили раствор соли Х, а через другую пропустили газ Y. В результате в первой пробирке наблюдалось выпадение цветного осадка, а во второй – белого. Из предложенного перечня выберите вещества Х и Y, которые могут вступить в описанные реакции.
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) K2SO3 | 1) O2, H2SO4, K3PO4 |
| Б) CO2 | 2) CuCl2 (p-p), CuO, KMnO4 (p-p) |
| В) NH3 | 3) CaO, K2CO3, HCl |
| Г) ZnO | 4) BaCl2, SO2 (p-p), Pb(NO3)2 |
| 5) C, KOH, Na2[Zn(OH)4] (p-p) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами в этой реакции: к каждой позиции, обозначенной буквой, подберите позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ РЕАКЦИИ |
| А) Zn и NaOH (p-p) | 1) цинкат натрия и водород |
| Б) Zn и NaOH (расплав) | 2) тетрагидроксоцинкат натрия и водород |
| В) Zn и H2O (нагревание) | 3) оксид цинка и водород |
| Г) Zn и H2SO4 (разб.) | 4) гидроксид цинка и вода |
| 5) сульфат цинка и водород | |
| 6) сульфат цинка, сероводород и вода |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана следующая схема превращений:

Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) амилопектин | 1) углеводороды |
| Б) целлюлоза | 2) моносахариды |
| В) мальтоза | 3) дисахариды |
| 4) полисахариды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня соединений выберите два соединения, которые изомерны гексанолу-2.
1) этиловый эфир бутановой кислоты
2) диизопропиловый эфир
4) бутилэтиловый эфир
- Из предложенного перечня выберите два вещества, которые не реагируют с водородом.
- Из предложенного перечня выберите два вещества, которые реагируют с этиленгликолем.
- Из предложенного перечня выберите два вещества, которые реагируют с метанолом, но не реагируют с метиламином.
- Установите соответствие между названием углеводорода и названием алкана, при дегидроциклизации которого образуется этот углеводород: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ УГЛЕВОДОРОДА | НАЗВАНИЕ АЛКАНА |
| А) циклопентан | 1) 2-метилгептан |
| Б) толуол | 2) 2-метилпентан |
| В) 1,3-диметилциклопентан | 3) пентан |
| Г) бензол | 4) 2-метилгексан |
| 5) 2,4-диметилпентан | |
| 6) гексан |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ при нагревании: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | УГЛЕРОДСОДЕРЖАЩИЙ ПРОДУКТ РЕАКЦИИ |
| А) этанол и оксид меди (II) | 1) этаналь |
| Б) этанол и оксид марганца (IV) | 2) ацетат меди (II) |
| В) этанол и уксусная кислота | 3) этилацетат |
| Г) уксусная кислота и оксид меди (II) | 4) ацетат марганца (II) |
| 5) углекислый газ | |
| 6) уксусная кислота |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами Х и Y.
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Из предложенного перечня выберите гетерогенные реакции.
1) этерификация метанола муравьиной кислотой
2) гидрирование жиров
3) сплавление серы с железом
4) хлорирование метана
5) нейтрализация гидроксида меди (II) азотной кислотой
Запишите номера выбранных ответов.
- Из предложенного перечня выберите внешние воздействия, которые уменьшают скорость реакции растворения мрамора в разбавленной соляной кислоте.
1) понижение общего давления
2) разбавление реакционной смеси
3) добавление раствора гидроксида натрия
4) повышение температуры
5) добавление небольшого количества твёрдого хлорида кальция
Запишите номера выбранных ответов.
- Установите соответствие между уравнением реакции и свойством атома галогена с более низкой электроотрицательностью: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | СВОЙСТВО АТОМА ГАЛОГЕНА С БОЛЕЕ НИЗКОЙ ЭЛЕКТРООТРИЦАТЕЛЬНОСТЬЮ |
| А) I2 + 5Cl2 + 6H2O = 10HCl + 2HIO3 | 1) является окислителем |
| Б) I2 + 2KBrO3 = 2KIO3 + Br2 | 2) является восстановителем |
| В) I2 + 2HClO4 = 2HIO4 + Cl2 | 3) является и окислителем, и восстановителем |
| 4) не изменяет степень окисления |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием вещества и способом его получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЗВАНИЕ ВЕЩЕСТВА | СПОСОБ ПОЛУЧЕНИЯ |
| 1) натрий | 1) только электролиз водного раствора соли |
| 2) магний | 2) только электролиз расплава соли |
| 3) серебро | 3) только электролиз расплава оксида с криолитом |
| 4) алюминий | 4) и электролиз водного раствора соли, и электролиз расплава соли |
| 5) только электролиз водного раствора основания | |
| 6) и электролиз расплава оксида с криолитом, и электролиз расплава соли |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между названием соли и характером среды её водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| НАЩВАНИЕ СОЛИ | ХАРАКТЕР СРЕДЫ |
| А) тетрагидроксоцинкат калия | 1) кислотная |
| Б) хлорид хрома (II) | 2) щелочная |
| В) сульфид цезия | 3) нейтральная |
| Г) нитрат аммония |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при уменьшении давления в системе: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| УРАВНЕНИЕ РЕАКЦИИ | НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ |
| А) Br2 (ж) + H2 (г) ↔ 2HBr (г) | 1) смещается в сторону прямой реакции |
| Б) H2 (г) + Se (к)↔ H2Se (г) | 2) смещается в сторону обратной реакции |
| В) SO2 (г) + Cl2 (г) ↔ SO2Cl2 (ж) | 3) практически не смещается |
| Г) NH3 (г) + HCl (г)↔ NH4Cl (тв) |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между реагентами и реактивом, с помощью которого можно их различить (все электролиты находятся в виде разбавленных водных растворов): к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГЕНТЫ | РЕАКТИВ |
| А) MgBr2 и (CH3COO)2Mg | 1) KCl |
| Б) K2SO3 и MgSO4 | 2) AgNO3 |
| В) Al и Mg | 3) ZnO |
| Г) HBr и CH3COOH | 4) KOH |
| 5) KNO3 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
- Установите соответствие между веществом и областью его применения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ВЕЩЕСТВО | ОБЛАСТЬ ПРИМЕНЕНИЯ |
| А) уголь | 1) дезинфекция воды и отбеливание тканей |
| Б) карборунд | 2) сварка и резка металлов |
| В) гипохлорит натрия | 3) топливо |
| 4) консервант | |
| 5) абразивный материал |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответом к заданиям 27–29 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами. Единицы измерения физических величин в бланке ответа указывать не нужно.
При проведении расчётов для всех элементов кроме хлора используйте значения относительных атомных масс, выраженных целыми числами (Ar(Cl) =35,5).
- К 220 г раствора NaOH с массовой долей щёлочи 10% добавили 23 г натрия. Найдите массовую долю (%) щёлочи в полученном растворе. (Запишите число с точность до сотых.)
- Разложение нитрата меди (II) происходит в соответствии с термохимическим уравнением
Рассчитайте количество энергии (в кДж), затраченное для получения 11,2 л газовой смеси кислорода и оксида азота (IV) (н.у.) по данной реакции. (Запишите число с точностью до десятых.)
- Какую массу (в граммах) оксида хрома (VI) можно растворить в 5,6 г гидроксида калия?(Запишите число с точностью до целых.)
Часть 2
Для записи ответов на задания 30–35 используйте БЛАНК ОТВЕТОВ № 2. Запишите сначала номер задания (30, 31 и т.д.), а затем его подробное решение. Ответы записывайте чётко и разборчиво.
Для выполнения заданий 30, 31 используйте следующий перечень веществ соляная кислота, гидроксид калия, азотная кислота, платина, оксид цинка, фосфорная кислота: Допустимо использование водных растворов веществ.
- Из предложенного перечня выберите вещества, в результате окислительно-восстановительной реакции между которыми выделяется бесцветный газ. Причём одна структурная единица восстановителя отдаёт 4 электрона, а окислителя – принимает 3 электрона. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
- Из предложенного перечня выберите два вещества, которые вступают в реакцию ионного обмена, которое описывается кратким ионным уравнением с суммой коэффициентов равной 8. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
- Смешали растворы сульфата меди (II) и карбоната натрия. Выпавший осадок выделили, высушили и прокалили. Затем полученный твёрдый остаток смешали с нашатырём и снова прокалили. В результате чего образовалось два простых и два сложных вещества. Образовавшееся твёрдое простое вещество растворили в растворе хлорида железа (III). Напишите уравнения четырёх описанных реакций.
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
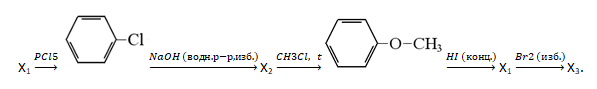
- В два последовательно соединённых электролизёра поместили по 100 г растворов: в первый 10% (по массе) раствор хлорида натрия, во второй – 20% (по массе) хлорида золота (III) и включили ток. Через некоторое время электролиз прекратили и масса раствора в первом электролизёре уменьшилась на 3,285 г. Определите массовую долю хлорида золота (III) во втором электролизёре после электролиза. В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
- Вещество А содержит 65,06% углерода, 6,02% водорода, 28,92% кислорода по массе. Известно, что вещество А окисляется до бензойной кислоты. Также известно, что вещество А при взаимодействии с бромоводородом даёт бромопроизводное Б. При воздействии на это бромопроизводное Б спиртового раствора щёлочи происходит дегидрогалогенирование и образуется соль ненасыщенной кислоты.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции окисления вещества А перманганатом калия в присутствии серной кислоты (используйте структурные формулы органических веществ).
Тренировочный вариант №11.
Ответом к заданиям 1–25 является последовательность цифр. Ответ запишите в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведёнными в бланке образцами.
Цифры в ответах на задания 7, 8, 10, 14, 15, 19, 20, 22–25 могут повторяться.
Из указанных в ряду химических элементов выберите два элемента, атомы которых на 3d-подуровне содержат десять электронов.
Запишите в поле ответа номера выбранных элементов.
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде.
Расположите выбранные элементы в порядке ослабления кислотных свойств образованных ими водородных соединений.
Запишите в поле ответа номера выбранных элементов в нужной последовательности.
Из предложенного перечня химических элементов выберите два таких, которые не проявляют постоянную степень окисления в сложных веществах.
Запишите в поле ответа номера выбранных элементов.
Из предложенного перечня соединений выберите два таких, в которых присутствует водородная связь.
Запишите в поле ответа номера выбранных соединений.
Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) соли; Б) гидроксида; В) оксида.
| 1) CsCrO2 | 2) FeOOH | 3) BaO2 |
| 4) H2SO3 | 5)SiCl4 | 6) CS2 |
| 7) PH3 | 8) CaO2 | 9) MnO2 |
Запишите в таблицу номера ячеек, в которых расположены вещества, под соответствующими буквами.
Гидроксид X подвергли нагреванию, в результате чего он разложился с образованием оксида Y. Из предложенного перечня выберите вещества X и Y, удовлетворяющие условию задания.
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ | ||||||||||||||||||||||||||||
| ИСХОДНЫЕ ВЕЩЕСТВА | ХРОМСОДЕРЖАЩИЙ ПРОДУКТ | ||||||||||||||||||||||||||
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА | ||||||||||||||||||||||||
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | ПРОДУКТ ВЗАИМОДЕЙСТВИЯ | ||||||||||||||||||||||
| СХЕМА РЕАКЦИИ | ПРОДУКТ РЕАКЦИИ | ||||||||||||||||||||
| УРАВНЕНИЕ РЕАКЦИИ | СВОЙСТВО ЖЕЛЕЗА | ||||||||||||||||||
| ВЕЩЕСТВО | АНОДНЫЙ ПРОЦЕСС | ||||||||||||||||
| ВОЗДЕЙСТВИЕ | СМЕЩЕНИЕ РАВНОВЕСИЯ | ||||||||||||||
| ВЕЩЕСТВО | NO | O2 | NO2 |
| ИСХОДНАЯ КОНЦЕНТРАЦИЯ, МОЛЬ/Л | 0,01 | 0,015 | |
| РАВНОВЕСНАЯ КОНЦЕНТРАЦИЯ, МОЛЬ/Л | 0,005 | 0,0375 |
Выберите из списка номера правильных ответов:
1) 0,025 моль/л
2) 0,020 моль/л
3) 0,035 моль/л
4) 0,040 моль/л
5) 0,050 моль/л
6) 0,055 моль/л
Запишите в таблицу выбранные цифры под соответствующими буквами.
Установите соответствие между реагирующими веществами и свойством образующегося газообразного продукта: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| РЕАГИРУЮЩИЕ ВЕЩЕСТВА | СВОЙСТВО ГАЗООБРАЗНОГО ПРОДУКТА РЕАКЦИИ | ||
| УГЛЕВОДОРОД | СПОСОБ ПОЛУЧЕНИЯ |
| № задания, ответ | №задания, ответ |