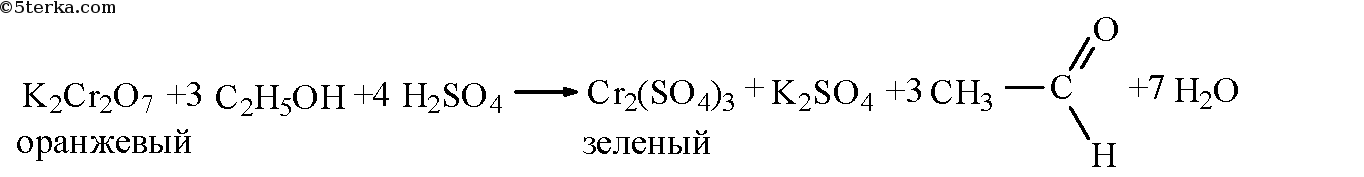Опыт 1. Растворимость спиртов в воде.
Условия выполнения работы:
В две пробирки налили примерно по 2 мл этилового и изоамилового спиртов. Добавили в каждую из пробирок по 3 мл воды и взболтали. Наблюдаем, что этиловый спирт растворился, а изоамиловый нет, и при стоянии образует верхний маслянистый слой, так как его плотность меньше плотности воды (0,8 г/мл). Причиной различного поведения спиртов в воде является природа веществ.
Опыт 2. Получение глицерата меди.
Условия выполнения работы:
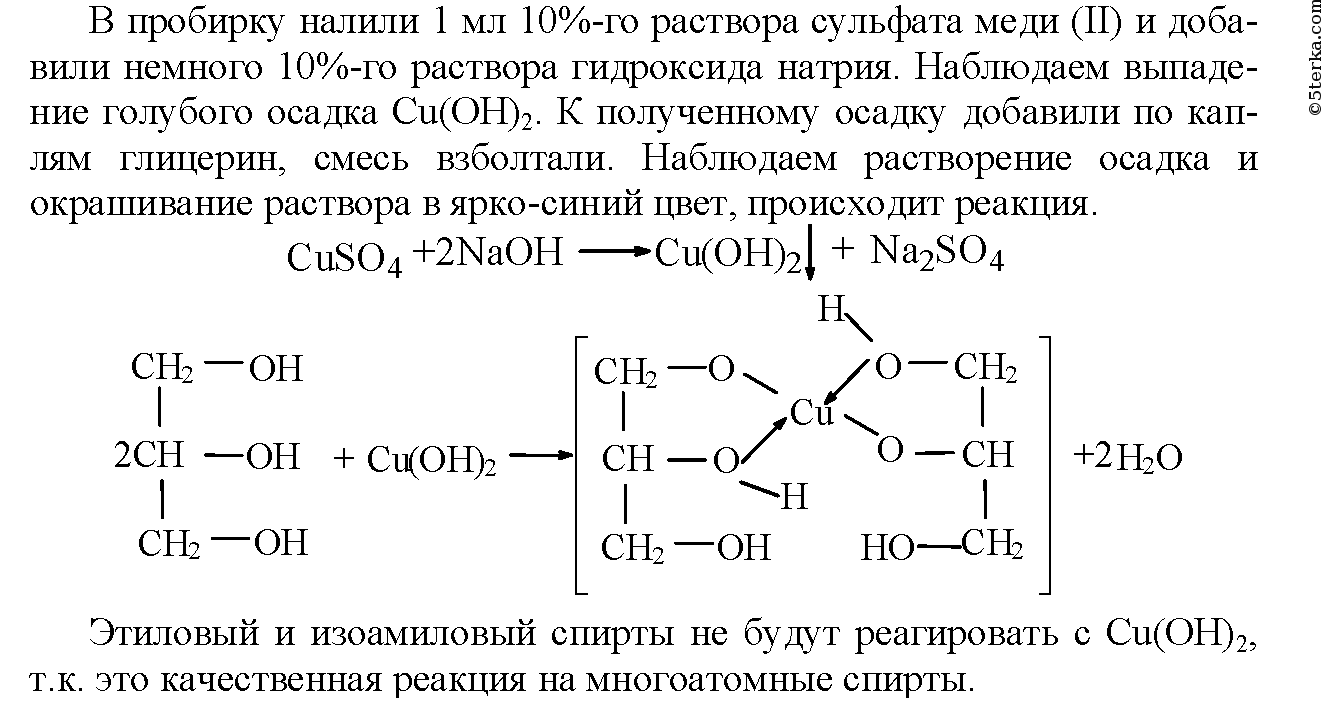
В пробирку налили 1 мл 10%-го раствора сульфата меди (II) и добавили немного 10%-го раствора гидроксида натрия. Наблюдаем выпадение голубого осадка Cu(OH)2. К полученному осадку добавили по каплям глицерин, смесь взболтали. Наблюдаем растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнения реакции взаимодействия сульфата меди (ΙΙ) с гидроксидом натрия:
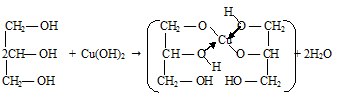
Качественной реакцией на многоатомные спирты является реакция с гидроксидом меди (ΙΙ). Например, при действии глицерина на осадок гидроксида меди (ΙΙ) н аблюдается растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнение реакции имеет вид:
Этиловый и изоамиловый спирты не будут реагировать с Cu(OH)2, так как это качественная реакция на многоатомные спирты.
Опыт 3. Окисление этилового спирта хромовой смесью.
Условия выполнения работы:
Налили в пробирку 2 мл 5%-го раствора дихромата калия, 1 мл 20%-го раствора серной кислоты и 0,5 мл этилового спирта, получили смесь оранжевого цвета. Пробирку нагрели. Наблюдаем изменение цвета раствора на зелёный и чувствуем характерный запах уксусного альдегида.
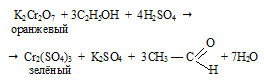
В данной реакции применяют серную кислоту, а не соляную, потому что соляная кислота может окислиться.
Практическая работа № 3. Спирты
Опыт 1. Растворимость спиртов в воде
В две пробирки налили по 2 мл этилового и изоамилового спиртов. Добавили в каждую из пробирок по 3 мл воды и взболтали. Наблюдаем, что этиловый спирт растворился, а изоамиловый нет и при стоянии образует верхний маслянистый слой, т. к. его плотность меньше плотности воды (0,8 г/мл). Причиной различного поведения спиртов в воде является природа веществ.
Также над водой будут отслаиваться бензол, бутиловый спирт, олеиновая кислота.
Опыт 2. Получение глицерата меди
Опыт 3. Окисление этилового спирта хромовой смесью
Налили в пробирку 2 мл 5%-го раствора дихромата калия, 1 мл 20%-го раствора серной кислоты и 0,5 мл этилового спирта, получили смесь
оранжевого цвета. Пробирку нагрели. Наблюдаем изменение цвета раствора на зеленый и чувствуем характерный запах уксусного альдегида.
Серную кислоту лучше не менять на соляную, т.к. последняя может окисляться.

задача №3
к главе «Химический практикум».
Спирты. Инструкция к выполнению лабораторной работы с дополнительным материалом для её оформления
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Тема: Химические свойства c пиртов.
Цель: изучить некоторые физические и химические свойства предельных одноатомных и многоатомных спиртов.
Реактивы и материалы: спирты:этиловый; глицерин; металлический натрий; сульфата меди (II); оксид меди (II); медная проволока; лучина; пробирки; фарфоровая чашка; прибор для окисления спирта.
Оборудование: набор пробирок, пробка с газоотводной трубкой, стаканчик, пипетка, спиртовка.
Опыт 1. Изучение физических свойств одно- и многоатомных спиртов.
Растворимость спиртов в воде.
В пробирку налейте нескольку миллилитров этилового спирта и прибавьте к нему подкрашенную воду.
Запишите свои наблюдения и сделайте вывод о растворимости одноатомных спиртов.
Изучение физических свойств глицерина.
В пробирку налейте 0,5 мл воды, добавьте 0,5 мл глицерина, перемешайте. Раствор глицерина не выливать!
Запишите свои наблюдения и сделайте вывод о растворимости глицерина в воде.
Опыт 2. Взаимодействие этилового спирта с металлическим натрием.
Приготовьте пробирку с этанолом и опустите в неё кусочек металлического натрия.
Запишите свои наблюдения, уравнение соответствующей реакции и сделайте вывод.
Опыт 3. Взаимодействие глицерина с металлическим натрием.
В пробирку с глицерином бросьте кусочек натрия. Пробирку слегка подогрейте. Выделяющийся водород можно поджечь.
Запишите наблюдения, уравнение соответствующей реакции и сделайте вывод о скорости протекания реакции.
Налейте немного этилового спирта в фарфоровую чашку. Поднесите к ней горящую лучину.
Запишите свои наблюдения и уравнение реакции горения этанола.
Опыт 5. Окисление этилового спирта оксидом меди (II). (Качественное определение этанола).
1-й способ. В сухую пробирку налейте приблизительно 1 мл этанола. Раскалите медную спираль в и быстро опустите спираль в пробирку со спиртом, выньте и, не нагревая ее, снова опустите в пары спирта. Осторожно понюхайте содержимое пробирки, направляя поток воздуха к себе рукой.
Запишите наблюдения и уравнения соответствующих реакций.
2-й способ. В прибор для окисления спиртов налейте немного этилового спирта. Присоедините к газоотводной трубке прибор для подачи воздуха. Раскалите в горелке медную спираль и поместим ее в прибор. Подавайте в прибор ток воздуха. Медная спираль в приборе продолжает быть раскаленной, так как начинается окисление спирта.
Запишите свои наблюдения и уравнение соответствующей реакции.
Опыт 6. Качественная реакция на глицерин.
В пробирку налейте 2 мл раствора гидроксида натрия и добавьте к нему немного раствора сульфата меди(II). К осадку прилейте раствор глицерина, который вы получили в первом опыте, перемешайте.
Запишите свои наблюдения и уравнения соответствующих реакций.
Сделайте вывод о растворимости в воде одно- и многоатомных спиртов.
Как в лабораторных условиях можно доказать наличие этанола?
Как в лабораторных условиях можно определить глицерин?
Сделайте общий вывод.
Опыт 1. Изучение физических свойств одно- и многоатомных спиртов.
Одноатомные спирты, содержащие в своем составе до десяти атомов углерода, в обычных условиях — жидкости. Спирты, в составе которых 11 атомов углерода и более — твердые тела. Этиловый, бутиловый и изоамиловый спирт – жидкости. Спирты имеют плотность меньше единицы, поэтому они образуют верхний слой. При взбалтывании пробирок происходит полное растворение этилового спирта, частично растворяется бутиловый спирт, почти не растворяется изоамиловый спирт. Краситель из водного раствора переходит в спирты. С повышением молекулярной массы и увеличением углеводородного радикала растворимость спиртов в воде уменьшается.
Глицерин – прозрачная, бесцветная, вязкая, сладковатая сиропообразная жидкость. Глицерин хорошо растворим в воде, и смешивается с ней в любых отношениях. Растворы глицерина замерзают при очень низких температурах. Если приготовить охлаждающую смесь из поваренной соли и кусочков льда и опустить в нее две пробирки. В одной из пробирок – вода, в другой – раствор глицерина. Через некоторое время вода замерзает. Раствор глицерина остается жидким. Глицерин и этиленгликоль используются в качестве антифризов в радиаторах автомобилей.
Опыт 2. Взаимодействие этилового спирта с металлическим натрием.
При взаимодействии спиртов с натрием образуются газообразный водород и соответствующие алкоголяты натрия. Приготовим пробирки с метиловым, этиловым и бутиловым спиртами. Опустим в пробирку с метиловым спиртом кусочек металлического натрия. Начинается энергичная реакция. Натрий плавится, выделяется водород.
Опустим натрий в пробирку с этиловым спиртом. Реакция идет немного медленней. Выделяющийся водород можно поджечь. По окончании реакции выделим этилат натрия. Для этого опустим в пробирку стеклянную палочку и подержим ее над пламенем горелки. Избыток спирта испаряется. На палочке остается белый налет этилата натрия.
В пробирке с бутиловым спиртом реакция с натрием идет еще медленнее.
Итак, с удлинением и разветвлением углеводородного радикала скорость реакции спиртов с натрием уменьшается.
Опыт 3. Взаимодействие глицерина с металлическим натрием.
Как и одноатомные спирты, многоатомные спирты реагируют с металлическим натрием. Если в пробирку с глицерином бросить кусочек натрия и пробирку слегка подогреть, то реакция идет вначале медленно, затем более энергично. Выделяющийся водород можно поджечь. Реакция протекает очень энергично, выделяется много теплоты, на завершающей стадии реакции происходит обугливание глицерина.
Если к чашкам с этиловым, бутиловым и изоамиловым спиртами поднести горящую лучину, то можем наблюдать как этиловый спирт быстро загорается и горит голубоватым, слабосветящимся пламенем. Бутиловый спирт горит светящимся пламенем. Труднее загорается изоамиловый спирт, он горит коптящим пламенем. С увеличением молекулярной массы одноатомных спиртов повышается температура кипения и возрастает светимость их пламени.
Опыт 5. Окисление этилового спирта оксидом меди (II). (Качественное определение этанола)
В сухую пробирку налейте приблизительно 1 мл этанола. Раскалите медную спираль в пламени — на ее поверхности образуется черный налет оксида меди(II). Быстро опустите спираль в пробирку со спиртом, выньте и, не нагревая ее, снова опустите в пары спирта. Осторожно понюхайте содержимое пробирки, направляя поток воздуха к себе рукой. В прибор для окисления спиртов нальем немного этилового спирта. Присоединим к газоотводной трубке прибор для подачи воздуха. Раскалим в горелке медную спираль и поместим ее в прибор. Подадим в прибор ток воздуха. Медная спираль в приборе продолжает быть раскаленной, так как начинается окисление спирта. Продукт окисления спирта — уксусный альдегид.
Альдегид обнаруживаем, пропуская через фуксинсернистую кислоту выходящие из прибора газы. Под действием альдегида фуксинсернистая кислота приобретает фиолетовую окраску. Покажем, что медная спираль раскалена. Извлечем спираль из прибора и поднесем к ней спичку. Спичка загорается. Мы убедились в том, что при окислении одноатомных спиртов образуются альдегиды.
Опыт 6. Качественная реакция на глицерин.
В пробирку налейте 2 мл раствора гидроксида натрия и добавьте к нему немного раствора сульфата меди(II). К осадку прилейте раствор глицерина, который вы получили в первом опыте, перемешайте.
Наблюдения. Голубой осадок растворяется, образуется раствор синего цвета.