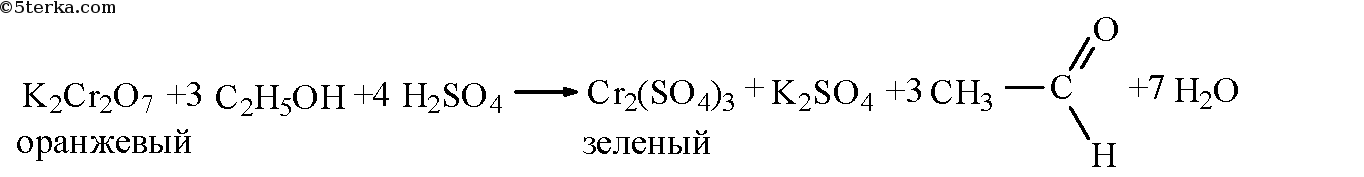Опыт 1. Растворимость спиртов в воде.
Условия выполнения работы:
В две пробирки налили примерно по 2 мл этилового и изоамилового спиртов. Добавили в каждую из пробирок по 3 мл воды и взболтали. Наблюдаем, что этиловый спирт растворился, а изоамиловый нет, и при стоянии образует верхний маслянистый слой, так как его плотность меньше плотности воды (0,8 г/мл). Причиной различного поведения спиртов в воде является природа веществ.
Опыт 2. Получение глицерата меди.
Условия выполнения работы:
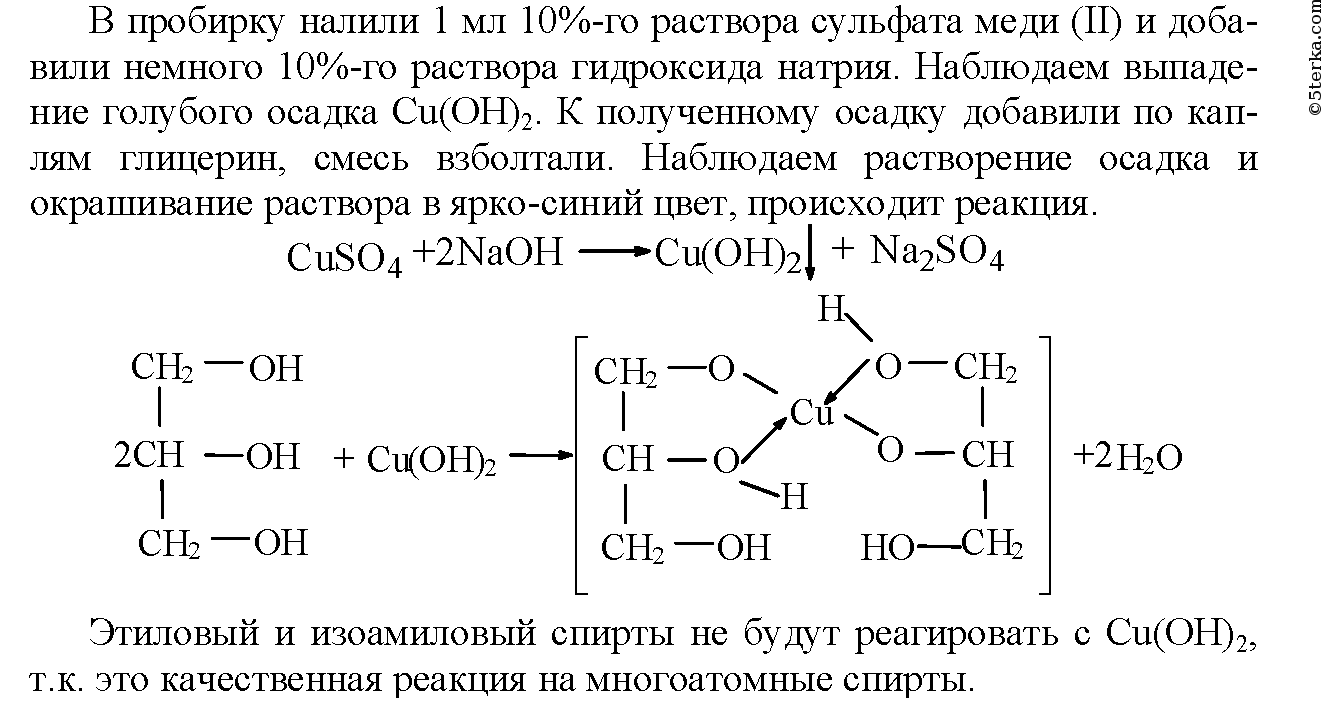
В пробирку налили 1 мл 10%-го раствора сульфата меди (II) и добавили немного 10%-го раствора гидроксида натрия. Наблюдаем выпадение голубого осадка Cu(OH)2. К полученному осадку добавили по каплям глицерин, смесь взболтали. Наблюдаем растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнения реакции взаимодействия сульфата меди (ΙΙ) с гидроксидом натрия:
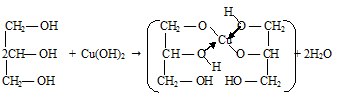
Качественной реакцией на многоатомные спирты является реакция с гидроксидом меди (ΙΙ). Например, при действии глицерина на осадок гидроксида меди (ΙΙ) н аблюдается растворение осадка и окрашивание раствора в ярко-синий цвет, происходит реакция.
Уравнение реакции имеет вид:
Этиловый и изоамиловый спирты не будут реагировать с Cu(OH)2, так как это качественная реакция на многоатомные спирты.
Опыт 3. Окисление этилового спирта хромовой смесью.
Условия выполнения работы:
Налили в пробирку 2 мл 5%-го раствора дихромата калия, 1 мл 20%-го раствора серной кислоты и 0,5 мл этилового спирта, получили смесь оранжевого цвета. Пробирку нагрели. Наблюдаем изменение цвета раствора на зелёный и чувствуем характерный запах уксусного альдегида.
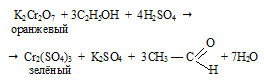
В данной реакции применяют серную кислоту, а не соляную, потому что соляная кислота может окислиться.
Практическая работа № 3. Спирты
Опыт 1. Растворимость спиртов в воде
В две пробирки налили по 2 мл этилового и изоамилового спиртов. Добавили в каждую из пробирок по 3 мл воды и взболтали. Наблюдаем, что этиловый спирт растворился, а изоамиловый нет и при стоянии образует верхний маслянистый слой, т. к. его плотность меньше плотности воды (0,8 г/мл). Причиной различного поведения спиртов в воде является природа веществ.
Также над водой будут отслаиваться бензол, бутиловый спирт, олеиновая кислота.
Опыт 2. Получение глицерата меди
Опыт 3. Окисление этилового спирта хромовой смесью
Налили в пробирку 2 мл 5%-го раствора дихромата калия, 1 мл 20%-го раствора серной кислоты и 0,5 мл этилового спирта, получили смесь
оранжевого цвета. Пробирку нагрели. Наблюдаем изменение цвета раствора на зеленый и чувствуем характерный запах уксусного альдегида.
Серную кислоту лучше не менять на соляную, т.к. последняя может окисляться.

задача №3
к главе «Химический практикум».
Т 1: Реакция серебряного зеркала
Практическая работа № 4
Спирты
Т 1: Растворимость спиртов в воде
Приборы и материалы:пробирки химические,этиловый спирт 
вода
Ход работы:
1. В определённые пробирки наливаем 1-2 мл/г этилового спирта, во вторую пробирку наливаем другого спирта.
2. К ним добавляем 2-3 мл/г воды и взбалтываем.
3. Отмечаем, что этиловый спирт полностью растворился в воде, а изоамиловый спирт отделяется при отстаивании в виде масляного слоя над водой.
Вопросы:
1. В чём причина различного «поведения» спиртов в воде?
2. Почему изоамиловый спирт отслаивается над водой?
3. Какие органические жидкие вещества при смешивании с водой будут отслаиваться над водой?
Ответы на вопросы:
1. Причина различного «поведения» спиртов в воде зависит от особенности химической природы спиртов, прежде всего проявляется в строении молекул.
2. Причина в том, что при увеличении числа метиловых групп реакции окисления замедляются.
3. Бутиловый спирт, изоамиловый спирт, пропиловый спирт, цетиловый спирт, амиловый спирт, пропаргиловый спирт.
Т 2: Получение глицерата меди
Приборы и материалы:пробирки химические, 10% раствор сульфата меди


глицирин
Ход работы:
1. В пробирку наливаем около 1 мл/г 10% раствора судьфата меди, сюда же добавляем 1 мл/г 10% раствора гидроксида натрия до образования голубого осадка гидроксида меди.
2. К полученному осадку добавили по каплям глицерин, взболтали смесь.
3. Отмечаем превращение голубуго осадка в растворе тёмно-синего цвета.
Вопросы:
1. Какая реакция лежит в основе получения гидроксида меди? Напишите уравнение реакции.
2. Почему при добавлении глицерина к осадку гидроксида меди осадок растворяется? С чем связано интенсивное окрашивание раствора? Напишите уравнение взаимодействия глицерина с гидроксидом меди.
3. Будут ли этиловый и изоамиловый спирты реагировать с гидроксидом меди?
Ответы на вопросы:
1.
2. Глицерин как многоатомный спирт образовывает растворимые в воде ярко-синие комплексные соединения при взаимодействии со свеже-полученным осадком 

| 


3. Нет, не будут, потому что свеже-осаждённый гидроксид меди реагирует только с многоатомными спиртами.
Т 3: Окисление этилового спирта дихроматом калия
Приборы и материалы:пробирка химическая, 5% раствор дихромата
калия, 20% раствор серной кислоты, спиртовая
Ход работы:
1. В пробирке смешиваем 2 мл/г 5% раствора дихромата калия, 1 мл/г 20% раствора серной кислоты, 0,5% мл/г этилового спирта.
2. Отмечаем цвет раствора.
3. Осторожно нагреваем смесь на пламени спиртовой горелки до начала изменения цвета, при этом ощущается запах уксусного альдегида, образовавшийся в результате реакции.
Вопросы:
1. Почему цвет раствора меняется с оранжевого до синевато-зелёного? Напишите уравнение окисления этилового спирта.
2. Можно ли заменить серную кислоту в данной реакции на соляную?
Ответы на вопросы:
1.
2. Да, я считаю, что можно заменить серную кислоту на соляную.
Практическая работа № 5
Альдегиды и Кетоны
Т 1: Реакция серебряного зеркала
Приборы и материалы:пробирка химическая ПХ-16, формалин
(формальдегид), аммиачный раствор оксида
серебра, спиртовая горелка
Ход работы:
1. В пробирку с 1 мл/г формальна добавляем несколько капель аммиачного раствора оксида серебра.
2. Пробирку слегка нагреваем, выделяющееся серебро выпадает или в виде чёрного осадка или в виде блестящего зеркального налёта.
3. Завершаем опыт.
Вопросы:
1. Что наблюдается в пробирке?
2. Почему поверхность стекла становится зеркальной?
Ответы на вопросы:
1. Наблюдается выделение газа и образование «зеркала».
2. Потому что на ней оседает металлическое серебро.