Ответ оставил Гость
K2CO3+2HNO3=2KNO3+Н2О+СО2реакция идут при обычных условиях признак реакции образование газа
Если твой вопрос не раскрыт полностью, то попробуй воспользоваться поиском на сайте и найти другие ответы по предмету Химия.
- Расставь коэффициенты в уравнении реакции и дополни её характеристику.Если перед формулой — коэффициент «1», то ячейку для него оставь пустой. ZN+. HCL=. ZNCL2+. H2Реакция возможнапри обычной температуре, только при освещении, при нагреванииПризнаком реакции являетсявыпадение осадка, изменение запаха, образование газообразного вещества
- Как расставлять коэффициенты в химических уравнениях
- Пример разбора простых реакций
- Пример разбора сложной реакции
- Видео
- Видео
Видео:Расстановка коэффициентов в химических реакциях: как просто это сделатьСкачать
Расставь коэффициенты в уравнении реакции и дополни её характеристику.Если перед формулой — коэффициент «1», то ячейку для него оставь пустой. ZN+. HCL=. ZNCL2+. H2Реакция возможнапри обычной температуре, только при освещении, при нагреванииПризнаком реакции являетсявыпадение осадка, изменение запаха, образование газообразного вещества
Zn + 2HCl = ZnCl2 + H2
Реакция возможна при обычной температуре
Признаком реакции является образование газообразного вещества(Н2)
Видео:Как расставлять коэффициенты в уравнении реакции? Химия с нуля 7-8 класс | TutorOnlineСкачать

Как расставлять коэффициенты в химических уравнениях
Содержание:
Все химические реакции, проходящие в окружающем мире можно описать при помощи специальных уравнений, представляющих собой химические формулы и математические знаки с коэффициентами. И от правильно расставленных коэффициентов в химических уравнениях порой зависит не много не мало, а то какой собственно и будет химическая реакция и будет ли она вообще. В нашей статье мы расскажем о том, как правильно расставлять коэффициенты в химии, чтобы химические уравнения были записаны верно.
Видео:Расстановка Коэффициентов в Химических Реакциях // Подготовка к ЕГЭ по ХимииСкачать

Пример разбора простых реакций
Главное правило, которым следует руководствоваться при составлении химических уравнений – принцип сохранения энергии вещества, то есть, сколько есть атомов каждого химического элемента в левой части уравнения, столько должно быть и в правой части того же уравнения.
Для примера возьмем химическую реакцию взаимодействия кальция (Ca) с кислородом (O2). Но для начала объясним, почему вообще кислород (как и некоторые другие химических элементы) в химических уравнениях записывается с индексом «2». Дело в том, что одна молекула кислорода имеет 2 атома, поэтому его записывают как O2. В свою очередь, к примеру, одна молекула воды, состоящая из кислорода и водорода, имеет всем известную формулу H2O. Это означает, что каждая молекула воды состоит из двух атомов водорода и одного атома кислорода. Заметьте, что по своему усмотрению индексы в химических уравнениях и формулах менять нельзя, так как они изначально должны быть написаны правильно.
Теперь вернемся к нашему простому примеру реакции взаимодействия кальция и кислорода. Ее можно записать следующим образом:
О чем говорит эта запись? О том, что в результате химической реакции взаимодействия кальция с кислородом образуется оксид кальция, который записан формулой CaO. Но также обратите внимание, что в правой части оксид кальция мы записали с коэффициентом 2 – 2CaO. Это значит, что каждый из двух атомов кислорода сцепился со своим атомом кальция, но тогда происходит несоответствие – в правой стороне у нас два атома кальция, в то время как в левой только лишь один. А значит, чтобы запись была правильной в левой части мы должны перед кальцием поставить коэффициент 2:
Теперь мы можем проверить наше уравнение – с левой стороны у нас два атома кальция и с правой тоже два, а значит между обеими частями можно вполне справедливо поставить знак равенства:
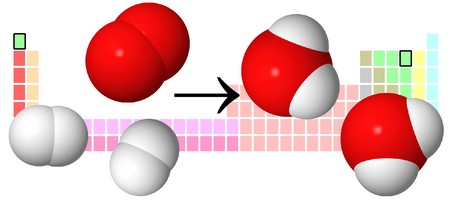
Разберем еще один простой пример, из взаимодействия кислорода и водорода как мы знаем, рождается одно из самых ценным и необычных веществ во Вселенной (и это без преувеличения) – вода, основа жизни на нашей планете. Образование воды можно записать следующим уравнением:
Но где же здесь закралась ошибка? Давайте разберем: в левой части у нас два атома кислорода, а в правой только один. Значит перед формулой воды необходимо поставить коэффициент 2:
Умножение 2 молекул воды на 2 атома водорода даст нам 4 атома водорода с правой стороны, но ведь с левой стороны атомов водорода лишь два! Значить перед водородом в уравнении мы также должны поставить коэффициент 2 и теперь получим правильное химическое уравнение, где вместо стрелочки → можно уже смело поставить знак равенства.
Видео:Расстановка коэффициентов в окислительно-восстановительных реакцияхСкачать

Пример разбора сложной реакции
Теперь давайте разберем то, как проставлять коэффициенты в более сложных химических уравнениях:
Перед вами запись так званой реакции нейтрализации – взаимодействие кислоты и основания, в результате которого образуются соли и вода.
Что же мы имеем тут: с левой стороны у нас один атом натрия (Na), а с правой индекс говорит, что атомов натрия уже стало два. Значит логично, что химическую формулу основания гидроксида натрия NaOH надо умножить на 2. Или другими словами поставить перед ней коэффициент 2:
Количество серы в серной кислоте (H2SO4) и соли сульфате натрия (Na2SO4) у нас одинаковое, тут все хорошо, а вот с количеством кислорода и водорода опять несоответствие, с левой стороны кислорода 6, а с правой 5. Водорода с правой стороны 4, а с левой только 2, непорядок. Чтобы правильно записать это химическое уравнение надо сравнять количество кислорода и водорода в левой и правой части уравнения, к счастью тут сделать это просто, надо перед H2O поставить коэффициент 2.
Таким образом, количество всех химических элементов в правой и левой части уравнения у нас сравнялись, а значит, мы неспроста поставили знак равенства.
Для закрепления материала разберем еще один пример сложного уравнения.
Это уравнение отображает химическую реакцию гидроксида бария (Ba(OH)2) с азотной кислотой (HNO3) в результате которой образуется нитрат бария (Ba(NO3)2) и вода.
Пример этот нам интересен тем, что тут используются скобки. Они означают, что если множитель стоит за скобками, то каждый элемент умножается на него. Начнем же разбирать это уравнение, первое, что бросается в глаза, несоответствие азота N, слева он один, а вот справа, если принимать во внимание скобки, его уже два. Получим следующее:
Теперь у нас слева стало 4 атома водорода, а справа только 2. Значит, перед формулой воды также ставим коэффициент 2.
Теперь все элементы уравнены, и мы справедливо поставили знак равенства.
Видео:Как расставить коэффициенты? Как превратить схему химической реакции в уравнение химической реакции.Скачать

Видео
И чтобы окончательно закрепить материал, рекомендуем посмотреть это образовательное видео.
🔍 Видео
Как расставить коэффициенты уравнении реакцииСкачать

25. Схема реакции и химическое уравнениеСкачать

Коэффициенты в уравнениях химических реакцийСкачать

Задача на расчёт переходной и импульсной характеристик цепи. Расчёт реакции через интеграл свёртки.Скачать

Упражнения на составление формул и названий гомологов и изомеров | Химия 10 класс #5 | ИнфоурокСкачать

Как расставить коэффициенты в органических ОВР? | Екатерина СтрогановаСкачать

140. Расставляем коэффициенты методом электронного балансаСкачать

Решение задач на вывод формул органических соединений | Химия 10 класс #8 | ИнфоурокСкачать

Урок 4. Расчет цепей постоянного тока. Законы КирхгофаСкачать

07 Кинетика 5 эксп опред параметров реакцииСкачать

Определение порядка реакции методом подбора кинетического уравненияСкачать

Установление эмпирической и молек. формул по массовым долям элем., входящих в состав в-ва. 10 класс.Скачать

Коэффициент ранговой корреляции Спирмена в MS Excel. Функция РАНГ.СРСкачать

Органика. Решение задачи на определение состава вещества по продуктам его сгорания.Скачать

Задание №35: вывод формулы органического соединения | Химия 10 класс | УмскулСкачать