В уроке 14 «Расчеты по уравнениям химических реакций» из курса «Химия для чайников» мы научимся решать задачи, используя уравнения химических реакций.
Вещества вступают в химические реакции в определенных массовых и количественных соотношениях. Следовательно, при проведении реакций в лабораториях и на химических заводах расходуются определенные массы исходных веществ для получения заданной массы продуктов реакции.
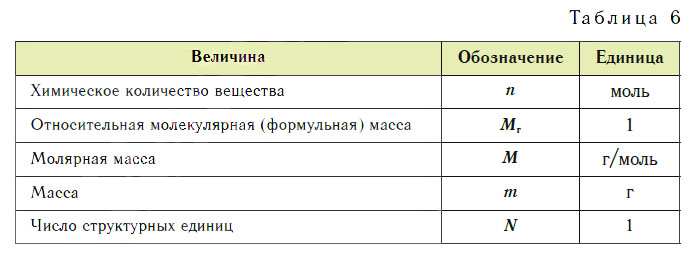
Эти расчеты проводят по уравнениям реакций. Единицы величин, которыми пользуются в химии, представлены в таблице 6.
При проведении любого вычисления по уравнению реакции нужно внимательно прочитать условие задачи. Особое в нимание обратите на расстановку коэффициентов, так как соотношение числа структурных единиц реагирующих веществ и получающихся продуктов реакции выражается в уравнениях коэффициентами так же, как и мольные отношения.
Для решения расчетной задачи необходим определенный порядок действий. Рассмотрим его на нескольких примерах.
Пример 1. Железо масс о й 224 г полностью прореагировало с хлором. Рассчитайте массу образовавшегося вещества FeCl3.
- Учимся решать задачи 8 класс Решение задач по теме: «Моль. Количество вещества».
- Дистанционное обучение как современный формат преподавания
- Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Химия: теория и методика преподавания в образовательной организации
- Дистанционные курсы для педагогов
- Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
- Материал подходит для УМК
- Другие материалы
- Вам будут интересны эти курсы:
- Оставьте свой комментарий
- Автор материала
- Дистанционные курсы для педагогов
- Подарочные сертификаты
- Расчеты по уравнениям реакций химия 8 класс моль объяснение задач
Учимся решать задачи 8 класс Решение задач по теме: «Моль. Количество вещества».
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Рабочие листы и материалы для учителей и воспитателей
Более 300 дидактических материалов для школьного и домашнего обучения
Учимся решать задачи 8 класс
Решение задач по теме: «Моль. Количество вещества».
n- количество вещества, ( моль , кмоль, ммоль)
m – масса, ( г , кг, мг)
M – молярная масса, ( г/ моль , кг/ кмоль, мг/ ммоль)
V – объем, ( л , м 3 , см 3 , мл)
V м – молярный объем ( л/ моль , м 3 / кмоль, мл/ ммоль) для любого газа при нормальных условиях (н.у.) равен 22,4 л/моль
N — число частиц (атомы, молекулы, ионы)
N А- постоянная Авогадро равна 6,02 . 10 23 частиц . моль -1
Задача 1 . Сколько молекул озона О3 содержится в 72 г его?
1) n (О3)= m / M = 72г:48г/моль=1,5моль
2) N (О3)= n NA = =1,5моль . 6,02 . 10 23 молекул . моль -1 =9 . 10 23 молекул
Задача 2. Какой объем занимают (при н.у.) 280 кг азота?
- n ( N 2 )= m / M = 280кг:28кг/ кмоль =10кмоль
M ( N 2 ) = 14 . 2= 28 г/моль= 28кг/ кмоль
Ответ: V ( N 2 )= 224 м 3
Задача 3 . Какую массу имеют 112л (при н.у.) углекислого газа?
Решите самостоятельно задачи:
1. Хлориду натрия массой 5,85 г соответствует количество вещества:
1) 1 моль; 2) 0,5 моль; 3) 0,1 моль; 4 ) 0,01 моль.
2. Оксиду кальция массой 28 г соответствует количество вещества:
1) 1 моль; 2) 0,1 моль; 3 )2 моль; 4) 0,5 моль.
3. Масса 0,25 моль хлорида меди ( II ) равна:
1) 64 г; 2) 24,75 г; 3) 24,875 г; 4) 33,75 г.
4. Какой объем при н.у. занимают 64г оксида серы ( IV )?
5 . Какую массу имеют 3 • 10 24 молекул углекислого газа (оксида углерода ( IV ))?
6. Какую массу имеют 44,8 л при н.у. угарного газа (оксид углерода ( II ))?
7. Какой объем занимают 6 • 10 23 молекул сероводорода H 2 S ?
9. Какой объем при н.у. занимают 96г озона О3?
10 . Сколько молекул хлора CI 2 c одержится в 284г его?
Тема 15. Молярный объём газов
1. 1 моль любого газа при н. у. занимает одинаковый объём, равный 22,4 л. Этот объём называется молярный и обозначается Vm.
2. Количество вещества (n) — отношение объёма газа при н. у. к молярному объёму:
n = V/Vm=> Vm измеряется в л/моль.
3. Следовательно, количество вещества
4. Дополните таблицу «Количественные характеристики веществ», делая необходимые вычисления.
1. Установите соотношение между названием и размерностью величины.
2. Укажите формулы, которые являются производными от основной формулы n = V/Vm.
2) V=n•Vm
3) Vm=V/n
3. Сколько молекул содержат 44,8 л (н. у.) углекислого газа? Решите задачу двумя способами.
4. Придумайте условие задачи, в которой нужно найти число молекул N, если известен объём V.
Найти число частиц оксида азота(II), если его объём равен 67,2 л.
Решите задачу любым способом.
5. Вычислите массу 78,4 л (н. у.) хлора.
6. Найдите объём 297 г фосгена (COCl2).
7. Вычислите массу 56 л аммиака, 10% -й водный раствор которого в медицине известен под названием «нашатырный спирт».
8. Придумайте задачу с использованием изученных понятий. С помощью компьютера создайте рисунок, иллюстрирующий данную задачу. Предложите способ её решения. Верно ли, что 22,4 л азота или 22,4 л водорода одинаковы по массе? Ответ подтвердите вычислениями.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 859 человек из 78 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Сейчас обучается 49 человек из 21 региона
Курс профессиональной переподготовки
Химия: теория и методика преподавания в образовательной организации
- Сейчас обучается 376 человек из 64 регионов
«Мотивация здорового образа жизни. Организация секций»
Свидетельство и скидка на обучение каждому участнику
- Для всех учеников 1-11 классов
и дошкольников - Интересные задания
по 16 предметам
«Как закрыть гештальт: практики и упражнения»
Свидетельство и скидка на обучение каждому участнику
Дистанционные курсы для педагогов
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 842 398 материалов в базе
Материал подходит для УМК
«Химия», Габриелян О.С.
§ 1. Химия — часть естествознания
Ищем педагогов в команду «Инфоурок»
Другие материалы
- 23.11.2017
- 675
- 0
- 23.11.2017
- 3463
- 37
- 23.11.2017
- 1337
- 9
- 23.11.2017
- 329
- 0
- 22.11.2017
- 634
- 0
- 22.11.2017
- 1036
- 0
- 22.11.2017
- 24439
- 12
- 18.11.2017
- 1264
- 81
«Учись, играя: эффективное обучение иностранным языкам дошкольников»
Свидетельство и скидка на обучение
каждому участнику
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 23.11.2017 129957
- DOCX 336.9 кбайт
- 2212 скачиваний
- Рейтинг: 4 из 5
- Оцените материал:
Настоящий материал опубликован пользователем Джабраилова Хурзадай Джунайдовна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 4 года и 5 месяцев
- Подписчики: 1
- Всего просмотров: 195335
- Всего материалов: 53
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Российские школьники начнут изучать историю с первого класса
Время чтения: 1 минута
Минпросвещения рекомендует школьникам сдавать телефоны перед входом в школу
Время чтения: 1 минута
Минпросвещения проведет Всероссийский конкурс для органов опеки и попечительства
Время чтения: 1 минута
Минобрнауки отменило плановые и внеплановые проверки вузов в 2022 году
Время чтения: 1 минута
С 1 сентября в российских школах будут исполнять гимн России
Время чтения: 1 минута
Около 20% детей до 15 лет не воспринимают прочитанную информацию
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Расчеты по уравнениям реакций химия 8 класс моль объяснение задач
Урок посвящен закреплению умений производить расчеты по уравнению реакции с учетом количественных соотношений участников реакции.
I. Алгоритмы решения задач по уравнению химических реакций
Внимательно изучите алгоритмы и запишите в тетрадь, решите самостоятельно предложенные задачи
- Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0,27 моль с достаточным количеством кислорода (4Al +3O2=2Al2O3).
2. Вычислите количество вещества оксида натрия, образовавшегося в результате взаимодействия натрия количеством вещества 2,3 моль с достаточным количеством кислорода (4Na+O2=2Na2O).
Алгоритм №1
Вычисление количества вещества по известному количеству вещества, участвующего в реакции
Пример. Вычислите количество вещества кислорода, выделившегося в результате разложения воды количеством вещества 6 моль.
Последовательность выполнения действий
1. Записать условие задачи
2. Вычислить молярные массы веществ,
о которых, идёт речь в задаче
3. Запишем уравнение реакции
и расставим коэффициенты
4. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –
стехиометрические коэффициенты,
отображаемые уравнением реакции
5. Для вычисления искомого количества вещества,
6. Записываем ответ
- Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите массу серы, необходимую для получения оксида серы (IV) количеством вещества 4 моль (S+O2=SO2).
2. Вычислите массу лития, необходимого для получения хлорида лития количеством вещества 0,6 моль (2Li+Cl2=2LiCl).
Алгоритм №2
Вычисление массы вещества по известному количеству другого вещества, участвующего в реакции
Пример: Вычислите массу алюминия, необходимого для получения оксида алюминия количеством вещества 8 моль.
Последовательность выполнения действий
Оформление решения задачи
1. Записать условие задачи
2. Вычислить молярные массы веществ,
о которых, идёт речь в задаче
3. Запишем уравнение реакции
и расставим коэффициенты
4. Над формулами веществ запишем
количества веществ из условия задачи,
а под формулами –стехиометрические коэффициенты, отображаемые уравнением реакции
5. Вычислим количества вещества, массу которого требуется найти. Для этого составим соотношение.
6. Вычисляем массу вещества, которую требуется найти
7. Записываем ответ
- Используя алгоритм, решите самостоятельно следующие задачи:
1. Вычислите количество вещества сульфида натрия, если в реакцию с натрием вступает сера массой 12,8 г (2Na+S=Na2S).
2. Вычислите количество вещества образующейся меди, если в реакцию с водородом вступает оксид меди (II) массой 64 г (CuO + H2 = Cu + H2O).
Алгоритм №3
Вычисление количества вещества по известной массе другого вещества, участвующего в реакции
Пример. Вычислите количество вещества оксида меди (I), если в реакцию с кислородом вступает медь массой 19,2г.
Последовательность выполнения действий
1. Записать условие задачи
2. Вычислить молярные массы веществ, о которых, идёт речь в задаче
3. Найдём количество вещества, масса которого дана в условии задачи
4. Запишем уравнение реакции
и расставим коэффициенты
5. Над формулами веществ запишем
количества веществ из условия задачи, а под формулами –стехиометрические коэффициенты, отображаемые уравнением реакции
6. Для вычисления искомого количества вещества, составим соотношение
7. Запишем ответ
- Используя алгоритм, решите самостоятельно задачу:
1. Вычислите массу кислорода, необходимую для реакции с железом массой 112 г (3Fe + 4O2=Fe3O4).
Алгоритм №4
Пример. Вычислите массу кислорода, необходимую для сгорания фосфора, массой 0,31г.
Последовательность выполнения действий
1. Записать условие задачи
2. Вычислить молярные массы веществ,
о которых, идёт реь в задаче
3. Найдём количество вещества, масса которого дана в условии задачи
4. Запишем уравнение реакции и расставим коэффициенты
5. Над формулами веществ запишем
количества веществ из условия задачи, а под формулами –стехиометрические коэффициенты, отображаемые уравнением реакции
6. Вычислим количества вещества, массу которого необходимо найти
7. Найдем массу вещeства, которую требуется вычислить
8. Запишем ответ
II. Задачи для самостоятельного решения
1. Вычислите количество вещества оксида алюминия, образовавшегося в результате взаимодействия алюминия количеством вещества 0,27 моль с достаточным количеством кислорода (4Al +3O2=2Al2O3).
2. Вычислите количество вещества оксида натрия, образовавшегося в результате взаимодействия натрия количеством вещества 2,3 моль с достаточным количеством кислорода (4Na+O2=2Na2O).
3. Вычислите массу серы, необходимую для получения оксида серы (IV) количеством вещества 4 моль (S+O2=SO2).
4. Вычислите массу лития, необходимого для получения хлорида лития количеством вещества 0,6 моль (2Li+Cl2=2LiCl).
5. Вычислите количество вещества сульфида натрия, если в реакцию с натрием вступает сера массой 12,8 г (2Na+S=Na2S).
6. Вычислите количество вещества образующейся меди, если в реакцию с водородом вступает оксид меди (II) массой 64 г (CuO + H2 = Cu + H2O).