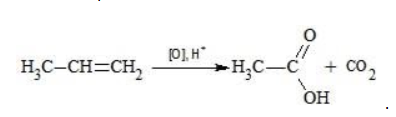
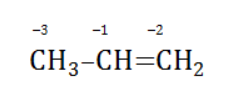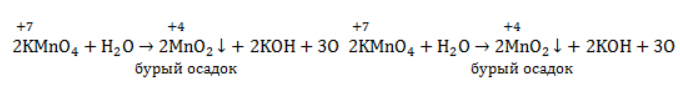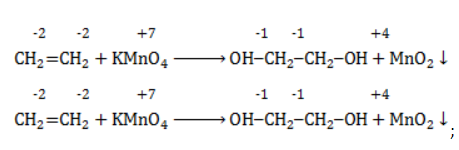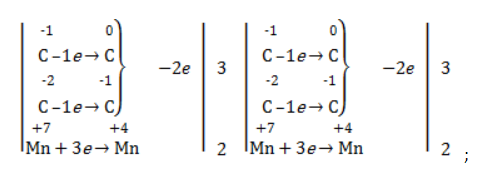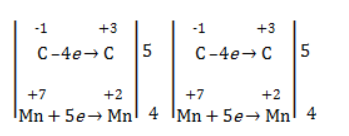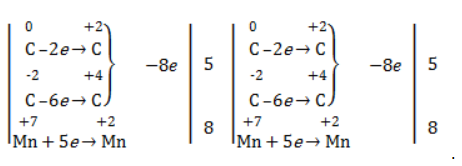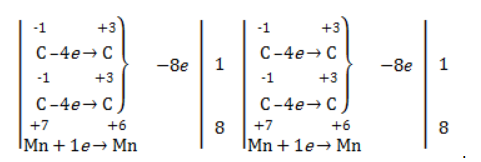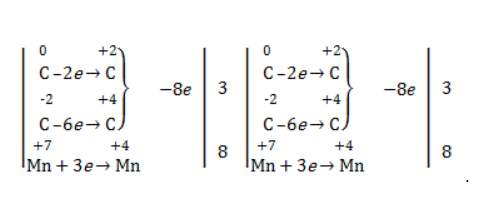В отличие от предельных углеводородов, алкены характеризуются высокой химической активностью, обусловленной особенностями строения молекулы. При обычных условиях алкены охотно вступают в реакции неполного окисления с превращением в органические соединения других классов. Универсальный реагент в процессах окисления алкенов – перманганат калия.
- Понятие о неполном окислении
- Определение степеней окисления
- Влияние среды на окислитель
- Мягкое окисление
- Жесткое окисление
- Окисление перманганатом калия в кислой среде
- Окисление алкенов в щелочной среде
- Окисление в нейтральном растворе
- Заключение
- Составление уравнений окислительно-восстановительных реакций с участием органических веществ
- Acetyl
Понятие о неполном окислении
В химии органических соединений под окислением понимается взаимодействие, при котором происходит обеднение реагента водородом или обогащение кислородом, сопровождающееся отдачей электронов молекулой. Обратный процесс называется восстановлением.
Полное окисление происходит при горении углеводородов с разрушением молекулы. Продуктами в этом случае являются углекислый газ и вода. При неполном окислении продуктами становятся различные вещества.
Высокая реакционная способность алкенов обусловливается присутствием в молекуле двойной связи. Один из ее компонентов – слабая 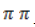
Определение степеней окисления
Для того чтобы правильно записать уравнение реакции неполного окисления алкена, нужно определить степени окисления атомов до вступления во взаимодействие и после него. Они рассчитываются исходя из электроотрицательности элементов.
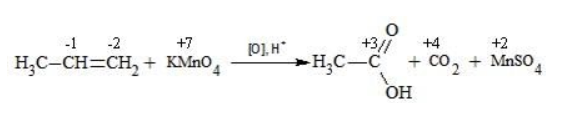
Например, при окислении пропена перманганатом калия 


- В составе группы
углерод, обладающий большей электроотрицательностью, смещает к себе электронные пары двух связей
, отнимая у водородных атомов по одному отрицательному заряду. На связи
сдвига электронов нет. Следовательно, атом углерода приобретает степень окисления -2 -2;
- В группе
аналогичный подсчет показывает для углерода степень окисления -1 -1 (для каждого водорода соответственно +1 +1);
- В радикале
углерод оттягивает на себя отрицательные заряды с трех водородных атомов и имеет степень окисления -3 -3.
В общем виде результат можно записать следующим образом:
Расчет степеней окисления в кислородсодержащих соединениях производится аналогично с учетом большей электроотрицательности кислорода.
Влияние среды на окислитель
Состав раствора (наряду с температурой) определяет, до какого соединения окислится восстановитель – алкен. Окислитель в растворах с различным уровнем кислотности (щелочности) также ведет себя неодинаково.
Неорганическая соль 


В нейтральной и слабощелочной среде марганец приобретает степень окисления +4 +4:
Кислород из перманганат-аниона присоединяется к алкену по месту двойной связи.
Под воздействием серной кислоты марганец восстанавливается до степени окисления +2 +2:
При окислении со щелочью (гидроксид лития достаточно высокой концентрации) марганец восстановится до +6 +6:
Мягкое окисление
Процесс в нейтральной или слабощелочной среде при обычной температуре представляет собой так называемое мягкое окисление перманганатом калия, или гидроксилирование. В алкене разрывается 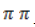
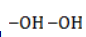
- кислород из перманганат-иона;
- вода.
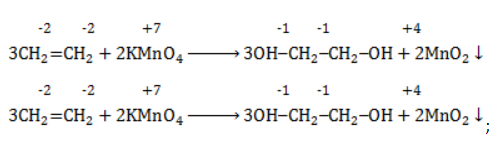
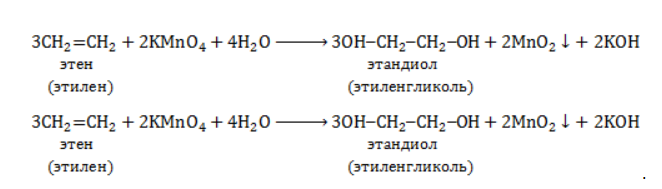
Продукт реакции – диол (двухатомный спирт). Например, окисление этилена перманганатом калия приводит к образованию этиленгликоля:
Для составления полного уравнения нужно:
- определить степени окисления реагентов:
- рассчитать электронный баланс:
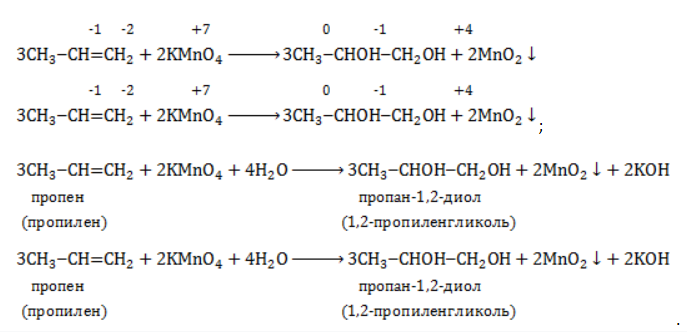
- расставить коэффициенты:
- ввести в уравнение недостающие реагенты и продукты, исходя из равенства состава в левой и правой частях уравнения, и определить окончательные коэффициенты:
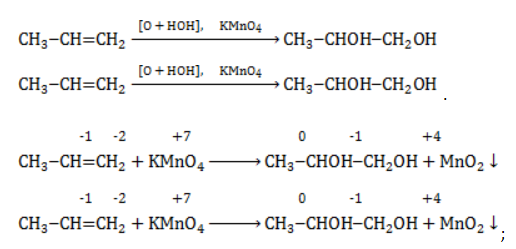
Реакция окисления пропена в нейтральной среде перманганатом калия составляется аналогично:
Дальше мягкое окисление не идет, так как 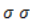
Жесткое окисление
Жесткими называют процессы окисления, протекающие в нейтральном растворе в условиях повышенной температуры, а также при добавлении кислоты или щелочи. В этих случаях двойная связь в алкене разрушается полностью, а продуктами реакции становятся кетоны, кислоты (с промежуточным окислением до альдегида) либо соли.
Окисление перманганатом калия в кислой среде
Пропен в содержащем кислоту растворе 

Степени окисления участвующих в реакции углеродных атомов и марганца составят:
Электронный баланс определяется только с учетом углерода, вошедшего в состав кислоты:
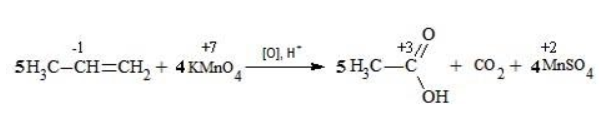
Сначала расставляются коэффициенты в окислителе, восстановителе и в продуктах окисления:
Затем вписываются недостающие вещества и полностью рассчитываются коэффициенты:
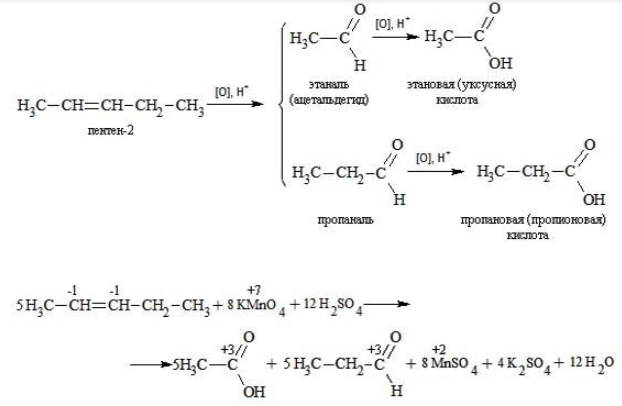
Еще один пример жесткого окисления алкенов перманганатом калия с серной кислотой – реакция с участием пентена-2. Молекула расщепляется по месту двойной связи, и ее фрагменты окисляются через промежуточное образование альдегидов до двух кислот:
Электронный баланс составляется для двух углеродных атомов алкена, поскольку оба они являются восстановителями.
Правило, по которому осуществляется окисление углерода, отражено в таблице:
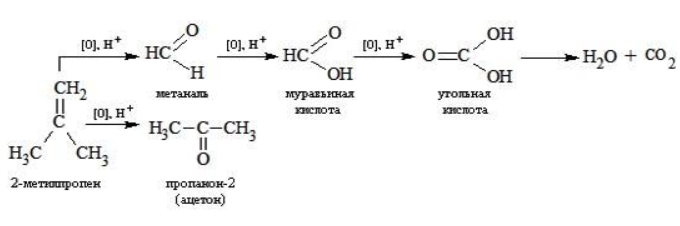
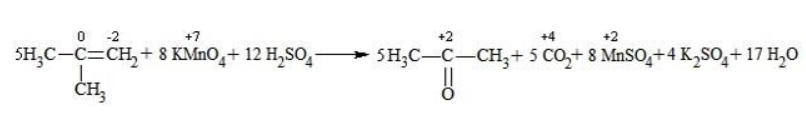
Так, в 2-метилпропене первичный атом окисляется через промежуточные формальдегид (метаналь) и муравьиную кислоту полностью – до углекислого газа, а третичный – только до ацетона:
Окисление алкенов в щелочной среде
При нагревании с концентрированной щелочью алкены окисляются до солей:
Если один из углеродных атомов – первичный, он окисляется до углекислого газа:
Окисление в нейтральном растворе
В условиях высокой температуры образующаяся щелочь вступает в реакцию, в результате которой окисление алкенов продолжается до образования кетонов или солей. Так, при жестком окислении пропена в нейтральной среде получаются те же продукты, что и в присутствии концентрированного гидроксида калия: ацетат 




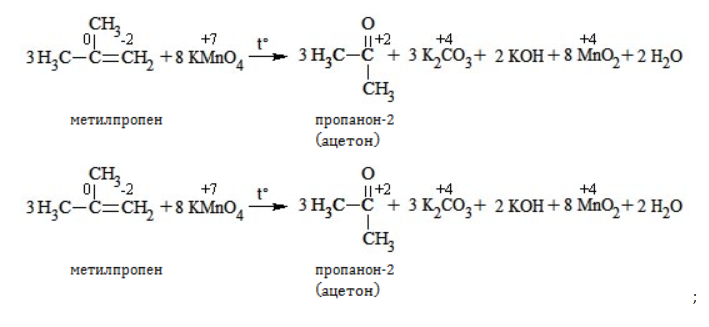
Кетон – результат окисления третичного углеродного атома, и дальнейшую реакцию они не поддерживают. Например, при окислении метилпропена как конечный продукт образуется ацетон:
Заключение
Взаимодействие с раствором перманганата калия в мягких или жестких условиях является показателем высокой реакционной способности алкенов, которая обусловлена присутствием в молекуле легко разрываемой -связи. Реакции мягкого и жесткого окисления относятся к числу характерных химических свойств алкенов как ненасыщенных углеводородов.
Составление уравнений окислительно-восстановительных реакций с участием органических веществ
В связи с введением в качестве единственной формы итоговой аттестации выпускников средней школы единого государственного экзамена (ЕГЭ) и переходом старшей школы на профильное обучение все большую актуальность приобретает подготовка старшеклассников к выполнению наиболее “дорогих” в балльном отношении заданий части “С” теста ЕГЭ по химии. Несмотря на то, что пять заданий части “С” считаются разными: химические свойства неорганических веществ, цепочки превращений органических соединений, расчетные задачи, – все они в той или иной мере связаны именно с окислительно-восстановительными реакциями (ОВР). Если усвоены основные знания теории ОВР, то можно правильно выполнить первое и второе задания полностью, а третье – частично. На наш взгляд, значительная часть успеха при выполнении части “С” заключается именно в этом. Опыт показывает, что если, изучая неорганическую химию, ученики достаточно хорошо справляются с заданиями по написанию уравнений ОВР, то аналогичные задания по органической химии вызывают у них большие трудности. Поэтому на протяжении изучения всего курса органической химии в профильных классах мы стараемся сформировать у старшеклассников навыки составления уравнений ОВР.
При изучении сравнительной характеристики неорганических и органических соединений мы знакомим учащихся с использованием степени окисления (с.о.) (в органической химии прежде всего углерода) и способами ее определения:
1) вычисление средней с.о. углерода в молекуле органического вещества;
2) определение с.о. каждого атома углерода.
Уточняем, в каких случаях лучше использовать тот или иной способ.
Статья опубликована при поддержке компании «ГЕО-Инжиниринг», представляющей на рынке продукцию под брендом «ProfKresla». Сфера деятельности компании — производство, продажа и установка кресел и стульев для различных залов. Высокий профессионализм сотрудников и собственные производственные мощности позволяют быстро и качественно реализовывать проекты любой степени сложности. Всю продукцию под брендом «ProfKresla», будь тоТеатральные кресла, сидения для залов ожидания или стулья для учебных заведений, отличают современный и эргономичный дизайн, а также высокая износостойкость, прочность и комфорт. Из огромного ассортимента продукции, представленного в каталоге на сайте profkresla.ru, Вы всегда сможете подобрать модели, наилучшим образом соответствующие корпоративному стилю, принятому в Вашей компании. Если же у Вас все-таки возникнут трудности с выбором, то специалисты компании всегда готовы дать консультацию, помочь определиться с моделью, после чего подготовить проект, на месте произвести все необходимые замеры и установку.
При изучении темы “Алканы” показываем, что процессы окисления, горения, галогенирования, нитрования, дегидрирования, разложения относятся к окислительно-восстановительным процессам. При написании уравнений реакций горения и разложения органических веществ лучше использовать среднее значение с.о. углерода. Например:
Обращаем внимание на первую половину электронного баланса: у атома углерода в дробном значении с.о. знаменатель равен 4, поэтому расчет передачи электронов ведем по этому коэффициенту.
В остальных случаях при изучении темы “Алканы” определяем значения с.о. каждого атома углерода в соединении, обращая при этом внимание учащихся на последовательность замещения атомов водорода у первичных, вторичных, третичных атомов углерода:
Таким образом мы подводим учащихся к выводу, что в начале протекает процесс замещения у третичных, затем – у вторичных, и, в последнюю очередь – у первичных атомов углерода.
При изучении темы “Алкены” рассматриваем процессы окисления в зависимости от строения алкена и среды протекания реакции.
При окислении алкенов концентрированным раствором перманганата калия KMnO4 в кислой среде (жесткое окисление) происходит разрыв 

Если двойная связь находится на конце молекулы (например, у бутена-1), то одним из продуктов окисления является муравьиная кислота, легко окисляющаяся до углекислого газа и воды:
Подчеркиваем, что если в молекуле алкена атом углерода при двойной связи содержит два углеродных заместителя (например, в молекуле 2-метилбутена-2), то при его окислении происходит образование кетона, т. к. превращение такого атома в атом карбоксильной группы невозможно без разрыва C–C-связи, относительно устойчивой в этих условиях:
Уточняем, что если молекула алкена симметрична и двойная связь содержится в середине молекулы, то при окислении образуется только одна кислота:
Сообщаем, что особенностью окисления алкенов, в которых атомы углерода при двойной связи содержат по два углеродных радикала, является образование двух кетонов:
Рассматривая окисление алкенов в нейтральной или слабощелочной средах, акцентируем внимание старшеклассников на том, что в таких условиях окисление сопровождается образованием диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам углерода, между которыми существовала двойная связь:
В аналогичном плане рассматриваем окисление ацетилена и его гомологов в зависимости от того, в какой среде протекает процесс. Так, уточняем, что в кислой среде процесс окисления сопровождается образованием карбоновых кислот:
Реакция используется для определения строения алкинов по продуктам окисления:
В нейтральной и слабощелочной средах окисление ацетилена сопровождается образованием соответствующих оксалатов (солей щавелевой кислоты), а окисление гомологов – разрывом тройной связи и образованием солей карбоновых кислот:
Все правила отрабатываются с учащимися на конкретных примерах, что приводит к лучшему усвоению ими теоретического материала. Поэтому при изучении окисления аренов в различных средах ученики могут самостоятельно высказать предположения, что в кислой среде следует ожидать образования кислот, а в щелочной – солей. Учителю останется только уточнить, какие продукты реакции образуются в зависимости от строения соответствующего арена.
Показываем на примерах, что гомологи бензола с одной боковой цепью (независимо от ее длины) окисляются сильным окислителем до бензойной кислоты по 
Подчеркиваем, что если в молекуле арена несколько боковых цепей, то в кислой среде каждая из них окисляется по a-углеродному атому до карбоксильной группы, в результате чего образуются многоосновные ароматические кислоты:
Полученные навыки составления уравнений ОВР для углеводородов позволяют использовать их при изучении раздела “Кислородсодержащие соединения”.
Так, при изучении темы “Спирты” учащиеся самостоятельно составляют уравнения окисления спиртов, используя следующие правила:
1) первичные спирты окисляются до альдегидов
2) вторичные спирты окисляются до кетонов
3) для третичных спиртов реакция окисления не характерна.
В целях подготовки к ЕГЭ учителю целесообразно дать дополнительные сведения к указанным свойствам, что, несомненно, будет полезным для учащихся.
При окислении метанола подкисленным раствором перманганата калия или дихромата калия образуется CO2, первичные спирты при окислении в зависимости от условий протекания реакции могут образовать не только альдегиды, но и кислоты. Например, окисление этанола дихроматом калия на холоду заканчивается oбразованием уксусной кислоты, а при нагревании – ацетальдегида:
3CH3–CH2OH + K2Cr2O7 + 4H2SO4 
Вновь напомним учащимся о влиянии среды на продукты реакций окисления спиртов, а именно: горячий нейтральный раствор KMnO4 окисляет метанол до карбоната калия, а остальные спирты – до солей соответствующих карбоновых кислот:
При изучении темы “Альдегиды и кетоны” акцентируем внимание учащихся на том, что альдегиды легче, чем спирты, окисляются в соответствующие карбоновые кислоты не только под действием сильных окислителей (кислород воздуха, подкисленные растворы KMnO4 и K2Cr2O7), но и под действием слабых (аммиачный раствор оксида серебра или гидроксида меди(II)):
CH3–CHO + 2[Ag(NH3)2]OH 
Особое внимание уделяем окислению метаналя аммиачным раствором оксида серебра, т.к. в этом случае образуется карбонат аммония, а не муравьиная кислота:
Как показывает наш многолетний опыт, предложенная методика обучения старшеклассников составлению уравнений ОВР с участием органических веществ повышает их итоговый результат ЕГЭ по химии на несколько баллов.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. |


 углерод, обладающий большей электроотрицательностью, смещает к себе электронные пары двух связей
углерод, обладающий большей электроотрицательностью, смещает к себе электронные пары двух связей