Решение задач. 10-й класс. Базовый курс
Предлагаемые два варианта заданий можно использовать при проведении урока с элементами коллективного и индивидуального соревнований, а также для зачетов. На уроке я делю класс на две команды. Вначале каждый участник пытается решить посильное самостоятельно, затем под руководством капитанов – в группе. Разрешается совещаться и обращаться с вопросами ко мне. В конце урока за индивидуальную работу ставится оценка (зачет).
1. Баллон емкостью 0,0831 м 3 содержит 1,6 кг кислорода. При какой температуре баллон может разорваться, если он выдерживает давление 2 • 10 6 Па?
2. Баллон, наполненный газом под давлением 2,84 МПа, находился на складе при температуре 7 °С. После того как половину газа израсходовали, баллон внесли в помещение. Какова температура в помещении, если давление газа в баллоне через некоторое время стало 1,52 МПа?
4. Определите молярную массу углекислого газа.
5. Прибор для измерения давления газа
6. Почему нагретая медицинская банка «присасывается» к телу человека?
7. Найдите ошибки:
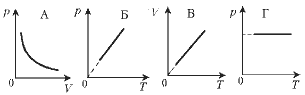
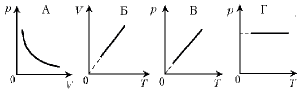
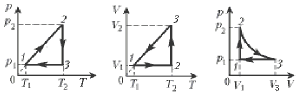
8. Какой график отражает закон Шарля?
9. Выразите величину V и проверьте правильность полученных единиц ее измерения:
V = 0,0831 м 3 ,
m = 1,6 кг,
M(O2) = 32 • 10 –3 кг/моль,
p = 2 • 10 6 Па.
_______________
T – ?
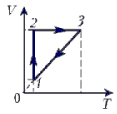
3. 1–2 – изотермический (расширение); 2–3 – изохорный (нагревание); 3–1 – изобарный (сжатие).
4. M(CO2) = (12 + 32) • 10 –3 = 44 • 10 –3 (кг/моль).
6. При нагревании воздуха в банке часть его выходит, так что при охлаждении давление в банке становится меньше атмосферного.
1. Определите массу углекислого газа, находящегося в баллоне емкостью 5 • 10 –2 м 3 при температуре 300 К. Давление газа 3 • 10 6 Па.
2. В сварочном цехе стоит 50 баллонов ацетилена (С2Н2) емкостью 40 л каждый. Все баллоны включены в общую магистраль. После 10 ч непрерывной работы давление во всех баллонах упало с 1,2 • 10 6 до 5 • 10 5 Па. Найдите средний расход ацетилена за секунду, если температура в цехе оставалась неизменной и равнялась 27 °С.
4. Определите молярную массу серной кислоты (H2SO4).
5. Прибор для измерения параметра состояния термодинамической системы.
6. Почему у глубоководных рыб плавательный пузырь выходит через рот наружу, если их извлечь из воды?
7. Найдите ошибки:
8. Какой график отражает закон Гей-Люссака?
9. Выразите величину р и проверьте правильность получаемых единиц ее измерения:
V = 5 • 10 –2 м 3 ,
T = 300 К,
p = 3 • 10 6 Па,
M(СО2) = 44 • 10 –3 кг/моль.
_________________
m – ?
M(C2H2) = 26 • 10 –3 кг/моль,
N = 50,
V1 = 40 л, СИ: 0,04 м 3
t = 10 ч, СИ: 36 • 10 3 с
p1 = 1,2 • 10 6 Па,
p2 = 5 • 10 5 Па,
t = 27 °С. СИ: T = 300 К
_____________


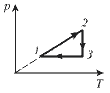
3. 1–2 – изохорный (нагревание); 2–3 – изотермический (расширение); 3–1 – изобарный (сжатие).
6. Давление на большой глубине намного превышает атмосферное, поэтому плавательный пузырь при подъеме рыбы значительно увеличивается в объеме.
7.
Решение задач по теме «Уравнение состояния идеального газа»
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Рабочие листы и материалы для учителей и воспитателей
Более 2 500 дидактических материалов для школьного и домашнего обучения
Столичный центр образовательных технологий г. Москва
Получите квалификацию учитель математики за 2 месяца
от 3 170 руб. 1900 руб.
Количество часов 300 ч. / 600 ч.
Успеть записаться со скидкой
Форма обучения дистанционная
311 лекций для учителей,
воспитателей и психологовПолучите свидетельство
о просмотре прямо сейчас!ТЕМА: Решение задач по теме «Уравнение состояния идеального газа»
Учебная: Диагностика степени усвоения знаний по теме «Уравнение состояния идеального газа» и формирование практических умений по их применению .
Развивающая: Развивать интерес к физике, развивать практические умения учащихся при решении задач.
Воспитательная : воспитывать сознательное отношение к учебе и заинтересованность в изучении физики.
Тип урока: урок комплексного применения знаний
I. Организационно — мотивационный этап
1) Организация начала урока
2) Проверка домашнего задания
II. Организационно — мотивационный этап
3) Актуализация имеющихся знаний.
4) Закрепление знаний и способов действия
6) Первоначальная проверка понимания
III. Рефлексийна — заключальны этап
7) Подведение итогов занятия. Выставление оценок
8) Домашнее задание
I. Организационно — мотивационный этап
1) Организация начала урока
Приветствие учащихся и учителя. Проверить подготовленность учащихся к уроку, правильную организацию рабочего места. Отметить отсутствующих в журнале.
2) Проверка домашнего задания
Фронтальная проверка выполнения домашнего задания. Обсуждения результатов выполнения
II. Операционно — познавательный этап.
3) Актуализация имеющихся знаний.
А) Фронтальный опрос
— Перечислите макроскопические параметры состояния идеального газа ( Р,V,Т)
— Какое уравнение называют уравнением состояния? (Уравнение, выражающее связь между макроскопическими параметрами состояния вещества)
-В чем заключается основная задача МКТ? ( Установление связи между макроскопическими параметрами, т.е. нахождение уравнения состояния того или иного тела)
-Сформулировать и доказать закон Дальтона (Давление смеси химически не взаимодействующих идеальных газов равно сумме парциальных давлений этих газов, p=p1 +…рn )
-Записать уравнение Клапейрона. При каких условиях оно справедливо? (PVT=P0V0\T0, m=const, M=const)
— Записать уравнение Менделеева — Клапейрона.
4) Закрепление знаний и способов действия
Задачи решаются на доске:
1. Определить массу водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если температура газа равна 17 °С.
Дано: V = 20 л, р = 830 кПа, t = 17 ° C , М = 2·10-3 кг/моль, R = 8,31 Дж/(моль·К).
Решение
Выведем размерность искомой физической величины:
Ответ: m = 1,38·10 -2 кг.
2 . Газ при давлении 0,2 МПа и температуре 15 0 С имеет объем 5 л. Чему будет равен объем этой массы газа при нормальных условиях?
3. В баллоне находится газ под давлением 40 Па и при температуре 27 °С. Когда из баллона выпустили 3/5 газа, содержавшегося в нем, его температура понизилась до -33 °С. Определить давление газа, оставшегося в сосуде.
Дано: V — const , р1 = 40 МПа, t 1 = 27 °С, t 2 = -33 °С, m 2 = 2/5 m 1
Решение
Ответ: р2 = 12,8 Па.
4. При уменьшении объема газа в 2 раза давление увеличилось на 120 кПа, а абсолютная температура возросла на 10 %. Каким было первоначальное давление?
6) Первоначальная проверка понимания
Задачи решаются самостоятельно учениками
1. Определите температуру кислорода массой 64 г, находящегося в сосуде объёмом 1 л при давлении 5 • 10 6 Па. Молярная масса кислорода М = 0,032 кг/моль.
Р е ш е н и е. Согласно уравнению Менделеева—Клапейрона
Отсюда температура
кислорода.
2. Найти плотность водорода при температуре 15 0 С и давлении 9,8·10 4 Па. (0,085 кг/м 3 )
3. В баллоне находится газ при температуре 15 0 С. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8 0 С?
( Ответы : m=16 кг ; Р =249300 Па ; V=0,03 м 3; Т =150 К )
III. Рефлексийно – заключительный этап
7) Подведение итогов занятия. Выставление оценок
8) Домашнее задание упр.3(5-7). Подготовится к проверочной работе
9) Рефлексия: Ребята высказываются одним предложением, выбирая начало фразы из рефлексивного экрана на доске: Сегодня я узнал… Было интересно… Было трудно… Я понял, что…
Решение задач по теме «Уравнение состояния идеального газа»
1. Определить массу водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если температура газа равна 17 °С.
2 . Газ при давлении 0,2 МПа и температуре 15 0 С имеет объем 5 л. Чему будет равен объем этой массы газа при нормальных условиях?
3. В баллоне находится газ под давлением 40 Па и при температуре 27 °С. Когда из баллона выпустили 3/5 газа, содержавшегося в нем, его температура понизилась до -33 °С. Определить давление газа, оставшегося в сосуде.
4. При уменьшении объема газа в 2 раза давление увеличилось на 120 кПа, а абсолютная температура возросла на 10 %. Каким было первоначальное давление?
1. Определите температуру кислорода массой 64 г, находящегося в сосуде объёмом 1 л при давлении 5 • 10 6 Па. Молярная масса кислорода М = 0,032 кг/моль.
2. Найти плотность водорода при температуре 15 0 С и давлении 9,8·10 4 Па. (0,085 кг/м 3 )
3. В баллоне находится газ при температуре 15 0 С. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8 0 С?
Решение задач по теме «Уравнение состояния идеального газа»
1. Определить массу водорода, находящегося в баллоне вместимостью 20 л при давлении 830 кПа, если температура газа равна 17 °С.
2 . Газ при давлении 0,2 МПа и температуре 15 0 С имеет объем 5 л. Чему будет равен объем этой массы газа при нормальных условиях?
3. В баллоне находится газ под давлением 40 Па и при температуре 27 °С. Когда из баллона выпустили 3/5 газа, содержавшегося в нем, его температура понизилась до -33 °С. Определить давление газа, оставшегося в сосуде.
4. При уменьшении объема газа в 2 раза давление увеличилось на 120 кПа, а абсолютная температура возросла на 10 %. Каким было первоначальное давление?
1. Определите температуру кислорода массой 64 г, находящегося в сосуде объёмом 1 л при давлении 5 • 10 6 Па. Молярная масса кислорода М = 0,032 кг/моль.
2. Найти плотность водорода при температуре 15 0 С и давлении 9,8·10 4 Па. (0,085 кг/м 3 )
3. В баллоне находится газ при температуре 15 0 С. Во сколько раз уменьшится давление газа, если 40 % его выйдет из баллона, а температура при этом понизится на 8 0 С?
Примеры решения задач по теме уравнение состояния идеального газа 10 класс
Репетитор
по физикеРепетитор
по алгебре( P ) — Давление газа (Паскали)
( nu ) — Количество вещества
( R ) — Универсальная газовая посиоянная
( T ) — Температура в Кельвинах
В баллоне находится газ под давлением (P= 8,31 cdot 10^6 ; Па ), температура газа (T=300 К ).
Количество вещества газа ( nu=100 Моль ).
Найти объем баллона
Универсальная газовая постоянная ( R=8,31 frac )
Дать ответ в литрах.
Показать ответ Показать решение ВидеорешениеЗапишем уравнение Менделеева-Клапейрона :
Задачи на газовые законы
методическая разработка по физике (10 класс) на тему
В данной работе предлагается определенный подход к классификации и способам решения задач на газовые законы. Такой подход позволит быстро сориентироваться в большом количестве задач на свойства газов и применить к ним те или иные приемы решения.
Скачать:
Вложение Размер algoritmy_resheniya_zadach_po_mkt.docx 213.89 КБ Предварительный просмотр:
В данной работе предлагается определенный подход к классификации и способам решения задач на газовые законы. Такой подход позволит быстро сориентироваться в большом количестве задач на свойства газов и применить к ним те или иные приемы решения.
Основные теоретические сведения
Состояние газа характеризуется совокупностью трех физических величин или термодинамических параметров: объемом газа V, давлением Р и температурой Т. Состояние газа, при котором эти параметры остаются постоянными считают равновесным состоянием. В этом состоянии параметры газа связаны между собой уравнением состояния. Самый простой вид уравнение состояния имеет для идеального газа. Идеальным газом называют газ, молекулы которого не имеют размеров (материальные точки) и взаимодействуют друг с другом лишь при абсолютно упругих соударениях (отсутствует межмолекулярное притяжение и отталкивание). Реальные газы тем точнее подчиняются законам идеальных газов, чем меньше размеры их молекул (т.е. газ одноатомный), и чем больше он разряжен.
Уравнение состояния идеального газа или уравнение Менделеева-Клапейрона имеет вид:
— универсальная газовая постоянная
Из этого закона вытекает, что для двух произвольных состояний газа справедливо равенство, называемое уравнением Клапейрона:
Так же для идеальных газов имеют место следующие экспериментальные законы:
Закон Бойля — Мариотта :
Если в сосуде находится смесь нескольких газов, не вступающих друг с другом в химические реакции, то результирующее давление определяется по закону Дальтона: давление смеси равно сумме давлений, производимых каждым газом в отдельности, как если бы он один занимал весь сосуд.
Р = Р 1 + Р 2 +. + Р N
Задачи, решение которых основывается на данных уравнениях, можно разделить на две группы:
- задачи на применение уравнения Менделеева-Клапейрона.
- задачи на газовые законы.
ЗАДАЧИ НА ПРИМЕНЕНИЕ УРАВНЕНИЯ МЕНДЕЛЕЕВА-КЛАПЕЙРОНА.
Уравнение Менделеева-Клапейрона применяют тогда, когда
- дано только одно состояние газа и задана масса газа (или вместо массы используют количество вещества или плотность газа).
- масса газа не задана, но она меняется, то есть утечка газа или накачка.
При решении задач на применение равнения состояния идеального газа надо помнить:
- если дана смесь газов, то уравнение Менделеева-Клапейрона записывают для каждого компонента в отдельности. Связь между парциальными давлениями газов, входящих в смесь и результирующим давлением смеси, устанавливается законом Дальтона.
- если газ меняет свои термодинамические параметры или массу, уравнение Менделеева-Клапейрона записывают для каждого состояния газа в отдельности и полученную систему уравнений решают относительно искомой величины.
- Необходимо пользоваться только абсолютной температурой и сразу же переводить значения температуры по шкале Цельсия в значения по шкале Кельвина.
- В задачах, где рассматривается движение сосуда с газом (пузырька воздуха, воздушного шара) к уравнению газового состояния добавляют уравнения механики.
- если между газами происходит реакция, то надо составить уравнение реакции и определить продукты реакции
ПЕРВЫЙ ТИП ЗАДАЧ: НЕТ ИЗМЕНЕНИЯ МАССЫ
- Определить давление кислорода в баллоне объемом V = 1 м 3 при температуре t=27 °С. Масса кислорода m = 0,2 кг .
Записываем уравнение Менделеева-Клапейрона и находим из него давление, производимое газом:
- Баллон емкостью V= 12 л содержит углекислый газ. Давление газа Р = 1 МПа, температура Т = 300 К. Определить массу газа.
Записываем уравнение Менделеева-Клапейрона и находим массу газа
- При температуре Т = 309 К и давлении Р = 0,7 МПа плотность газа ρ = 12 кг/м 3 . Определить молярную массу газа.
Записываем уравнение Менделеева-Клапейрона
Так как масса газа может быть определена через плотность газа и его объем имеем:
Отсюда находим молярную массу газа:
- Какова плотность водорода при нормальном атмосферном давлении и температуре 20°С.
Нормальное атмосферное давление – это давление, равное 10 5 Па. И эту информацию запишем как данные задачи. Записываем уравнение Менделеева-Клапейрона
Так как масса газа может быть определена через плотность газа и его объем имеем:
Отсюда находим плотность газа:
- До какой температуры Т 1 надо нагреть кислород, чтобы его плотность стала равна плотности водорода при том же давлении ,но при температуре Т 2 = 200 К?
Записываем уравнение Менделеева-Клапейрона для кислорода и для водорода через плотности газов:
Так как по условию давление у двух газов одинаковое, то можно приравнять правые части данных уравнений:
Сократим на R и на плотность ρ (по условию плотности газов равны) и найдем Т 1
- В сосуде объемом 4·10 -3 м 3 находится 0,012 кг газа при температуре 177°С. При какой температуре плотность этого газа будет равна 6·10 -6 кг /см 3 , если давление газа остается неизменным.
ρ 2 =6·10 -6 кг /см 3
- В баллоне объемом 25 литров находится 20 г азота и 2 г гелия при 301К. Найдите давление в баллоне.
μ 1 = 0,028кг/моль
μ 2 = 0,004кг/моль
Записываем уравнение Менделеева для каждого газа и находим из него давление газов
По закону Дальтона результирующее давление в сосуде равно сумме парциальных давлений газов:
- Определить плотность смеси, состоящей из 4 граммов водорода и 32 граммов кислорода при давлении 7°С и давлении 93кПа?
μ 1 = 0,002кг/моль
μ 2 = 0,032кг/моль
По закону Дальтона:
- Сосуд емкостью 2V разделен пополам полупроницаемой перегородкой. В одной половине находится водород массой m В и азот массой m А . В другой половине вакуум. Во время процесса поддерживается постоянная температура Т. Через перегородку может диффундировать только водород. Какое давление установиться в обеих частях сосуда?
m 1 = m 2 = m 3 = m
Диффундирует только водород. Следовательно, после завершения установочных процессов, в отсеке I будет водород, массой на
половину меньшей, чем была, и весь азот. А во втором отсеке только половина массы водорода. Тогда для первого отсека установившееся давление равно:
Для отсека II можно так же определить установившееся давление:
- Вакуумированный сосуд разделен перегородками на три равных отсека, каждый объемом V. В средний отсек ввели одинаковые массы кислорода, азота и водорода. В результате чего давление в этом отсеке стало равно Р. Перегородка I проницаема только для молекул водорода, перегородка II проницаема для молекул всех газов. Найти давления Р 1 Р 2 и Р 3 , установившиеся в каждом отсеке, если температура газа поддерживается постоянной и равной Т.
m 1 = m 2 = m 3 = m
После диффундирования газов через перегородки в первом отсеке окажется треть массы водорода. Во втором и в третьем отсеках будет треть водорода, половина массы кислорода и половина всей массы азота. Тогда для первого отсека установившееся давление равно:
Если до диффундирования первоначальное давление во втором отсеке было Р, то можно записать:
Отсюда можно найти
Находим выражение для давления во втором и в третьем отсеках
И тогда давление в первом отсеке равно:
С химическими реакциями
- В сосуде находится смесь азота и водорода. При температуре Т, когда азот полностью диссоциирован на атомы, давление равно Р (диссоциацией водорода можно пренебречь). При температуре 2Т, когда оба газа полностью диссоциированы, давление в сосуде 3Р. Каково отношение масс азота и водорода в смеси?
При температуре Т параметры газов в сосуде следующие:
И результирующее давление в сосуде по закону Дальтона равно:
При температуре 2Т параметры газов в сосуде следующие:
И результирующее давление в сосуде по закону Дальтона равно:
- В герметично закрытом сосуде находится 1 моль неона и 2 моля водорода. При температуре Т 1 =300К, когда весь водород молекулярный, атмосферное давление в сосуде Р 1 =10 5 Па. При температуре Т 2 =3000К давление возросло до Р 2 =1,5∙10 5 Па. Какая часть молекул водорода диссоциировала на атомы?
При температуре Т 1 давление газа в сосуде складывается из парциальных давлений двух газов и равно:
При температуре Т 2 давление газа равно:
Из первого находим объем V:
- В закрытом баллоне находится смесь из m 1 = 0,50 г водорода и m 2 = 8,0 г кислорода при давлении Р 1 = 2,35∙10 5 Па. Между газами происходит реакция с образованием водяного пара. Какое давление Р установится в баллоне после охлаждения до первоначальной температуры? Конденсации пара не происходит.
В сосуде будет происходить реакция водорода с кислородом с образованием воды:
Из уравнения реакции видно, что если в реакцию вступит весь водород, то кислорода только половина
В результате образуется ν 3 =0,25 молей водяного пара и останется ν 4 = 0,125молей кислорода.
По закону Дальтона результирующее давление в сосуде равно сумме парциальных давлений
Так как известно, что до реакции давление в сосуде было Р 1 , то для этого момента можно так же применить закон Дальтона:
Решаем полученные уравнение в системе относительно неизвестного:
С добавлением законов механики.
- На дне сосуда, заполненного воздухом, лежит шарик радиусом r и массой m. До какого давления надо сжать воздух в сосуде, чтобы шарик поднялся вверх. Температура воздуха Т известна.
Запишем уравнение динамики и уравнение Менделеева-Клапейрона. Решаем полученную систему уравнений относительно неизвестного:
- Тонкостенный резиновый шар массой 50г наполнен азотом и погружен в озеро на глубину 100 м. Найти массу азота, если шар находится в положении равновесия. Атмосферное давление 760мм. рт. ст. Температура воды в озере на глубине 100м равна 4°С.
Запишем второй закон Ньютона в проекции на вертикальную ось.
Объем шара равен объему азота в нем. Запишем уравнение Менделеева-Клапейрона для азота и выразим из него объем азота
Давление азота на этой глубине равно давлению внешнему на шар, так как по условию оболочка шара не пульсирует. Следовательно:
- Надувной шарик, заполненный гелием, удерживают на нити. Найдите натяжение нити, если масса оболочки шарика 2г, объем 3литра, давление гелия 10 5 Па, температура 27°С. Плотность воздуха 1,3 кг/м 3
μ гел =0,004кг/моль
μ воз =0,029 кг/моль
Запишем второй закон Ньютона в проекции на вертикальную ось х.
Объем шара равен объему гелия в нем, а значит 3литра; Запишем уравнение Менделеева-Клапейрона для воздуха (среда, в которой находится шар), и введем в него плотность воздуха:
Тогда уравнение (1) принимает вид:
Теперь надо записать уравнение Менделеева-Клапейрона для гелия и выразить из него массу гелия. Надо учесть, что объем азота равен объему шара. А так же температура окружающего воздуха и температура гелия равны, как равны и давления воздуха и гелия.
С учетом определенной массы гелия, сила натяжения равна:
- В вертикально расположенном цилиндре находится кислород массой m = 64 г, отделенный от атмосферы поршнем, который соединен с дном цилиндра пружиной жесткостью k = 830 H/м. При температуре T 1 = 300 К поршень располагается на расстоянии h = 1 м от дна цилиндра. До какой температуры T 2 надо нагреть кислород, чтобы поршень расположился на высоте H = 1,5м от дна цилиндра? Универсальная газовая постоянная R= 8,31 Дж/(моль∙ К), молярная масса кислорода μ = 32 г/моль.
Поскольку в условии задачи не сказано, что поршень невесом, будем полагать, что он обладает некоторой массой, которую обозначим через m 0 . Ничего не говорится также про атмосферное давление, поэтому будем считать, что оно равно Р 0 Таким образом, на поршень действуют в общем случае четыре силы: сила тяжести, сила упругости пружины, сила атмосферного давления, направленные вниз, и сила давления газа в цилиндре, направленная вверх. Условия равновесия поршня в начальном и конечном состояниях имеют вид:
Здесь через Р 1 и через Р 2 обозначено давление газа в первом и во втором состояниях. Через х 1 и х 2 обозначена деформация пружины в двух состояниях.
Вычтем из второго уравнения первое уравнение:
Запишем уравнение Менделеева-Клапейрона для двух состояний газа:
Приравняем разности давлений газа, найденные двумя способами:
Из полученного уравнения находим Т 2 :
ВТОРОЙ ТИП ЗАДАЧ: ЕСТЬ ИЗМЕНЕНИЯ МАССЫ
- Температуру воздуха в комнате подняли с t 1 = 7 °С до t 2 = 27 °С. Какая масса воздуха должна выйти из комнаты, чтобы давление осталось неизменным, Р = 10 5 Па? Объем воздуха в комнате V = 50 м 3 .
Так как при нагревании все тела расширяются, а комната не герметична, следовательно, масса воздуха в комнате при нагревании уменьшается (есть утечка газа), но при этом, понятно, что объем газа не меняется и остается равным объему комнаты. Для каждого состояния газа запишем уравнение Менделеева-Клапейрона, и определим из них массу воздуха в комнате при разной температуре.
- Стеклянная колба закрыта пробкой и взвешена при температуре t 1 = 15 °С. Открыв пробку, колбу нагрели до температуры t 2 = 80 °С. При следующем взвешивании масса колбы оказалась на m = 0,25 г меньше. Чему равен объем колбы?
Масса стеклянной колбы не меняется, меняется масса газа в ней, так как есть утечка: при нагревании все тела расширяются, а колба не герметична, следовательно, масса воздуха в ней при нагревании уменьшается, но при этом, понятно, что объем газа не меняется и остается равным объему колбы. Будем считать, что атмосферное давление нормальное.
Для каждого состояния газа запишем уравнение Менделеева-Клапейрона, и определим из них массу воздуха в колбе при разной температуре.
Выразим отсюда объем колбы:
- В баллоне емкостью V = 12 л находится азот массой m 1 = 1,5 кг при температуре t 1 = 37°С. Каким станет давление в баллоне при температуре t 2 =50 °С, если выпустить 35% азота? Первоначальное давление считать нормальным.
Для каждого состояния газа запишем уравнение Менделеева-Клапейрона.
- В сосуде объемом V = 1 л находится идеальный газ. В сосуде объемом V = 1 л находится идеальный газ. Сколько молекул газа нужно выпустить из сосуда, чтобы при понижении температуры в k=2 раза его давление уменьшилось в z =4 раза?
Для каждого состояния газа запишем уравнение Менделеева-Клапейрона.
- Когда из сосуда выпустили некоторое количество газа, давление в нем упало на 40%, а абсолютная температура на 20%. Какую часть газа выпустили?
Для каждого состояния газа запишем уравнение Менделеева-Клапейрона.
- В сосуде объемом V = 0,5 л находится идеальный газ при давлении Р 1 =1 атм. и температуре t = 27 °С. Сколько молекул газа нужно выпустить из сосуда, чтобы давление в нем уменьшилось в 2 раза? Температура газа не изменяется.
Для каждого состояния газа запишем уравнение Менделеева-Клапейрона.
- В пустой сосуд объемом V нагнетают воздух при помощи поршневого насоса, объем цилиндра которого V 0 . Каким будет давление воздуха в сосуде после N качаний?
Задачи про насосы решаются так же на основе уравнения Менделеева-Клапейрона. Надо записать уравнение для накаченной массы, то есть той, что поступила в сосуд. И так же записать уравнение Менделеева-Клапейрона для газа, поступающего в рабочий резервуар насоса. И учесть, что вся масса газа, попавшая в сосуд – это масса газа, попадавшая в резервуар насоса N раз. Будем считать, что в насос газ поступает при атмосферном давлении
Запишем уравнение Менделеева-Клапейрона для газа, поступившего в цилиндр насоса:
Запишем уравнение Менделеева-Клапейрона для газа, поступившего в сосуд:
Поделим второе уравнение на первое:
- Компрессор засасывает из атмосферы каждую секунду 3 литра воздуха, которые подаются в баллон емкостью 45 литров. Через сколько времени давление в баллоне будет превышать атмосферное в 9 раз? Начальное давление в баллоне равно атмосферному.
Данная задача решается так же, как предыдущая, но с одним отличием: в баллоне уже был воздух при атмосферном давлении. Поэтому, записывая уравнение Менделеева-Клапейрона для накаченного воздуха, надо учесть, что создаваемое им давление превышает атмосферное в 8 раз.
Так как по условию задачи компрессор работает так, что ежесекундно засасывает воздух, то число секунд равно числу «засасываний»
Запишем уравнение Менделеева-Клапейрона для газа, поступившего в цилиндр компрессора:
Запишем уравнение Менделеева-Клапейрона для газа, поступившего в баллон:
Поделим второе уравнение на первое:
Время, потребовавшееся для такого накачивания, так же составляет 120с
Задачи на применение газовых законов .
Газовые законы применяют тогда, когда даны два состояния газа и при переходе газа из одного состояния в другое масса газа не меняется.
ГРАФИЧЕСКИЕ ЗАДАЧИ НА ГАЗОВЫЕ ЗАКОНЫ
- На диаграмме РT изображен цикл идеального газа постоянной массы. Изобразите его на диаграмме Р,V .
Проведем поэтапный анализ представленного цикла:
1–2: изохорический процесс; V – const; Р ↑ T ↑
2–3: изотермический процесс; V ↑ Р ↓ Т – const
3–1: изобарический процесс; V ↓ ; Р – const; T ↓
Теперь результаты поэтапного анализа перенесем на диаграмму РV ⇒
- Для постоянной массы идеального газа представлен цикл на диаграмме РV. Изобразить этот цикл на диаграмме VT.
- Изобразите на диаграмме РТ цикл постоянной массы идеального газа, представленный на диаграмме РV.
- Какая из двух линий графика соответствует большему давлению данной массы идеального газа?
Прежде всего установим, что это за линии. Эти линии выражают прямо пропорциональную зависимость между объемом газа и его температурой, а это возможно для идеального газа только при изобарическом процессе, следовательно, изображенные линии графика – изобары.
Проведем изотерму до пересечения с обеими изобарами, а точки их пересечения спроецируем на ось ординат (объемов). Из построения видно, что V 2 > V 1 . Поскольку при изотермическом процессе газ подчиняется закону Бойля–Мариотта: Р 1 V 1 = Р 2 V 2 , то Р 1 > Р 2 .
- При нагревании идеального газа постоянной массы получена зависимость Р(T) при переходе из состояния 1 в состояние 2. Как при этом переходе менялась плотность газа?
Прежде всего обратим внимание на то, что линия графика не описывается ни одним из изопроцессов («неявная форма»). Проведем через начальную и конечную точки линии графика две изохоры. Проведя еще изобару (или, как вариант, изотерму) и, спроецировав точки ее пересечения с изохорами на ось Т, убедимся, что Т 2 > Т 1 .
При изобарическом процессе, по закону Гей-Люссака, V
T, следовательно, V 2 > V 1 . А так как плотность и объем связаны обратной зависимостью (при данной массе), то ρ 1 > ρ 2 , откуда следует, что газ расширялся, а значит, его плотность уменьшилась.
- Как менялась температура постоянной идеального массы газа на протяжении цикла?
Точки 1 и 2 лежат на одной изотерме. Проведем изотермы через характерные точки 1, 2, 3 и касательную к участку 1–2. Как следует из теории, изотермы, более удаленные от координатных осей, соответствуют более высоким температурам. В этом можно убедиться, используя методы, предложенные в предыдущих задачах ⇒
- Идеальный газ с молярной массой М участвует в изотермическом процессе. При этом получена зависимость между объемом V и давлением р. Представьте этот цикл на диаграмме V, m.
Запишем уравнение Клапейрона–Менделеева:
По условию, T, M и R – постоянные, следовательно, m
Рассмотрим процессы цикла поэтапно:
1–2: T = const, V = const; m
2–3: T = const, р = const; m
3–4: T = const, V = const; m
4–1: T = const, р = const; m
Аналитические задачи на газовые законы
При решении аналитических задач на газовые законы надо:
- Убедиться, что при изменении состояния масса газа остается постоянной.
- Сделать схематический чертеж, на котором условно отметить состояния газа параметрами Р, V, Т. Записать закон Клапейрона для данных двух состояний.
- Если какой-либо параметр при переходе газа из одного состояния в другое остается неизменным (могут меняться все три параметра), то уравнение Клапейрона перевести в закон Бойля — Мариотта, Гей-Люссака или Шарля.
В случае, когда газ заключен в цилиндрический сосуд и объем газа меняется только за счет изменения высоты его столба h, уравнение Клапейрона можно сразу записывать в виде:
- Используя условия задачи, определить термодинамические параметры, выразив их через заданные величины. И если газ граничит с жидкостью, то особое внимание следует обратить на определение давления. Для его определения тех случаях, когда газ производит давление на жидкость, следует использовать закон Паскаля: провести нулевой уровень через границу, отделяющую газ от жидкости, и записать уравнение равновесия жидкости.
- Полученную систему уравнений решить относительно неизвестной величины.
- Если в задаче рассматривают состояния нескольких газов, отделенных друг от друга поршнями или входящих в состав смеси, то все указанные действия нужно проделать для каждого газа отдельно.
- В задачах на газовые законы используется только абсолютная температура.
- При увеличении абсолютной температуры газа в 2 раза давление увеличилось на 25%. во сколько раз изменился объем газа?
Запишем уравнение Клапейрона, так как меняются все три параметра идеального газа:
С учетом данных, уравнение принимает вид:
- Газ изотермически сжат от объема V 1 = 8 л до объема V 2 = 6 л. Давление при этом возросло на Δ Р = 4∙10 3 Па. Определить первоначальное давление.
Запишем уравнение Клапейрона и, так как процесс изотермический, переведем его в закон Бойля-Мариотта
Поэтому можно записать:
Отсюда находим первоначальное давление:
И объемы газов можно оставить в литрах, не переводить в систему СИ.
- При нагревании газа при постоянном давлении на 1К его объем увеличился на 5% от первоначального. При какой температуре находился газ?
- Сколько ртути войдет в стеклянный баллончик объемом V 0 , нагретый до Т 0 , если плотность ртути при температуре Т равна ρ.
- Закрытый с обоих концов цилиндрический сосуд разделен на две равные части теплонепроницаемым поршнем. Длина каждой части 42см. В обеих половинках находится одинаковое количество азота при температуре 27°С и давлении 1 атмосфера. На сколько надо нагреть газ в одной части сосуда, чтобы поршень переместился на 2 см?
Для газа в отделе I:
Для газа в отделе II:
- Объем баллона, содержащего газ под давлением 1,2·10 5 Па составляет 6 литров. Каким станет давление газа, если этот баллон соединить с другим баллоном объем которого 10 литров и он практически не содержит газа.
- Два одинаковых стеклянных шара соединены трубкой. При 0° С капелька ртути находится посередине трубки. Объем воздуха в каждом шаре и части трубки У= 200 см 3 . На какое расстояние х сместится капелька, если один шар нагреть на 2° С, а другой на столько же охладить? Поперечное сечение трубки S=20 мм 2
Для газа в отделе I:
- Температура воздуха в цилиндре 7°С. На сколько переместиться поршень при нагревании воздуха на 20К, если ℓ 1 =14см?
Газ граничит с жидкостью
- Электрическая лампа наполнена азотом при давлении Р= 600 мм рт. ст. Объем лампы V = 500 см 3 . Какая масса воды войдет в лампу, если у нее отломить кончик под водой? Атмосферное давление 760 мм рт. ст.?
Объем воды, поступившей в сосуд равен изменению объема газа при изотермическом процессе. Вода будет заходить в колбу до тех пор, пока давление внутри колбы не станет равным давлению наружному, то есть атмосферному.
Запишем закон Бойля-Мариотта для газа в колбе:%
Отсюда определим изменение объема:
Масса поступившей воды равна:
- Объем пузырька воздуха по мере всплывания со дна озера на поверхность увеличивается в 3 раза. Какова глубина озера?
- Открытую стеклянную трубку длиной ℓ=1м наполовину погружают в ртуть.Затем трубку закрывают пальцем и вынимают из ртути. Какой длины столбик ртути останется в трубке? атмосферное давление нлормальное.
- Узкая вертикальная цилиндрическая трубка длиной L,закрытая с одного конца, содержит воздух, отделенный от наружного воздуха столбиком ртути длиной h. Плотность ртути ρ. Трубка расположена открытым концом вверх. Какова была длина ℓ столбика воздуха в трубке, если при перевертывании трубки открытым концом вниз, из трубки вылилось половина ртути. атмосферное давление Р 0
- В стеклянной трубке, запаянной с одного конца и расположенной горизонтально, находится столбик воздуха длиной 300мм, закрытый столбиком ртути длиной 200мм. На сколько изменится длина воздушного столбика, если трубку расположить открытым концом вверх? Атмосферное давление нормальное.
- Длинная пробирка открытым концом погружена в сосуд с ртутью. При температуре t 1 = 47 °С уровни ртути в пробирке и в сосуде совпадают. Над уровнем ртути остается часть пробирки длины L = 76см. На какую высоту ℓ поднимется ртуть в пробирке, если ее охладить до температуры t 2 = -33 °С? Атмосферное давление Р 0 = 0,1 МПа.
- Посередине откачанной и запаянной с обоих концов горизонтально расположенной трубки длины L = 1 м находится столбик ртути длины h = 20 см. Если трубку поставить вертикально, столбик ртути сместится на расстояние ℓ = 10 см. До какого давления Р была откачана трубка? Плотность ртути ρ= 13,6∙10 3 кг/м 3 .
В обоих концах трубки воздух первоначально занимал объем
где S — площадь поперечного сечения трубки, и имел давление Р.
Когда трубку поставили вертикально, объем воздуха в верхней части трубки стал
а давление стало Р 1 ;
В нижней части трубки объем стал V 2 = S[(L — h)/2 — ℓ], а давление стало равным Р 2
Согласно закону Бойля-Мариотта для верхней части трубки PV = P 1 V 2
Откуда (L — h) P =(L-h + 2ℓ)P 1 ;
Для нижней части трубки
PV = P 2 V 2 , откуда (L-h)P = (L-h-2ℓ)Р 2 .
С другой стороны, столбик ртути находится в равновесии, когда давление воздуха в нижней части трубки равно сумме давлений воздуха в верхней части трубки и столбика ртути, т.е.
Исключив Р 1 иР 2 из уравнений, найдем = 50 кПа.

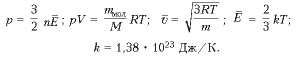
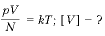
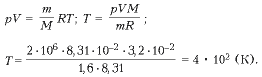
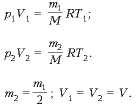
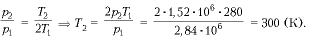
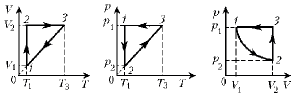
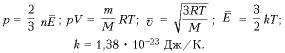
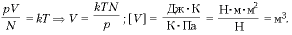
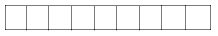
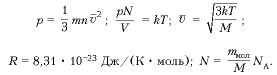
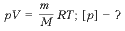
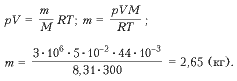
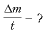
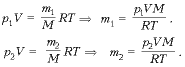
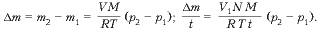
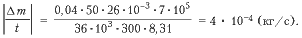
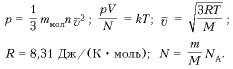
 Выведем размерность искомой физической величины:
Выведем размерность искомой физической величины:


 Отсюда температура
Отсюда температура  кислорода.
кислорода. ( Ответы : m=16 кг ; Р =249300 Па ; V=0,03 м 3; Т =150 К )
( Ответы : m=16 кг ; Р =249300 Па ; V=0,03 м 3; Т =150 К )