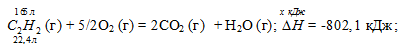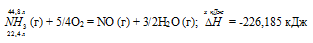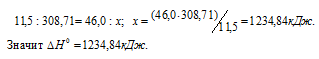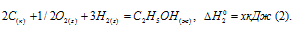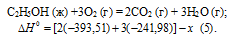Химия | 5 — 9 классы
Какое количество теплоты выделиться при сгорании угля массой 240 г, если термохимическое уравнение реакции С + О2 = СО2.
240г углерода — это 20 молей.
Значит при сгорании одного моля выделится 8200 / 20 = 410 кДж
И уравнение реакции будет следующим :
С + О2 = > ; СO2 + 410 кДж.
- Вычислите количество теплоты которая выделится при сгорании 11, 2м ^ 3 метана если термохимическое уравнение реакции его горения CH4 + 2O2 = CO2 + H2O + 900кДж?
- Решить задачу?
- Согласно термохимическому уравнению реакции ch4 + 2o2 = co2 + 2h2o + 802кДж определить количество теплоты , выделившейся при сгорании 24 Г метана Плиз полное решение?
- Теплота сгорания угля равна 393?
- Теплота сгорания угля равна 393?
- СРОЧНО?
- Какое количество теплоты выделится при сгорании 1, 12 л метана при н?
- По термохимическому уравнению : 2NH3 = 3H2 + N2 — 92 кДж — вычислите количество теплоты которое выделится в реакции, если масса аммиака равна 95г?
- Составьте термохимическое уравнение реакции горения натрия в хлоре, если известно, что при сгорании 1, 8 * 10 в 23 степени его атомов выделилось количество теплоты, равное 1233 кДж?
- При сгорании серы массой 1 грамм выделилась теплота 9?
- Составление термохимического уравнения реакции и вычисление теплот образования веществ
- Теплота образования веществ
- Теплота образования
- Тепловой эффект реакции
- Термохимическое уравнение реакции
- При сжигании 240 г углерода выделилось 8200 кдж теплоты составьте термохимическое уравнение реакции
- 🎥 Видео
Видео:Решение задач на термохимические уравнения. 8 класс.Скачать

Вычислите количество теплоты которая выделится при сгорании 11, 2м ^ 3 метана если термохимическое уравнение реакции его горения CH4 + 2O2 = CO2 + H2O + 900кДж?
Вычислите количество теплоты которая выделится при сгорании 11, 2м ^ 3 метана если термохимическое уравнение реакции его горения CH4 + 2O2 = CO2 + H2O + 900кДж.
Видео:Рудзитис Фельдман 2016 задача 4 стр 11 9 класс решениеСкачать

Решить задачу?
С помощью термохимического уравнения C + O2 = CO2 + 393, 5кДж вычислите, какое количество теплоты выделится при сгорании 18г угля.
Видео:Химия | Тепловой эффект химической реакции (энтальпия)Скачать

Согласно термохимическому уравнению реакции ch4 + 2o2 = co2 + 2h2o + 802кДж определить количество теплоты , выделившейся при сгорании 24 Г метана Плиз полное решение?
Согласно термохимическому уравнению реакции ch4 + 2o2 = co2 + 2h2o + 802кДж определить количество теплоты , выделившейся при сгорании 24 Г метана Плиз полное решение.
Видео:Уравнивание реакций горения углеводородовСкачать

Теплота сгорания угля равна 393?
Теплота сгорания угля равна 393.
Напишите термохимическое уравнение реакции.
Рассчитайте кол — во теплоты, которое выделится при сгорании 1 кг.
Какой объем углекислого газа (н.
У. ) образовался, если при сгорании угля выделилось 157, 4 кДж теплоты?
Видео:Установление эмпирической и молек. формул по массовым долям элем., входящих в состав в-ва. 10 класс.Скачать

Теплота сгорания угля равна 393?
Теплота сгорания угля равна 393.
Напишите термохимическое уравнение реакции.
Рассчитайте кол — во теплоты, которое выделится при сгорании 1 кг угля.
Какой объём углекислого газа образовался, если при сгорании угля выделилось 157.
Видео:Составление уравнений реакций горения. 11 класс.Скачать

СРОЧНО?
По термохимическому уравнению реакции горения метана СН4 + 2О2 = СО2 + 2Н2О + 803кДж рассчитайте, какое количество теплоты выделится при сгорании 5 м3 метана (н.
У. ) и какое количество вещества кислорода потребуется на это горение.
Видео:Органика. Решение задачи на определение состава вещества по продуктам его сгорания.Скачать

Какое количество теплоты выделится при сгорании 1, 12 л метана при н?
Какое количество теплоты выделится при сгорании 1, 12 л метана при н.
У если дано термохимическое уравнение.
Видео:10 класс(база).Решение задач на нахождение формулы по продуктам сгорания и массовой доли элемента.Скачать
По термохимическому уравнению : 2NH3 = 3H2 + N2 — 92 кДж — вычислите количество теплоты которое выделится в реакции, если масса аммиака равна 95г?
По термохимическому уравнению : 2NH3 = 3H2 + N2 — 92 кДж — вычислите количество теплоты которое выделится в реакции, если масса аммиака равна 95г.
Видео:Химия. 8 класс. Свойства углерода. Практическая работа «Физические и химические свойства углерода»Скачать

Составьте термохимическое уравнение реакции горения натрия в хлоре, если известно, что при сгорании 1, 8 * 10 в 23 степени его атомов выделилось количество теплоты, равное 1233 кДж?
Составьте термохимическое уравнение реакции горения натрия в хлоре, если известно, что при сгорании 1, 8 * 10 в 23 степени его атомов выделилось количество теплоты, равное 1233 кДж.
Видео:Физика 8 кл(2019г)Пер §10 Упр 9 № 2 . Какое количество теплоты выделяется при полном сгорании древесСкачать
При сгорании серы массой 1 грамм выделилась теплота 9?
При сгорании серы массой 1 грамм выделилась теплота 9.
Составить термохимическое уравнение.
На этой странице находится вопрос Какое количество теплоты выделиться при сгорании угля массой 240 г, если термохимическое уравнение реакции С + О2 = СО2?. Здесь же – ответы на него, и похожие вопросы в категории Химия, которые можно найти с помощью простой в использовании поисковой системы. Уровень сложности вопроса соответствует уровню подготовки учащихся 5 — 9 классов. В комментариях, оставленных ниже, ознакомьтесь с вариантами ответов посетителей страницы. С ними можно обсудить тему вопроса в режиме on-line. Если ни один из предложенных ответов не устраивает, сформулируйте новый вопрос в поисковой строке, расположенной вверху, и нажмите кнопку.
А) 2 — метилбутан б) 3 — метилгексан в) 2, 3 — диметилбутан г) 5 — метил — 4 — этилгептан д) 2, 2, 3, 4 — тетраметилпентан е) 3, 3, 4, 5 — тетраметилгексан.
Поскольку натрий находится в 3 периоде, то у него будет 3 электронных слоя. Они будут заполнены соответственно )2)8)1. Оформляя графическую формулу, можно заметить, что на 3s уровне остаётся один неспаренный электрон. Оформим электронную формулу .
1)Задача на фотографии 2) Это название относится к Ca(OH)2. 3) 2 — ая фотография, на ней решение смотри. 4) Дано : w (NaF) = 10% w (MgCl2) = 10% m (MgF2) = 6, 2 г Найти : m (NaF) и m (MgCl2) — ? Решение : MgCl2 + 2NaF — MgF2 + 2NaCl M (MgF2) = 24 ..
H2S — ковалентная полярная Cu — металлическая LiCl2 — ионная O2 — ковалентная неполярная.
Дано : Q = 33520кдж — — — — — — — — — — — — — — — — m(C) — ? Xg 33520кдж C + O2 — — >CO2 + 402. 24 кдж Mr(C) = 12 (при сгорании 1 моль углерода выделяется Q = 402. 24кдж) m(1 моль С) = 12г 12 г — 402, 24 кдж хг — 33520 кдж х = 12 * 33520 / 402, 24..
Na — металлическая NaCl — ионная Cl2 — ковалентная неполярная SCl — ковалентная полярная.
AlPO4 + H2 Al — валентность 3 PO4 валентность 3 H2 валентность 1.
Я ответила на ваш вопрос .
Х — число атомов кремния у — число атомов железа а) 14х = 26у х / у = 26 / 14 = 1, 857 б) m(Fe) / m(Si) = 56у / 28х = 1, 077.
1)Ca — металлическая. 2)Сl2 — ковалентная неполярная. 3)H2O, HCl — ковалентная полярная.
Видео:§34, 9 кл. Кислородные соединения углеродаСкачать

Составление термохимического уравнения реакции и вычисление теплот образования веществ
Видео:Углерод: химические свойства, аллотропия #углерод #химшкола #неметаллы #егэхимияСкачать

Теплота образования веществ
Задание 88.
Тепловой эффект какой реакции равен теплоте образования метана? Вычислите теплоту образования метана, исходя из следующих термохимических уравнений:
а) Н2 (г) + 1/2О2 (г) = Н2О (ж); 
б) С (к) + О2 (г) = СО2 (г); 
в) СН4 (г) + 2О2 (г) = 2Н2О (ж) + СО2 (г); 
Ответ: -74,88 кДж.
Решение:
Стандартная теплота образования равна теплоте реакции образования 1 моль этого вещества из простых веществ при стандартных условиях (Т = 298 К; р = 1,0325 . 105 Па). Образование метана из водорода и углерода можно представить так:
С (графит) + 2Н2 (г) = СН4 (г); 
Исходя из данных уравнений по условию задачи, учитывая, что водород сгорает до воды, углерод — до углекислого газа, метан – до углекислого газа и воды и, на основании закона Гесса, с термохимическими уравнениями можно оперировать также как и с алгебраическими. Для получения искомого результата нужно уравнение горения водорода (а) умножить на 2, а затем, сумму уравнений горения водорода (а) и углерода (б) вычесть из уравнения горения метана (в):
СН4 (г) + 2О2 (г) — 2 Н2 (г) + О2 (г) — С (к) + О2 (г) =
= 2Н2О (ж) + СО2 — 2Н2О — СО2;

СН4 (г) = С (к) + 2Н2 (к); 
Так как теплота образования равна теплоте разложения с обратным знаком, то

Ответ: -74,88 кДж.
Задание 89.
Тепловой эффект какой реакции равен теплоте образования гидроксида кальция? Вычислите теплоту образования гидроксида кальция, исходя из следующих термохимических уравнений:
Са (к) + 1/2О (г) = СаО (к); 
Н2 (г) + 1/2О2 (г) = Н2О (ж); 
СаО (к) + Н2О (ж) = Са(ОН)2 (к); 
Ответ: —986,50 кДж.
Решение:
Стандартная теплота образования равна теплоте реакции образования 1 моль этого вещества из простых веществ при стандартных условиях (Т = 298 К; р = 1,0325 . 105 Па). Образование гидроксида кальция из простых веществ можно представить так:
Са (к) + О2 (г) + Н2 (г) = Са(ОН)2 (к); 
Исходя из уравнений, которые даны по условию задачи и, учитывая, что водород сгорает до воды, а кальций, реагируя с кислородом, образует СаО, то на основании закона Гесса с термохимическими уравнениями можно оперировать также как с алгебраическими. Для получения искомого результата нужно все три уравнения сложить между собой:
СаО (к) + Н2О (ж) + Са (к) + 1/2О (г) + Н2 (г) + 1/2О2 (г = (ОН)2 (к) + СаО (к) + Н2О (ж); 
Так как стандартные теплоты образования простых веществ условно принята равными нулю, то теплота образования гидроксида кальция будет равна тепловому эффекту реакции образования его из простых веществ (кальция, водорода и кислорода):


Ответ: -986,50 кДж.
Задание 90.
Тепловой эффект реакции сгорания жидкого бензина с образованием паров воды и диоксида углерода равен -3135,58 кДж. Составьте термохимическое уравнение этой реакции и вычислите теплоту образования С6Н6 (ж). Ответ: +49,03 кДж.
Решение:
Уравнения реакций, в которых около символов химических соединений указываются их агрегатные состояния или кристаллическая модификация, а также числовое значение тепловых эффектов, называют термохимическими. В термохимических уравнениях, если это специально не оговорено, указываются значения тепловых эффектов при постоянном давлении Qp равные изменению энтальпии системы 

Термохимическое уравнение реакции имеет вид:
С6Н6 (ж) + 7/2O2 = 6CO2 (г) + 3Н2О (г); 
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствии е из закона Гесса:









Ответ: +49,03 кДж.
Видео:9 класс § 34 "Кислородсодержащие соединения углерода"Скачать

Теплота образования
Задание 91.
Вычислите, сколько теплоты выделится при сгорании 165 л (н.у.) ацетилена С2Н2, если продуктами сгорания являются диоксид углерода и пары воды? Ответ: 924,88 кДж.
Решение:
Уравнения реакций, в которых около символов химических соединений указываются их агрегатные состояния или кристаллическая модификация, а также числовое значение тепловых эффектов, называют термохимическими. В термохимических уравнениях, если это специально не оговорено, указываются значения тепловых эффектов при постоянном давлении Qp равные изменению энтальпии системы 

Уравнение реакции имеет вид:
С2Н2 (г) + 5/2O2 (г) = 2CO2 (г) + Н2О (г); 
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:





Термохимическое уравнение будет иметь вид:
Теплоту, выделившуюся при сгорании 165 л ацетилена по этой реакции, определим из пропорции:
22,4 : -802,1 = 165 : х; х = 165 (-802,1)/22,4 = -5908,35 кДж; Q = 5908,35 кДж.
Ответ: 5908,35 кДж.
Задание 92.
При сгорании газообразного аммиака образуются пары воды и оксид азота. Сколько теплоты выделится при этой реакции, если было получено 44,8 л NO в пересчете на нормальные условия? Ответ: 452,37 кДж.
Решение:
Уравнение реакции имеет вид:
Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:





Термохимическое уравнение будет иметь вид:
Теплоту, выделившуюся при сгорании 44,8 л аммиака, вычислим из пропорции:
22,4 : -226,185 = 44,8 : х; х = 44,8 (-226,185)/22,4 = -452,37 кДж; Q = 452,37 кДж.
Ответ: 452,37 кДж
Тепловой эффект реакции
Задание 93.
Реакция горения метилового спирта выражается термохимическим уравнением:
СН3ОН (ж) +3/2О2 (г) = СО2 (г) + 2Н2О (ж); 
Вычислите тепловой эффект этой реакции, если известно, что молярная теплота парообразования СН3ОН (ж) равна +37,4 кДж. Ответ: -726,62 кДж.
Решение:
(СН3ОН (ж)) = (СН3ОН (г)); 
+37,4 кДж = -201,17 — 

Значения стандартных теплот образования веществ приведены в специальных таблицах. Учитывая, что теплоты образования простых веществ условно приняты равными нулю. Тепловой эффект реакции можно вычислить, используя следствие из закона Гесса:





Ответ: -726,62 кДж.
Термохимическое уравнение реакции
Задание 94.
При сгорании 11,5 г жидкого этилового спирта выделилось 308,71 кДж теплоты. Напишите термохимическое уравнение реакции, в результате которой образуются пары воды и диоксид углерода. Вычислите теплоту образования С2Н5ОН(ж). Ответ: —277,67 кДж.
Решение:
Мольная масса С2Н5ОН равна 46,0г/моль.
Находим тепловой эффект реакции горения этилового спирта из пропорции:
Следовательно, термохимическое уравнение реакции будет иметь вид:
С2Н5ОН (ж) +3О2 (г) = 2СО2 (г) + 3Н2О (г); 
Обозначим искомую величину через х, запишем термохимическое уравнение образования С2Н5ОН из простых веществ:
Запишем также термохимические уравнения образования СО2(г) и Н2О(ж):
Из уравнений (2), (3) и (4) можно получить уравнение (5). Для этого умножим уравнение (4) на три, уравнение (2) — на два, а затем из суммы уравнений (3) и (4) вычтем уравнение (2), получим:
Сравнивая уравнения (1) и (5), находим:
Ответ: 
Видео:ОПРЕДЕЛЕНИЕ ФОРМУЛЫ ОРГАНИЧЕСКОГО ВЕЩЕСТВА ПО ПРОДУКТАМ СГОРАНИЯ. ХИМИЯ ЕГЭСкачать

При сжигании 240 г углерода выделилось 8200 кдж теплоты составьте термохимическое уравнение реакции
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 2
Какие данные нужно обязательно указывать при составлении термохимических уравнений? Агрегатное состояние вещества (твёрдое, жидкое, газообразное) .
Поясните на конкретных примерах.
BaCO3 (тв.) = BaO (тв.) + CO2↑ (г.) ― 267 кДж
2H2O (ж.) постоянный ток ⟶ 2H2(г.)+ O2 (г.) ― 484 кДж
2H2 (г.) + O2 (г.) = 2H2O (г.) + 484 кДж
С (тв) + О2 (г) = СО2 (г) + 410 кДж
Задание 3
Какое количество теплоты выделится при сжигании 100 л водорода, взятого при нормальных условиях, в избытке кислорода? Термохимическое уравнение реакции: 2H2 (г.) + O2 (г.) = 2H2O (г.) + 484 кДж Ответ
По термохимическому уравнению реакции с 44,8 л (2 моль) Н2 выделяется 484 кДж теплоты,
по условию задачи с 100 л Н2 ― х кДж теплоты.
х = 100 л ● 484 кДж : 44,8 л=1080 кДж
Ответ: 1080 кДж
Задание 4
Вычислите, сколько сгорело угля, если при этом выделилось 33520 кДж теплоты.
Термохимическое уравнение реакции С (тв) + О2 (г) = СО2 (г) + 402,24 кДж
По термохимическому уравнению реакции с 1 моль С выделяется 402,24 кДж теплоты,
по условию задачи с х моль С ― 33520 кДж теплоты.
х= n(C)= 33520 кДж ● 1 моль : 402,24 кДж=83,3 моль
Рассчитаем массу углерода количеством вещества 83,3 моль.
m(C)=n(C)●VM=83,3 моль ● 12 г/моль=999,6 г=1 кг
Ответ: 1 кг
🎥 Видео
Химические свойства углеродаСкачать

Химия 9 класс : УглеродСкачать

Химия. 9 класс (Урок№17 - Углерод. Аллотропные модификации углерода.Химические свойства. Адсорбция.)Скачать

Химия. 11 класс. Особенности строения атома углерода /09.09.2020/Скачать

Валентные состояния атома углерода. Химия 10 классСкачать

9 класс Химия Практическая работа Получение углекислого газа и изучение его свойств.Скачать