Задача 911.
Как получают фосфор в промышленности? Написать уравнения соответствующих реакций.
Решение:
Белый фосфор получают при нагревании в электрической печи смеси фосфорита или аппатита, кокса и кварцевого песка. Природный фосфорит или апатит
измельчают, смешивают с песком и углем и прокаливают в электрических печах без доступа воздуха. Уравнение реакции можно представить так:
4Са5(РО4)3F +30C + 21SiO2 
Фосфор выделяется в виде паров, которые конденсируются в приёмнике под водой. Белый фосфор получается в твёрдом состоянии при быстром охлаждении паров фосфора. В результате длительного нагревания белого фосфора без доступа воздуха при атмосферном давлении образуется красный фосфор, а при высоком давлении – кристаллический чёрный фосфор.
Задача 912.
Указать аллотропные модификации фосфора и различия в их свойствах. Сохраняются ли эти различия после перехода фосфора в газообразное состояние? Как доказать, что красный и белый фосфор представляют собой аллотропные модификации одного и того же элемента?
Решение:
Фосфор образует несколько аллотропных модификаций. Важнейшие среди них белый, красный и черный. Белый и красный фосфор термодинамически неустойчивы, но могут существовать при нормальных условиях из-за малых скоростей превращения в устойчивую модификацию — черный фосфор.
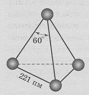
Белый фосфор белое мягкое воскообразное вещество или прозрачные кристаллы, состоящие из тетраэдрических молекул Р4 (рис. 1.). Углы Р—Р—Р в таких тетраэдрах равны 60°:
Рис. 1. Структура молекулы
белого фосфора
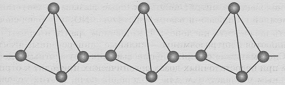
Рис. 2. Структура молекулы красного фосфора
что гораздо меньше 90° между осями р-орбиталей. Эти углы, таким образом, очень напряжены, что придает белому фосфору большую химическую активность. Так как он легко окисляется и может самовоспламеняться на воздухе, его хранят под водой. Белый фосфор ядовит и очень огнеопасен. Молекулярный характер кристаллов придает этой модификации легкоплавкость (tпл. = 44 °С), летучесть (tкип. = 257 °С) и растворимость в органических растворителях.
Красный фосфор существует в нескольких кристаллических формах, которые состоят из связанных между собой бесконечных цепей, образующихся при размыкании тетраэдров (рис. 2.). Он обладает меньшей химической активностью, чем белый, не ядовит, загорается только при поджигании, не растворим в органических растворителях.
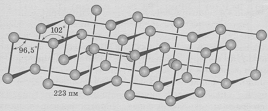
Черный фосфор имеет графитоподобную слоистую структуру, в которой каждый атом Р связан с тремя другими (рис. 3.). Слои связаны между собой слабо. Черный фосфор — наименее химически активная аллотропная модификация фосфора.
Рис. 3. Структура молекулы чёрного фосфора
Доказательством того, что белый и красный фосфор являются аллотропными модификациями одного и того же элемента служат реакции горения белого и красного фосфора, их активного взаимодействия с с галогенами, с образованием тригалогенидов:
А также то, что при хранении белый фосфор постепенно (очень медленно) переходит в более устойчивую красную форму. Переход сопровождается выделением тепла (теплота перехода):
- Фосфор. Химия фосфора и его соединений
- Фосфор
- Положение в периодической системе химических элементов
- Электронное строение фосфора
- Физические свойства и нахождение в природе
- Соединения фосфора
- Способы получения фосфора
- Химические свойства фосфора
- Фосфин
- Строение молекулы и физические свойства
- Способы получения фосфина
- Химические свойства фосфина
- Фосфиды
- Способы получения фосфидов
- Химические свойства фосфидов
- Оксиды фосфора
- Оксид фосфора (III)
- Оксид фосфора (V)
- Фосфорная кислота
- Строение молекулы и физические свойства
- Способы получения
- Химические свойства
- Фосфористая кислота
- Соли фосфорной кислоты — фосфаты
- Превращение красного фосфора в белый уравнение реакции
- ПОЛУЧЕНИЕ БЕЛОГО ФОСФОРА
- ОЧИСТКА БЕЛОГО ФОСФОРА
- ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛОГО ФОСФОРА
- СВЕЧЕНИЕ БЕЛОГО ФОСФОРА
- РАСТВОРИМОСТЬ БЕЛОГО ФОСФОРА
- ПРЕВРАЩЕНИЕ БЕЛОГО ФОСФОРА В КРАСНЫЙ
- ГОРЕНИЕ БЕЛОГО ФОСФОРА
- ВОССТАНОВЛЕНИЕ СОЛЕЙ СЕРЕБРА И МЕДИ БЕЛЫМ ФОСФОРОМ
- КРАСНЫЙ ФОСФОР
- ПРИМЕСИ
- ОЧИСТКА И ХРАНЕНИЕ КРАСНОГО ФОСФОРА
- СВОЙСТВА
- ПРИМЕНЕНИЕ ФОСФОРА
- СОЕДИНЕНИЯ ФОСФОРА
- ПОЛУЧЕНИЕ
- ПОЛУЧЕНИЕ И СВОЙСТВА ЙОДИСТОГО ФОСФОНИЯ
- СВОЙСТВА ГАЗООБРАЗНОГО ФОСФОРИСТОГО ВОДОРОДА
- ФОСФИД КАЛЬЦИЯ
- ЖИДКИЙ ФОСФОРИСТЫЙ ВОДОРОД Р2Н4 (ДИФОСФИН)
- КИСЛОРОДНЫЕ СОЕДИНЕНИЯ ФОСФОРА
Видео:Получение БЕЛОГО ФОСФОРАСкачать

Фосфор. Химия фосфора и его соединений
Фосфор
Положение в периодической системе химических элементов
Фосфор расположен в главной подгруппе V группы (или в 15 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение фосфора
Электронная конфигурация фосфора в основном состоянии :
Атом фосфора содержит на внешнем энергетическом уровне 3 неспаренных электрона и одну неподеленную электронную пару в основном энергетическом состоянии. Следовательно, атом фосфора может образовывать 3 связи по обменному механизму. Однако, в отличие от азота, за счет вакантной 3d орбитали атом фосфора может переходить в возбужденное энергетическое состояние.
Электронная конфигурация фосфора в возбужденном состоянии:
При этом один электрон из неподеленной электронной пары на 3s-орбитали переходит на переходит на 3d-орбиталь. Для атома фосфора в возбужденном энергетическом состоянии характерна валентность V.
Таким образом, максимальная валентность фосфора в соединениях равна V (в отличие от азота). Также характерная валентность фосфора в соединениях — III.
Степени окисления атома фосфора – от -3 до +5. Характерные степени окисления -3, 0, +1, +3, +5.
Физические свойства и нахождение в природе
Фосфор образует различные простые вещества (аллотропные модификации).
Белый фосфор — это вещество состава P4. Мягкий, бесцветный, ядовитый, имеет характерный чесночный запах. Молекулярная кристаллическая решетка, а следовательно, невысокая температура плавления (44°С), высокая летучесть. Очень реакционно способен, самовоспламеняется на воздухе.
Покрытие бумаги раствором белого фосфора в сероуглероде. Спустя некоторое время, когда сероуглерод испаряется, фосфор воспламеняет бумагу (процесс лег в основу различных фокусов с самовозгоранием или получением огня из ничего):
Белый фосфор можно расплавить в ёмкости с тёплой водой, поскольку он имеет температуру плавления в 44,15 °C.
Красный фосфор – это модификация с атомной кристаллической решеткой . Формула красного фосфора Pn, это полимер со сложной структурой. Твердое вещество без запаха, красно-бурого цвета, не ядовитое. Это гораздо более устойчивая модификация, чем белый фосфор. В темноте не светится. Образуется из белого фосфора при t=250-300 о С без доступа воздуха.
Черный фосфор – то наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Чёрный фосфор — это чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, полностью нерастворимое в воде или органических растворителях.
Известны также такие модификации, как желтый фосфор и металлический фосфор. Желтый фосфор – это неочищенный белый фосфор. При очень высоком давлении фосфор переходит в новую модификацию – металлический фосфор , который очень хорошо проводит электрический ток.
В природе фосфор встречается только в виде соединений. В основном это апатиты (например, Ca3(PO4)2), фосфориты и др. Фосфор входит в состав важнейших биологических соединений —фосфолипидов.
Соединения фосфора
Типичные соединения фосфора:
| Степень окисления | Типичные соединения |
| +5 | оксид фосфора (V) P2O5 ортофосфорная кислота H3PO4 метафосфорная кислота HPO3 Галогенангидриды: PОCl3, PCl5 |
| +3 | Оксид фосфора (III) P2O3 Галогенангидриды: PCl3 |
| +1 | Фосфорноватистая кислота H3PO2 Соли фосфорноватистой кислоты — гипофосфиты: MeH2PO2 |
| -3 | Фосфин PH3 Фосфиды металлов MeP |
Способы получения фосфора
1. Белый фосфор получают из природных фосфатов , прокаливая их с коксом и песком в электрической печи:
2. Вместо фосфатов можно использовать другие неорганические соединения фосфора, например , метафосфорную кислоту.
4HPO3 + 10C → P4 + 2H2O + 10 CO
3. Красный и черный фосфор получают из белого фосфора.
Химические свойства фосфора
При нормальных условиях фосфор довольно химически активен.
1. Фосфор проявляет свойства окислителя (с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому фосфор реагирует с металлами и неметаллами .
1.1. При взаимодействии с кислородом воздуха образу
ются оксиды – ангидриды соответствующих кислот :
Горение белого фосфора:
Горение красного фосфора:
1.2. При взаимодействии фосфора с галогенами образуются галогениды с общей формулой PHal3 и PHal5:
Фосфор реагирует с бромом:
1.3. При взаимодействии фосфора с серой образуются сульфиды:
1.4. При взаимодействии с металлами фосфор проявляет свойства окислителя, продукты реакции называют фосфидами.
Например , кальций и магний реагируют с фосфором с образованием фосфидов кальция и магния:
Еще пример : натрий взаимодействует с фосфором с образованием фосфида натрия:
P + 3Na → Na3P
1.5. С водородом фосфор непосредственно не взаимодействует.
2. Со сложными веществами фосфор реагирует, проявляя окислительные и восстановительные свойства. Фосфор диспропорционирует при взаимодействии с некоторыми веществами.
2.1. При взаимодействии с окислителями фосфор окисляется до оксида фосфора (V) или до фосфорной кислоты.
Например , азотная кислота окисляет фосфор до фосфорной кислоты:
Серная кислота также окисляет фосфор:
Соединения хлора, например , бертолетова соль , также окисляют фосфор:
Реакция красного фосфора с бертолетовой солью. Этот процесс заложен в принципе возгорания спички при трении её о шершавую поверхность коробка.
Некоторые металлы-сильные окислители также окисляют фосфор. Например , оксид серебра (I) :
2.2. При растворении в щелочах фосфор диспропорционирует до гипофосфита и фосфина.
Например , фосфор реагирует с гидроксидом калия:
Или с гидроксидом кальция:
Фосфин
Строение молекулы и физические свойства
Фосфин PH3 – это бинарное соединение водорода с фосфором, относится к летучим водородным соединениям. Следовательно, фосфин газ, с неприятным запахом, бесцветный, мало растворимый в воде, химически нестойкий и ядовитый. Водородные связи между молекулами фосфина не образуются. В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы фосфина похожа на структуру аммиака — правильная треугольная пирамида. Но валентный угол H-P-H меньше, чем угол H-N-H в аммиаке и составляет 93,5 о .
У атома фосфора в фосфине на внешнем энергетическом уровне остается неподеленная электронная пара. Эта электронная пара оказывает значительное влияние на свойства фосфина, а также на его структуру. Электронная структура фосфина — тетраэдр , с атомом фосфора в центре.
Способы получения фосфина
В лаборатории фосфин получают водным или кислотным гидролизом фосфидов – бинарных соединений фосфора и металлов.
Например , фосфин образуется при водном гидролизе фосфида кальция:
Или при кислотном гидролизе, например , фосфида магния в соляной кислоте:
Еще один лабораторный способ получения фосфина – диспропорционирование фосфора в щелочах.
Например , фосфор реагирует с гидроксидом калия с образованием гипофосфита калия и фосфина:
Химические свойства фосфина
1. В водном растворе фосфин проявляет очень слабые основные свойства (за счет неподеленной электронной пары). Принимая протон (ион H + ), он превращается в ион фосфония. Основные свойства фосфина гораздо слабее основных свойств аммиака. Проявляются при взаимодействии с безводными кислотами .
Например , фосфин реагирует с йодоводородной кислотой:
Соли фосфония неустойчивые, легко гидролизуются.
2. Фосфин PH3 – сильный восстановитель за счет фосфора в степени окисления -3. На воздухе самопроизвольно самовоспламеняется:
3. Как сильный восстановитель, фосфин легко окисляется под действием окислителей.
Например , азотная кислота окисляет фосфин. При этом фосфор переходит в степень окисления +5 и образует фосфорную кислоту.
Серная кислота также окисляет фосфин:
С фосфином также реагируют другие соединения фосфора, с более высокими степенями окисления фосфора.
Например , хлорид фосфора (III) окисляет фосфин:
2PH3 + 2PCl3 → 4P + 6HCl
Фосфиды
Фосфиды – это бинарные соединения фосфора и металлов или некоторых неметаллов .
Способы получения фосфидов
Фосфиды получают при взаимодействии фосфора с металлами . При этом фосфор проявляет свойства окислителя.
Например , фосфор взаимодействует с магнием и кальцием:
Фосфор взаимодействует с натрием:
P + 3Na → Na3P
Химические свойства фосфидов
1. Фосфиды легко разлагаются водой или кислотами с образованием фосфина.
Например , фосфид кальция разлагается водой:
Фосфид магния разлагается соляной кислотой:
2. Фосфиды металлов проявляют сильные восстановительные свойства за счет фосфора в степени окисления -3 .
Оксиды фосфора
| Оксиды азота | Цвет | Фаза | Характер оксида |
| P2O3 Оксид фосфора (III), фосфористый ангидрид | белый | твердый | кислотный |
| P2O5 Оксид фосфора(V), фосфорный ангидрид | белый | твердый | кислотный |
Оксид фосфора (III)
Оксид фосфора (III) – это кислотный оксид . Белые кристаллы при обычных условиях. Пары состоят из молекул P4O6.
Получить оксид фосфора (III) можно окислением фосфора при недостатке кислорода :
Химические свойства оксида фосфора (III):
Оксид фосфора (III) очень ядовит и неустойчив. Для P2O3 (P4O6) характерны два типа реакций.
1. Поскольку фосфор в оксиде фосфора (III) проявляет промежуточную степень окисления, то он принимает участие в окислительно-восстановительных процессах, повышая либо понижая степень окисления атома фосфора. Характерны для P2O3 реакции диспропорционирования.
Например , оксид фосфора (III) диспропорционирует в горячей воде:
2. При взаимодействии с окислителями P2O3 проявляет свойства восстановителя.
Например , N2O окисляется кислородом:
3. С другой стороны Р2О3 проявляет свойства кислотного оксида (ангидрид фосфористой кислоты), взаимодействуя с водой с образованием фосфористой кислоты:
а со щелочами – с образованием солей (фосфитов):
Оксид фосфора (V)
Оксид фосфора (V) – это кислотный оксид. В нормальных условиях образует белые кристаллы. В парах состоит из молекул P4О10. Очень гигроскопичен (используется как осушитель газов и жидкостей).
Способы получения. Оксид фосфора (V) получают сжиганием фосфора в избытке кислорода.
Химические свойства.
1. Оксид фосфора (V) – очень гигроскопичное вещество, которое используется для осушения газов. Обладая высоким сродством к воде, оксид фосфора (V) дегидратирует до ангидридов неорганические и органические кислоты.
Например , оксид фосфора (V) дегидратирует серную, азотную и уксусную кислоты:
2. Фосфорный ангидрид является типичным кислотным оксидом , взаимодействует с водой с образованием фосфорных кислот:
В зависимости от количества воды и от других условий образуются мета-фосфорная, орто-фосфорная или пиро-фосфорная кислота:
Видеоопыт взаимодействия оксида фосфора с водой можно посмотреть здесь.
3. Как кислотный оксид, оксид фосфора (V) взаимодействует с основными оксидами и основаниями .
Например , оксид фосфора (V) взаимодействует с гидроксидом натрия. При этом образуются средние или кислые соли:
Еще пример : оксид фосфора взаимодействует с оксидом бария (при сплавлении):
Фосфорная кислота
Строение молекулы и физические свойства
Фосфор в степени окисления +5 образует несколько кислот: орто-фосфорную H3PO4, мета-фосфорную HPO3, пиро-фосфорную H4P2O7.
Фосфорная кислота H3PO4 – это кислота средней силы, трехосновная, прочная и нелетучая. При обычных условиях фосфорная кислота – твердое вещество, хорошо растворимое в воде и гигроскопичное.
Валентность фосфора в фосфорной кислоте равна V.
При температуре выше +213 °C орто-фосфорная кислота переходит в пирофосфорную H4P2O7.
При взаимодействии высшего оксида фосфора с водой на холоде образуется метафосфорная кислота HPO3, представляющая собой прозрачную стекловидную массу.
Способы получения
Наибольшее практическое значение из фосфорных кислот имеет орто-фосфорная кислота.
1. Получить орто-фосфорную кислоту можно взаимодействием оксида фосфора (V) с водой:
2. Еще один способ получения фосфорной кислоты — вытеснение фосфорной кислоты из солей (фосфатов, гидрофосфатов и дигидрофосфатов) под действием более сильных кислот (серной, азотной, соляной и др.) .
Промышленный способ получения фосфорной кислоты обработка фосфорита концентрированной серной кислотой:
3. Фосфорную кислоту также можно получить жестким окислением соединений фосфора в водном растворе в присутствии кислот.
Например , концентрированная азотная кислота окисляет фосфор до фосфорной кислоты:
Химические свойства
Фосфорная кислота – это кислота средней силы (по второй и третьей ступени слабая) .
1. Фосфорная кислота частично и ступенчато диссоциирует в водном растворе.
HPO4 2– ⇄ H + + PO4 3–
2. Фосфорная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , фосфорная кислота взаимодействует с оксидом магния:
Еще пример : при взаимодействии фосфорной кислоты с гидроксидом калия образуются фосфаты, гидрофосфаты или дигидрофосфаты:
3. Фосфорная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов и др.). Также фосфорная кислота вступает в обменные реакции с солями.
Например , фосфорная кислота взаимодействует с гидрокарбонатом натрия:
4. При нагревании H3PO4 до 200°С происходит отщепление от нее молекулы воды с образованием пирофосфорной кислоты H2P2O7:
5. Фосфорная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Например , фосфорная кислота реагирует с магнием:
Фосфорная кислота взаимодействует также с аммиаком с образованием солей аммония:
7. Качественная реакция на фосфат-ионы и фосфорную кислоту — взаимодействие с нитратом серебра. При этом образуется ярко-желтый осадок фосфата серебра:
Видеоопыт взаимодействия фосфата натрия и нитрата серебра в растворе (качественная реакция на фосфат-ион) можно посмотреть здесь.
Фосфористая кислота
Фосфористая кислота H3PO3 — это двухосновная кислородсодержащая кислота. При нормальных условиях бесцветное кристаллическое вещество, хорошо растворимое в воде.
Валентность фосфора в фосфористой кислота равна V, а степень окисления +3.
Получение фосфористой кислоты.
Фосфористую кислоту можно получить гидролизом галогенидов фосфора (III).
Например , гидролизом хлорида фосфора (III):
Фосфористую кислоту можно получить также взаимодействием оксида фосфора (III) с водой:
Химические свойства.
1. Фосфористая кислота H3PO3 в водном растворе — двухосновная кислота средней силы. Взаимодействует с основаниями с образованием солей-фосфитов.
Например , при взаимодействии с гидроксидом натрия фосфористая кислота образует фосфит натрия:
2. При нагревании фосфористая кислота разлагается на фосфин (Р -3 ) и фосфорную кислоту (Р +5 ):
3. За счет фосфора в степени окисления +3 фосфористая кислота проявляет восстановительные свойства .
Например , H3PO3 окисляется перманганатом калия в кислой среде:
Еще пример : фосфористая кислота окисляется соединениями ртути (II):
Соли фосфорной кислоты — фосфаты
Фосфорная кислота образует разные типы солей: средние – фосфаты, кислые – гидрофосфаты, дигидрофосфаты.
1. Качественная реакция на фосфаты — взаимодействие с нитратом серебра. При этом образуется желтый осадок фосфата серебра.
2. Нерастворимые фосфаты растворяются под действием сильных кислот, либо под действием фосфорной кислоты.
Например , фосфат кальция реагирует с фосфорной кислотой с образованием дигидрофосфата кальция:
Фосфат кальция растворяется под действием серной кислоты:
3. За счет фосфора со степенью окисления +5 фосфаты проявляют слабые окислительные свойства и могут взаимодействовать с восстановителями.
Например , фосфат кальция при сплавлении реагирует с углеродом с образованием фосфида кальция и угарного газа:
Фосфат кальция также восстанавливается алюминием при сплавлении:
4. Гидрофосфаты могут взаимодействовать и с более сильными кислотами, и с щелочами . Под действием фосфорной кислоты гидрофосфаты переходят в дигидрофосфаты.
Например , гидрофосфат калия взаимодействует с фосфорной кислотой с образованием дигидрофосфата калия:
Под действием едкого кали гидрофосфат калия образует более среднюю соль — фосфат калия:
5. Дигидрофосфаты могут взаимодействовать с более сильными кислотами и щелочами , но не реагируют с фосфорной кислотой.
Например , дигидрофосфат натрия взаимодействует с избытком гидроксида натрия с образованием фосфата:
Видео:Получение белого фосфора из красногоСкачать

Превращение красного фосфора в белый уравнение реакции
ФОСФОР
Р. Рипан, И. Четяну
(часть книги РУКОВОДСТВО К ПРАКТИЧЕСКИМ РАБОТАМ ПО НЕОРГАНИЧЕСКОЙ ХИМИИ)
Видео:Белый и красный фосфорСкачать

ПОЛУЧЕНИЕ БЕЛОГО ФОСФОРА
При проведении опытов необходимо учитывать, что белый фосфор и его пары ядовиты; при соприкосновении с кожей он оставляет болезненные и долго не заживающие раны ( см. правила обращения с белым фосфором ).
Опыт. Получение фосфора в результате взаимодействия ортофосфата кальция, угля и двуокиси кремния.
Реакция протекает по уравнению:
Этот опыт позволяет получить белый и красный фосфор и наблюдать его холодное пламя.
Реакционной камерой служит колба из огнеупорного стекла емкостью 2 л с двумя тубусами. Диаметр колбы 150 мм, длина тубусов около 50 мм, внутренний диаметр 40 мм.
При сборке прибора колбу устанавливают, как показано на рис., на обернутое асбестом кольцо штатива и укрепляют вверху в зажиме штатива. Оба тубуса закрывают резиновыми пробками, в середине которых имеется по одному отверстию для угольных электродов и сбоку по одному отверстию для впуска и удаления газа. Нижний электрод диаметром около 12 мм вставляют так, чтобы конец его не доходил до середины колбы. На введенном в колбу конце электрода укрепляют небольшую железную муфту, которая должна быть опорой для керамического тигля с отверстием внизу. Применяемая муфта должна иметь винтовую резьбу и латунный винтик; диаметр муфты около 9 мм. Муфту привинчивают так, чтобы одна ее сторона была выше конца электрода. На муфту устанавливают керамический тигель (с верхним диаметром менее 40 мм), в отверстие дна которого вводят кончик электрода. На нижний конец электрода укрепляют медную муфту, служащую для соединения электрода с электрическим проводом.
 Белый фосфор |
 Белый фосфор |
 Прибор для получения фосфора |
В пробку верхнего тубуса вставляют толстостенную стеклянную тугоплавкую трубку длиной около 100 мм с таким расчетом, чтобы она примерно на 10 мм входила в колбу. Через эту трубку должен легко проходить верхний угольный электрод, который может быть тоньше нижнего. На верхний конец стеклянной трубки (с оплавленными краями) и проходящий через нее электрод надевают кусочек резиновой трубки длиной 50 мм. Верхний электрод укрепляют таким образом, чтобы его заостренный конец находился на расстоянии 8-10 мм от верхнего конца нижнего электрода. На верхнем конце верхнего электрода в качестве изолированной ручки укрепляют корковую пробку с отверстием посередине. Под пробкой укрепляют медную муфту, к которой присоединяют электрический провод.
Применяемый в приборе электрический провод должен быть тщательно изолирован. Медные муфты и концы проводов обвертывают изоляционной лентой.
При легком нажатии на пробковую ручку верхний электрод должен прикасаться к нижнему и по прекращении нажима должен вернуться в первоначальное положение. Промывную склянку с концентрированной Н2SO4 соединяют с баллоном водорода.
Отводную трубку, проходящую через нижнюю пробку реакционной камеры, соединяют с тройником. Нижнее колено тройника доходит почти до дна склянки, наполовину наполненной водой. К верхнему колену при помощи резиновой трубки с надетым на нее винтовым зажимом I присоединяют короткую латунную трубку, в нижний конец которой вставляют рыхлый тампон стеклянной ваты. Отводную трубку склянки с водой при помощи резиновой трубки с зажимом II соединяют с короткой стеклянной трубкой.
Реакционную смесь готовят растиранием в ступке 6 г ортофосфата кальция, 4 г кварцевого песка и 3 г кокса или древесного угля. После прокаливания на сильном огне в закрытом тигле смесь охлаждают в эксикаторе.
Перед опытом смесь высыпают в тигель электрода и прижимают ее к стенкам таким образом, чтобы посередине смеси, вплоть до нижнего электрода, оставалось пустое пространство в виде конуса.
Вместо колбы с двумя тубусами можно воспользоваться тугоплавкой стеклянной трубкой диаметром около 50 мм. За отсутствием тигля реакционную смесь можно поместить в выемку конической формы глубиной 15 мм, сделанную в верхнем конце нижнего электрода; угольный электрод в этом случае должен иметь диаметр 20 мм. В качестве верхнего электрода пользуются угольным электродом диаметром 5 мм, применяемым для электрической дуги. Опыт проводят в темноте. Закрывают зажим II, открывают зажим I и пропускают через прибор сильный ток водорода. Убедившись в чистоте выходящего из прибора водорода, зажигают его у конца латунной трубки и регулируют ток таким образом, чтобы пламя было спокойным и не очень большим. Включают ток и нажимом на верхний электрод создают электрическую дугу (10-15 с). Через некоторое время пламя водорода окрашивается в изумрудно-зеленый цвет (чтобы заметнее было изменение цвета, в пламя вносят фарфоровую чашку).
Пары образовавшегося в реакционном сосуде белого фосфора уносятся с газами в склянку с водой и здесь конденсируются в виде мелких шариков. Если открыть зажим II и закрыть зажим I, то у конца газоотводной трубки, выходящей из склянки с водой, можно наблюдать холодное пламя фосфора.
Круговыми движениями верхнего электрода в вольтову дугу вносят новые порции реакционной смеси.
Для получения красного фосфора уменьшают ток водорода, чтобы пары фосфора не так быстро выходили из реакционной камеры.
Если выключить дугу, то на внутренних стенках колбы можно заметить налет красного, а на холодных частях стенки — белого фосфора.
Холодное свечение или холодное пламя фосфора наблюдается в течение всего опыта.
После некоторого охлаждения тигля отключают конденсационную склянку, не прекращая тока водорода.
По окончании опыта и полного охлаждения прибора в токе водорода удаляют электроды, а колбу оставляют на некоторое время во влажном воздухе под тягой. Чтобы отмыть колбу, пользуются водой с песком или концентрированной Н2SO4.
Вместо водорода в опыте можно пользоваться углекислым газом, но образование фосфора в этом случае не так эффективно. Холодное свечение или холодное пламя фосфора в этом случае также имеет зеленый цвет.
Мелкие шарики сконденсировавшегося белого фосфора помещают в склянку с холодной водой и хранят для следующих опытов.
Опыт. Получение белого фосфора восстановлением метафосфата натрия порошком алюминия в присутствии двуокиси кремния. Уравнение реакции:
Восстановление ведут при нагревании в тугоплавкой трубке длиной 25 см и диаметром 1-1,5 см, соединенной с одной стороны с источником чистого водорода (баллоном или аппаратом Киппа), а с другой стороны с трубкой, по которой газообразные продукты отводятся в кристаллизатор с водой.
В тугоплавкую трубку насыпают смесь, состоящую из 1 вес. ч. NaРO3, 3 вес. ч. SiO2 и 0,5 вес. ч. алюминиевых опилок. При помощи асбестовых пробок трубку соединяют с одной стороны через промывную склянку, содержащую концентрированную Н2SO4, с источником водорода, а с другой — с отводной трубкой.
Удалив из прибора воздух сильным током водорода и убедившись в чистоте выходящего водорода накаливают тугоплавкую трубку при помощи горелки Теклу с «ласточкиным хвостом». Фосфор, образующийся по приведенной выше реакции, перегоняется и конденсируется в виде мелких шариков в кристаллизаторе с водой. В темноте можно заметить зеленое свечение фосфора в трубке.
По окончании опыта прибор разбирают только после полного его охлаждения в токе водорода.
Полученный фосфор помещают для хранения в банку с холодной водой.
Метафосфат натрия можно получить прокаливанием гидрата гидроортофосфата натрия-аммония; уравнение реакции:
Опыт. Получение небольшого количества белого фосфора из красного. Опыт проводят в пробирке длиной 17-20 см и диаметром 1,5 см в атмосфере углекислого газа.
В пробирку, которую держат в вертикальном положении, вносят 0,3-0,5 г сухого красного фосфора таким образом, чтобы стенки пробирки оставались чистыми.
Пробирку неплотно закрывают резиновой пробкой с доходящей почти до дна стеклянной трубкой, по которой в пробирку поступает слабый ток углекислого газа. После наполнения пробирки углекислым газом стеклянную трубку выдвигают так, чтобы оставшийся в пробирке кончик трубки был не длиннее 5-6 см. Пробирку у самого отверстия закрепляют в зажиме штатива в горизонтальном положении и слегка нагревают ту ее часть, где находится фосфор. При этом наблюдают испарение красного фосфора и осаждение капелек белого фосфора на холодных стенках пробирки.
Осаждение белого фосфора в темноте хорошо заметно благодаря свечению из-за медленного окисления. В темноте же наблюдают и образование холодного пламени (свечения) фосфора у отверстия пробирки. Если опыт проводить при свете, свежеприготовленный белый фосфор частично переходит в красный.
На дне пробирки остаются только содержавшиеся в фосфоре примеси.
По окончании опыта пробирку охлаждают в токе углекислого газа и время от времени постукивают по ней, чтобы облегчить застывание переохлажденного белого фосфора. После охлаждения пробирку с белым фосфором помещают в стакан с водой и нагревают до 50°, чтобы расплавить весь фосфор и собрать его на дне пробирки. После того как белый фосфор застынет, его извлекают охлаждением пробирки струей холодной воды. При получении очень малого количества фосфора его удаляют из пробирки сжиганием или нагреванием с концентрированным раствором щелочи.
Для удаления следов фосфора с трубки, по которой поступал углекислый газ, и резиновой пробки пользуются раствором КМnO4 или АgNO3.
Видео:ФОСФОРНЫЕ экспериментыСкачать

ОЧИСТКА БЕЛОГО ФОСФОРА
Белый фосфор можно очищать перегонкой с парами воды в атмосфере углекислого газа, фильтрованием в безвоздушном пространстве расплавленного в воде фосфора через замшу, обработкой хромовой смесью или гипобромитом натрия с последующим промыванием дистиллированной водой.
Видео:Горение красного фосфораСкачать

ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛОГО ФОСФОРА
Фосфор известен в нескольких аллотропических модификациях: белый, красный, фиолетовый и черный. В лабораторной практике приходится встречаться с белой и красной модификациями.
Белый фосфор — твердое вещество. В обычных условиях он желтоватый, мягкий и по внешнему виду похож на воск. Он легко окисляется и воспламеняется. Белый фосфор ядовит — на коже оставляет болезненные ожоги. В продажу белый фосфор поступает в виде палочек разной длины диаметром 0,5-2 см.
Белый фосфор легко окисляется, и поэтому его хранят под водой в тщательно закупоренных сосудах из темного стекла в мало освещенных и не очень холодных помещениях (во избежание растрескивания банок из-за замерзания воды). Количество кислорода, содержащееся в воде и окисляющее фосфор, очень невелико; оно составляет 7-14 мг на литр воды.
Под воздействием света белый фосфор переходит в красный.
При медленном окислении наблюдается свечение белого фосфора, а при энергичном окислении происходит его воспламенение.
Белый фосфор берут пинцетом или металлическими щипцами; ни в коем случае нельзя дотрагиваться до него руками.
При ожоге белым фосфором промывают обожженное место раствором АgNO3 (1:1) или КМnO4 (1:10) и накладывают мокрую повязку, пропитанную теми же растворами или 5%-ным раствором сульфата меди, затем рану промывают водой и после разглаживания эпидермиса накладывают вазелиновую повязку с метиловым фиолетовым. При тяжелых ожогах обращаются к врачу.
Растворы нитрата серебра, перманганата калия и сульфата меди окисляют белый фосфор и тем прекращают его поражающее действие.
При отравлении белым фосфором принимают внутрь по чайной ложке 2%-ного раствора сульфата меди до появления рвоты. Затем при помощи пробы Митчерлиха на основе свечения устанавливают присутствие фосфора. Для этого к рвоте отравленного добавляют воды, подкисленной серной кислотой, и перегоняют в темноте; при содержании фосфора наблюдают свечение паров. В качестве прибора пользуются колбой Вюрца, к боковой трубке которой присоединяют холодильник Либиха, откуда перегоняемые продукты поступают в приемник. Если пары фосфора направлять в раствор нитрата серебра, то выпадает черный осадок металлического серебра, образующийся по уравнению, приведенному в опыте восстановления солей серебра белым фосфором.
Уже 0,1 г белого фосфора является смертельной дозой для взрослого человека.
Режут белый фосфор ножом или ножницами в фарфоровой ступке под водой. При пользовании водой комнатной температуры фосфор крошится. Поэтому лучше пользоваться теплой водой, но не выше 25-30°. После разрезания фосфора в теплой воде его переносят в холодную воду или охлаждают струей холодной воды.
Белый фосфор — очень огнеопасное вещество. Он воспламеняется при температуре 36-60° в зависимости от концентрации кислорода в воздухе. Поэтому при проведении опытов во избежание несчастного случая необходимо учитывать каждую его крупинку.
Высушивание белого фосфора производят быстрым прикладыванием к нему тонкой асбестовой или фильтровальной бумаги, избегая трения или надавливания.
При воспламенении фосфора его гасят песком, мокрым полотенцем или водой. Если горящий фосфор находится на листе бумаги (или асбеста), этот лист запрещается трогать, так как расплавленный горящий фосфор можно легко разлить.
Белый фосфор плавится при 44°, кипит при 281°. Плавят белый фосфор под водой, так как в соприкосновении с воздухом расплавленный фосфор воспламеняется. Сплавлением и последующим охлаждением белый фосфор можно легко извлечь из отходов. Для этого отходы белого фосфора от различных опытов, собранные в фарфоровом тигле с водой, нагревают на водяной бане. Если на поверхности расплавленного фосфора заметно образование корки, добавляют немного НNО3 или хромовой смеси. Корка окисляется, мелкие крупинки сливаются в общую массу и после охлаждения струей холодной воды получают один кусок белого фосфора.
Остатки фосфора ни в коем случае нельзя бросать в раковину, так как, скопляясь в изгибах колена сточных труб, он может причинить ожоги ремонтным рабочим.
Опыт. Плавление и переохлаждение расплавленного белого фосфора. В пробирку с водой кладут кусочек белого фосфора величиной с горошину. Пробирку помещают в стакан, почти доверху наполненный водой, и укрепляют в вертикальном положении в зажиме штатива. Стакан слегка нагревают и при помощи термометра определяют температуру воды в пробирке, при которой плавится фосфор. После окончания плавления пробирку переносят в стакан с холодной водой и наблюдают застывание фосфора. Если пробирка находится в неподвижном состоянии, то при температуре ниже 44° (вплоть до 30°) белый фосфор остается в жидком состоянии.
Жидкое состояние белого фосфора, охлажденного ниже температуры его плавления, представляет собой состояние переохлаждения.
После окончания опыта, чтобы легче извлечь фосфор, его снова расплавляют и погружают пробирку отверстием вверх в наклонном положении в сосуд с холодной водой.
Опыт. Прикрепление кусочка белого фосфора к концу проволоки. Для плавления и застывания белого фосфора пользуются маленьким фарфоровым тиглем с фосфором и водой; его помещают в стакан с теплой, а затем с холодной водой. Проволоку для этой цели берут железную или медную длиной 25-30 см и диаметром 0,1-0,3 см. При погружении проволоки в застывающий фосфор он легко прикрепляется к ней. В отсутствие тигля пользуются пробиркой. Однако из-за недостаточно ровной поверхности пробирки иногда приходится ее разбивать, чтобы извлечь фосфор. Для удаления белого фосфора с проволоки ее погружают в стакан с теплой водой.
Опыт. Определение удельного веса фосфора. При 10° удельный вес фосфора равен 1,83. Опыт позволяет убедиться, что белый фосфор тяжелее воды и легче концентрированной Н2SO4.
При введении небольшого кусочка белого фосфора в пробирку с водой и концентрированной Н2SO4 (уд. вес 1,84) наблюдают, что фосфор в воде тонет, но плавает на поверхности кислоты, расплавляясь за счет тепла, выделяемого при растворении концентрированной Н2SO4 в воде.
Для наливания концентрированной Н2SO4 в пробирку с водой пользуются воронкой с длинной и узкой шейкой, доходящей до конца пробирки. Наливать кислоту и вынимать воронку из пробирки следует осторожно, чтобы не вызвать перемешивания жидкостей.
По окончании опыта содержимое пробирки перемешивают стеклянной палочкой и охлаждают извне струей холодной воды до тех пор, пока не застынет фосфор, чтобы можно было его извлечь из пробирки.
При пользовании красным фосфором наблюдают, что он тонет не только в воде, но и в концентрированной Н2SO4, так как его удельный вес (2,35) больше удельного веса как воды, так и концентрированной серной кислоты.
Видео:Химия 9 класс (Урок№16 - Фосфор. Аллотропия фосфора. Свойства фосфора. Оксид фосфора(V).)Скачать

СВЕЧЕНИЕ БЕЛОГО ФОСФОРА
Из-за медленного окисления, протекающего даже при обычной температуре, белый фосфор светится в темноте (отсюда и название «светоносный»). Вокруг кусочка фосфора в темноте появляется зеленоватое светящееся облачко, которое при колебании фосфора приводится в волнообразное движение.
Фосфоресценция (свечение фосфора) объясняется медленным окислением кислородом воздуха паров фосфора до фосфористого и фосфорного ангидрида с выделением света, но без выделения тепла. При этом выделяется озон, а воздух вокруг ионизируется (см. опыт, показывающий медленное горение белого фосфора).
Фосфоресценция зависит от температуры и концентрации кислорода. При 10° и нормальном давлении фосфоресценция протекает слабо, а в отсутствие воздуха не происходит вовсе.
Вещества, реагирующие с озоном (Н2S, SO2, Сl2, NН3, С2Н4, скипидарное масло), ослабляют или вовсе прекращают фосфоресценцию.
Превращение химической энергии в световую называется «хеми-люминесценцией».
Опыт. Наблюдение свечения белого фосфора. Если наблюдать в темноте за кусочком белого фосфора, находящегося в стакане и не полностью покрытого водой, то заметно зеленоватое свечение. В этом случае влажный фосфор медленно окисляется, но не воспламеняется, так как температура воды ниже точки воспламенения белого фосфора.
Свечение белого фосфора можно наблюдать после того, как кусочек белого фосфора непродолжительное время побудет на воздухе. Если в колбу на стеклянную вату положить несколько кусочков белого фосфора и наполнить колбу углекислым газом, опустив конец отводной трубки на дно колбы под стеклянную вату, а затем колбу слегка нагреть, опустив ее в сосуд с теплой водой, то в темноте можно наблюдать образование холодного бледного зеленоватого пламени (можно безопасно внести в него руку).
Образование холодного пламени объясняется тем, что выходящий из колбы углекислый газ увлекает пары фосфора, которые начинают окисляться при соприкосновении с воздухом у отверстия колбы. В колбе белый фосфор не воспламеняется, ибо находится в атмосфере углекислого газа. По окончании опыта колбу наполняют водой.
При описании опыта получения белого фосфора в атмосфере водорода или углекислого газа уже упоминалось, что проведение этих опытов в темноте позволяет наблюдать свечение белого фосфора.
Если фосфорным мелом сделать надпись на стене, листе картона или бумаги, то благодаря фосфоресценции надпись длительное время остается заметной в темноте.
Такую надпись нельзя делать на классной доске, так как после этого к ней не пристает обыкновенный мел и доску приходится мыть бензином или другим растворителем стеарина.
Фосфорный мел получают растворением жидкого белого фосфора в расплавленном стеарине или парафине. Для этого в пробирку к одной весовой части сухого белого фосфора добавляют приблизительно две весовые части стеарина (кусочков свечи) или парафина, закрывают пробирку ватой, чтобы предохранить от поступления кислорода, и нагревают при непрерывном взбалтывании. После окончания плавления пробирку охлаждают струей холодной воды, затем разбивают пробирку и извлекают застывшую массу.
Фосфорный мел хранят под водой. При пользовании кусочек такого мела обертывают мокрой бумагой.
Фосфорный мел можно также получить внесением небольших кусочков просушенного белого фосфора в расплавленный в фарфоровой чашке парафин (стеарин). Если при внесении фосфора парафин воспламенится, его гасят, накрывая чашку куском картона или асбеста.
После некоторого охлаждения раствор фосфора в парафине разливают в сухие и чистые пробирки и охлаждают струей холодной воды до тех пор, пока он не застынет в твердую массу.
После этого разбивают пробирки, извлекают мел и хранят его под водой.
Видео:Как горит белый фосфор и насколько он опасен?Скачать

РАСТВОРИМОСТЬ БЕЛОГО ФОСФОРА
В воде белый фосфор труднорастворим, слабо растворяется в спирте, эфире, бензоле, ксилоле, йодистом метиле и глицерине; хорошо растворяется в сероуглероде, хлористой сере, треххлористом и трех-бромистом фосфоре, четыреххлористом углероде.
Опыт. Растворение белого фосфора в сероуглероде. Сероуглерод — бесцветная, очень летучая, легко воспламеняющаяся, ядовитая жидкость. Поэтому при работе с ней избегают вдыхать ее пары и выключают все газовые горелки.
Три-четыре кусочка белого фосфора величиной с горошину растворяют при легком взбалтывании в стакане с 10-15 мл сероуглерода.
Если небольшой листок фильтровальной бумаги смочить этим раствором и подержать на воздухе, бумага через некоторое время воспламеняется. Это происходит потому, что сероуглерод быстро испаряется, а оставшийся на бумаге тонко измельченный белый фосфор быстро окисляется при обычной температуре и воспламеняется вследствие выделяющегося при окислении тепла. (Известно, что температура воспламенения различных веществ зависит от степени их измельчения.) Бывает, что бумага не воспламеняется, а только обугливается. Бумагу, смоченную раствором фосфора в сероуглероде, держат на воздухе при помощи металлических щипцов.
Опыт проводят осторожно, чтобы капли раствора фосфора в сероуглероде не попали на пол, на стол, на одежду или на руки.
При попадании раствора на руку ее быстро моют водой с мылом, а затем раствором КМnO4 (чтобы окислить попавшие на руки частицы белого фосфора).
Оставшийся после опытов раствор фосфора в сероуглероде в лаборатории не хранят, так как он легко может воспламениться.
Видео:Взаимодействие красного фосфора с хлоромСкачать

ПРЕВРАЩЕНИЕ БЕЛОГО ФОСФОРА В КРАСНЫЙ
Белый фосфор превращается в красный по уравнению:
Процесс превращения белого фосфора в красный значительно ускоряется при нагревании, под действием света и в присутствии следов иода (1 г иода на 400 г белого фосфора). Иод, соединяясь с фосфором, образует йодистый фосфор, в котором белый фосфор растворяется и быстро превращается в красный с выделением тепла.
Красный фосфор получают при длительном нагревании белого фосфора в замкнутом сосуде в присутствии следов иода до 280-340°
При длительном хранении белого фосфора на свету он постепенно превращается в красный.
Опыт. Получение небольшого количества красного фосфора из белого. В закрытую на одном конце стеклянную трубку длиной 10-12 см и диаметром 0,6-0,8 см вводят кусочек белого фосфора величиной с пшеничное зерно и очень маленький кристаллик иода. Трубку запаивают и подвешивают в воздушной бане над подносом с песком, затем нагревают до 280-340° и наблюдают превращение белого фосфора в красный.
 |
Частичное превращение белого фосфора в красный можно также наблюдать при слабом нагревании пробирки с небольшим кусочком белого фосфора и очень маленьким кристалликом иода. Перед началом нагревания пробирку закрывают тампоном из стеклянной (асбестовой или обычной) ваты и подставляют под пробирку поднос с песком. Пробирку нагревают в течение 10-15 минут (не доводя фосфор до кипения) и наблюдают превращение белого фосфора в красный.
Оставшийся в пробирке белый фосфор можно удалить нагреванием с концентрированным раствором щелочи или сжиганием.
Превращение белого фосфора в красный можно также наблюдать при нагревании в пробирке небольшого кусочка фосфора в атмосфере углекислого газа до температуры ниже кипения.
Видео:РЕАКЦИЯ КАЛЬЦИЯ С ФОСФОРОМ - НПО ДУСТХИМПРОМСкачать

ГОРЕНИЕ БЕЛОГО ФОСФОРА
При горении белого фосфора образуется фосфорный ангидрид:
Можно наблюдать горение фосфора на воздухе (медленное и быстрое) и под водой.
Опыт. Медленное горение белого фосфора и состав воздуха. Этот опыт не был описан как способ получения азота, так как он не позволяет полностью связать кислород, содержащийся в воздухе.
Медленное окисление белого фосфора кислородом воздуха происходит в две стадии; на первой стадии образуются фосфористый ангидрид и озон по уравнениям:
Во второй стадии фосфористый ангидрид окисляется до фосфорного ангидрида.
Медленное окисление белого фосфора сопровождается свечением и ионизацией окружающего воздуха.
Опыт, показывающий медленное горение белого фосфора, должен продолжаться не менее трех часов. Необходимый для опыта прибор изображен на рис.
 Прибор для медленного окисления белого фосфора |
 |
В расширенный у отверстия цилиндр, почти наполненный водой, опускают в перевернутом положении градуированную трубку с закрытым концом, содержащую около 10 мл воды. Длина трубки 70 см, диаметр 1,5-2 см. После опускания градуированной трубки отводят от отверстия трубки палец, приводят воду в трубке и цилиндре к одинаковому уровню и отмечают объем воздуха, содержащегося в трубке. Не поднимая трубки выше уровня воды в цилиндре (чтобы не впустить дополнительное количество воздуха), вводят в воздушное пространство трубки закрепленный на конце проволоки кусочек белого фосфора.
Через три-четыре часа или даже через два-три дня отмечают поднятие воды в трубке.
По окончании опыта вынимают из трубки проволоку с фосфором (не поднимая трубки выше уровня воды в цилиндре), приводят воду в трубке и цилиндре к одинаковому уровню и отмечают объем воздуха, оставшийся после медленного окисления белого фосфора.
Опыт показывает, что в результате связывания фосфором кислорода объем воздуха уменьшился на одну пятую, что соответствует содержанию кислорода в воздухе.
Чтобы сохранить фосфор, вынутую из трубки проволоку с фосфором сразу же опускают в сосуд с водой.
Опыт. Быстрое горение белого фосфора. Ввиду того что при реакции соединения фосфора с кислородом выделяется большое количество тепла, на воздухе белый фосфор самовоспламеняется и сгорает ярким желтовато-белым пламенем, образуя фосфорный ангидрид — твердое белое вещество, очень энергично соединяющееся с водой.
 Горение белого фосфора |
Ранее уже упоминалось о том, что белый фосфор воспламеняется при 36-60°. Чтобы наблюдать за его самовоспламенением и сгоранием, кусочек белого фосфора кладут на лист асбеста и прикрывают стеклянным колоколом или большой воронкой, на шейку которой надевают пробирку.
Фосфор легко можно поджечь стеклянной палочкой, нагретой в горячей воде.
Опыт. Сравнение температур воспламенения белого и красного фосфора. На один конец медной пластинки (длиной 25 см, шириной 2,5 см и толщиной 1 мм) кладут небольшой кусочек просушенного белого фосфора, на другой конец насыпают небольшую кучку красного фосфора. Пластинку кладут на треножник и одновременно к обоим концам пластинки подносят приблизительно одинаково горящие газовые горелки.
Белый фосфор воспламеняется немедленно, а красный только тогда, когда его температура достигнет приблизительно 240°.
Опыт. Воспламенение белого фосфора под водой. Пробирку с водой, в которой находится несколько небольших кусочков белого фосфора, опускают в стакан с горячей водой. Когда вода в пробирке нагреется до 30-50°, в нее по трубке начинают пропускать ток кислорода. Фосфор воспламеняется и сгорает, разбрасывая яркие искры.
Если опыт проводится в самом стакане (без пробирки), стакан помещают на треножник, установленный на подносе с песком.
 Горение белого фосфора, который разлился из железнодорожных цистерн во время аварии в Львовской области (Украина) [rulez-t.info] Видео:Белый фосфор - ужасен![NileRed]Скачать ![Белый фосфор - ужасен![NileRed]](https://i.ytimg.com/vi/I_bVnvr_ut8/0.jpg) ВОССТАНОВЛЕНИЕ СОЛЕЙ СЕРЕБРА И МЕДИ БЕЛЫМ ФОСФОРОМОпыт. При внесении кусочка белого фосфора в пробирку с раствором нитрата серебра наблюдают выпадение осадка металлического серебра (белый фосфор является энергичным восстановителем): Если белый фосфор внести в пробирку с раствором сульфата меди, то выпадает металлическая медь: Видео:Галилео. Эксперимент. Воспламенение фосфораСкачать  КРАСНЫЙ ФОСФОРСпособы получения красного фосфора из белого описаны выше. Видео:Опыты по химии. Получение и обнаружение следовых количеств белого фосфораСкачать  ПРИМЕСИКрасный фосфор содержит следы белого фосфора, фосфорной и пирофосфорной кислот. Присутствие фосфорной кислоты объясняется соединением фосфорного ангидрида с влагой воздуха, а образование фосфорного ангидрида — медленным окислением следов белого фосфора. При окислении влажного фосфора кислородом кроме фосфористого и фосфорного ангидридов образуется также и фосфорноватистая кислота.
|