| Ацетат кальция | |
|---|---|
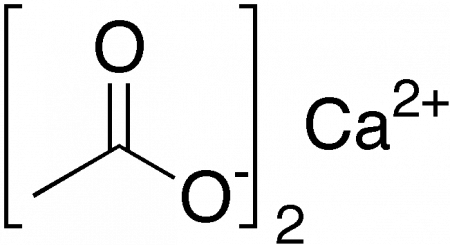 | |
| Систематическое наименование | Ацетат кальция |
| Сокращения | Ca(OAc)2 |
| Традиционные названия | Пригорело-древесная соль |
| Хим. формула | Ca(CH3COO)2 |
| Рац. формула | CaC4H6O4 |
| Состояние | твёрдое |
| Молярная масса | 158.138 г/моль |
| Плотность | 1.6 г/см³ |
| Температура | |
| • плавления | 160 (с разложением) |
| • разложения | 160 ± 1 °C |
| Растворимость | |
| • в воде | 40 г/100 мл |
| Рег. номер CAS | 62-54-4 |
| PubChem | 6116 |
| Рег. номер EINECS | 200-540-9 |
| SMILES | |
| Кодекс Алиментариус | E263 |
| RTECS | AF7525000 |
| ChEBI | 3310 |
| ChemSpider | 5890 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат кальция — кальциевая соль уксусной кислоты. Бесцветное кристаллическое или аморфное вещество, хорошо растворимое в воде. Технический моногидрат может быть в форме гранул или некрупных игл. Обладает слабым вкусом и запахом уксуса. Химическая формула — Ca(CH3COO)2, однако чаще получают его моногидрат Ca(CH3COO)2•H2O.
- Содержание
- История названия
- Получение
- Применение
- Пищевая промышленность
- Медицина
- Ацетат кальция
- Получение ацетата кальция
- Применение ацетата кальция в пищевой промышленности
- Вред ацетат кальция – пищевого консерванта Е263
- Acetyl
- Кальций: способы получения и химические свойства
- Способ получения
- Качественная реакция
- Химические свойства
Содержание
- 1 История названия
- 2 Получение
- 3 Применение
- 3.1 Пищевая промышленность
- 4 Медицина
История названия
Пригорело-древесная соль — старинное название ацетата кальция — в старину получалась при сухой перегонке древесины, из-за чего древесина, естественно, обугливалась, «пригорала». Из-за того, что метод сухой перегонки древесины использовался алхимиками с незапамятных времён, установить человека, давшего такое название этой соли или впервые получившего её, невозможно.
Получение
В лаборатории получают действием уксусной кислоты на карбонат, оксид или гидроксид кальция.
Применение
Не имеет промышленного применения.
Используется в лаборатории для получения диметилкетона (ацетона). Эту реакцию осуществляют, нагревая ацетат кальция до 160 °С:
Именно из-за этой реакции ацетат кальция нельзя хранить или сушить вблизи открытого огня, а помещения, в которых происходят работы с ацетатом кальция, должны быть оборудованы приточно-вытяжной вентиляцией.
Также может применяться в лаборатории для получения сложных эфиров уксусной кислоты — алкилацетатов:
Также ацетат кальция используется для получения ацетата калия обменными реакциями из карбоната и/или бикарбоната калия:
Также ацетат кальция применяют при получении лавсана в качестве катализатора.
Ещё одним способом применения ацетата кальция является приготовление аналога сухого спирта — твёрдого спиртового сольвата ацетата кальция — при смешивании ацетата кальция и этилового спирта.
Пищевая промышленность
Ацетат кальция зарегистрирован в пищевой промышленности в качестве пищевой добавки группы консервантов E263. Может применяться как консервант, регулятор кислотности, уплотнитель растительных тканей. Останавливает развитие болезнетворных бактерий в хлебобулочных изделиях, смягчает ярко выраженный кислый вкус консервированных овощей и фруктов. В сельскохозяйственной промышленности используется для консервации кормов. Так как действие ацетата кальция ограничено наличием в продуктах сульфатов, фосфатов, карбонатов и гидрокарбонатов, которые в конечном итоге дают осадки с катионом Ca 2+ , то применять его лучше в сочетании с другими консервантами.
| Массовая доля основного вещества,безводная форма, %, не менее | 98 |
| Потери при просушке, %, не более | 11 |
| pH 10%-го водного раствора | 6-9 (включительно) |
| Массовая доля нерастворимых веществ, %, не более | 0,3 |
Медицина
Ацетат кальция оказывает абсорбирующее действие на анионы фосфорных кислот:
Также ацетат кальция восстанавливает положительный кальциевый баланс у больных с почечной недостаточностью в легкой, средней и тяжелой форме и у больных, находящихся на гемодиализе или перитонеальном диализе. Является безалюминиевым и безмагниевым фосфат-связывающим препаратом (фосфат-биндером). Фосфат-связывающая способность ацетата кальция в 2 раза выше, а всасываемость его в кишечнике значительно меньше, чем у кальция карбоната.
Ацетат кальция
Ацетат кальция является химическим соединением – кальциевой солью уксусной кислоты, представляющей собой хорошо растворимое в воде бесцветное кристаллическое вещество с химической формулой (CH3COO)2Ca.
Ацетат кальция применяют:
- В химической промышленности – при производстве ацетона;
- В пищевой промышленности в качестве консерванта;
- При производстве кормов;
- В фармакологическом производстве – при производстве дезинфицирующих средств с сильными антимикробными и противовирусными свойствами.
Получение ацетата кальция
Раньше это соединение имело название «пригорело-древесная соль». Это было связано со способом получения ацетата кальция, для чего использовали сухую перегонку древесины, вызывающую в большинстве случаев обугливание или пригорание.
В промышленных масштабах это соединение не производят. В лабораторных условиях получение ацетата кальция происходит воздействием уксусной кислоты на гидроксид, оксид или карбонат кальция.
Применение ацетата кальция в пищевой промышленности
Ацетат кальция (Е263) относится к группе пищевых консервантов с индексом от E-200 до E-299, которые применяют для увеличения срока хранения продуктов, что происходит благодаря подавлению роста и размножения бактерий или грибков.

Помимо увеличения срока хранения, ацетат кальция также применяют в качестве регулятора кислотности и уплотнителя растительных тканей. Это соединение смягчает природный кислый вкус некоторых продуктов питания.
Наиболее широкое применение ацетат кальция (Е263) получил при производстве хлебобулочных изделий как средство для борьбы с «картофельной болезнью».
Данное заболевание чаще всего развивается в пшеничном хлебе на фоне сниженной кислотности и повышенной влажности при длительном хранении в теплом помещении, что способствует образованию в хлебе чрезмерного количества декстринов, альдегидов и других соединений с неприятным резким запахом. От этого мякоть хлеба становится липкой, что делает его непригодным для употребления в пищу.
Предотвратить развитие «картофельной болезни» в готовом хлебе невозможно, поскольку споры картофельной палочки термостойки. Поэтому ацетат кальция добавляют в муку в процессе замешивания теста.
Вред ацетат кальция – пищевого консерванта Е263
Доказано, что Е263 не оказывает канцерогенное, токсичное или ядовитое воздействие на человеческий организм. Однако основной вред этого пищевого консерванта заключается в его химическом составе, который небезопасен для людей с непереносимостью пищевых добавок.
Также согласно многим исследованиям ацетат кальция является мощным аллергеном, способным провоцировать приступы удушья и стойкие аллергические реакции. Однако исследованиями не выявлены предельно допустимые нормы ежедневного потребления Е263 в составе продуктов питания.
Таким образом, ацетат кальция в составе продуктов питания представляет опасность для людей с:
- Индивидуальной непереносимостью пищевых добавок;
- Аллергическими болезнями.
Также медики советуют родителям стараться исключать из детского рациона питания продукты, содержащие этот небезопасный консервант.
Нашли ошибку в тексте? Выделите ее и нажмите Ctrl + Enter.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Кальций: способы получения и химические свойстваКальций Ca — это щелочноземельный металл, серебристо-белый, пластичный, достаточно твердый. Реакционноспособный. Сильный восстановитель. Относительная молекулярная масса Mr = 40,078; относительная плотность для твердого и жидкого состояния d = 1,54; tпл = 842º C; tкип = 1495º C. Способ получения1. В результате электролиза жидкого хлорида кальция образуются кальций и хлор : 2. Хлорид кальция взаимодействует с алюминием при 600 — 700º С образуя кальций и хлорид алюминия: 3CaCl2 + 2Al = 3Ca + 2AlCl3 3. В результате разложения гидрида кальция при температуре выше 1000º С образуется кальций и водород: 4. Оксид кальция взаимодействует с алюминием при 1200º С и образует кальций и алюминат кальция: 4CaO + 2Al = 3Ca + Ca(AlO2)2 Качественная реакцияКальций окрашивает пламя газовой горелки в коричнево-красный цвет. Химические свойства1. Кальций — сильный восстановитель . Поэтому он реагирует почти со всеми неметаллами : 1.1. Кальций взаимодействует с азотом при 200 — 450º С образуя нитрид кальция: 1.2. Кальций сгорает в кислороде (воздухе) при выше 300º С с образованием оксида кальция: 2Ca + O2 = 2CaO 1.3. Кальций активно реагирует при температуре 200 — 400º С с хлором, бромом и йодом . При этом образуются соответствующие соли : 1.4. С водородом кальций реагирует при температуре 500 — 700º C с образованием гидрида кальция: 1.5. В результате взаимодействия кальция и фтора при комнатной температуре образуется фторид кальция: 1.6. Кальций взаимодействует с серой при 150º С и образует сульфид кальция: Ca + S = CaS 1.7. В результате реакции между кальцием и фосфором при 350 — 450º С образуется фосфид кальция: 1.8. Кальций взаимодействует с углеродом (графитом) при 550º С и образует карбид кальция: Ca + 2C = CaC2 2. Кальций активно взаимодействует со сложными веществами: 2.1. Кальций при комнатной температуре реагирует с водой . Взаимодействие кальция с водой приводит к образованию гидроксида кальция и газа водорода: 2.2. Кальций взаимодействует с кислотами: 2.2.1. Кальций реагирует с разбавленной соляной кислотой, при этом образуются хлорид кальция и водород : Ca + 2HCl = CaCl2 + H2 ↑ 2.2.2. Реагируя с разбавленной азотной кислотой кальций образует нитрат кальция, оксид азота (I) и воду: если азотную кислоту еще больше разбавить, то образуются нитрат кальция, нитрат аммония и вода: 2.3. Кальций вступает в реакцию с газом аммиаком при 600 — 650º С. В результате данной реакции образуется нитрид кальция и гидрид кальция: если аммиак будет жидким, то в результате реакции в присутствии катализатора платины образуется амид кальция и водород: |


