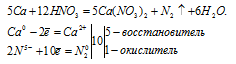Оксид железа (II, III)
Оксид железа (II, III) (железная окалина, магнетит) – это твердое, нерастворимое в воде вещество черного цвета.
Фото с сайта wikipedia.ru
Способы получения
Оксид железа (II, III) можно получить различными методами :
1. Горение железа на воздухе:
2. Частичное восстановление оксида железа (III) водородом или угарным газом :
3. При высокой температуре раскаленное железо реагирует с водой, образуя двойной оксид железа (II, III):
Химические свойства
Свойства оксида железа (II, III) определяются свойствами двух оксидов, из которых он состоит: основного оксида железа (II) и амфотерного оксида железа (III).
1. При взаимодействии оксида железа (II, III) с кислотными оксидами и кислотами образуются соли железа (II) и железа (III).
Например , оксид железа (II, III) взаимодействует с соляной кислотой. При это образуются две соли – хлорид железа (II) и хлорид железа (III):
Еще пример : оксид железа (II, III) взаимодействует с разбавленной серной кислотой.
2. Оксид железа (II, III) взаимодействует с сильными кислотами-окислителями (серной-концентрированной и азотной).
Например , железная окалина окисляется концентрированной азотной кислотой:
Разбавленной азотной кислотой окалина окисляется при нагревании:
Также оксид железа (II, III) окисляется концентрированной серной кислотой:
Также окалина окисляется кислородом воздуха :
3. Оксид железа (II, III) не взаимодействует с водой.
4. Оксид железа (II, III) окисляется сильными окислителями до соединений железа (VI), как и прочие оксиды железа (см. выше).
5. Железная окалина проявляет окислительные свойства .
Например , оксид железа (II, III) реагирует с угарным газом при нагревании. При этом возможно восстановление как до чистого железа, так и до оксида железа (II):
Также железная окалина восстанавливается водородом:
Оксид железа (II, III) реагирует с более активными металлами .
Например , с алюминием (алюмотермия):
Оксид железа (II, III) реагирует также с некоторыми другими сильными восстановителями (йодидами и сульфидами).
Например , с йодоводородом:
Окислительно-восстановительные свойства металлов. Ряд напряжения металлов
Вопрос 1.
Уравнение реакции образования железной окалины имеет вид:
Fe3O4 — представляет собой смесь двух оксидов FeO и Fe2O3. Поэтому уравнение реакции (І) можно условно представить в виде двух уравнений и для каждого составить уравнение электронного баланса.
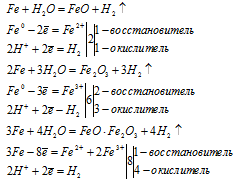
Таким образом, в реакции образования железной окалины три атома железа отдают не 6 и не 9, а 8 электронов.
Вопрос 2.
Вопрос 3.
Вопрос 4.
Щелочные и щелочноземельные металлы очень активны и реагируют практически со всем, с чем соприкасаются. Например, на воздухе эти металлы легко окисляются и, при этом разрушаются. Их хранят под слоем керосина, к которому они инертны, этим они сберегаются от ненужных взаимодействий. Литий — самый легкий из металлов. Он легче керосина и в отличие от других металлов всплывает в нем, поэтому его хранят в вазелине.
Вопрос 5.
Вопрос 6.
По правилу, которое гласит, что металлы, стоящие в ряду напряжения левее водорода, вытесняют его из растворов кислот, водород при реакции свинца с раствором серной кислоты должен получиться. Но данное правило соблюдается, если в реакции металла с кислотой образуется растворимая соль, а так как PbSO4 — нерастворимая соль то правило не соблюдается, и водород нельзя получить при взаимодействии свинца с раствором серной кислоты.
Вопрос 7. 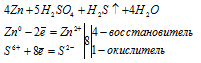
В данной реакции цинк проявляет восстановительные свойства, а сера – окислительные.
Оксид железа (II,III)
| Оксид железа (II,III) | |
|---|---|
| Систематическое наименование | Оксид железа (II,III) |
| Традиционные названия | закись-окись железа, железная окалина, магнетит, магнитный железняк |
| Хим. формула | Fe3O4 |
| Состояние | чёрные кристаллы |
| Молярная масса | 231,54 г/моль |
| Плотность | 5,11; 5,18 г/см³ |
| Твёрдость | 5,6-6,5 |
| Температура | |
| • плавления | разл. 1538; 1590; 1594 °C |
| Мол. теплоёмк. | 144,63 Дж/(моль·К) |
| Энтальпия | |
| • образования | −1120 кДж/моль |
| Рег. номер CAS | 1317-61-9 |
| PubChem | 16211978 |
| Рег. номер EINECS | 215-277-5 |
| SMILES | |
| ChEBI | CHEBI:50821 |
| ChemSpider | 17215625 , 21169623 и 21250915 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Оксид железа (II,III), закись-окись железа, железная окалина — неорганическое соединение, двойной оксид металла железа с формулой Fe3O4 или FeO·Fe2O3, чёрные кристаллы, не растворимые в воде, образует кристаллогидрат.
Содержание
- 1 Получение
- 2 Физические свойства
- 3 Химические свойства
- 4 Применение
Получение
- В природе встречаются большие залежи минерала магнетита (магнитного железняка) — Fe3O4 с различными примесями.
- Сжигание порошкообразного железа на воздухе:
3Fe + 2O2 → 150−600oC Fe3O4
- Действие перегретого пара на железо:
3Fe + 4H2O → 800oC Fe3O4 + 4H2
- Осторожное восстановление оксида железа (III) водородом:
3Fe2O3 + H2 → 400oC 2 Fe3O4 + H2O
Физические свойства
Оксид железа (II,III) при комнатной температуре образует чёрные кристаллы кубической сингонии, пространственная группа F d3m, параметры ячейки a = 0,844 нм , Z = 8 (структура шпинели). При 627 °С α -форма переходит в β -форму. При температуре ниже 120—125 К существует моноклинная форма.
Ферромагнетик с точкой Кюри 858 К (585 °С).
Обладает электрической проводимостью. Полупроводник. Электропроводность низкая. Истинная удельная электропроводность монокристаллического магнетита максимальна при комнатной температуре ( 250 Ом −1 ·см −1 ), она быстро снижается при понижении температуры, достигая значения около 50 Ом −1 ·см −1 при температуре перехода Вервея (фазового перехода от кубической к низкотемпературной моноклинной структуре, существующей ниже TV = 120—125 К ). Электропроводность моноклинного низкотемпературного магнетита на 2 порядка ниже, чем кубического (
1 Ом −1 ·см −1 при TV ); она, как и у любого типичного полупроводника, очень быстро уменьшается с понижением температуры, достигая нескольких единиц ×10 −6 Ом −1 ·см −1 при 50 К . При этом моноклинный магнетит, в отличие от кубического, проявляет существенную анизотропию электропроводности — проводимость вдоль главных осей может отличаться более чем в 10 раз . При 5,3 К электропроводность достигает минимума
10 −15 Ом −1 ·см −1 и растёт при дальнейшем понижении температуры. При температуре выше комнатной электропроводность медленно уменьшается до ≈180 Ом −1 ·см −1 при 780—800 К , а затем очень медленно растёт вплоть до температуры разложения.
Кажущаяся величина электропроводности поликристаллического магнетита в зависимости от наличия трещин и их ориентировки может отличаться в сотни раз.
Образует кристаллогидрат состава Fe3O4·2H2O.