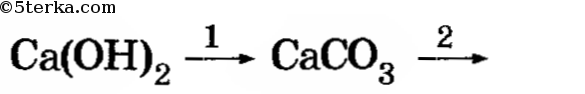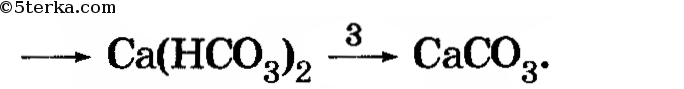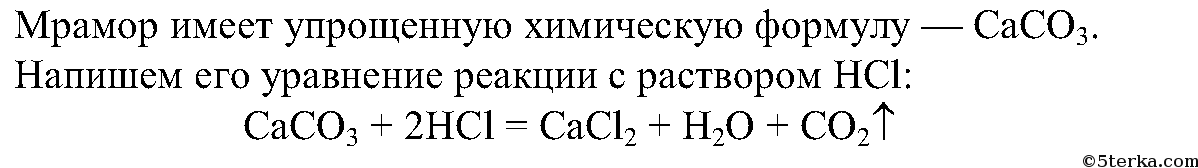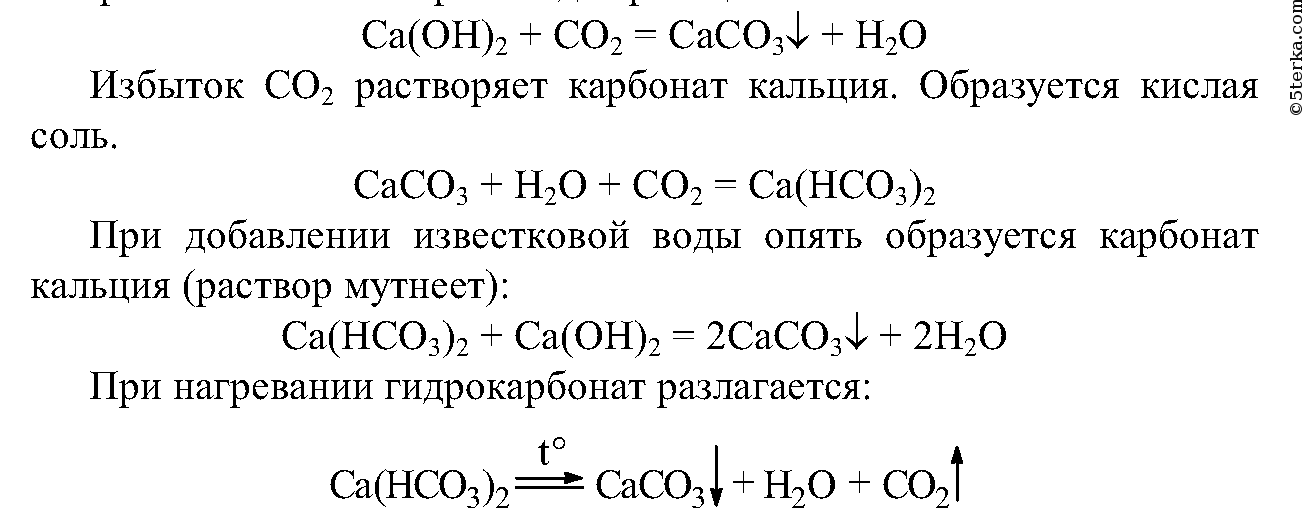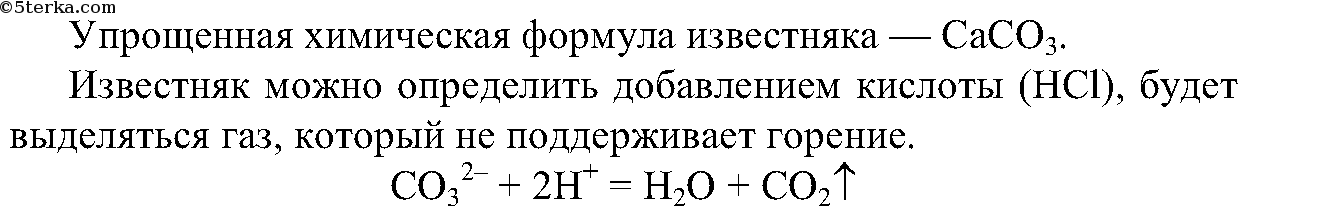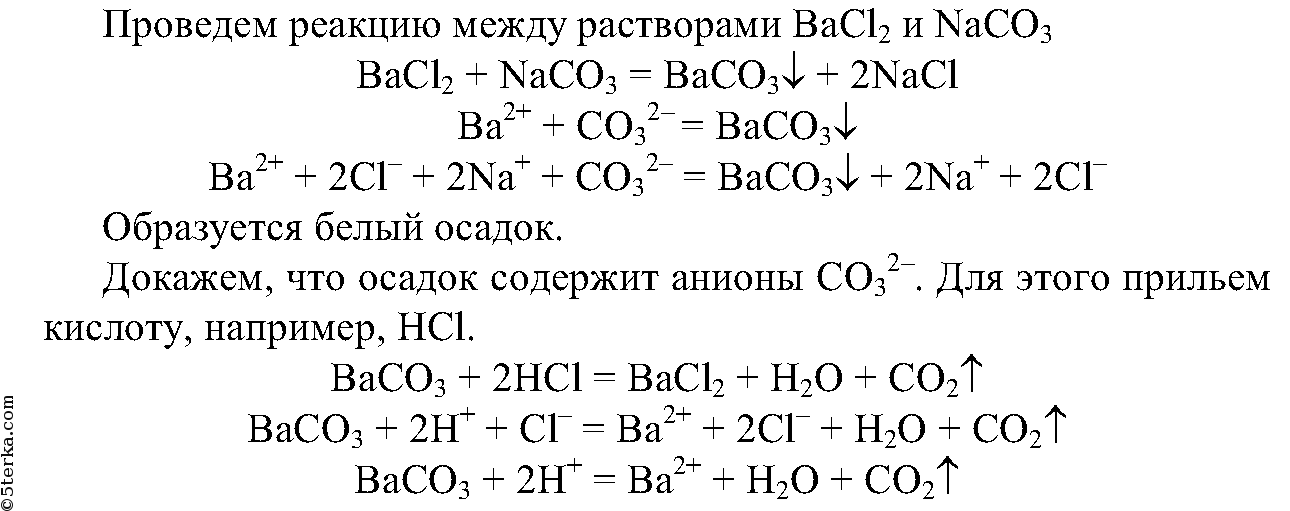Задания. 1. Получите углекислый газ взаимодействием мрамора с соляной кислотой.
2. Изучите некоторые физические свойства диоксида углерода (IV) (цвет, запах, растворимость в воде, относительную плотность).
3. а) Изучите взаимодействие углекислого газа с водой;б) осуществите следующие превращения;
4. Распознайте известняк среди выданных образцов минералов.
5. Получите карбонат бария с помощью реакции обмена.
Оборудование. Прибор для получения газов, заправленный кусочками мрамора и соляной кислотой, лабораторный штатив, штатив с пробирками, пипетки, стаканы на 150 мл (2 шт.), картонный кружок для стакана, пробиркодержатели (2 шт.), нагревательный прибор.
Вещества. 10%-е растворы карбоната натрия и хлорида бария, 10%-я соляная кислота, известковая вода, раствор лакмуса, дистиллированная вода, минералы гипс, каолин, известняк, кварц.
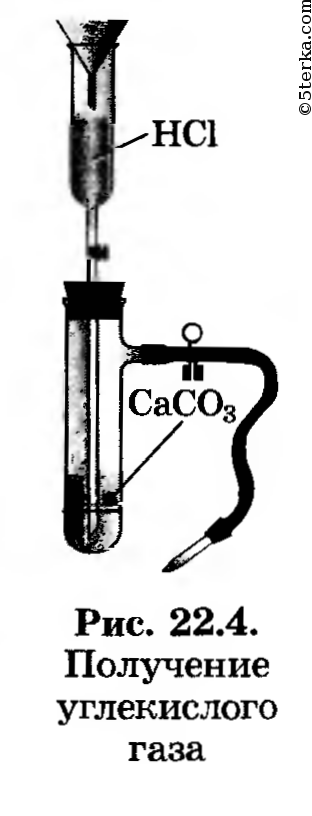
1. Получение оксида углерода (IV). Зарядите прибор для получения углекислого газа (рис. 22.4). Получите углекислый газ, соберите его в химический стакан и прикройте картонным кружком. (Для чего?)
2. Изучение свойств оксида углерода (IV). Внесите в стакан горящую спичку. Что наблюдаете? «Перелейте» содержимое в другой стакан. Убедитесь с помощью горящей спички, что углекислый газ действительно «перелился» из одного стакана в другой.
Какое свойство углекислого газа лежит в основе этого опыта? Опишите физические свойства исследуемого газа.
Налейте в пробирку (на 1 /4 ее объема) дистиллированную воду, подкрасьте ее фиолетовым раст
вором лакмуса и пропускайте через эту воду углекислый газ до изменения окраски индикатора. Почему изменилась окраска лакмуса? Составьте уравнение соответствующей реакции. Нагрейте содержимое пробирки до начала кипения. Почему снова изменился цвет лакмуса? Объясните это с помощью уравнения реакции.
3. Прилейте в пробирку (на 1/4 ее объема) известковую воду и пропускайте через нее углекислый газ. Что вы наблюдаете? Где используется в практике эта реакция? Продолжайте пропускать углекислый газ через мутную смесь до полного осветления раствора. Что произошло? Составьте уравнения наблюдаемых реакций.
Содержимое пробирки с полученным гидрокарбонатом кальция разделите на две равные части. В одну пробирку добавьте известковую воду, а другую нагрейте до начала кипения раствора. Что вы наблюдаете? Объясните происходящее явление с помощью уравнений реакций. Сделайте выводы: а) каким образом карбонаты можно превратить в гидрокарбонаты;б) как можно гидрокарбонаты превратить в карбонаты.
4. Из выданных вам минералов с помощью химических реакций определите известняк. Составьте ионные уравнения проделанной реакции.
5. Получите реакцией обмена карбонат бария. Опытным путем докажите, что выпавший осадок действительно является карбонатом. Составьте полные и сокращенные ионные уравнения проделанных реакций.
Картонным кружком стакан прикрывают для того, чтобы не улетучивался углекислый газ.
При внесении в стакан с углекислым газом спичка тухнет, т.к. углекислый газ не поддерживает горения. Углекислый газ можно переливать из одного стакан в другой, т.к. он тяжелее воздуха и оседает на дне.
Наблюдается помутнение раствора, на практике это используется при побелке стен. Происходит реакция:
а) карбонаты можно перевести в гидрокарбонаты, пропуская через них углекислый газ;
б) гидрокарбонаты можно перевести в карбонаты нагреванием или добавлением известковой воды.
Выделяется газ, который не поддерживает горение.
задача №5
к главе «Практические занятия».
- Please wait.
- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Привет! Это онлайн школа «Умскул»
- Задание № 20569
- Уравнение реакции по получению углекислого газа, путём помещения в пробирку с кусочками мрамора или мела соляной кислоты?
- Получите CO2(углекислый газ) воздействием мрамора и соляной кислоты?
- Лабораторный опыт № 5 Качественная реакция на карбонат — ионы в растворе 1?
- Что будет наблюдаться если поместить в прибор для получения газов кусочки мрамора и добавить соляную кислоту налить в пробирку известквою воду и начать пропускать через неё углекислый газ из прибора д?
- Помогите с лабораторной?
- Получите углекислый газ с помощью аппарата, заряженного мелом или мрамором и соляной ккислотой?
- Поместите в пробирку несколько кусочков мела или мрамора ии прилейте немного разбавленой соляной кислоты?
- В пробирку поместите несколько кусочков мрамора или мела, прилейте к ним разбаывленную соляную кислоту объемом 2 — 3 см3?
- Составьте уравнение реакции получение углекислого газа из мрамора карбоната кальция?
- Получить углекислый газ при реакции мела с соляной кислотой?
- Помогите нужно составить реакции мрамора с соляной кислотой?
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 708278975e750119 • Your IP : 85.95.179.80 • Performance & security by Cloudflare
Привет! Это онлайн школа «Умскул»
Легендарный курс — Предбанник. Повтори весь материал ЕГЭ и ОГЭ за 5-9 дней!
Задание № 20569
1) Составьте сокращённое ионное уравнение оговорённой в тексте реакции получения углекислого газа взаимодействием соляной кислоты с мрамором.
2) Объясните, почему нежелательно использование серной кислоты при получении оксида углерода(IV) в аппарате Киппа.
Углекислый газ (СO2) — газ без запаха и цвета, тяжелее воздуха, при сильном охлаждении кристаллизуется в виде белой снегообразной массы — «сухого льда». При атмосферном давлении он не плавится, а испаряется. Содержится в воздухе и в воде минеральных источников, выделяется при дыхании животных и растений. Растворим в воде (1 объём оксида углерода в одном объёме воды при 15 °С).
Степень окисления +4 для углерода является устойчивой, тем не менее углекислый газ может проявлять окислительные свойства, взаимодействуя, например, с магнием. По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует кислоту. Реагирует с щёлочами с образованием карбонатов и гидрокарбонатов.
Организм человека выделяет приблизительно 1 кг углекислого газа в сутки. Он переносится от тканей, где образуется в качестве одного из конечных продуктов метаболизма, по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие.
В промышленных количествах оксид углерода(IV) выделяется из дымовых газов или в качестве побочного продукта химических процессов, например при разложении природных карбонатов (известняк, доломит) или при производстве алкоголя (спиртовое брожение). Смесь полученных газов промывают раствором карбоната калия, который поглощает оксид углерода(IV), переводя его в гидрокарбонат. Раствор гидрокарбоната при нагревании или при пониженном давлении разлагается, высвобождая диоксид углерода.
В лабораторных условиях небольшие количества его получают взаимодействием карбонатов и гидрокарбонатов с кислотами, например мрамора или соды с соляной кислотой в аппарате Киппа. Использование серной кислоты в данном случае менее желательно.
2) В случае использования серной кислоты образец мрамора покрывается сверху слоем малорастворимого сульфата кальция, что препятствует протеканию реакции.
Уравнение реакции по получению углекислого газа, путём помещения в пробирку с кусочками мрамора или мела соляной кислоты?
Химия | 5 — 9 классы
Уравнение реакции по получению углекислого газа, путём помещения в пробирку с кусочками мрамора или мела соляной кислоты.
Там есть учебник химия .
Выбери класс свой.
Получите CO2(углекислый газ) воздействием мрамора и соляной кислоты?
Получите CO2(углекислый газ) воздействием мрамора и соляной кислоты?
Лабораторный опыт № 5 Качественная реакция на карбонат — ионы в растворе 1?
Лабораторный опыт № 5 Качественная реакция на карбонат — ионы в растворе 1.
Положите в пробирку несколько кусочков мрамора (мела) и прилейте 1 — 2 мл соляной кислоты.
2. Налейте в пробирку 1 — 2 мл раствора карбоната натрия и прилейте равный объем соляной кислоты.
Что будет наблюдаться если поместить в прибор для получения газов кусочки мрамора и добавить соляную кислоту налить в пробирку известквою воду и начать пропускать через неё углекислый газ из прибора д?
Что будет наблюдаться если поместить в прибор для получения газов кусочки мрамора и добавить соляную кислоту налить в пробирку известквою воду и начать пропускать через неё углекислый газ из прибора для получения газов?
Помогите с лабораторной?
Помогите с лабораторной!
Почему для получения углекислого газа используют мрамор, а не мел или известняк.
Получите углекислый газ с помощью аппарата, заряженного мелом или мрамором и соляной ккислотой?
Получите углекислый газ с помощью аппарата, заряженного мелом или мрамором и соляной ккислотой.
Напишите сокращенное ионно — молекулярное уравнение реакции.
Поместите в пробирку несколько кусочков мела или мрамора ии прилейте немного разбавленой соляной кислоты?
Поместите в пробирку несколько кусочков мела или мрамора ии прилейте немного разбавленой соляной кислоты.
В пробирку поместите несколько кусочков мрамора или мела, прилейте к ним разбаывленную соляную кислоту объемом 2 — 3 см3?
В пробирку поместите несколько кусочков мрамора или мела, прилейте к ним разбаывленную соляную кислоту объемом 2 — 3 см3.
Закройте пробирку пробкой с газоотводной трубкой.
Соберите выделяющийся газ в пробирку методом вытеснения воздуха.
Как надо расположить пробирку — вверх или вниз дном?
Составьте уравнение реакции получение углекислого газа из мрамора карбоната кальция?
Составьте уравнение реакции получение углекислого газа из мрамора карбоната кальция.
Получить углекислый газ при реакции мела с соляной кислотой?
Получить углекислый газ при реакции мела с соляной кислотой.
Помогите нужно составить реакции мрамора с соляной кислотой?
Помогите нужно составить реакции мрамора с соляной кислотой.
На этой странице находится вопрос Уравнение реакции по получению углекислого газа, путём помещения в пробирку с кусочками мрамора или мела соляной кислоты?, относящийся к категории Химия. По уровню сложности данный вопрос соответствует знаниям учащихся 5 — 9 классов. Здесь вы найдете правильный ответ, сможете обсудить и сверить свой вариант ответа с мнениями пользователями сайта. С помощью автоматического поиска на этой же странице можно найти похожие вопросы и ответы на них в категории Химия. Если ответы вызывают сомнение, сформулируйте вопрос иначе. Для этого нажмите кнопку вверху.
M p — pa (h2so4) = 147 г (h2so4) = 5% m p — pa (naoh) = 480 г (na2so4) = 5% найти : m(so3) — ? Решения : 1)so3 + h20 = >h2so4 + 2naoh = >na2so4 + 2h20 2)(h2so4) = (h2so4) * (h2so4) / 100% = 5% * 147 / 100% = 7. 35 г 3)n(h2so4) = m(h2so4) / mr(h2so4..
1) 2Fe + 3Ba(NO3)2 — — — >3Ba + 2Fe(NO3)3 2)FeCl3 + 3AgNO3 — — >3AgCl + Fe(NO3)3.
5 задание Если что — то непонятно, то спрашивай.
А)CO2 б)P2O5 в)FeO г)SO2.
Маша и Владимир родились и воспитывались в разных семьях. Семья Маши Троекуровой была очень обеспеченной, а Владимир рос в бедной семье. По взглядам и характеру они тоже сильно различаются. Владимира никогда не беспокоило будущее, он растрачивал с..
Настоящая любовь возвышает человека, делает его терпимее, добрее, милосерднее. Именно такое сильное и глубокое чувство овладело сердцем главного героя повести А. С. Пушкина «Дубровский», когда он увидел дочь своего врага, жестокого и своенравного с..
Смотри + это легко ты просто складываешь электроны и их сумма будет равна порядковому номеру элемента в таблице менделеева.
Это Натрий (2 + 8 + 1 = 11) Два полностью заполненных энергетических уровня. )2 и )8.
1) KNO2 + NH4(стрелка вверх) — — — > Kl + N2(стрелка вверх) + 2H2O 2)KMnO4 + KNO2 + H2O — — — > 2MnO2 + 3KNO3 + 2KOH.
Можно было и не переводить задачу с украинского языка на русский. Я тебе напишу решение на твоем языке. Якщо елемент знаходиться в шостій групі, то він має найвищу валентність шість. Тобто його найвищий оксид має загальну формулу ХО3. Якщо вся ре..