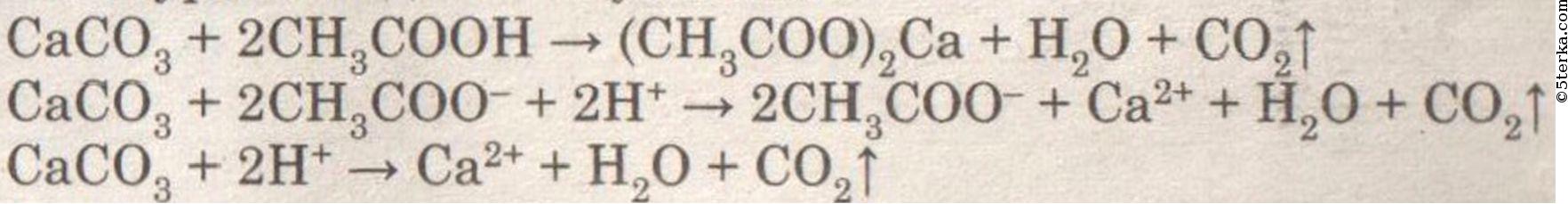Вариант 3. Получение, собирание и распознавание углекислого газа. При добавлении раствора уксусной кислоты к мрамору (мелу) наблюдается бурное выделение углекислого газа.
При внесении в пробирку горящей лучины лучина гаснет.
При пропускании углекислого газа через раствор известковой воды она мутнеет, а потом вновь становится прозрачной.

задача №3
к главе «Практическая работа №1 Получение, собирание и распознавание газов».
- Практическая работа №4
- Опыт 1. Получение, собирание и распознавание водорода.
- Опыт 2. Получение, собирание и распознавание углекислого газа.
- Опыт 3. Изучение состава солей.
- Опыт 4. Распознавание соединений неметаллов.
- Опыт 1. Получение, собирание и распознавание водорода.
- Опыт 2. Получение, собирание и распознавание углекислого газа.
- Опыт 3. Изучение состава солей.
- Опыт 4. Распознавание соединений неметаллов.
- Практическая работа №6. Получение, собирание и распознавание газов. —
- 🎥 Видео
Видео:Практическая работа №5. Получение, собирание и распознавание водорода.Скачать

Практическая работа №4
Видео:Дистанционный урок по химии. Тема "Получение, собирание и распознавание углекислого газа".Скачать

Опыт 1. Получение, собирание и распознавание водорода.
Поместите в пробирку (рис. 113), закреплённую в штативе вертикально, 2 гранулы цинка и налейте 3 мл соляной кислоты. Закройте пробирку пробкой с вертикальной газоотводной трубкой. На трубку наденьте пробирку. Подождите 2-3 минуты, чтобы верхняя пробирка наполнилась водородом. Осторожно снимите пробирку с водородом и, не переворачивая её, а слегка наклонив, поднесите отверстием к пламени спиртовки. Каков характер получившегося хлопка? О чём это свидетельствует? Напишите уравнения протекающих реакций.
Видео:Получение, собирание и распознавание углекислого газаСкачать

Опыт 2. Получение, собирание и распознавание углекислого газа.
Поместите в пробирку, закреплённую в штативе наклонно, кусочек мрамора. Налейте 2-3 мл соляной кислоты и закройте пробирку пробкой с газоотводной трубкой (рис. 114). Опустите свободный конец трубки в пробирку, содержащую известковую воду, так, чтобы пузырьки выделяющегося газа проходили через раствор. Что наблюдаете?
Напишите уравнения реакций в молекулярной и ионной формах.
Видео:Получение углекислого газа и тест на его обнаружениеСкачать

Опыт 3. Изучение состава солей.
Докажите опытным путём, что в состав хлорида аммония входят катион аммония NH4 + и хлорид-анион Cl — .
Докажите опытным путём, что в состав сульфата аммония входят катион аммония NH4 + и сульфат-анион SO4 2-
Докажите опытным путём, что в состав гидрокарбоната аммония входят катион аммония NH4 + и гидрокарбонат-анион HCO3 — .
Напишите уравнения реакций в молекулярной и ионной формах.
Видео:9 класс Химия Практическая работа Получение углекислого газа и изучение его свойств.Скачать

Опыт 4. Распознавание соединений неметаллов.
В четырёх пробирках под номерами без этикеток находятся кристаллические соли: сульфат калия, хлорид магния, карбонат натрия, силикат натрия. С помощью предложенных вам реактивов распознайте каждую соль, проведя качественные реакции на анионы. Напишите уравнения проведённых реакций в молекулярной и ионной формах.
Видео:Получение углекислого газа и изучение его свойствСкачать

Опыт 1. Получение, собирание и распознавание водорода.
При действии соляной кислоты на цинк наблюдается выделение газа:
Zn + 2HCl ⟶ ZnCl2 + H2↑
При поджоге собранного газа раздаётся глухой хлопок, это свидетельствует о том, что водород не содержит примесей.
2H2 + O2 ⟶ 2H2O
Видео:Практическая работа №4 Получение, собирание и распознавание кислородаСкачать

Опыт 2. Получение, собирание и распознавание углекислого газа.
При действии соляной кислоты на известняк наблюдается выделение газа:
CaCO3 + 2HCl ⟶ CaCl2 + H2O + CO2↑
CaCO3 + 2H + + 2Cl — ⟶ Ca 2+ + 2Cl — + H2O + CO2↑
CaCO3 + 2H + ⟶ Ca 2+ + H2O + CO2↑
При пропускании углекислого газа через известковую воду наблюдается помутнение раствора:
Ca(OH)2 + CO2 ⟶ CaCO3↓ + H2O
Ca 2+ + 2OH — + CO2 ⟶ CaCO3↓ + H2O
Ca 2+ + 2OH — + CO2 ⟶ CaCO3↓ + H2O
При дальнейшем пропускании углекислого газа наблюдается растворение выпавшего карбоната кальция:
CaCO3 + H2O + CO2 ⟶ Ca(HCO3)2
CaCO3 + H2O + CO2 ⟶ Ca 2+ + 2HCO3 —
Видео:Практическая работа №5. Получение углекислого газа, качественная реакция на карбонат ионыСкачать

Опыт 3. Изучение состава солей.
Хлорид аммония
Доказательство того, что в состав входит катион аммония NH4 + :
NH4Cl + NaOH ⟶ NH3↑ + H2O + NaCl
NH4 + + Cl — + Na + + OH — ⟶ NH3↑ + H2O + Na + + Cl —
NH4 + + OH — ⟶ NH3↑ + H2O
Доказательство того, что в состав входит хлорид-анион Cl — :
NH4Cl + AgNO3 ⟶ NH4NO3 + AgCl↓
NH4 + + Cl — + Ag + + NO3 — ⟶ NH4 + + NO3 — + AgCl↓
Ag + + Cl — ⟶ AgCl↓
Сульфат аммония
Гидрокарбонат аммония
Видео:8 класс Практическая работа Получение кислорода и изучение его свойствСкачать

Опыт 4. Распознавание соединений неметаллов.
1) Во все пробирки добавить воды.
2) Добавить щелочь. В пробирке с хлоридом магния выпадет белый осадок:
MgCl2 + 2NaOH ⟶ 2NaCl + Mg(OH)2↓
Mg 2+ + 2Cl — + 2Na + + 2OH — ⟶ 2Na + + 2Cl — + Mg(OH)2↓
Mg 2+ + 2OH — ⟶ Mg(OH)2↓
3) Добавить соляную кислоту.
В пробирке с карбонатом натрия выделится газ:
Na2CO3 + 2HCl ⟶ 2NaCl + H2O + CO2↑
2Na + + CO3 2- + 2H + + 2Cl — ⟶ 2Na + + 2Cl — + H2O + CO2↑
2H + + CO3 2- ⟶ H2O + CO2↑
В пробирке с силикатом натрия выпадет белый осадок:
Na2SiO3 + 2HCl ⟶ 2NaCl + H2O + SiO2↓
2Na + + SiO3 2- + 2H + + 2Cl — ⟶ 2Na + + 2Cl — + H2O + SiO2↓
2H + + SiO3 2- ⟶ H2O + SiO2↓
4) В оставшуюся пробирку (с сульфатом калия) добавим хлорид бария, выпадет белый осадок:
K2SO4 + BaCl2 ⟶ 2KCl + BaSO4↓
2K + + SO4 2- + Ba 2+ + 2Cl — ⟶ 2K + + 2Cl — + BaSO4↓
Ba 2+ + SO4 2- ⟶ BaSO4↓
Видео:Опыты по химии. Получение кислорода из перманганата калияСкачать

Практическая работа №6. Получение, собирание и распознавание газов. —
Вариант 1.
Опыт 1. Получение, собирание и распознавание водорода
Соберите прибор для получения газов и проверьте его на герметичность. В пробирку положите 1—2 гранулы цинка и прилейте в нее 1—2 мл соляной кислоты. Закройте пробирку пробкой с газоотводной трубкой (см. рис. 43) и наденьте на кончик трубки еще одну пробирку. Подождите некоторое время, чтобы пробирка заполнилась выделяющимся газом.
Снимите пробирку с водородом и, не переворачивая ее, поднесите к горящей спиртовке. Если водород взрывается с глухим хлопком, то он чистый, а если с «лающим» звуком, значит, водород собран в смеси с воздухом («гремучий газ»).
Вопросы и задания
1. Что происходит при взаимодействии цинка с соляной кислотой? Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций.
2. Рассмотрите записанную реакцию с точки зрения процессов окисления-восстановления.
3. Опишите физические свойства водорода, непосредственно наблюдаемые при проведении опыта.
4. Опишите, как можно распознать водород.
Ответ:
Собрали прибор для получения газов и проверили его на герметичность. В пробирку положили 1-2 гранулы цинка и прилили в нее 1-2 мл соляной кислоты. Закрыли пробирку пробкой с газоотводной трубкой и надели на кончик трубки еще одну пробирку, подождали некоторое время, чтобы пробирка заполнилась выделяющимся газом.
Сняли пробирку с водородом и не переворачивая ее поднесли к горящей спиртовке. Чистый водород взрывается с глухим хлопком.
Опыт 2. Получение, собирание и распознавание аммиака
Соберите прибор, как показано на рисунке 113, и проверьте его на герметичность.
В фарфоровую чашку насыпьте хлорид аммония и гидроксид кальция объемом по одной ложечке для сжигания веществ. Смесь перемешайте стеклянной палочкой и высыпьте в сухую пробирку. Закройте ее пробкой и укрепите в лапке штатива (обратите внимание на наклон пробирки относительно отверстия!). На газоотводную трубку наденьте сухую пробирку для собирания аммиака.
Пробирку со смесью хлорида аммония и гидроксида кальция прогрейте сначала всю (2—3 движения пламени), а затем в том месте, где находится смесь.
Для обнаружения аммиака поднесите к отверстию перевернутой вверх дном пробирки влажную фенолфталеиновую бумажку.
Прекратите нагревание смеси. Пробирку, в которой собран аммиак, снимите с газоотводной трубки. Конец газоотводной трубки сразу же закройте кусочком мокрой ваты.
Немедленно закройте отверстие снятой пробирки большим пальцем и опустите в сосуд с водой. Палец отнимите только под водой. Что вы наблюдаете? Почему вода поднялась в пробирке? Закройте пальцем отверстие пробирки под водой и выньте ее из сосуда. Добавьте в пробирку 2—3 капли раствора фенолфталеина. Что наблюдаете?
Проведите аналогичную реакцию между растворами щелочи и соли аммония при нагревании. Поднесите к отверстию пробирки влажную индикаторную бумажку. Что наблюдаете?
Вопросы и задания
1. Что происходит при взаимодействии хлорида аммония и гидроксида кальция? Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций.
2. Опишите физические свойства аммиака, непосредственно наблюдаемые в опыте.
3. Опишите не менее двух способов распознавания аммиака.
Ответ:
Собрали прибор для получения аммиака и проверили его на герметичность. В фарфоровую чашку насыпали хлорид аммония и гидроксид кальция объемом по 1 ложечке для окисления веществ. Смесь перемешали стеклянной палочкой и высыпали в сухую пробирку. Закрыли ее пробкой и укрепили на лапке штатива. На газоотводную трубку надели сухую пробирку для собирания аммиака. Пробирку со смесью хлорида аммония и гидроксида кальция нагрели.
Вариант 2.
Опыт 1. Получение, собирание и распознавание кислорода
Соберите прибор, как показано на рисунке 114, и проверьте его на герметичность. В пробирку насыпьте примерно на ¼ ее объема перманганата калия KMnO4 и у отверстия пробирки положите рыхлый комочек ваты. Закройте пробирку пробкой с газоотводной трубкой. Укрепите пробирку в лапке штатива так, чтобы конец газоотводной трубки доходил почти до дна сосуда, в котором будет собираться кислород. Наличие кислорода в сосуде проверьте тлеющей лучинкой.
Вопросы и задания
1. Что происходит при нагревании перманганата калия? Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций.
2. Рассмотрите записанную реакцию с точки зрения процессов окисления-восстановления.
3. Опишите физические свойства кислорода, непосредственно наблюдаемые в опыте.
4. Опишите, как вы распознавали кислород.
Ответ:
Собрали прибор для получения кислорода и проверили его на герметичность. В пробирку насыпали примерно на 1/4 ее объема перманганата калия у отверстия пробирки положили рыхлый комочек ваты.
Закрыли пробирку пробкой с газоотводной трубкой. Укрепили пробирку в лапке штатива так, чтобы конец газоотводной трубки доходил почти до дна сосуда, в котором будет собираться кислород.
Опыт 2. Получение, собирание и распознавание оксида углерода (IV)
В пробирку поместите несколько кусочков мела или мрамора и прилейте 1—2 мл разбавленной соляной кислоты. Быстро закройте пробирку пробкой с газоотводной трубкой. Конец трубки опустите в другую пробирку, в которой находится 2—3 мл известковой воды.
Несколько минут наблюдайте, как через известковую воду проходят пузырьки газа.
Вопросы и задания
1. Что происходит при взаимодействии мела или мрамора с соляной кислотой? Составьте уравнение реакции и дайте ее характеристику по всем изученным признакам классификации химических реакций.
2. Рассмотрите проведенную реакцию в свете теории электролитической диссоциации.
3. Опишите физические свойства оксида углерода (IV), непосредственно наблюдаемые в опыте.
4. Опишите, как вы распознавали оксид углерода (IV).
Ответ:
В пробирку поместили несколько кусочков мела и прилили 1 мл разбавленной соляной кислоты. Закрыли пробирку пробкой с газоотводной трубкой. Конец трубки опустили в другую пробирку, в которой находится 2-3 мл известковой воды. Наблюдаем как через известковую воду проходят пузырьки газа.
Эта реакция является качественной на углекислый газ.
🎥 Видео
Опыты по химии. Получение и собирание аммиакаСкачать

8 класс. Химия. Получение углекислого газа.Скачать

Практическая работа 5. Получение водорода и изучение его свойствСкачать

Получение, собирание и распознавание кислородаСкачать

Химия 9 класс (Урок№18 - Угарный газ. Углекислый газ.)Скачать

Химия-9. Практическая работа 5. Получение углекислого газа. Качественная реакция на карбонат-ион.Скачать

Качественная реакция на углекислый газ.Скачать

Получение, собирание и распознавание этиленаСкачать

Практическая работа №6. Получение аммиака и опыты с ним. 9 класс.Скачать

получение водорода и изучение его свойств/химия 8 классСкачать